バッテリーチャージャー - 鉛蓄電池の充電
電池とは、活物質中の化学エネルギーを電気エネルギーに変換する電気化学デバイスと定義されます。 このように、あるエネルギーが他のエネルギーに変換される反応が可逆的であれば、充電池や二次電池、蓄電池となります。 このようなセルは、放電後に繰り返し充電することで、反応の方向を逆転させることができる。 バッテリーが設計通りの寿命を発揮するためには、必要に応じて適切な充電を行う必要があります。
非可逆的な反応をする細胞を一次細胞と呼ぶ。
鉛蓄電池は、正極と負極をセパレーターと呼ばれる絶縁フィルムで隔てた構造になっています。 電解質には硫酸の希薄な溶液を使用します。 正の活物質は二酸化鉛(PbO2)、負の活物質は鉛です。
バッテリーチャージャーの詳細を説明する前に、バッテリーに関するいくつかの事柄を簡単に理解しておく必要があります。
アンペアは、電流(電子の連続的な流れと定義される)の単位です。 1秒間に1クーロン(または1アンペア秒)が点を通過するとき、その電流を1アンペアと定義する。
電圧とは、電子導体の中で電子が流れるための駆動力のことで、単位は「ボルト」です。 1アンペア・秒が1ジュールのエネルギーを持つとき、1ボルトの電位差があると言います。
この2つの用語は、建物の天井の水槽に例えられます。 水槽の高さが高ければ高いほど、水が流れる力も大きくなります。 同様に、タンクからユーザーに水を運ぶパイプの直径が大きければ大きいほど、ユーザーが受け取る水の量も多くなります。 パイプの中を流れる水は、水が流れる速度と比較することができます。
アンペアアワー(Ah)とは電気の量のことで、電流と時間の積である。
1Ah = 1A *1時間。
ワット(W)は電力であり、電流とボルトの積である。 高い方の単位はkW(=1000W)です。
メガワット(MW)(=1000kW)、ギガワット(GW)(10億W(1,000,000,000W))1。 w = 1 a * 1 v= va.
エネルギー(Wh)は、単位時間に供給される電力量です。 上位の単位はkWh(=1000Wh)です。
メガワットアワー(MWh)(=1000kWh)、ギガワットアワー(GWh)(=(10億Wh(1,000,000,000ワットアワー))。
大規模な発電所の出力を示すのにGW単位が使われる。 GWhは、大型電気自動車(EV)用電池産業や大容量蓄電システムの生産能力を示すのに使用されている Wh = 1 W* 1 h = 1 Wh
電池用語では、電圧が12、容量(Ah)が100であれば、1200Wh(または1.2kWh)の電池を持っていると言えます。
12 V * 100 Ah = 1200 Wh または 1.2 kWh。
電池の単位質量あたりの電力を比電力といい、単位はW/kgです。
比電力=W/kg、kW/kg。
同様に、単位質量の電池から供給されるエネルギーを比エネルギーといい、単位はkgあたりWhです。
比エネルギー=Wh / kg、kWh / kg。 (Wh kg-1と表記されることもあります)。
同様に、電池の単位体積あたりの供給電力を電力密度といい、単位はW/Lです。
電力密度=W/L、kW/L。
電池の単位体積あたりのエネルギー供給量をエネルギー密度といい、単位はWh/Lです。
1W=1J/秒
エネルギー密度=Wh/L、kWh/L。 (W L-1またはW l-1とも表記されます)。
鉛蓄電池の放電・充電反応は
Pb (NP) +PbO2(PP) + 2H2SO4放電⇔充電 PbSO4(PP) + PbSO4(NP) + 2H2O (PP付近)
注。 NP=ネガティブプレート=放電時の負極=放電時の電子の供与者。 PP = 正極板=放電中の正極=放電中の電子の受容体
充電中は電極の役割が逆転し、陽極が陰極に、陰極が陽極になります。 これで電子アクセプターは電子を放出し、ドナーは電子を受け取ることになる。
熱力学的自由エネルギーという言葉は、システムから抽出できる仕事の尺度です。 ガルバニ電池の場合は、反応物の化学的相互作用による荷電粒子の移動によって電気的な仕事が行われ、結果物(製品)が生成されます。
したがって、エネルギーはΔで与えられます。
G
,ギブの自由エネルギーの変化であり、これはエネルギー変換プロセスから抽出される可能性のある化学エネルギーの最大量を表します。
もし
E
は細胞の起電力(電圧または電位)であり、起こっているプロセス(すなわち 鉛蓄電池の放電)の経過と関連しています。
n
最近では(
F
)を反応物1モル当たり、一方の電極から他方の電極に移動させると、セルが行う電気仕事は次のように与えられます。
nFE
. これに伴う自由エネルギーの増加は、システムにかかる電気的な仕事と同じです。 ゆえに。
ΔG = nFE または
ΔG = -nFE または
-ΔG° = nFE°」となります。
(標準状態で、E°は標準電極電位または標準セル電圧を意味する)。
ギブス方程式
(標準状態とは、25℃(摂氏298.1度、ケルビン)、1気圧、反応種であるPb2+の活性(濃度と近似した値)が1である状態をいう)。
この方程式は
ギブズ方程式です。
ギブス方程式 は、セル電圧と自由エネルギー(DG)の変化を結びつける。 反応が自然に起こる場合(例:鉛蓄電池の放電)、ΔG は負(エネルギーが解放される)、emfは正、すなわちnFの電荷が細胞反応で想定される方向に自然に流れる。
一方、ΔG が正であれば、電気分解の現象を起こすことができます(例:鉛蓄電池の充電時)。
セルの起電力
セルの起電力は
集中熱力学的特性
すなわち,反応物の質量とセルの大きさの両方に依存しない。 濃厚な特性(とは対照的に
広範な特性
)は、反応物の質量に依存せず、したがって電池の大きさにも依存しません。 数ミリグラムの材料でも、数キログラムの材料でも、システムは同じ電圧を示し、材料の質量を増やすことで電圧を上げることはできません。 個々の電極電位は、その電極材料の固有の電気化学的特性であり、同様の条件でその値を変えることはできません。
濃厚な性質の例としては、電極やセルの電圧が挙げられます。一方、濃厚な性質は
広範な特性
は物質の量に依存します。例えば、質量、体積、エネルギー、アンペア時間、ワット時間などです。 このように、二酸化鉛活物質を鉛蓄電池に4.5グラム入れると、理論上は1アンペア時(Ah)が得られますが、45グラムあれば10倍のAhが得られることになります。 同様のことは、鉛や硫酸の活物質にも言えます。
標準的な細胞電位(E°)は、上記のように標準的な自由エネルギー変化(DG°)と関連しています。
鉛蓄電池の起電力は、以下の式から求められます。
生成物のΣΔGºƒ–反応物のΣΔGºƒ
ここで、ΔG°ƒは、反応種の標準的な生成自由エネルギーを意味します。
標準的な形成の自由エネルギー
表1
細胞反応に関与する化学種の標準的な生成自由エネルギーΔG°ƒ
(Hans Bode, Lead-Acid Batteries, John Wiley, New York, 1977, Appendix IV, p366.)
| 反応物・製品 | 数値(kcal mole-1) |
|---|---|
| PbO2 | -52.34 |
| Pb | 0 |
| H2SO4 | -177.34 |
| PbSO4 | -193.8 |
| H2O | -56.69 |
全体の反応は次のように書かれます。
Pb +PbO2+ 2H2SO4 ⇄2PbSO4+ 2H2O E° = 2.04 V.
ΔG° =生成物のΣΔGºƒ–反応物のΣΔGºƒ
のそれぞれの値を代入することで、例えば、標準的な教科書から得られる[1. Hans Bode, Lead-Acid Batteries, John Wiley, New York, 1977, Appendix IV, p.366]。
= [2(-193.89) + 2(-56.69)] – [ 0– (-52.34) + 2(-177.34)]
= –94.14kcalモル
–
1
= –94.14kcalモル
–
1 × 4.184 kJ モル
–
1(kcalをkJに変換するには4.184をかける)
= –393.88kJ/mole
E° = -ΔG°/nF
= -(-393.88× 1000)/2× 96485
= 鉛蓄電池の場合、2.04V
鉛蓄電池の標準セル電圧は2.04Vです。
と書かれており、鉛蓄電池の全体または全セル反応は
Pb +PbO2+ 2H2SO4 放電⇔充電 PbSO4(PP) + PbSO4(NP) + 2H2O (PP付近)
鉛蓄電池の充電と放電の詳細を説明する前に、電気化学の用語について知っておく必要があります。
標準状態の意味はすでにわかっています。
細胞の反応を(順方向であれ逆方向であれ)乱すと、細胞は平衡状態ではなく、乱れ た状態にあると言います。
電気化学系が乱されると、必ず標準電位との差が生じます。 このように、鉛蓄電池を強制的に放電させると、電流の大きさに応じて一定の値だけセル電圧が低下します。 現在の値が大きいほど、標準値からのずれが大きくなります。
これで、セルの電圧は
EDisch= E° – δV.
EDischの値はE°の値よりも低くなります。
逆に、セルを強制的に逆方向に移動させた場合(充電モード)には、セル電圧は電流の大きさに応じて一定の値だけ上昇します。
ECh=E°+δVとなります。
の値をδVと呼びます。
過電圧または過電位
で示されます。
記号η
.
δVの値は、放電反応ではマイナス、充電反応ではプラスになります。
このようにセルの電圧が低下したり上昇したりする現象を
分極
で、電極は分極状態にあると言われています。
そこで、方程式を次のように書き換えます。
EDisch= E° – η.
ECh=E°+ηです。
このように、放電時には
EDisch < E°と
充電中
ECh > E°.
この電圧のずれの理由は何ですか?
この偏差値の原因はいくつかあります。
- 内部抵抗(IR)による損失(ηohmic)
- プロセス開始時の両電極上の電荷移動による活性化分極ηt.
- 電解質や他の参加種の枯渇による濃度分極(ηc)。
IR分極による損失は、導電性の高い電極集電体や電解液を使用することで軽減することができます。 また、抵抗値の低いセパレータも有効です。
活性化分極は、電極の相境界を越えた電荷キャリアの移動に関連しており、このプロセスは転送反応と呼ばれています。 電池の電極では、相性の良い多孔質構造にすることで、両電極の電荷移動反応による移動過電圧を大幅に低減することができます。 後者は、反応に利用できる見かけの表面積ではなく、実際の内部表面積(BET表面積:孔、亀裂、裂け目の面積を含む)を大きくする。
電流密度
これにより、電流密度(1平方センチメートルあたりのアンペア数)が低下します。 したがって、空隙率が40%のプレートは、空隙率が50%のプレートよりも活性化分極による損失が大きくなります。
濃度の偏り(ηcは、反応生成物(鉛蓄電池の場合は硫酸鉛と水分子)が電極表面から移動して、新たな反応物(鉛蓄電池の場合は両電極からの鉛イオンと電解液からの硫酸イオンなど)に置き換わらなければ、より大きくなります。cは放電反応の終盤になるほど顕著になります。 細胞内では、イオンの輸送は、拡散と移動によって行われる。
拡散は濃度差によって起こり、移動は電界の力によって起こります。
拡散は、電解液やセパレーターのバルクで起こります。一方の電極でイオンが生成され、もう一方の電極で消費されると、イオンは電極間を移動しなければなりません。
また、電気化学反応の進行に伴い、多孔質電極でも発生します。 反応生成物は、拡散によって活性質量内を最終的な場所まで移動することができる。
特定のイオン種(荷電粒子)が移動によって運ばれる総電流の割合は、その伝達数の関数である。 陽イオンと陰イオンに分解された二元系電解質では、転移数は次の式で表されます。
ɩC+ ɩA= 1となります。
ここで、ɩC+ ɩA は、陽イオンと陰イオンの輸送数を示す。
転移数は、イオンの濃度と温度に依存する。 塩の二液性溶液では、これらはほぼ0.5に近い値を示します。 このように、両方のイオン種がイオン伝導度を等しく分担しています。
強酸とアルカリでは、プロトン(H+)とヒドロキシルイオン(OH-)のイオン移動度が高くなるため、大きなずれが生じる。 電池の電解質である硫酸(H+とHSO2-4に解離)と水酸化カリウム(K+とOH–に解離)の値を以下に示す。4
ιH+ =0.9; ɩHSO4
2-
= 0.1; ιK+ =0.22; ιOH- = 0.78
転移数とは、電流が流れることで特定のイオンの濃度がどれだけ移動の影響を受けているかを示す指標です。 値が小さいほど、移行プロセスへの影響が小さいことを示し、値が大きいほど移行プロセスへの影響が大きいことを示します。
2.D. Berndt, in Battery Technology Handbook, Ed. H.A. Kiehne, Second Edition, 2003, Marcel Dekker, Inc., New York, Table 1.2.
3.J S ニューマン 電気化学システム。 Englewood Cliffs:Prentice-Hall, 1991, p 255.
4.S U Falk, A J Salkind. アルカリ乾電池。 New York:John Wiley & Sons, 1969, p 598
それを明確にするためには、放電反応がどのように進んでいるかを理解する必要があります。 電池の端子が消費装置に接続されると同時に、電子が負極板から外部回路を通って正極板に流れ始めます。 細胞内では、電流の流れを整えるのは荷電粒子の役目である。 荷電粒子はプロトン(H+)と重硫酸イオン(HSO¯4 )である。
放電時には、負のHSO¯4イオン(ここでは、電解質である硫酸からH+ とHSO¯4に解離する重硫酸イオン)が負極板に向かって移動する。 これらのマイナスイオンは、活性物質であるPbと結合して、PbSO4という硫酸鉛を作り出します。 また、この反応では、プロトンと呼ばれる正電荷の水素イオンが生成され、これが移動する。 鉛活物質の陽極反応によって放出された2つの電子は、外部回路を経由して正端子に到達します。
ネガティブプレートまたはネガティブハーフセル反応。Pb + HSO¯4 ⇄ Pb2+ +SO42- +H+ + 2eE°= -0.35 V
2価の鉛イオンと硫酸イオンは直ちに結合して硫酸鉛となり、硫酸鉛として負極板に沈着する。
ここまでは、ネガティブなプレート反応の絵を見てきました。
次に、正極板上で同時に起こる現象を見てみましょう。
負極板からの電子は、正極端子に到達した後、正極活物質であるPbO2と反応し、硫酸鉛と2つの水分子を形成します。
正板反応または正半球反応。PbO2+ 3H+ +HSO¯4 + 2e- ⇄Pb2+ +SO4 2- +2H2O E° = 1.69 V
2価の鉛イオン(Pb2+)と硫酸イオン( )は直ちに結合して硫酸鉛となり、硫酸鉛として正極板に析出する。
溶解析出または溶解沈澱のメカニズム
このような反応は、鉛と二酸化鉛が鉛イオンとして溶解し、直ちに硫酸鉛としてそれぞれの電極上に析出することで起こる。
溶解-析出または溶解-沈澱のメカニズムで起こる。
ここで、2つの半減期の反応を組み合わせると
ネガティブプレートまたはネガティブハーフセル反応。Pb + HSO¯4 ⇄ Pb2+ +SO42- +H+ + 2ee
ポジティブプレートまたはポジティブハーフセル反応。PbO2+ 3H+ +HSO¯4 + 2e- ⇄Pb2+ +SO42- +2H2O
全体または全反応Pb +PbO2+ 2H2SO4Discharge⇔Charge 2PbSO4+ 2H2O
この反応理論は1881年にグラッドストーンとトライブが提唱したものだが、鉛蓄電池は1859年にフランスの物理学者レイモン・ガストン・プランテが発明したものである。
J.H.グラッドストーン、A.トライブ、Chemistry of the Planté and Fauré Accumulators,
ネイチャー
, 25 (1881) 221 & 461.
J.H. Gladstone and A. Tribe, Chemistry of the Planté and Fauré Accumulator, Nature, 26 (1882) 251, 342 & 602; 27 (1883) 583
放電反応は、20時間や10時間などの遅い放電速度の場合、活物質の約半分が硫酸鉛に変わるまで進行する。 この時点では、活物質の抵抗率が非常に高くなっており、さらに放電するとセル電圧が非常に速く低下します。 通常、セル電圧は1セルあたり1.75V以下になることはありません。
放流深度(DOD)が80%を超えるような深い放流は、その後の涵養を困難にする。
放電反応で鉛が鉛イオンとして溶解すると同時に、硫酸イオンと結合して負極板に沈着する。 鉛イオンや硫酸鉛の分子は、負極板から遠くには行きません。 これは、希薄な硫酸溶液に対する硫酸鉛の溶解度が非常に低いためです。 1リットルあたり1mg以上のオーダーで、二価の鉛イオンの硫酸鉛への析出は、電解質の濃度が高い場所の方が早くなります。 放電がさらに進むと、電解液への硫酸鉛の溶解度は1リットルあたり4mgまで増加する。
これは、酸がさらに排出されて希薄になり、そのような希薄な酸の中では、硫酸鉛の溶解度が高くなり、最大で1リットルあたり4mgになるためです。
このようにして堆積した硫酸鉛は、表面と隙間の両方で様々な大きさの結晶に成長していく。 . 本作は不連続な構造になります。 ゆっくりとした放電プロセスでは、この不連続な硫酸鉛の構造は、イオンが入りやすいオープンな構造になっているため、活物質の内部が反応に参加しやすくなります。 そのため、プレートの内部深くまで放電処理を進めることができます。
逆に、放電率が高い場合は、放電生成物であるPbSO4によって表面が塞がれ、切れ目のない連続した構造を形成することになる。 そのため、プレートの内部での反応が妨げられ、より高い放電率で期待通りの容量を得ることができないのです。
鉛蓄電池の充電
充電反応の際には、逆の現象が起こり、電流の流れが逆になり、酸化が起こります。
正極で発生し、負極で還元されます。
表2
充電・放電時の両電極の特性
| 電極 | 排出します。 | 充電 |
|---|---|---|
| ネガティブプレート |
多孔質(スポンジー)リード アノード 2つの電子を与える Pb -2e → Pb2+ 電圧が低下する(正の値が小さくなる)。 PbSO4に変換される |
~ 40% Pb + ~60% PbSO4 カソード 2つの電子を吸収する PbSO4のPb2+が2つの電子を取り込む 電圧が下がる(マイナスになる) 金属鉛に回収される 過充電で発生したH2 |
| ポジティブプレート |
多孔質二酸化鉛 カソード 2つの電子を吸収する Pb4+ (PbO2から) + 2e- → Pb2+ 電圧が低下する(正の値が小さくなる)。 PbSO4に変換される |
~ 50% PbO2 + ~50% PbSO4 アノード 2つの電子を放出 PbSO4のPb2+がPbO2になる。 PbO2に再変換される 電圧上昇 過充電時に発生したO2 |
図1
充放電反応における鉛蓄電池の電位変化値
セル電圧は、ガルバニックセルの機能のどの段階においても、2つの値の組み合わせである。
このように
セル電圧=正電極の電位-負電極の電位
そのため
鉛蓄電池の開放電圧または平衡電圧=1.69-(-0.35)=2.04V
放電終了時または終了間際には、セル電圧 EDisch = 1.50 – (- 0.20) = 1.70 V となる。
充電終了時または終了間際のセル電圧 ECh = 2.05 – (-0.65) = 2.70 V

バッテリーチャージャー - 充電係数
二次電池は、前回の放電で消費したAh容量を取り戻すために、充電が必要です。
以前の満充電の状態にするために必要なAhの量は、以前の出力と比較して10~15%多くなります。 この入力された電荷と出力された電荷の比率を電荷係数と呼びます。
充電係数=入力Ah/前回出力Ah=~1.1~1.2。
つまり、水を分解する過充電反応とグリッドの腐食反応で構成される二次反応を補うために、10~20%程度のAhを追加投入する必要があるのです。 また、内部抵抗によるロスもわずかながら発生します。
バッテリーチャージャー - 鉛蓄電池の充電効率
アンペアアワー効率
(アンペアアワーまたはクーロン効率とエネルギーまたはワットアワー効率)。
以上の議論から、「充電効率」という言葉を定義しなければならないことがわかります。
アンペアアワー効率
インドの規格であるIS1651には、以下のように試験方法が記載されている。
- 完全に充電されたバッテリーは、10時間のレートで、セルあたりの最終電圧が1.85ボルトになるまで放電させる。
- 正確なAhの出力を算出すること。
- これで、同じ電流で同じアンペア数のバッテリーが充電されたことになります。
- 今度は、先ほどと同じように2回目の放電を行います。
- Ah(クーロン)効率= ηAh= 2回目の放電時に供給されたAh / 入力されたAh。
エネルギー効率またはワットアワー効率
ワット時効率は、上記で求めたアンペア時効率に、平均放電電圧と充電電圧の比を乗じて算出する。
エネルギー効率またはワットアワー効率 = ηWh= ηAh* (平均放電電圧 / 平均充電電圧)
前回の放電の100%に等しい入力を同じ割合で行った場合の鉛蓄電池セルの充電のアンペアアワー(またはクーロン)効率はほぼ95%に等しく、エネルギーまたはワットアワー効率は85〜90%程度である。 また、インド規格(IS1651)では、アンペアアワー効率の最小値が90%、ワットアワー効率の最小値が75%と規定されている。
充電効率は、負極板よりも正極板で制限されます。 正極の硫酸鉛の約4分の3が二酸化鉛に戻り、水が内板の多孔質構造に十分な速度で拡散できなくなると、酸素の発生などの二次反応が起こる。 ある期間、充電電流は、PbSO4をPbO2 に変換する一次過程と二次の過充電反応の間で分配されます。 充電が十分に長く続き、硫酸鉛のほとんどが二酸化鉛に変換されると、充電電流のすべてが二次反応に使われます。
充電器の充電電圧
先に説明したように
ECh > E°.
そのため、この反応を促進するためには、もう少し高い電圧を供給する必要があります。 通常、優れた充電器は、充電のための十分に高い電圧源を持つように設計されています。 目安としては、2Vのセルに3V以上の電圧を供給し、1セルあたり2.7Vの電圧で満充電になるようにします。 しかし、ケーブルの損失なども考慮しなければなりません。
したがって、12Vのバッテリーの場合、バッテリーチャージャーは少なくとも18~20Vを供給する必要があります。
この電圧が15V以下になると、バッテリーは完全に充電された状態になりません。
再充電時:2PbSO4+ 2H2O →PbO2+ Pb + 2H2SO4
両電極上の硫酸鉛は、鉛イオンとして溶解し、直ちに負極板には鉛として、正極板にはPbO2として析出する。
正極板で
PbSO4+ 2H2O →PbO2+ 4H+ +SO4² – + 2ee
電子は負極板に移動してさらに反応する
負のプレートで
PbSO4+ 2e- →Pb +SO4²-。
両方のプレートに硫酸イオンが再現されているので、プロトンと結合して硫酸が生成され、電解液の比重が大きくなります。
電池のガス化
これまでは、充電中の有用な反応だけを見てきました。 しかし、過充電時には副反応や二次反応が起こることもあります。 主な副反応・副々反応は2つ。
- 水の電気分解と
- 正極板の腐食
これらの反応は次のように表されます。
水の電気分解
2H2O → O2↑ + 2H2↑ (過剰に浸水した電解液入り鉛蓄電池の両極に)
正極板からの酸素と負極板からの水素が進化し、ベントプラグホールから大気中に排出される。
しかし、バルブ式鉛蓄電池(VRLA)のセルでは、酸素は発生しますが、水素は発生しません。 また、発生した酸素は外に排出されず、AGMセパレーターの空隙を通って拡散し、負極材と反応して水分子を再生します。 これは、VRLAセルが水を補給しなくても成長できるようにするためのステップです。
2H2O → O2+ 4H+ + 4e – Starved electrolyte or VRLA cellの正極板上では
鉛蓄電池の正極板の腐食について
どちらのタイプの鉛蓄電池でも、ポジティブグリッドの腐食は同じように起こります。
グリッド腐食。Pb + 2H2O →PbO2+ 4H+ +4e-。
白金化した白金電極を陰極にすると、ほぼ可逆的に水素が発生する。
ソリューションの水素ポテンシャル 鉛などの他の電極では、より負の電位が必要です。
この反応が起こるためには
セル電圧が2.3Vになるまでは、ガスの発生はほとんどありません。 しかし、ガスが発生するのはセルあたり2.4Vからです。 2.4Vを超えるとガスの発生が多くなり、充電効率が低下してしまいます。 2.5Vになると、ガスが大量に発生し、電池の電解液の温度が上昇し始めます。 これで十分なガスが発生して電解液が撹拌され、比重が均等になり始めます。 電池が空回りしているときは、電解液の比重が上層部よりも下層部の方が少し高くなります。 これはセルの高さが高いと悪化します。
鉛蓄電池は、過度のガス発生や高温、端子の電圧が非常に高くならない範囲であれば、どのような速度でも充電することができます。 完全に放電した電池は、ガスが発生したり、電圧や温度が大きく上昇したりすることなく、充電開始時に高い充電率を吸収することができます。
充電工程のある時点で、プラスのプラットで硫酸鉛のほとんどが二酸化鉛に変わると、二次反応が優勢になる。 それは、先に挙げた水の電気分解反応とポジティブグリッドの腐食です。
このような正グリッド腐食は、形成段階(ジャー形成の場合は最初の充電)から始まっている。 この腐食は、鉛蓄電池の寿命に最も悪影響を与えるものです。 セルが過充電領域に入るたびに正極板の腐食が発生するため、グリッド構造の一部が二酸化鉛に変化し、腐食期間ごとにグリッドの重量が少しずつ減少していきます。 最終的には、連続したグリッド構造が利用できないため、グリッド上の反応サイトからの電子がバスバーに移動できない段階に到達します。
その結果、活物質の一部がエネルギー生成プロセスに参加できなくなり、容量が低下して電池の寿命が尽きてしまいます。
鉛蓄電池のメーカーは、この問題を解決するために、鉛合金の耐食性を高める合金元素を配合している。 砒素(As)や銀(Ag)のような合金成分が何分の1か含まれています。 原則として、正極材中のAsは約0.2%、Agは約0.03~0.05%となります。
バッテリーチャージャー - 現在の受け入れ意味
現在の受け入れ態勢は、セルのデザインによって決定されています。 例えば、同じAhの電池でも、プレートの数が多い(つまりプレートが薄い)場合は、表面積が増えるため、より高い充電電流を受け入れることができます。 個々のプレートの充電効率を測定するための詳細な手順については、K.Petersの論文を参照してください。. [8]
これは主に、ネガティブプレートの方がポジティブプレートよりも電荷受容性が高く(図1参照)、プレート内部への酸の拡散を容易にする、粗くて開放的な細孔構造によるものです。 ポジティブは、いくつかの設計要素にもよりますが、SOC70〜80%で過充電になり始めます。 内側のパラメトリック設計要素としては、細孔構造、真の表面積などがあります。 その他の外部パラメータとしては、充電電流(アンペア)、電解液の温度などがあります。
負のプレートの充電受容性が高く、SOC90%と比較的遅い時期に過充電領域に入る[8.K. Peters, A.I. Harrison, W.H. Durant, Power Sources 2.Research and Development in Non-mechanical Electrochemical Power Sources, Pergamon Press, New York, USA, 1970, pp.1-16.].
[9. A.M. Hardman, Journal of Power Sources Vol. 23, Year 1988, page, 128] となっています。

しかし、ある時点から負極で二次反応が始まり、主に単純な電子移動による水素イオン(プロトン)の水素ガスへの還元(負極板可逆電位E°値である-350mVよりはるかに低い電位で発生)が起こり、約-0.6~0.95Vとなる。
2H+ +2e- →H2↑のようになります。
負極板に蓄積される重要な不純物の一つにアンチモン(Sb)がある。アンチモンは、グリッド中のアンチモン量が相対的に多いセルでアンチモンマイグレーションと呼ばれる現象により析出する。 アンチモンは、ほとんどの鉛蓄電池のグリッド合金に不可欠な成分ですが、電池の性能に悪影響を及ぼします。
充電の腐食段階(各サイクルの充電終了時)では、ポジティブグリッドがアノード攻撃を受け、アンチモンがSb5+イオンとして溶液中に移行し、その一部がポジティブ活物質に吸収され、局所的なセル形成による自己放電が促進されることになります。 溶け残ったアンチモンはSb3+として正極表面(負極板表面)に析出し(アンチモンマイグレーション)、鉛に比べて水素過剰電位が低いため、水素の発生を早めることになる。 その後、大量のガスが発生する時期には、好ましい条件の下でアンチモンがプロトンと結合してスチビンガス(SbH3)としてある程度放出されることもある。
好ましい条件下では、ヒ素(As)とも同様の反応が起こり、有毒ガスであるアルシン(AsH3)が発生することがある。 そのため、潜水艦のように閉鎖された環境で使用される場合には、当然ながらこの合金成分は使用されません。
熱力学的には、一次充電反応よりも低い電位で起こりますが、正極での酸素発生と同様に、リード電極での水素発生のオーバーポテンシャルが比較的大きいため(約-0.650V)、水素発生が本格的に始まる前に充電がほぼ完了してしまいます。
これらのガスは、ベントプラグホールを介してセルから排出されます。 どちらのプレートも不純物によるオーバーポテンシャルの影響を受けるため、完全に効率的な充電はできません。 例えば、酸素発生の反応電位と水素発生の反応電位を組み合わせると、次のようになります。
1.95 + (-0.95) = 2.9 Vで大量のガスが発生します。
また、基本的な法則として、1.23Vで水が分解し、この電位では正電極上で酸素が発生することになっています。 しかし、実際の細胞ではそうはいきません。 そうなれば、鉛蓄電池そのものの安定性が問われることになる。 標準的な正極板電位(E°=1.69V)は、水が分解するはずの電圧(1.23V)よりも約0.46V高い。 原因はやはり過電圧です。 つまり、硫酸溶液中で二酸化鉛に酸素を発生させるための電圧は、正極板のE°値1.95Vをはるかに超えています。
このように、硫酸溶液中の二酸化鉛の酸素発生反応が阻害され、正極板のE°値より0.26V(1.95-1.69=0.26)、水の分解電位より約0.72V(1.95-1.23=0.72V)高くなり、厳密に純粋な溶液中では過電圧値に達するまで酸素が発生しないことになります。
同様に、硫酸溶液中の鉛上での水素の発生は、鉛上での水素のオーバーポテンシャルのために強く抑制される。 このオーバーポテンシャルの値は、約0.6Vマイナスで、硫酸溶液中の鉛の標準電極電位E°=-0.35Vを下回っています。 したがって、厳密に純粋な溶液では、電極値が-0.95Vになるまで、水素発生反応が負極板の完全な充電を妨げることはありません。 これが、負極板の方が正極板よりも充電効率が良い理由です。
しかし、実用的なセルでは、この電圧よりもずっと前にこの段階に到達します。 実際には、この2.9Vは実用的なセルでは全く実現されていません。なぜなら、不純物による反応が優勢になり、体積による完全なガス発生(H2:O2 = しかし、充電電圧が高すぎると2.9Vになることがあり、特にSbフリー合金電池では2.8V、アンチモン電池では0.2V低い2.6Vとなります。
さらにサイクルを進めていくと、アンチモン細胞の場合にはガス発生量が非常に減少しますが、他の細胞ではこの影響がほとんどありません。 この大幅な減少は、先に説明した「アンチモン・マイグレーション」という現象によるものです。
当然のことながら、新電池とサイクル電池の電圧差は、250mVから400mVに増加する。 そうすると、活物質が電荷を受け取れなくなり、電流のほとんどが水素や酸素を発生させることになります。 図3はこの点を示しています。[10. Hans Tuphorn, Chapter 17, Figure 17.2 in Battery Technology Handbook, Ed. H.A. Kiehne, Second Edition, 2003, Marcel Dekker, Inc, New York.]

12Vのバッテリーチャージャーの仕組みは?
バッテリーを充電する際には、プラスの出力リード線をバッテリーのプラス端子に、マイナスをマイナス端子に接続します。 その後、適切な方法で充電器をAC電源に接続します。
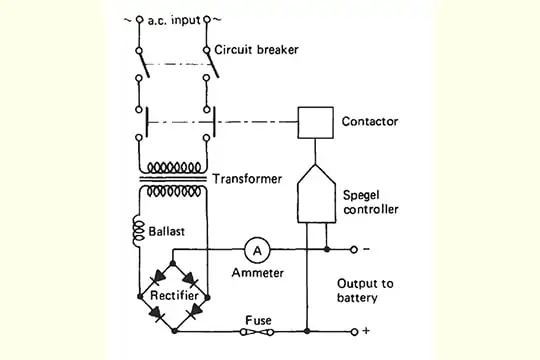
AC入力は整流回路でDCに変換され、降圧トランスで必要な電圧に変換されます。 整流器は、双方向性の交流電流(AC)を一方向性に変換する。 そのため、負荷に対して一定の極性を保つことができます。 降圧された低電圧の交流をブリッジ整流器で直流に整流し、さらに大容量の電解コンデンサー(フィルタリング回路)で平滑化します。
濾過された直流は電子回路に送られ、一定の電圧に調整され、充電が必要なバッテリーに印加されます。
充電器には、電流(電流計)、電圧(電圧計)のほか、特別な場合にはタイマーやアンペアアワーメーターなどの表示もあります。
バッテリーがメーカーの指示通りに充電されていること
バッテリー充電の手順 - バッテリーチャージャー
充電が必要なバッテリーは、外側を徹底的に洗浄し、端子に腐食物がある場合はそれを取り除いた後、白色ワセリンを薄く塗布しなければならない。 また、電解質レベルもチェックされます。 水位がセパレーターの高さを下回らない限り、この時点では補充する必要はありません。
バッテリーを充電するための充電器は、電圧や電流などの仕様が適切である必要があります。 必要な電流は、バッテリーの容量や充電時間によって異なりますが、例えば12Vのバッテリーの場合、出力Cの電圧は18V以上が必要です。 通常は、バッテリーのAh容量の10分の0アンペアで充電されます。 そのため、100AHのバッテリーを普通に充電するには、最低でも10アンペアの出力が必要となります。 急速に充電したい場合は、15アンペアの出力が必要になります。
完全に放電したバッテリーには、容量の約110%の入力が必要です。 しかし、すでに部分的に充電されている場合は、SOCを知る必要があります。 いずれにしても、電圧と比重は、充電の状態を判断するための重要なモニター項目です。 比重値は、電池のラベルから読み取る必要があります。 完全に充電されたバッテリーは、良好な状態であれば通常16.5V以上に達します。 老朽化したバッテリーの場合、この電圧には簡単に到達できません。
これは、電解液中の水分の電気分解によるガス発生や、蓄積された硫酸鉛による抵抗値の上昇などの副次的な反応が主な原因です。
ゴムシートや木の台などの絶縁体の上に電池を置きます。 充電器のリード線は十分な通電容量があること。 通常、1mm角の銅線は、3アンペアの直流(DC)を安全に流すことができます。 充電器がオフになっていることを確認した後、充電器のリード線をそれぞれの端子(プラスとプラス、マイナスとマイナス)に接続します。 電圧、比重、温度の測定値はログシートに記録されますが、そのモデルを以下に示します。
バッテリー充電記録テンプレート

測定値は1時間ごとに記録する。
カドミウムの測定値は、特定のプレートが完全に充電されているかどうかを示します。 カドミウム参照電極は、絶縁されたカドミウムの棒の上端に銅線をはんだ付けしたものです。 下端は電解液に浸して、ちょうど液に触れるようにして、中のプレートなどのリード部品に触れないようにします。
満充電の正極板の場合、カドミウムの測定値は2.4V以上、負極板の場合はマイナス0.2V以下となります。
表4
鉛蓄電池の反応と対応するカドミウムの電位測定値
カドミウムの潜在的測定値
| リアクション | 潜在的な価値 | カドミウムの測定値 |
|---|---|---|
| 酸素発生ポテンシャル 2 H2O → O2 + 4 H+ + 4e- (注) | 1.95~2.00 V | 2.00 - (-0.4) = 2.4 V |
| 正極板の標準電極電位 PbO2/PbSO4/H2SO4 | 1.69 V | [1.69 - (-0.4) = 2.09 V] |
| 正極板の放電終了 | 1.40~1.5V |
1.40 - (-0.4) = 1.8 V 1.50 - (-0.4) = 1.9 V |
| 標準水素電極電位(SHE) 2H+ + 2e- → H2 | 0.00 V | 0.00 V |
| 負極板の放電終了 | -0.15, -0.20, -0.25 V (異なる電流密度の場合) | -0.15 - (-0.4) = 0.25 V -0.20 - (-0.4) = 0.20 V -0.25 - (-0.4) = 0.15 V |
| 標準電極 負極板の電位 Pb/PbSO4/H2SO4 | -0.35 V | [-0.35 - (-0.4) = 0.05 V] |
| カドミウム参照電極 E°値 Cd/Cd2+ | -0.40 V | -0.40 V |
| 水素発生の可能性-。 2H+ + 2e- →H2 (市販の携帯電話の場合)。 | -0.60 V | -0.60 - (-0.4) = -0.20 |
| 水素発生の可能性 2H+ + 2e- →H2 純粋な実験用セルの場合 | -0.95 V | -0.95 - (-0.4) = -0.55 |
バッテリーチャージャーの動作原理
12Vバッテリーの充電終了時には、端子電圧が16.5以上になることもあります。 この端子電圧を1時間維持すると、充電を終了することができます。 バッテリー残量が16に近づくと 0 V、必要に応じて承認された水を追加することができます。
充電終了間際になると、バッテリーから激しいガスが発生します。 充電室に直火を近づけてはいけません。 水素が2、酸素が1というように、気体はその組み合わせの比率で発生します。 そのため、これらのガスが適切な換気をせずに充電エリアに溜まってしまうと、火花や直火がガスに引火して爆発的な暴力を伴い、バッテリーやその周辺を破損したり、周囲の人に危害を加えたりする可能性があります。
水素の空気中での爆発性混合物の下限は4.1%ですが、安全のためには水素が2%を超えてはいけません。 上限は74%です。 これらのガスが化学量論的な比率(水素2に対して酸素1)で混合されていると、重度の爆発が暴力的に起こります。 この状態は、ベントプラグがカバーにしっかりとねじ込まれている過充電のバッテリー内で得られます。 そのため、ベントプラグはベントホールにゆるくかぶせておき、強くねじ込まないようにすることをお勧めします。
電池の充電方法の違いと充電器の種類の違い
鉛蓄電池の充電方法にはさまざまなものがあるが、いずれも反応生成物である両極の硫酸鉛を、正極のPbO2と負極のPbというそれぞれの活物質に変換するという点では共通している。
2 PbSO4+ 2 H2O →PbO2+ Pb + 2 H2SO4
充電方式にはいくつかのバリエーションがあります。 しかし、これらの方法では、定電流充電方式と定電圧充電方式という2つの基本原理しか使われていません。 この2つの原則を組み合わせて、目的を達成するためのいくつかの方法が用意されています。
適切な充電方法の選択は、タイプ、デザイン、使用条件、充電に使える時間によって異なります。 これらの充電方法はすべて、充電プロセスを制御して終了するために多くの方法を使用しています。
これらの方法は、以下のように分類されます。
表5
バッテリーチャージャー&バッテリー充電方法の違いによる方式の分類
異なるバッテリー充電方法
| 定電流方式(CC) | 定電圧駆動方式(CVまたはCP) | コンビネーション方式 | テーパー充電 | 特別な方法 |
|---|---|---|---|---|
| シングルステップのCC充電方式 | 定電圧方式 | CC-CV方式 | シングルステップテーパー充電方式 |
1.初期費用 2.均等割増金 3.チャンスチャージ 4.ガス制御式充電 5.トリクル充電 6.ブースト充電 7.パルス充電 8.高速充電または急速充電 |
| 2段階のCC充電方式 | 電流制限法または修正CV法 | 2段階のテーパー充電方式 |
シングルステップ 定電流充電方式(CC方式) バッテリーチャージャー
短時間で充電を終えたい場合や、入力をAhで知りたい場合には、定電流充電方式を採用することがあります。 前回の出力がわかっている場合は定電流充電が好ましく、5~10%の過充電でもSOC100%に戻すのに効果的です。 また、無理な過充電によってバッテリーの寿命に悪影響を与えないように、適切な入力を行うことができます。 この方法では、通常の充電時間は15~20時間です。
この方法では、充電期間中、電流を一定に保つことができます。
充電電流は、20時間の容量の5~10%を目安にしてください。
充電中の電池の逆起電力の増加を補うためには、使用する直列抵抗を変えるか、トランスの電圧を上げることで、充電電流を一定に保つ必要があります。 通常、電流が一定になるように直列抵抗を変化させます。
この方法は、最もシンプルでコストのかからない充電方法です。 しかし、充電効率が低いという欠点があります。 これは、一部の電力が抵抗で消費されていることと、バッテリーが1セルあたり2.5Vに達すると、水を分けるために電流が使われることが原因です。 バッテリーが70~75%程度の充電量になるとガスが発生し始めます。 この方法で充電すると、常にわずかな過充電になり、特に充電の終わりには激しいガスが発生します。
定電流充電方式の一般的なイメージを図5に示します。 充電特性を図6に示します。


2段階の定電流充電方式 バッテリーチャージャー
2段階定電流充電方式では、スタートレートとフィニッシュレートの2つの充電レートを使用します。 終了時のレートは通常、開始時のレートの半分です。 バッテリーからガスが発生し始めた時点で、仕上げ速度が開始されます。 この方法は、一般的に電池をベンチで充電する際に好まれる方法です。 充電特性は、図7[11] のようになります。P G バラクリシュナン、鉛蓄電池。 サイテックパブリケーションズ(インド)社 Ltd., Chennai, 2011, page 12.8].

定電圧・電位充電方式 バッテリーチャージャー
定電圧・定電位(CV・CP)充電方式は、充電期間中、電源電圧を一定に保つ方式です。 通常、この電圧は1セルあたり2.25~2.4Vになります。
この方法は、VRLA(valve-regulated lead-acid)セルおよびバッテリーを充電する際に推奨される方法です。 CV方式でVRLAバッテリーを充電する際には、前回の放電の深さ(DOD)を気にする必要はありません。 VRLAバッテリーは、メーカーが推奨するCV充電電圧を使用することで、有害な影響を受けることなく充電することができます。 ほぼすべてのVRLABメーカーは、0.25~0.30Cアンペアの起動電流を推奨しています。
つまり、100Ahのバッテリーの場合、初期電流は25〜30アンペアを選択することができます。 高い電流は深放電したバッテリーの充電に、低い電流は通常の放電したバッテリーの充電に使われます。 充電電圧を下げると、電流を上げて充電した場合に比べて温度上昇が少なくなりますが、満充電までの時間は長くなります。
充電終了時には、バッテリー電圧が印加した電圧と同程度になり、充電電流は非常に小さくなります。 一般的には、バッテリーの容量1Ahあたり2〜4mAの電流が流れると言われています。 セルあたり2.25~2.3Vの電圧では、適切に作製された電池ではガスの発生は見られない。 しかし、1セルあたり2.4Vではガスの発生が顕著になります。 6V/1500AhのVRLABでは、1セルあたり2.4Vで40〜50分で約1000mlのガスが発生する。
条項6.1.aによる。 日本工業規格JIS 8702-1:1998の規定により、充電時間は約16時間、または連続した2時間の間に20時間率電流(I20)アンペアの10%以上の電流変化がなくなるまでとなっています[JIS 8702-1:1998] 。 例えば、電池の20h容量(電池の電圧に関わらず)が60Ahの場合は20であれば、電流が300mA以上変化しなければ充電が完了したことになる(すなわち、I20= 60 Ah /20 A = 3 A. したがって、0.1のI20= 0.3A)
VRバッテリーのCPチャージの詳細は図の通りです。
充電効率は定電流方式よりも優れています。 この方法のデメリットは、大電流のドレインに安定した電圧を必要とするため、コストがかかることです。 この方式は、通信機器やUPS用の定置型セルのフロート動作に使用されています。


変形定電位充電 - バッテリーチャージャー
産業用途では、充電回路がシステムの一部となっている場合に、このような方法が用いられます。 例えば、自動車やUPSなどです。 回路内には電流を制限するための直列抵抗が含まれており、あらかじめ設定された電圧に達するまでその値が維持されます。 その後、始動電流や非常用電源など、バッテリーの役割を果たすまで、電圧は一定に保たれます。
固定直列抵抗の選択は、電池のセル数とそのアンペア・アワー容量、および充電可能な時間に依存する。 印加電圧は、1セルあたり約2.6~2.65ボルトと一定に保たれています。
充電が進むにつれ、充電電流は初期値から減少していきます。 セルあたりの電圧が2.35~2.40ボルトまで徐々に上昇すると、ガス化電圧が急激に上昇する傾向にあり、そのため充電電流の低下も速くなります。
改良された定電位充電は、トラクション・バッテリーのようなディープサイクルのバッテリーによく見られます。 工場では通常、フォークリフトを6時間運転して放電深度(DOD)を80%にし、8時間かけて再充電するなど、放電と充電の時間が決まっています。 充電器はガス抜き用の電圧に設定され、起動電流は100Ahあたり15~20Aに制限されています。 電流は定電圧で漸減し始め、100Ahあたり4.5〜5Aの仕上がりとなり、これを充電の最後まで維持することができる。 トータルの充電時間はタイマーで制御されます。
充電完了後も電池を接続しておき、満充電の状態を維持する機能を持つ充電器もあります。 このため、6時間ごとに短時間のリフレッシュ充電を行い、コンディションを維持しています。
その詳細を図12[12.鉛蓄電池特集,J. Power Sources2(1) (1977/1978) 96-98]に掲載されています。

コンビネーション方式(CC-CV方式) - バッテリーチャージャー
この方法は、定電流充電と定電位充電を組み合わせたものです。 この方式は、(IU)(Iは電流、Uは電圧)充電方式とも呼ばれています。 充電の初期段階では、バッテリーがガス抜き電圧に達するまで定電流モードで充電し、その後、定電位モードに切り替わります。 この方法では、定電流充電方式のような充電終了時の悪影響がありません。
この方法での充電特性を右図11に示します。

テーパー充電 ・バッテリーチャージャー
テーパーの意味は、傾斜をつけることです。 この言葉が示すように、充電開始電圧をセルあたり約2.1Vに固定し、セルあたり2.6Vで終了させることで、電流を高い値から低い値へと減少させることができます。 これらの電圧における電流値の比をテーパー値と呼ぶ。
例えば、2.1Vで50A、2.6Vで25Aの出力を持つ充電器は、テーパー特性が2:lであると表現されます。
1段階のテーパー充電と2段階のテーパー充電がある
シングルステップテーパー充電 - バッテリーチャージャー
このタイプの充電では、電流は開始時の高い値から終了時の低い値に向かって先細りになり、通常はバッテリーの20時間率容量の4〜5%程度になります。 ガス抜きは、電解液の密度勾配を均一にするために必要な現象です。 つまり、成層化現象を中和することができるのです。 そのため、このプロセスを可能にし、同時に正極板を過度に腐食しないように、仕上げ率は十分に高い値に固定されています。 ここでは、充電器の出力電圧を最初は1セルあたり約2.7ボルトに設定し、充電終了時には1セルあたり約2.1〜2.2ボルトになるようにしています。
充電電流は、ガス化電圧(セルあたり約2.4V)に達するまで(SOC=75〜80%)、ゆっくりと先細りになり、その後はより速いペースで先細りになります。 通常、テーパー比は2対1または1.7対1に固定されています。 充電完了までの時間は約12時間。 ガス化電圧に達した後の充電期間は、ガス化電圧に達したときに動作を開始するタイミングデバイスを組み込むことで制御します。
充電時間は8〜10時間に短縮できますが、起動電流を高める必要があり、そのためには経済性や消費者の買いやすさを考慮しなければなりません。

シングルステップテーパー充電の充電特性を図12に示す。

2段テーパー充電 - バッテリーチャージャー
この充電方法は、総充電時間が約8〜10時間に短縮されることを除けば、シングルステップテーパー充電と同様です。 バッテリーは深い放電状態の方がより早く充電を受け入れることができるため、最初のステップでは、バッテリーがガス化するまで大電流を流します。 バッテリーに戻すべきアンペア数の7〜8割近くを、第1段階で高速にバッテリーに与え、残りのアンペア数を第2段階で供給する。
12V、500Ahのバッテリーの1段テーパー充電による充電特性を図13に示す。
テーパー充電方式は、通常は深く放電しているトラクション・バッテリーの充電に適しています。 郵便配達車や牛乳配達車などの電気自動車のフリートオペレーターは、バッテリーの性能を最大限に引き出し、多額の投資を保護するために、高性能なバッテリーチャージャーを必要としています。
初期費用
新品の鉛蓄電池には活性化が必要で、この初めての充電を初期充填充電といいます。 電池に必要な量の電解液を入れ、完全に充電してから出荷します。 通常、この初期充電は、満充電となる16.5V以上の電圧になるまで、低電流で長時間かけて行う定電流充電方式で行われます。
現在では、工場で充電してすぐに使える電池や、電解液を入れるだけの乾電池があり、この工程は不要になっている。
均等割増金
イコライジングチャージセルとセルの違いは、受け入れざるを得ない事実です。 すべての面で同じ細胞は存在しません。 活物質の重さの違い、電解液の比重の細かな違い、電極の空隙率などがあります。 このような理由から、電池の各セルにはそれぞれ特徴があり、必要な充電量も少しずつ異なります。 たまには均等に充電することで、バッテリーの寿命を遠ざけることができます。 12Vの自動車用バッテリーは14.4Vに浮いています。 完全に充電されたバッテリーは16.5Vの電圧を必要としますが、これは車両に搭載された状態では実現しません。
そのため、自動車用バッテリーを長持ちさせるためには、均等充電(ベンチチャージとも呼ばれる)が必要です。 このように、6ヶ月ごとに定期的にベンチチャージを受けている電池は、ベンチチャージを受けていない電池よりも、少なくとも10~12ヶ月は長持ちする可能性があります。 均等化充電の頻度や範囲については、バッテリーメーカーと相談してください。 事前にプログラムされた充電器では、スイッチを介して「均等充電」が可能な場合があります。これは、電圧とセルの電解質の相対的な密度を安定させるために、連続的な低電流を供給するものです。
同様に、UPSの非常用電源のバッテリーやフォークリフトのバッテリーにも、このような均等化料金が必要です。 インバーターで使用されるバッテリーは、13.8〜14.4Vまでしか充電されません。先に述べたように、これではバッテリーのセル間のアンバランスを解消するには不十分です。 この電池は、定期的に均等に充電することで、より長く使用することができます。
バッテリーは6ヶ月ごとに均等に充電してください。 しかし、フォークリフトのバッテリーに使用されているトラクション・バッテリーは、新品か経年劣化かにもよりますが、6回目か11回目のサイクルに一度、均等化充電を行う必要があります。 新しいバッテリーは11サイクルに1回、古いバッテリーは6サイクルに1回、均等化充電を行うことができます。 毎日定期的にフル充電する場合は、均等化充電の頻度を10回目と20回目にすることができます。 均等化充電は、2~3時間の間にセルの電圧と比重の測定値がそれ以上上昇しなくなったときに終了します。
の詳細記事を読む
均等割増金についてはこちらをご覧ください。
オポチュニティ・チャージ
オフロードやオンロードの電気自動車を集中的に運転する場合、休憩時間などの短い休息時間に充電器に接続することで、電気自動車の有効な作業シフトを延ばし、ダウンタイムを短縮することができます。 機会充電とは、昼休みや休憩時間に部分的に充電することを言います。
このような機会損失は電池の寿命を縮める原因となります。 バッテリーは、このような充電とその後の放電を1つの浅いサイクルとして数えます。 機会損失はできる限り避けるべきです。 通常の充電では100Ahの容量に対して15~20A、機会充電では100Ahの容量に対して25Aと、やや高めの電流が流れます。 その結果、温度が上昇し、正極板の腐食が促進されます。 そして、それゆえに命が縮む。
ガス制御式充電
蒸発した水素ガスの熱伝導率を利用して、充電電流をモニターする。 発熱した素子の冷却には、優れた冷却剤である水素ガスを使用します。 発熱体の抵抗値の変化を利用して、電流を調整します。 また、電流を調整するためにサーミスタを使用することもあります。 また、セル内で発生した水素ガスと酸素ガスが適切な触媒を介して再結合することによる加熱効果を利用して、電流を調整するヒートスイッチを動作させることもある。
トリクル充電
連続充電では、自己放電と間欠放電による損失を充電器が均等化します。 自己放電を補うのがメンテナンスチャージです。 この2つの動作モードの特徴は、端子電圧が一定であることです。
メンテナンスチャージ 2.20~2.25V/セル
連続充電 2.25~2.35V/セル
バッテリーの使用年数や状態によっては、維持充電(トリクル充電)時に公称容量40~100mA/100Ahの電流密度が必要になる場合があります。
連続充電電流は、負荷プロファイルに大きく左右されます。 メンテナンス充電中のバッテリーは、停電のたびに再充電する必要があります。 予定外の負荷がかかった後、連続して充電しているバッテリーも同様です。
ブースト充電
ブースト充電は、放電したバッテリーを緊急時に使用する際、他のバッテリーがなく、SOCが緊急作業に十分でない場合に行われます。 このように、鉛蓄電池は時間や電池のSOCに応じて大電流で充電することができます。 急速充電器が使えるようになったので、今ではブースト充電が身近になりました。 通常、ブーストチャージャーは、100Aで充電を開始し、80Aまで漸減します。 最も重要なことは、温度が48~50℃を超えないようにすることです。
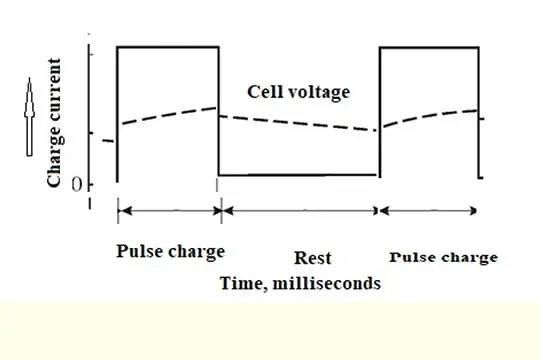
パルス充電
パルスカレント充電とは?
充電は非常に短い時間、つまり現在のオンタイム(ミリ秒)で行われ、その後にアイドル期間(オフタイム(ミリ秒))が続きます。 また、パルス充電の前に放電が行われることもあります。
自動車用の鉛蓄電池の急速充電には、パルス電流技術が応用されています。 次のような結論が得られました。
- パルス状の電流は、非常に有利な効果をもたらします。
- 充電率が向上します。
- 特にオンタイムが100ms以上の場合、鉛/酸電池のサイクル寿命性能に影響を与えます。
- さらに、この技術は、定電流充電を繰り返した細胞も若返らせることができます。
- 充電時間が約10時間から約1時間と桁違いに短縮可能
- サイクル寿命は3~4倍になります。
- サイクルした電池(容量=初期値80%)にパルス電流充電を行うことで、電池容量の回復を促すことができます。
- Pb-SbとPb-Ca-Snの両方のセルで、定電流充電で高率の放電を行うと、早期の容量低下が起こります。
詳しくは、上記のLam氏らの記事を参照してください。
海底のセルは、パルス充電の対象となっている[14.Melvyn James, Jock Grummett, Martin Rowan and Jeremy Newman, Journal of Power Sources 162 (2006) 878-883 879].著者らは次のように結論づけている。
- パルス充電で容量アップが可能です。 この能力向上
は、比較的新しい細胞では劇的に変化しました。 しかし、古いセル(4〜5年前のもの)では、容量が向上するまでに15回以上のパルス充電が必要でした。
- 古い細胞ほど硫酸化が激しく、分解にはより多くのサイクルが必要となります。
- 硫酸化の中には、元に戻すことができないものもあります。
- また、パルス充電を行うことで、ガスの発生を大幅に抑えることができました。
- ガス発生量は、パルス周波数を上げると減少します。 これは酸素発生量が多いほど顕著で、ガス充電時に正極板から酸素が発生するため、正極板の腐食に悩む潜水艦用バッテリーにとっては重要な要素です。
- パルス充電を行った後、通常の充電を再開しても、その効果は持続します。
代表的なパルス充電プログラムを以下に示します。
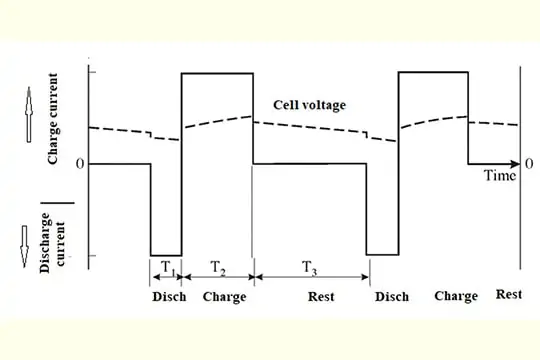
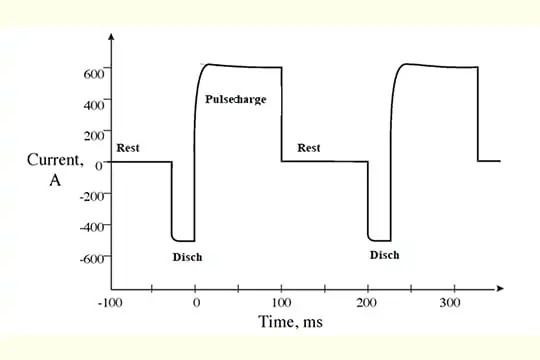
パルス充電を適用することで、時間の経過とともに蓄積されるサルフェーションを防ぐことができます。 最初からパルス充電を使えば、適切な充電とメンテナンスでセルの硫酸化蓄積を抑えられるかもしれません。 すでに発生してしまったサルフェーションの蓄積は、この方法では元に戻すことはできません。 常に均等化された状態や過充電の状態が続くと、セルが損傷し、容量や寿命が減少します。 マイクロテックスでは、バッテリーの寿命を知るためにも、弱ったセルや故障したセルを特定し、充電状態を確認するためにも、定期的にバッテリーの比重を検査することをお勧めしています。 硫酸が蓄積したり、充電のバランスが崩れたりした場合には、以下の手順を踏むことができます。
急速充電、高速充電、バッテリーチャージャー
25年前、鉛蓄電池は正極活物質が壊れてしまうため、高い充電率で充電してはいけないと言われていました。 急速充電を行うと、グリッドの腐食やガスが過剰に発生し、VRLAバッテリーが早期かつ急速に故障すると考えられていました。
急速充電は、時間とエネルギーの節約になるだけでなく、ガスの発生をなくし、メンテナンスを減らすことができることがわかっています。 急速充電は,1972年にKordeschが密閉型のNi-Cd電池で初めて提案したもので[17. K. Kordesch, J. Electrochem. Soc., 113 (1972) 1053],その後1993年にカナダのNorvik Technologies社がVRLA電池用に開発したものである。
彼らのMinitcharger™は、深放電したNi-Cd電池の再充電を5~10分で行えることを証明した[18. J.K.Nor, U.S. Patent 5,202,617(1993)]。
1990年代前半には、カナダ・コミンコ社のバレリオテ、ノル、エテルらが、この技術を従来の鉛蓄電池に発展させた[19]。 E.M. Valeriote, J. Nor, V.A. Ettel, Proc. 5th International Lead-Acid Battery Seminar, Vienna, VA, USA, 17-19 April 1991, pp 93-122].. 1994年、Valeriote、Chang、Jochimの3人は、このプロセスが薄板のVRLA電池にも適していることを証明した[M. Valeriote, T.G. Chang, D.M. Jochim, Proc.Valeriote, T.G.Chang, D.M.Jochim, Proc. of the9th Annual Battery Conference on Applications and Advances, Long Beach, CA, USA, January 1994, pp.33-38] となっている。
90年代初頭から、この技術はあらゆる種類のトラクション・バッテリーに応用されている[20]。 K.Nor and J.L. Vogt, Proc. 13th Annual Battery Conference on Application and Advances, January 13-16, 1998, Long Beach, CA, 191-197] となっている。
1994年にMinitchargerÔ(Norvik Traction Inc.、カナダ)を用いて、以下の2種類のディープサイクルハイブリッド鉛/酸電池に対する超急速充電の効果を研究した[21 .T.G. Chang, E.M. Valeriote and D.M. Jochim, J. Power Sources 48 (1994) 163-175].
- 正極には4.7%のアンチモン合金、負極には高カルシウム-低錫合金(Pb-0.1wt.%Ca-0.3wt.%Sn)のエキスパンドタイプを用いた浸水型ハイブリッド電池(本稿では「AP」と表記)。 各セルのPAM重量は~800g、NAMは~540gでした。 深放電タイプで、容量は80Ah20、54.4Ah5、50.9Ah3)。
- 低アンチモン合金(Pb -1.5wt.% Sb -0.3wt.% Sn)を用いて、重力鋳造の正極板を持つバルブレギュレーション式電池を製作した。構成は、5P+6N。負極はPb-O.12wt%Ca-O.4wt.%Sn合金から鋳造されました。これらの電池は、ディープサイクル用途を目的としたものである。電池の容量は54.5Ah。5および52.5Ah3
その結果,浸水型電池の場合,5分/50%充電と15分/80%充電の両方を,許容範囲内の温度上昇で達成できることがわかった。 80%の放電深度の後、300A(5~6C3アンペア)という非常に高いレートで戻ってきた充電の最初の40%の間、熱の主な原因はオーミックであった。 温度はバッテリー内で不均一に分布していました。 この後、非オーミックな偏光が徐々に重要になってきます。 ハイブリッド再結合電池では、酸素サイクルが充電の後期にかなりの熱源となり、特にこれまで調査されてきた非反発型の電池と比較して、その傾向が強い[21 T.G. Chang, E.M. Valeriote and D.M. Jochim, J. Power Sources48 (1994) 163-175]。
浸水型およびVRLAバッテリーの急速充電
表6.
[21. T.G.Chang, E.M.Valeriote and D.M.Jochim, J. Power Sources48 (1994) 163-175].
| 浸水したバッテリー | バルブレギュレーション式バッテリー | |
|---|---|---|
| 5分/50%の充電と15分/80%の充電が可能 | はい。 | はい。 |
| 温度上昇 | 受け入れ可能 | 受け入れ可能 |
| 熱源 | オーミック(最大40%の充電が可能) | 酸素サイクルは、充電の後期にはかなりの熱源となる |
| 充電 | 無抵抗の定電圧2.45V/セル(14.7V/バッテリー)で充電。 | 無抵抗の定電圧2.45V/セル(14.7V/バッテリー)で充電。 |
| 現在 | 250~300A(5~6C3アンペア) | 250~300A(5~6C3アンペア) |
| 最初の3分間は | VRBより1V高い | |
| 現在の低減 | 充電開始3分後に300Aレベルから低下し始める | 充電開始3分後に300Aレベルから低下し始める |
| 温度 | より高いオーム性の加熱で、温度上昇率が非常に高く、4分後には低下し始めた | 電流が減少し始めたのは充電開始4分後で、その後はずっと浸水型よりも高い値を示していた。 |
| VRバッテリーの電流が減少すると、温度上昇の割合が大きくなります。 6分後、温度はまだ上昇しているものの、上昇率は低下し始めました。 温度が緩やかに下がり始めたのは、充電開始から約20分後のことでした。同じ一定の無抵抗電圧でも、VRバッテリーはより大きな電流を受け入れるため、さらに発熱しました。 水の分解だけでは約40%であるのに対し、酸素サイクルに費やしたエネルギーは完全に(100%)熱に変換されます。 |
図17. 充電中。Vref=2.45V/セル、電流I=3OO A max、DOD=80%。 [21.T.G.Chang, E.M.Valeriote and D.M.Jochim, J. Power Sources 48 (1994) 163-175.].
浸水型バッテリーとVRLAバッテリーの急速充電の比較。

表7. MinitCharger®によるバッテリー駆動時間
[22. K.Tomantschger、E.V.Valeriote、J.S.Klarchuk、T.G.Chang、M.J.Dewar、V. Ferrone, and D.M. Jochim, Proc. 13
th
Annual Battery Conference on Applicationand Advances, January 13-16, 1998, Long Beach, CA, 173-178.].
| バッテリータイプ | バッテリーサイクル寿命 | ||
|---|---|---|---|
| 従来のバッテリーチャージャー | MinitCharger®(ミニット・チャージャー | ソース | |
| ニッケル・カドミウム電池、タイプA | 500 | 1400 | INCO(1989) |
| ニッカド電池、タイプB | 450 | 1900 | INCO(1996) |
| Ni-MHセル、タイプA | 400 | 1600 | INCO (1996年) |
| Ni-MHセル、タイプB | 1500 | 4000以上 | INCO (1996年) |
| 鉛蓄電池 トラクションバッテリー VRLAタイプ | 250 | 1500 | COMINCO (1997年) |
ChangとJochimも同様の結果を得ています。 彼らは12VのVRLAバッテリー(螺旋状に巻かれたタイプ)を、通常充電と急速充電のサイクル試験にかけた[21]。 T.G. Chang, E.M. Valeriote and D.M. Jochim, J. Power Sources48 (1994) 163-175.23.Chang, T.G., Jochim, D.M., J. Power Sources, 91 (2000) 177-192].サイクル寿命は、通常の充電レジームでは250サイクル、急速充電レジームでは1000サイクルであった。
非常に高速な充電は、大きな成功を収め、より高いライフをもたらしました。 ある調査によると、コミンコ・リサーチ・チーム [ 22. K.Tomantschger, E.V. Valeriote, J.S. Klarchuk, T.G. Chang, M.J. Dewar, V. Ferrone, and D.M. Jochim, Proc. 13th Annual Battery Conference on Application and Advances, January 13-16, 1998, Long Beach, CA, 173-178]で調査を行ったところ、市販されている30種類の鉛蓄電池は、5分で50%、15分で80%、30分で100%に充電できることがわかったという。 この点では、VRLABの性能は、浸水したSLI電池よりも優れています。
従来の帯電した正極活物質は、粒子が大きく、大きな孔が多数あるのが特徴でした。 急速充電されたプレートでは、大きな粒子、ポア、ボイドは観察されなかった。 従来の充電プレートは PAM の表面積が 2m2/g であったが,大電流で充電したプレートは 900 サイクル後でも 3m2/g の表面積値を示した[22 .K. Tomantschger, E.V. Valeriote, J.S. Klarchuk, T.G. Chang, M.J. Dewar, V. Ferrone, and D.M. Jochim, Proc. 13th Annual Battery Conference on Application and Advances, January 13-16, 1998, Long Beach, CA, 173-178] となっている。
後者の場合、PAMはゆっくりとしか膨張せず、その結果、セパレーターやネガティブプレートにかかる圧力が少なくなり、セパレーターの「ソークスルー」ショートやNAMの高密度化のリスクを低減することができました。 急速充電の劇的な効果は、12V/50Ahの渦巻き型VR LABをライフサイクルテストにかけた場合(10時間と15分の充電体制でテストした場合)、通常の充電では250サイクル(初期容量の80%まで)しか得られなかったのに対し、急速充電体制では約4倍のサイクル数を得ることができました。
従来型および高速充電プレートのPAMおよびNAMのSEM写真

同様の結果はP.T.Moseleyの作品でも得られている[Journal of Power Sources 73 _1998. 122-126] ALABC-CSIRO Project No. AMC-009)を使用しています。 VRLA電池を高率で充電すると、正極活物質は針状の癖を持つ高表面積の形態で復元し、低率で充電すると正極活物質はより大きな粒子を形成する。

バッテリーチャージャー図



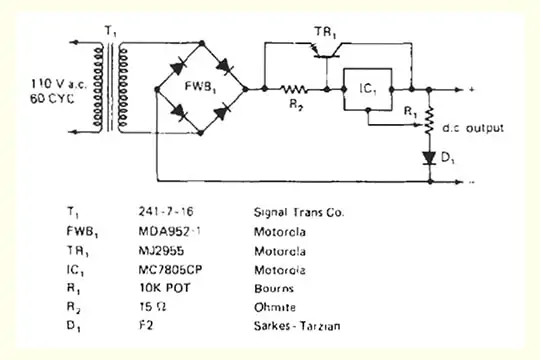


充電器はどれくらいの時間バッテリーに置いておけるのでしょうか?
これには2つの要素があります。
- 充電器が生きているかどうか?
- 充電器に断続的なリフレッシュ充電を行う規定があるかどうか?
充電器のスイッチが切れていても、充電器につながるAC線の接続ミスなど、充電の一部に不具合がなければ、バッテリーを充電器に接続したままにしておいても、おそらく支障はありません。
ただし、充電器のスイッチが入っている場合は、過充電による悪影響でバッテリーの寿命が短くならないように、バッテリーを切り離すことが望ましい。
また、充電器に断続的にリフレッシュ充電を行う機能がある場合は、充電器に接続したままで使用することができます。 これにより、バッテリーを満充電の状態に保つことができ、バッテリーが必要なときにいつでも使用することができます。
カーバッテリーチャージャーの仕組みは?
自動車の電気系統は、以下の部品で構成されています。
始動・照明・点火システム(SLIシステム)には、機械的および電気的な部品・機器があり、それらが一体となってエンジンを始動させ、車両を正常に作動させます。
主なコンポーネントは以下の通りです。
- イグニッションスイッチ
- 12Vまたは24Vのバッテリー。
- 高トルクDCスターターモーター(またはクランキングモーター)と関連部品
- オルタネーター・レクチファイヤー配列
- 電圧調整器またはレギュレーター(カットアウトおよびカットインリレー)
ドライバーがイグニッションスイッチをオンにすると、バッテリーから制御回路を介してスターターモーターに大電流が流れ、スターターモーターが車輪を回転させることで、クルマが動き出します。
スターターモーターの目的は、エンジンがある程度の速度を得て働くことができるようにすることです。 そのため、スターターは、エンジンが車を走らせるために必要な速度を得るのに役立ちます。 それが終わると、スターターはもう役に立たないので、オフになります。
自動充電器には、充電中の電池の電圧を感知する電圧センサー回路が組み込まれています。 バッテリーの電圧が必要な最適レベルに達すると、充電器は自動的にオフになります。
電流は1本のケーブルに沿って、バッテリーのプラス端子から電力を供給される部品へと流れ、さらに車の金属製のボディ(バッテリーのマイナス端子は車のボディに接続されているので、大地となっている)を介してバッテリーに戻る。 ボディは、バッテリーのアース端子(マイナス端子)と太いケーブルでつながっています。
バッテリーからスターターモーターに供給される電流は、バッテリーの容量の3〜4倍、150〜400アンペア)。 つまり、バッテリーからスターターモーターに3C〜4Cアンペアの電流が供給されているのです。 そのため、この電流を流すケーブルは、電圧降下が最小限になるように十分に設計する必要があります。 自動車の点火システムの主な機能は、空気と燃料の混合物を燃焼させるための火花を容易に生成できるように十分な電圧を生成することと、火花のタイミングを制御して適性シリンダーに伝達することの2つです。 一般的な自動車の点火システムでは、12ボルトの電源から20000ボルトから50000ボルトの電圧が発生します。
バッテリーのサイズは車の容量によって異なります。 したがって、Maruti 800やAltoのような小型車には12V/33Ahのバッテリーが使われ、TataやBenzのトラックには12Vまたは24V/180Ahのバッテリーが使われます。
自動車の充電システムでは、エンジン稼働時に13.5〜14.4ボルトの電圧が発生しています。 自動車のライト、ミュージックシステム、ヒーター、エンジンの電気系統を動かすための電流を作り出します。 その昔、自動車には直流発電機が使われていました。 60年代初頭には、オルタネーター・レクティファイヤー方式が直流発電機よりも優れていたため、オルタネーター・レクティファイヤー方式に取って代わりました。 しかし、電気・電子技術の進歩により、すべての自動車にはオルタネーター・整流器の配置が採用されている(交流を発生させて直流に変換する)。
スパークイグニッションエンジンでは、圧縮された空気と燃料の混合物を圧縮行程の終わりに点火するための装置が必要です。 この条件を満たすのがイグニッションシステムです。 必要な電圧の電流をスパークプラグに流し、適切なタイミングで火花を発生させる電気系統の一部です。 バッテリー、スイッチ、ディストリビューター、イグニッションコイル、スパークプラグ、そして必要な配線で構成されています。
圧縮着火エンジン(ディーゼルエンジン)では、圧縮行程の終わりに高温の圧縮空気中にディーゼルを噴射すると、混合気の自己着火が起こるため、点火装置を必要としない。
バッテリーの消耗を防ぐために、メーカーはボルテージレギュレーター/カットアウトを採用しています。 ジェネレーターとバッテリーの接続/切断を行います。
発電機の出力がバッテリーの電圧より低くなると、バッテリーから発電機を切り離します。 一方、出力が大きくなると、発電機をバッテリーに戻して接続します。 そのため、エンジンの低速回転時にバッテリーが放電するのを防ぐことができます。 バッテリー端子電圧が約14.0〜14.4Vになると、カットアウトリレーがバッテリーを充電回路から切り離します。
バッテリーチャージャーを装着したまま車を始動できますか?
既存のバッテリーで始動できない場合は、充電器のリード線を同種のバッテリーの端子に見立てて取り付けることで、充電器から適切な直流電圧を供給することができます。 これはちょうど、ジャンプスタートによる車の始動と同じです。 この作業を行う前に、適切な予防措置を取る必要があります。 専門家の助けを求めなければなりません。
用途に応じた最適な充電器とは?
インバーターバッテリーチャージャー
インバーターは、電池からの直流を家庭や小規模な事業所で必要とされる交流に変換する電気・電子機器です。 整流器はその逆の働きをする。 それは、整流器がACをDCに変換することです。 直流は、バッテリーの充電や一部の機器の動作に必要な電流のことです。
家庭用インバータには、各家庭の電力需要に応じて、通常1個または2個の12Vバッテリーが搭載されています。
UPS(Uninterrupted Power Supply)も同様の装置ですが、主電源の停電からUPSによる再開までのタイムラグが即時(ゼロタイムディレイ)であるのに対し、インバータでは10〜20ミリ秒のタイムラグがあります。 一部の生産部門や銀行では、このような遅延が発生すると、顧客や銀行員に莫大な損失や恥をかかせることになります。 例えば、家庭用のデスクトップパソコンでは、インバータに接続すると画面がブラックアウトしてしまいますが、UPSの場合は停電を感じることはありません。
よく知られているように、12V電池あたり14.4V以上の電圧で充電すると、電池から不快な悪臭や卵の腐ったような臭いがしたり、端子やコネクタの周りに腐食生成物が発生したりして、ユーザーに不快感を与えてしまう。充電電圧が下がることで、電気分解による水の損失が減り、2回の水補給の間隔が長くなります。また、フィルター付きの全波整流も良いアクセントになっています。
車載用バッテリーチャージャー
車載用SLIバッテリーの充電は、自動車の電気系統で行います。 修正充電定電位充電で述べたように、初期のサージ電流を許容範囲内に抑えるために、システムには直列に抵抗が含まれています。 最大充電電圧は、12Vバッテリーの場合、14.0~14.4Vです。 シャローサイクルバッテリーであるSLIバッテリーは、電圧が所定のレベルまで下がるたびに充電されます。
充電のために、バッテリーはダイオードと呼ばれる電子デバイスを介してオルタネーターのステーターに接続されています。このダイオードは、オルタネーターがアイドリング状態の時に、ステーターからバッテリーへの一方向の電流のみを流し、逆方向の電流を流さないようにします。
そのため、バッテリーパックの不要な放電を防ぐことができます。
カットアウトリレーは、オルタネーターが電流を生成していないときに、充電システムとバッテリーの間のサーキットブレーカーとして機能します。 ジェネレーターが作動していない場合や、非常に低い速度で作動している場合に、バッテリーの放電を防ぎます。
初期のバッテリーでは、定期的に水を加えることがメンテナンスの条件となっています。 しかし、進化した電池はガス濃度が低く、水の添加はほとんどないか、12〜18ヶ月に1回程度です。
据え置き型のバッテリーチャージャー
定置型バッテリーは、ほんの数秒の停電も許されないような設備において、非常用電源として使用されています。 非常に短い時間だけ電力を供給する大規模な電池設備は、定置用電源、待機用電源、非常用電源と呼ばれる。 これらの製品は、ユーティリティー、スイッチギア、およびその他の産業環境で使用されます。 このようなバッテリーは、発電機を起動して機能を引き継ぐまでの最初の期間、電力を供給するために使用されます。
この用途には、数種類の鉛蓄電池(平板型、プランテ型、円錐型など)やニッケル・カドミウム(Ni-Cd)電池がありますが、ほとんどのユーザーは、この用途では、浸水型の筒型定置電池、特にOPzS型を好んで使用しています。
据え置き型バッテリーバンクの最大の特徴は、通常の主電源が停止した場合に、即座にバッテリー電源を供給できることです。 そのため、バッテリーは常にフル充電の状態にしておく必要があります。 そのため、充電システムが重要になってきます。 その信頼性は非常に重要です。
これらのバッテリーは定電位モードでフロート充電されます。 電圧は24V、48V、72V、120V、130Vのグループがあり、容量は40Ahから数千アンペア時間のものまであります。
DC6~50アンペア。 DC高電圧、DC低電圧、正負の地絡、放電終了のアラームを内蔵しています。 産業用バッテリーチャージャーは、デジタルコントロールとLCDディスプレイを備えています。 すべてのフィールド端子のワイヤー保護、AC入力とDC出力の完全保護など、多くの安全機能を備えています。
バッテリーチャージャーを購入するための簡単なガイドライン
バッテリーチャージャーを選ぶ際の目安は以下の通りです。
- 充電するバッテリーの電圧を知る。 鉛蓄電池の場合、各セルが正常に充電されるためには、3ボルトが必要です。 したがって、12Vのバッテリーの場合は、端子に20VのDC出力がある充電器を購入します。
- アンペアの詳細(電流)については、バッテリーのラベルからバッテリーの容量を確認します。 10時間のレートで100Ahの容量であれば、10%の電流出力で十分です。 そのため、10Aの充電器を推奨しています。 しかし、15Aの充電器にすることもできますが、その場合はコストが高くなります。 少ない時間で充電できるというメリットがあります。 初期の段階では、より大きな電流をバッテリーに吸収させることができます。 そのため、最初の50%の入力に対しては15Aで充電し、その後は通常の10 %. まで電流を下げることができます。
- 充電器には、デジタルまたはアナログの電圧計と電流計が装備されています。 追加の設備としては、デジタルAhメーターがあります。 また、逆極性の保護機能を付加することもできます。 これにより、バッテリーと充電器の両方が保護されます。
- 電池を長持ちさせるには、フィルター付きの全波整流器がよい。 このような充電器はACリップルの発生が少ないため、充電中の正極板の腐食や電解液の温度上昇が少なくて済みます。
- 要約すると、12V/100Ahのバッテリーには、デジタルメーターと全波整流と逆極性保護機能を持つフィルターを備えた定格20V/10Aの充電器が良い買い物だと思います。
電車用バッテリーチャージャー
[参考文献SG TL &ACコーチの25kW/4.5kW電子整流器兼レギュレータユニット(ERRU)に関するハンドブック、)2019年9月。 “General Services:Train Lighting”, by Institution of Railway Electrical Engineers (IREE), Government of India, Ministry of Railways, Sept 2010.].
どこに行っても電気は必要だし、鉄道の客車でもライトやファンの操作は例外ではない。 エアコン付きのバスでは、車内に設置されたエアコンユニットを動かすために、かなりの電力が必要になります。
従来の発電方法の一つとして、鉄道車両の車軸で駆動するオルタネーターと、十分なアンペア数のバッテリーを並列に接続し、低電圧時に車両に電力を供給する方法があります。 このようなタイプのコーチを「SG(Self-Generating)コーチ」と呼びます。
このSGコーチでは、オルタネーターの交流出力を直流に変換し、オルタネーターの界磁電流を調整することで発生する直流電圧を調整・制御するために、まず磁気増幅器制御の整流器兼レギュレータユニット(RRU)が使用されます。 また、非発電時にバッテリーからオルタネーターへの電流の逆流を防ぐことができます。
この整流・調整された直流電力は、コーチ内の様々な電気機器やアクセサリーを作動させたり、バッテリーを充電するために使用されます。
容量110V/120Ah10の鉛酸電池は、3セルのモノブロックユニットから下架箱に入れてブロードゲージ(B.G.)の客車に配置されています。 B.G.客車用に4個、M.G.客車用に1個の非常用給電端子ボックスが両端の壁に設置されており、発電ができなくなった場合に、隣の客車と相互に接続して給電を受けることができるようになっています。
アンダーフレームの両サイドには、外部からバッテリーを充電するための緊急用端子ボックスが1つずつ設置されています。 (例えば、鉄道ジャンクションのホームで列車が休止している場合など)。 BGのACコーチには、18kW/25kWのブラシレスオルタネーターが採用されています。 このようなオルタネーターは、AC-2 Tier /AC-3 Tier / Chair Carsでは2台使用され、First AC coachでは1台のみ使用されています。 B.G.CoachesのI AC/AC-2 Tier/AC-3 Tier/chair carには、容量800Ah/1100Ahのバッテリーが10時間定格で搭載されています。
インド初の列車は、1883年4月16日に400人を乗せてボリブンダー(現在のムンバイCST)からタネまでの34kmを走行したが、M/S.D.A.が先駆的に開発した車軸駆動のダイナモによる列車照明システム(TL)があった。 J.ストーン社がインド鉄道に参入したのは1930年のことである。 ダイナモ/ブラシレスオルタネーターは、車軸からフラットベルト/Vベルトを介して駆動され、列車の走行時に負荷を供給し、バッテリーを充電します。 ホームなどで停車しているときは、電池で負荷をかけています。
現在、電車の照明には次のようなシステムが使われています。
1) 110VのDC電源で動作するアクスルドライブシステム。
2)415V、3相発電のAC110V利用のミッドオン発電。
3) 3相415Vの発電とAC110Vの利用によるエンドオン発電
4) 三相750Vの発電とAC110Vの利用によるエンドオン発電
今作られているコーチはすべて110Vシステムのみです。 24Vシステムで運用されていたコーチは、すでに110Vシステムに変更されています。
オルタネーターの異なる定格に対するERRUのDC出力端子の標準定格を以下に示す。
(i) 25kW, 130V, 193A
(ii) 4.5kW 128.5V 35A
ERRUはコーチのアンダーフレームに搭載されており、気温-5度から55度、相対湿度98%の環境下で十分に動作するように設計されています。 また、粉塵の多い場所での作業、サービスの振動やシャントの衝撃にも耐えられるように設計されています。
動力伝達にはVベルトを使用しています。 ACとTLのオルタネーターには、C-122サイズがそれぞれ12台(片側6台)と4台(片側のみ)搭載されています。(C-122サイズのACオルタネーターとTLオルタネーターがそれぞれ12台(片側6台)と4台(片側のみ)設置されています。 オルタネーターの回転数は、0~2500RPMの範囲で変化します。 新車時の車輪の直径は915mm、摩耗しきった状態では813mmであり、オルタネーターのカットイン速度およびフル出力のための最小速度(MFO)に対応する列車の速度をkm/hで計算する際には、新品時の車輪の直径を考慮しなければならない。
ERRU(Electronic Rectifier cum regulator unit)の出力特性(25kW、4.5kWとも)を以下に示します。
無負荷時のDC出力電圧は最大135Vで、これは次のように設定できます。 128±0.5V、97A(1100および650Ahのバッテリー用)および 128±0.5、120Ah バッテリーで19A )を1500rpm(最低速度と最高速度の中間)で使用した場合、電圧調整は±2 %, 効率は95%(最低)。 電圧リップルは2 %.以内に抑えられています。 負荷変動は,400rpm~2500rpm(1100Ahと650Ahのバッテリーの場合),350rpm~2500rpm(120Ahのバッテリーの場合)の速度で10A~193Aとなっている。
高容量バッテリーの場合、15%過負荷時の電圧は120V(最小)、222A、電流は230A(最大)に制限されます。 120Ahのバッテリーの場合、40Aの過負荷時の電圧は115V(最小)に設定されています。
バッテリー充電電流の制限は、1100Ahのバッテリーで220A、650Ahのバッテリーで130A、120Ahのバッテリーで24A(最大)となります。 最後の2つのパラメータは、ユニバーサル・ボルテージ・コントローラ(UVC)およびコーチ・インディケーション・パネル(CIP)から設定できます。
4.5kWのEERUの場合、負荷変動は350RPMから2500RPMで1Aから37.5Aとなります。 40Aの過負荷時の電圧は115V(最小)、電流は43A(最大)に制限されています。
充電電流は1100/220=5、650/130=5、120/24=5であることがわかります。 つまり、これらのバッテリーの充電電流はC/5アンペアに制限され、最大電圧は128V(バッテリーバンクのOCVより16%高い)となります。
The Overall Coachのブロック図の詳細については、以下の図のような配線になります。また、Alternator-ERRU Systemのブロック図については、以下のリンクを参照してください。
トラクションバッテリーチャージャー
フォークリフト用バッテリーの性能と寿命は、トラクション・バッテリーチャージャーとその充電方法によって左右されます。 フォークリフト用バッテリーチャージャーは、バッテリーの電圧やAhに合わせて選択する必要があります。
フォークリフト用充電器
-
- 充電中の温度上昇を抑えるべき
- 無理な過充電をせず、適切なタイミングで充電器がバッテリーへの電流供給を停止すること
- 均等充電機能(例:より高い電流での充電)を持つこと。
- 危険な状況下では、オートシャットオフ機能を備えていること。
- マイクロプロセッサーやPCでプログラム可能であること。
- 一部の充電器では、セル内の細いエアパイプによる空気の撹拌も行われています。
充電電圧の範囲は24Vから96Vです。
電流はバッテリーの容量によって異なり、250Ahから4000Ahまであります。
トラクションバッテリーの充電方法
シングルステップのテーパー充電。充電器は約16A/100Ahで動作を開始し、セル電圧の上昇とともに電流が細くなっていきます。 セル電圧が2.4V/セルになると、電流は8A/100Ahまで細くなり、その後は3〜4A/100Ahの仕上げになります。 充電はタイマーでオフになります。 80%放電した電池を空気撹拌せずに使用した場合、約11~13時間(Ah入力係数1.20)かかることがあります。
充電時間の違いは起動電流の変動によるもので、起動電流が16A/100Ahであれば持続時間は短く、12A/100Ahであれば持続時間は長くなるということです。 空気撹拌装置を使うと、所要時間は9〜11時間に短縮されます(AH入力係数1.10)。
2段階のテーパー充電(CC-CV-CCモード)を採用。従来の方法よりも改善されています。 充電器は、32A / 100Ahの高い電流でスタートします。 セル電圧がセルあたり2.4Vになると、充電器は自動的にテーパーモードに切り替わり、電流はセルあたり2.6Vになるまで漸減し続け、電流は3~4A/100Ahの仕上げ速度になり、3~4時間続きます。 80%放電した電池を空気撹拌せずに使用した場合、約8~9時間(Ah入力係数1.20)かかることがあります。 空気撹拌装置を使えば、7〜8時間に短縮されます(AH入力係数1.10)。
Gelled VRLAバッテリーの充電。(CC-CV-CCモード):
充電器は15A/100Ahの電流でスタートします。 セル電圧が1セルあたり2.35Vになると、充電器は自動的にテーパーモードに切り替わり、同じ電圧でCVモードになります。 これには最大で12時間かかります。 CVステップは、充電電流が1.4A/100Ahの制限値まで低下する限り一定に保たれます。 第2段階は数時間、最大で4時間ほど続きます。 この期間は、第1フェーズの期間に依存します。
高周波フォークリフト用バッテリーチャージャー
既存の充電器には、一般的にフェロ-レゾナント方式とSCR(Silicon Controlled Rectifier)方式の2種類があります。 手頃な価格で購入できますが、その分、効率も悪くなります。
MOSFET(Metal Oxide Semiconductor Field-Effect Transistor)やIGBT(Isolated Gate Bipolar Transistor)などの高周波スイッチングパワーデバイスを搭載したバッテリーチャージャーは、回線よりもはるかに高い周波数(数kHz~数百kHz)で動作します。 一方、フルオン/フルオフが可能なMOSFETやIGBTは、充電器の出力を任意のタイミングで正確に制御することができます。 SCRは、ターンオフが制御できない半制御のデバイスです。
HF充電器はスイッチング電源として機能します。つまり、高周波(50〜170kHz)で電子スイッチをオン・オフするのです。
このHF技術の利点は以下の通りです。
| 高周波バッテリーチャージャー | |
|---|---|
| 最大170kHz 高周波数 | 転換による損失が少ない |
| 充電効率の向上(87~95%) | 省エネルギーによるエネルギーコストの低減(最大20%)。 |
| ACリップル電流の低減 | 温度上昇が少ないため、寿命が長い。 水の損失が少ないことによるメンテナンスコストの低減 |
| 普遍的な適応性がある | フラッド型、AGM型、ゲル型のいずれのバッテリーも過不足なく充電することができます。 |
| 小型化、軽量化、省スペース化を実現 | 足元のスペースが狭く、船上に簡単に搭載できる |
| このような充電器は、充電電流が40〜300Aの24V〜80Vバッテリー用の充電器まで様々な種類があります。 | |
地下鉱山のバッテリーアプリケーション用のバッテリーチャージャー
地下鉱山用のバッテリーは、主にディープサイクルの鉛蓄電池です。 代表的な電圧は48~440V、容量は700Ah~1550Ahです。
このバッテリーの充電は、トラクション・バッテリーの充電と同様です。 で充電されています。
最初は2.6V、電流は21A、100Ahあたり17A、最終的には100Ahあたり4.5Aの割合で仕上げます。 充電は6~8時間で完了します。
IS 5154:2013 Part 1 (IEC 60254-2006)に準拠したバッテリーです。
マリンバッテリーチャージャー
マリン用のバッテリーは、2つのタイプに分類されます。 スターターバッテリーは板厚が薄く、短時間で大容量の電力を供給することができます。 もう一つのタイプは、電子アクセサリー、トローリングモーター、船上の電気・電子機器など、その他のマリンアプリケーションに使用されるディープサイクルバッテリーです。 また、デュアルファンクションバッテリーは、SLIバッテリーとディープサイクルバッテリーの両方の機能を備えています。 特定のバッテリーには特定の充電器を使用します。 CC-CVモードはVR鉛蓄電池で使用してください。
また、最大4個のバッテリーを同時に充電できる充電器もあります。 あらゆる種類のマリンバッテリー、VRバッテリー(AGM、ゲル式)、メンテナンス性の高い水陸両用バッテリーの充電が可能です。
バッテリーと充電器はボートで使用されるため、乾燥した状態を保ち、十分な換気を行う必要があります。 また、防水性、耐衝撃性、耐振動性を備え、必要に応じて完全に密閉されていなければなりません。 さらに、充電器に逆極性保護機能やスパーク防止機能があるかどうかも確認する必要があります。
ソーラー用バッテリーチャージャー
日射量の変化により、SPVパネルの出力は変動します。 そのため、SPVパネルとバッテリーの間には、デジタル式のMPPT(Maximum Power Point Tracker)が接続され、安心して充電ができるようになっています。 MPPTは、太陽電池アレイ(PVパネル)とバッテリーバンクのマッチングを最適化するために設計された電子的なDC-DCコンバータです。 ソーラーパネルからのDC出力を感知し、高周波のACに変更し、バッテリーの電力要求に正確に一致するように異なるDC電圧と電流にステップダウンします。 MPPTを搭載することのメリットを以下に説明します。
ほとんどのPVパネルは、SPVパネルの公称電圧定格が12Vであっても、16~18Vの出力を想定して作られています。しかし、公称12Vのバッテリーは、充電状態(SOC)に応じて、実際の電圧範囲が11.5~12.5V(OCV)になることがあります。 充電時には、バッテリーに余分な電圧成分を供給する必要があります。 通常のチャージコントローラーでは、SPVパネルで作られた余分な電力は熱として放散されますが、MPPTはバッテリーの要求を感知し、SPVパネルで作られた電力が大きければ、より大きな電力を与えます。 このように、MPPTを使用することで、無駄な充電、過小充電、過大充電を防ぐことができます。
温度はSPVパネルの性能に影響を与えます。 温度が上昇するとSPVパネルの効率は低下します。 (注:SPVパネルが高温にさらされると,SPVパネルから発生する電流は増加し,電圧は減少します。電流の増加よりも電圧の減少の方が早いため、SPVパネルの効率は低下します。) 逆に温度が低くなると、効率が上がります。 標準試験条件(STC)の温度である25℃より低い温度では、効率が上がります。 しかし、長い目で見れば、効率はバランスするでしょう。




