Caricabatterie - caricare una batteria al piombo
Una batteria può essere definita come un dispositivo elettrochimico che può convertire l’energia chimica all’interno dei suoi materiali attivi in energia elettrica. Se la reazione che porta a tale conversione di una forma di energia nell’altra è reversibile, allora abbiamo una cella ricaricabile o secondaria o di accumulazione. Tali celle possono essere ricaricate ripetutamente dopo ogni scarica per invertire la direzione della reazione. Affinché una batteria fornisca la durata prevista, deve ricevere una carica adeguata ogni volta che è necessario.
Le cellule con reazioni irreversibili sono chiamate cellule primarie.
Una batteria al piombo-acido è composta da elettrodi positivi e negativi separati da pellicole isolanti chiamate separatori. Come elettrolita si usa una soluzione diluita di acido solforico. Il materiale attivo positivo è il biossido di piombo (PbO2) e il materiale attivo negativo è il piombo.
Prima di addentrarci nei dettagli di Battery Charger, è necessario capire brevemente alcune questioni relative alla batteria.
L’ampere è l’unità di misura della corrente (che è definita come un flusso continuo di elettroni). Quando un coulomb (o un ampere-secondo) passa davanti a un punto in un secondo, la corrente è definita come 1 ampere.
Latensione può essere presa come la forza che spinge gli elettroni a fluire in un conduttore elettronico e l’unità è il volt. Quando 1 ampere-secondo ha 1 joule di energia, diciamo che ha 1 volt di differenza di potenziale elettrico.
Questi due termini possono essere paragonati al serbatoio d’acqua sopraelevato di un edificio. Maggiore è l’altezza del serbatoio dell’acqua, maggiore sarà la forza con cui l’acqua scorrerà. Allo stesso modo, più il diametro del tubo che porta l’acqua dal serbatoio ai punti d’utenza, più alto sarà il volume d’acqua che l’utente riceve. L’acqua che scorre nel tubo può essere paragonata alla velocità di scorrimento dell’acqua.
L’ampere ora (Ah) è la quantità di elettricità, ed è un prodotto della corrente e del tempo.
1 Ah = 1 A *1 ora.
Iwatt (W) sono la potenza, ed è un prodotto della corrente e dei volt. Le unità superiori sono i kW (= 1000 W).
mega watt, MW (=1000 kW) e Giga watt, GW (un miliardo di W (1.000.000.000.000 Watt).1 W = 1 A * 1 V= VA.
L’energia (Wh) è la quantità di potenza fornita nell’unità di tempo. Le unità superiori sono i kWh (= 1000 Wh)
megawatt-ora, MWh (= 1000 kWh) e Giga Watt-ora, GWh (=(un miliardo di Wh (1.000.000.000.000 Watt-ora).
Le unità GW sono usate per riferirsi alla produzione di grandi centrali elettriche. GWh è usato per riferirsi alla capacità di produzione delle grandi industrie di batterie per veicoli elettrici (EV) e dei sistemi di stoccaggio delle batterie di grande capacità Wh = 1 W* 1 h = 1 Wh
Nel linguaggio delle batterie, si può dire che una batteria possiede 1200 Wh (o 1,2 kWh) se la sua tensione è 12 e la sua capacità in Ah è 100.
12 V * 100 Ah = 1200 Wh o 1,2 kWh.
La potenza fornita per unità di massa di una batteria è chiamata potenza specifica e l’unità è W per kg.
Potenzaspecifica= W/kg e kW/kg.
Allo stesso modo, l’energia fornita per unità di massa di una batteria è chiamata energia specifica e l’unità è Wh per kg.
Energia specifica = Wh / kg e kWh / kg. (Scritto anche come Wh kg-1)
Allo stesso modo, la potenza fornita per unità di volume di una batteria è chiamata densità di potenza e l’unità è W per litro.
Densità di potenza = W / litro e kW / litro.
L’energia fornita per unità di volume di una batteria è chiamata densità di energia e l’unità è Wh per litro.
1 W = 1 J al secondo
Densità di energia = Wh / litro e kWh / litro. (Scritto anche come W L-1 o W l-1)
La reazione di scarica-carica di una cella al piombo-acido è
Pb (NP) + PbO2 (PP) + 2H2SO4 Scarica ⇔ Carica PbSO4 (PP) + PbSO4 (NP) + 2H2O (vicino a PP)
Nota: NP = piastra negativa= anodo durante la scarica=donatore di elettroni durante la scarica. PP = piastra positiva = catodo durante la scarica = accettore di elettroni durante la scarica
I ruoli degli elettrodi saranno invertiti durante una carica; l’anodo si comporterà come catodo e viceversa. L’accettore di elettroni ora rilascerà elettroni e il donatore li riceverà.
Il termine energia libera termodinamica è una misura del lavoro che può essere estratto da un sistema. Nel caso della cella galvanica, il lavoro elettrico è fatto attraverso il movimento di particelle cariche dovuto all’interazione chimica tra i reagenti per produrre i risultati (prodotti).
Quindi, l’energia è data in termini di Δ G la variazione dell’energia libera di Gibb, che rappresenta la quantità massima di energia chimica che può essere estratta dai processi di conversione energetica.
Se E è l’emf (forza elettromotrice o tensione o potenziale) della cella e il processo che sta avvenendo (cioè, una scarica di una cella al piombo-acido), è associato a un passaggio di n Oggi ( F ) per mole di reagenti da un elettrodo all’altro, allora il lavoro elettrico fatto dalla cella è dato come nFE . L’aumento corrispondente dell’energia libera è uguale al lavoro elettrico fatto sul sistema. Quindi,
ΔG = nFE o
ΔG = -nFE o
-ΔG° = nFE°
(in condizioni standard; E° si riferisce al potenziale standard dell’elettrodo o alla tensione standard della cella).
Equazione di Gibbs
(Cosa si intende per condizioni standard? 25°C o Celsius (298,1°K o Kelvin), 1 bar di pressione, e l’attività (che può essere approssimativamente presa come valore di concentrazione) della specie reagente, Pb2+, è una).
Questa equazione è chiamata Equazione di Gibbs.
L’equazione di Gibbs collega la tensione della cella al cambiamento dell’energia libera (DG). Se la reazione avviene spontaneamente (per esempio la scarica di una cella al piombo), ΔG è negativo (si libera energia) ed emf è positivo, cioè una carica di nF fluirà spontaneamente nella direzione assunta nella reazione della cella.
D’altra parte, se ΔG è positivo, permette al sistema di realizzare il fenomeno dell’elettrolisi (cioè, durante una carica della cella al piombo-acido).
EMF di una cella
L’emf della cella è un proprietà termodinamica intensiva cioè indipendente sia dalla massa dei reagenti che dalle dimensioni della cella. La proprietà intensiva (al contrario della proprietà estensiva ) non dipende dalla massa dei reagenti e quindi dalle dimensioni della batteria. Sia che abbiate pochi milligrammi o pochi chilogrammi di materiale, il sistema mostrerà la stessa tensione e non può essere aumentata aumentando la massa del materiale. Il potenziale individuale dell’elettrodo è una proprietà elettrochimica inerente al materiale dell’elettrodo, e non si può cambiare il suo valore in condizioni simili.
Esempi di proprietà intensive sono la tensione degli elettrodi e delle celle; d’altra parte, la proprietà estensiva dipende dalla quantità di sostanza, per esempio, massa, volume, energia, ampere ora e watt ora. Così, 4,5 grammi di materiale attivo di biossido di piombo in una cella al piombo-acido forniranno un ampere ora (Ah) teoricamente, ma se avete 45 grammi, fornirà dieci volte gli Ah. Quindi, è una proprietà estensiva; ma in entrambi i casi il potenziale dell’elettrodo sarà lo stesso, cioè 1,69 V. Argomenti simili possono essere presentati per i materiali attivi di piombo e acido solforico.
Il potenziale cellulare standard (E°) è legato al cambiamento di energia libera standard (DG°) come indicato sopra.
L’emf di una cella al piombo-acido può essere determinata dall’espressione
ΣΔGº ƒ dei prodotti – ΣΔGº ƒ dei reagenti
Dove ΔG°ƒ si riferisce all’energia libera standard di formazione della specie che reagisce.
Energia libera standard di formazione
Tabella 1
Energia libera standard di formazione, ΔG°ƒ delle specie chimiche che partecipano alla reazione cellulare
(Hans Bode, Lead-Acid Batteries, John Wiley, New York, 1977, Appendice IV, p. 366.)
| Reagenti/Prodotti | Valore numerico (k cal mole-1 ) |
|---|---|
| PbO2 | -52.34 |
| Pb | 0 |
| H2SO4 | -177.34 |
| PbSO4 | -193.8 |
| H2O | -56.69 |
La reazione complessiva è scritta come
Pb + PbO2 + 2H2SO4⇄ 2PbSO4 + 2H2O E° = 2,04 V.
ΔG° = ΣΔGº ƒ dei prodotti – ΣΔGº ƒ dei reagenti
Sostituendo i rispettivi valori di (che otteniamo dai libri di testo standard, per esempio, [1. Hans Bode, Lead-Acid Batteries, John Wiley, New York, 1977, Appendice IV, p. 366]
= [2(-193.89) + 2(-56.69)] – [0 – (-52.34) + 2(-177.34)]
= -94,14 kcal mole – 1
= -94,14 kcal mole – 1 × 4,184 kJ mole – 1 (per convertire le kcal in kJ moltiplicare per 4,184)
= -393,88 kJ per mole
E° = -ΔG°/nF
= –(-393.88 × 1000)/2 × 96485
= 2,04 V per una cella al piombo
La tensione standard di una cella al piombo è di 2,04 V
e la reazione complessiva o totale di una cella al piombo-acido si scrive come:
Pb + PbO2 + 2H2SO4 Scarica⇔Carica PbSO4 (PP) + PbSO4 (NP) + 2H2O (vicino a PP)
Prima di entrare nei dettagli della carica e della scarica di una cella al piombo-acido, dovremmo avere qualche conoscenza di alcuni termini usati in elettrochimica.
Conosciamo già il significato delle condizioni standard.
Quando disturbiamo la reazione della cellula (sia nella direzione in avanti che in quella inversa), diciamo che la cellula è in una condizione disturbata e non in condizioni di equilibrio.
Ogni volta che un sistema elettrochimico è disturbato, ci sarà sempre una differenza dal potenziale standard. Così, se una cella al piombo-acido è forzata nella direzione di scarica, la tensione della cella diminuisce di un certo valore, che dipende dalla grandezza della corrente. Più alto è il valore attuale, più sarà la deviazione dal valore standard.
Ora la tensione della cella sarà
EDisch = E° – δV.
Il valore diEDisch sarà inferiore a quello di E°.
Al contrario, se la cella è forzata nella direzione inversa (cioè, modalità di carica), la tensione della cella aumenterà di un certo valore che dipende ancora dalla grandezza della corrente.
ECh = E° + δV.
Il valore di δV è chiamato sovratensione o sovrapotenziale e viene indicato con il simbolo simbolo η .
Il valore di δV sarà negativo per una reazione di scarica e positivo per una reazione di carica.
Questo fenomeno di diminuzione o aumento della tensione della cella è chiamato polarizzazione e si dice che gli elettrodi sono in uno stato polarizzato.
Quindi, riscriviamo le equazioni come segue:
EDisch = E° – η.
ECh = E° + η.
Così si vede che durante una scarica
EDisch < E° e
Durante una carica
ECh > E°.
Quali sono le ragioni di questa deviazione di tensione?
Ci sono alcune cause per questa deviazione:
- Perdita dovuta a resistenze interne (IR) (ηohmic)
- Polarizzazione di attivazione dovuta al trasferimento di carica sui due elettrodi durante l’inizio del processo ηt.
- Polarizzazione di concentrazione dovuta all’esaurimento dell’elettrolita e di altre specie partecipanti (ηc).
Le perdite dovute alla polarizzazione IR possono essere mitigate utilizzando elettrodi collettori di corrente ed elettroliti con migliori conducibilità. Un separatore con una resistenza più bassa aiuterà anche.
La polarizzazione di attivazione è legata al trasferimento di portatori di carica attraverso i confini di fase dell’elettrodo e questo processo è designato come reazione di trasferimento. La sovratensione di trasferimento dovuta alle reazioni di trasferimento di carica sui due elettrodi può essere molto ridotta negli elettrodi di batteria avendo una struttura porosa compatibile. Quest’ultima aumenta la superficie interna effettiva (superficie BET, che include le aree di pori, crepe e fessure) rispetto alla superficie apparente ottenuta dalla moltiplicazione delle dimensioni, lunghezza e larghezza) disponibile per le reazioni.
Densità di corrente
Questo a sua volta riduce la densità di corrente (cioè l’ampere per cm quadrato). Così, una piastra con una porosità aggregata del 40% porterà a perdite più elevate dovute alla polarizzazione di attivazione rispetto a una con il 50% di porosità.
Polarizzazione di concentrazione (ηc) sarà maggiore se i prodotti di reazione (solfato di piombo e molecole di acqua, nel caso di una cella piombo-acido) non vengono trasferiti via dalle superfici degli elettrodi per far posto a nuovi reagenti (ad esempio ioni di piombo da entrambi gli elettrodi e ioni di solfato dall’elettrolita nel caso di una cella piombo-acido). ηc sarà più pronunciato verso la fine di una reazione di scarica. All’interno di una cellula, il trasporto di ioni avviene per diffusione e per migrazione.
La diffusione è causata dalle differenze di concentrazione, mentre la migrazione è causata dalle forze del campo elettrico.
La diffusione può avvenire nella massa dell’elettrolita o nel separatore: poiché gli ioni sono generati in un elettrodo e sono consumati nell’altro elettrodo, gli ioni devono muoversi tra gli elettrodi.
Si verifica anche negli elettrodi porosi mentre la reazione elettrochimica procede. I prodotti di reazione possono muoversi all’interno della massa attiva fino alla loro posizione finale per diffusione.
La quota della corrente totale che è trasportata dalle particolari specie ioniche (particelle cariche) per migrazione è una funzione del loro numero di trasferimento. In un elettrolita binario, dissociato in cationi e anioni, i numeri di trasferimento sono correlati dall’equazione
ɩC + ɩA= 1,
dove ɩC + ɩA indicano il numero di trasporto di cationi e anioni.
I numeri di trasferimento dipendono dalla concentrazione degli ioni e dalla temperatura. Nelle soluzioni binarie di sale sono quasi vicini a 0,5. Così entrambe le specie ioniche condividono ugualmente la conduttività ionica.
Deviazioni significative si verificano in acidi forti e alcali a causa della maggiore mobilità ionica dei protoni (H+) e degli ioni idrossili (OH-). I valori per l’elettrolita della batteria acido solforico (dissociato in H+ e HSO2-4) e idrossido di potassio (dissociato in K+ e OH-) sono riportati di seguito. 4
ιH+ = 0,9; ɩHSO4 2- = 0,1; ιK+ = 0,22; ιOH-= 0,78
Il numero di transfert è una misura di quanto la concentrazione di un particolare ione è influenzata dalla migrazione dovuta al flusso di corrente. Un valore più piccolo è indicativo di una minore influenza sui processi di migrazione e un valore più alto indica una maggiore influenza sul processo di migrazione.
2. D. Berndt, in Battery Technology Handbook, Ed. H.A. Kiehne, seconda edizione, 2003, Marcel Dekker, Inc., New York, tabella 1.2.
3. J S Newman. Sistemi elettrochimici. Englewood Cliffs: Prentice-Hall, 1991, p 255.
4. S U Falk, A J Salkind. Batterie alcaline di stoccaggio. New York: John Wiley & Sons, 1969, p 598
Per renderlo chiaro, dobbiamo capire come procede la reazione di scarico. Non appena i terminali della batteria sono collegati all’apparato di consumo, gli elettroni cominciano a fluire dalla piastra negativa al terminale positivo attraverso il circuito esterno. All’interno della cellula, è compito delle particelle cariche occuparsi del flusso di corrente. Le particelle cariche sono protoni (H+) e ioni bisolfato (HSO¯4 ).
Durante una scarica, gli ioni negativi HSO¯4 (in questo caso, ioni bisolfato dall’acido solforico elettrolitico che si dissocia come H+ e HSO¯4) si muovono verso la piastra negativa. Questi ioni negativi si combinano con il materiale attivo, Pb, producendo solfato di piombo, PbSO4. La reazione produce anche uno ione idrogeno carico positivamente (chiamato protone) che si allontana. I due elettroni rilasciati a seguito della reazione anodica del materiale attivo al piombo, raggiungono il terminale positivo attraverso il circuito esterno.
Reazione di piastra negativa o di mezza cella negativa: Pb + HSO¯4 ⇄ Pb2+ + SO42- +H+ + 2e- E°= -0,35 V
Gli ioni bivalenti di piombo e gli ioni di solfato si combinano immediatamente per formare solfato di piombo e si depositano sulla piastra negativa come solfato di piombo.
Finora abbiamo visto il quadro delle reazioni negative della piastra.
Ora vediamo cosa succede contemporaneamente sulla piastra positiva.
Gli elettroni dalla piastra negativa, dopo aver raggiunto il terminale positivo, reagiscono con il marziale attivo positivo, PbO2, per formare solfato di piombo e due molecole d’acqua.
Reazione di piastra positiva o di mezza cella positiva: PbO2 + 3H+ + HSO¯4 + 2e- ⇄ Pb2+ + SO4 2- + 2H2O E° = 1,69 V
Gli ioni bivalenti di piombo (Pb2+) e gli ioni di solfato ( ) si combinano immediatamente per formare solfato di piombo e si depositano sulla piastra positiva come solfato di piombo.
Meccanismo di dissoluzione-deposizione o dissoluzione-precipitazione
Questo tipo di reazione, in cui il piombo e il biossido di piombo si dissolvono come ioni di piombo e si depositano immediatamente come solfato di piombo sui rispettivi elettrodi avviene attraverso un meccanismo di dissoluzione-deposizione o dissoluzione-precipitazione.
Ora, combinando le due reazioni di semicella, abbiamo
Reazione di piastra negativa o di semicella negativa: Pb + HSO¯4 ⇄ Pb2+ + SO42- +H+ + 2e-
Reazione di piastra positiva o di semicella positiva: PbO2 + 3H+ + HSO¯4 + 2e- ⇄ Pb2+ + SO42- + 2H2O
Complessivamente o la reazione totale: Pb + PbO2 + 2H2SO4 Scarica⇔Carica 2PbSO4 + 2H2O
Questa teoria di reazione fu proposta da Gladstone e Tribe nel 1881, ma la cella al piombo-acido fu inventata nel 1859 da Raymond Gaston Planté, fisico francese.
J.H. Gladstone e A. Tribe, Chimica degli accumulatori Planté e Fauré, Natura , 25 (1881) 221 & 461.
J.H. Gladstone e A. Tribe, Chemistry of the Planté and Fauré Accumulators, Nature, 26 (1882) 251, 342 & 602; 27 (1883) 583
La reazione di scarico procederà fino a quando circa la metà dei materiali attivi sarà convertita in solfato di piombo per un tasso di scarico lento, come i tassi di 20 o 10 ore. A questo punto, la resistività dei materiali attivi sarebbe aumentata a un valore tale che un’ulteriore scarica provocherebbe una caduta molto rapida della tensione della cella. Normalmente, la tensione della cella non può scendere al di sotto di 1,75 V per cella.
Scarichi profondi oltre l’80% di profondità di scarico (DOD) renderanno più difficile la successiva ricarica.
Non appena il piombo si dissolve come ioni di piombo durante la reazione di scarica, si combina con gli ioni di solfato e si deposita sulla piastra negativa. Gli ioni di piombo o la molecola di solfato di piombo non si allontanano molto dalla piastra negativa. Questo perché la solubilità del solfato di piombo in soluzioni diluite di acido solforico è molto bassa. È dell’ordine di oltre 1 mg per litro, la deposizione di ioni di piombo bivalente in solfato di piombo sarà più veloce nei luoghi dove ci sono alte concentrazioni di elettrolita. Man mano che la scarica procede ulteriormente, la solubilità del solfato di piombo nell’elettrolita aumenta fino a 4 mg per litro.
Questo perché l’acido diventa più diluito a causa dell’ulteriore scarico e in acidi così diluiti, la solubilità del solfato di piombo è maggiore, fino a 4 mg per litro.
Il solfato di piombo così depositato continuerà a crescere in cristalli di varie dimensioni sia in superficie che in fessure e crepe. . Il film avrà una struttura discontinua. Durante un processo di scarica lenta, questa forma discontinua della struttura del solfato di piombo aiuta le porzioni interne dei materiali attivi a partecipare alla reazione in quanto fornisce una struttura aperta che facilita l’ingresso degli ioni. Pertanto, il processo di scarico può procedere in profondità all’interno della piastra.
Al contrario, ad alti tassi di scarica, la superficie è bloccata dal prodotto di scarica, PbSO4, che forma una struttura continua senza alcuna rottura. Così, ulteriori reazioni all’interno delle piastre sono ostacolate e questo è il motivo per cui non possiamo ottenere la capacità prevista a tassi di scarica più elevati.
Carica di batterie al piombo-acido
Durante una reazione di carica, si verifica il fenomeno inverso, il flusso di corrente è invertito e l’ossidazione avviene
all’elettrodo positivo e la riduzione all’elettrodo negativo.
Tabella 2
Caratteristiche dei due elettrodi durante la carica e la scarica
| Elettrodo | Scarico di | Carica |
|---|---|---|
| Piastra negativa |
Piombo poroso (spugnoso) Anodo Cede 2 elettroni Pb -2e- → Pb2+ La tensione diminuisce (diventa meno positiva). Convertito in PbSO4 |
~ 40% Pb + ~60% PbSO4 Catodo Assorbe 2 elettroni Pb2+ in PbSO4 prende 2 elettroni La tensione diminuisce (diventa più negativa) Recuperato in Pb metallico H2 evoluto durante il sovraccarico |
| Piastra positiva |
Biossido di piombo poroso Catodo Assorbe 2 elettroni Pb4+ (da PbO2) + 2e- → Pb2+ La tensione diminuisce (diventa meno positiva). Convertito in PbSO4 |
~ 50% PbO2 + ~ 50% PbSO4 Anodo Rilascia 2 elettroni Pb2+ in PbSO4 diventa PbO2 Riconvertito in PbO2 Aumenti di tensione O2 evoluto durante il sovraccarico |
Figura 1
Cambiamento dei valori di potenziale per la cella al piombo durante le reazioni di carica e scarica
La tensione di cella è una combinazione di due valori in qualsiasi fase del funzionamento di una cella galvanica
Così
Tensione della cella = potenziale dell’elettrodo positivo – potenziale dell’elettrodo negativo
Pertanto
Tensione a circuito aperto o tensione di equilibrio della cella al piombo = 1,69 – (-0,35) = 2,04 V
Alla fine o vicino alla fine di una scarica, la tensione della cella, EDisch = 1,50 – (- 0,20) = 1,70 V
Alla fine o vicino alla fine di una carica, la tensione della cella, ECh = 2,05 – (-0,65) = 2,70 V

Caricabatterie - Coefficiente di carica
Le batterie ricaricabili hanno bisogno di essere caricate per recuperare la capacità Ah spesa nella precedente scarica.
La quantità di Ah necessaria per portare la batteria allo stato precedente di piena carica rispetto alla produzione precedente sarà dal 10 al 15 % in più. Questo rapporto tra l’input di carica e l’output precedente è chiamato coefficiente di carica
Coefficiente di carica = Ah di ingresso / Ah di uscita precedente = ~ 1,1 a 1,2.
Cioè, circa il 10-20% di Ah in più dovrebbe essere messo per compensare le reazioni secondarie, che sono costituite dalle reazioni di sovraccarico di scissione dell’acqua e dalle reazioni di corrosione della griglia. Inoltre, una piccola parte sarà persa a causa della resistenza interna.
Caricabatterie - Efficienza di carica della batteria al piombo
Efficienza ampere-ora
(Ampere ora o efficienza coulombica e energia o efficienza watt-ora)
Dalle argomentazioni precedenti, si può vedere che dobbiamo definire ciò che viene definito “efficienza di carica”.
Efficienza ampere-ora
La norma indiana IS 1651 descrive la procedura di prova come segue:
- Una batteria completamente carica deve essere sottoposta a una scarica al ritmo di dieci ore fino a una tensione finale di 1,85 volt per cella.
- Si calcola l’uscita esatta di Ah.
- La batteria è ora ricaricata con lo stesso numero di ampere-ora alla stessa corrente.
- La batteria è ora sottoposta a una seconda scarica come prima.
- L’efficienza Ah (coulombiana) = ηAh = Ah consegnati durante la seconda scarica / Ah immessi.
Efficienza energetica o watt-ora
L’efficienza in watt-ora deve essere calcolata moltiplicando l’efficienza in ampere-ora ottenuta come descritto sopra per il rapporto tra la tensione media di scarica e di ricarica.
Efficienza energetica o wattora = ηWh = ηAh * (tensione media di scarica / tensione media di carica)
L’efficienza ampere-ora (o coulombica) di carica della cella al piombo-acido nel caso di un ingresso pari al 100% della scarica precedente alla stessa velocità è quasi pari al 95% e l’efficienza energetica o watt-ora è circa 85-90%. Gli standard indiani (IS 1651) specificano anche un’efficienza minima di ampere-ora del 90% e un’efficienza minima di watt-ora del 75%.
L’efficienza di carica è limitata dalla piastra positiva piuttosto che da quella negativa. Quando circa tre quarti del solfato di piombo sull’elettrodo positivo è stato riconvertito in biossido di piombo e l’acqua non può diffondersi abbastanza velocemente nella struttura porosa della piastra interna, avvengono reazioni secondarie come l’evoluzione dell’ossigeno. Per un certo periodo di tempo, la corrente di carica è distribuita tra il processo primario di conversione del PbSO4 in PbO2 e le reazioni secondarie di sovraccarico. Se la carica continua per un tempo sufficientemente lungo in modo che quasi tutto il solfato di piombo sia stato convertito in biossido di piombo, tutta la corrente di carica va per le reazioni secondarie.
Tensione di carica di un caricabatterie
Come spiegato in precedenza
ECh > E°.
Quindi, dobbiamo fornire una tensione un po’ più alta per facilitare questa reazione. Normalmente, un buon caricatore sarà progettato con una fonte di tensione sufficientemente alta per la ricarica. È una buona regola empirica che per una cella da 2 V si devono fornire almeno 3 V in modo che la cella possa raggiungere la piena carica raggiungendo una tensione di 2,7 V per cella. Ma dobbiamo prendere in considerazione le perdite nel cavo, ecc.
Quindi, per una batteria da 12 V, il caricabatterie dovrebbe fornire almeno 18-20 V.
Se questa tensione è ridotta a meno di 15 V, la batteria non può raggiungere lo stato di carica completa.
Durante una ricarica: 2PbSO4 + 2H2O → PbO2 + Pb + 2H2SO4
Il solfato di piombo su entrambi gli elettrodi si dissolve come ioni di piombo e si deposita immediatamente come piombo sulla piastra negativa e come PbO2 sull’elettrodo positivo.
Alla piastra positiva
PbSO4 + 2H2O → PbO2 + 4H+ +SO4 ²- + 2e-
Gli elettroni viaggiano verso la piastra negativa per un’ulteriore reazione
Alla piastra negativa
PbSO4 + 2e- → Pb +SO4 ²-
Poiché gli ioni di solfato si riproducono su entrambe le piastre, si combinano con i protoni per formare acido solforico e quindi il peso specifico dell’elettrolita aumenta.
Gassificazione della batteria
Finora abbiamo visto solo le reazioni utili durante il processo di carica. Ma ci sono alcune reazioni collaterali o secondarie che si verificano nei periodi di sovraccarico. Le due principali reazioni secondarie o collaterali sono:
- Elettrolisi dell’acqua e
- Corrosione delle griglie positive
Queste reazioni possono essere rappresentate come segue:
Elettrolisi dell'acqua
2H2O → O2 ↑ + 2H2 ↑ (Su entrambe le piastre di celle al piombo-acido inondate in eccesso)
L’ossigeno della piastra positiva e l’idrogeno delle piastre negative si evolvono e vengono espulsi nell’atmosfera attraverso i fori dei tappi di sfiato.
Ma in una cella VRLA (valve regulated lead acid battery), l’ossigeno si sviluppa, ma non l’idrogeno. L’ossigeno così evoluto non viene lasciato sfogare ma si diffonde attraverso i vuoti disponibili nel separatore AGM (absorptive glass mat) e reagisce con il materiale attivo negativo per rigenerare le molecole d’acqua. Questo è il passo che rende possibile alla cella VRLA di prosperare senza rabbocco d’acqua.
2H2O → O2 + 4H+ + 4e – Sulla piastra positiva delle celle Starved electrolyte o VRLA
Corrosione delle griglie positive in una batteria al piombo
In entrambi i tipi di celle al piombo-acido la corrosione della griglia positiva si verifica nello stesso modo:
Corrosione della griglia: Pb + 2H2O → PbO2 + 4H+ + 4e-
Se un elettrodo di platino platinato è fatto un catodo, l’idrogeno si evolve quasi alla reversibilità
potenziale di idrogeno della soluzione. Con altri elettrodi, per esempio il piombo, è necessario un potenziale più negativo
perché questa reazione avvenga.
Fino a quando la tensione della cella raggiunge un valore di 2,3 V, il gas è trascurabile. Ma il gas inizia a 2,4 V per cella. Oltre i 2,4 V, la gassificazione è maggiore e quindi l’efficienza della carica sarà ridotta. A 2,5 V, il gas sarà copioso e la temperatura dell’elettrolito della batteria comincerà a salire. Ora c’è abbastanza gas per fornire l’agitazione dell’elettrolito e il peso specifico comincia ad equalizzarsi. Quando la batteria è inattiva, il peso specifico dell’elettrolito sarà un po’ più alto nella parte inferiore che in quella superiore. Questo si aggrava se le cellule sono più alte.
La batteria al piombo-acido può essere caricata a qualsiasi ritmo che non porti a una gassificazione eccessiva, a una temperatura elevata e a una tensione molto alta ai terminali. Una batteria completamente scarica può assorbire un alto tasso di carica all’inizio della carica senza gassificazione e senza un aumento apprezzabile della tensione e della temperatura.
Ad un certo punto del processo di carica, quando quasi tutto il solfato di piombo è stato convertito in biossido di piombo nel plat positivo, le reazioni secondarie prendono il sopravvento. Questi sono la reazione di elettrolisi dell’acqua e la corrosione della griglia positiva, come indicato in precedenza.
Tale corrosione positiva della griglia inizia fin dalla fase di formazione (o, nel caso della formazione di un vaso, dalla prima carica). Questa corrosione è l’aspetto più negativo per la vita della batteria al piombo. Poiché la corrosione della griglia positiva avviene ogni volta che la cella entra nella regione di sovraccarico, una parte della struttura della griglia viene convertita in biossido di piombo e quindi il peso della griglia scende un po’ ad ogni periodo di corrosione. Alla fine, si raggiungerà una fase in cui gli elettroni dai siti di reazione sulle griglie non potranno viaggiare verso la sbarra, a causa dell’indisponibilità di una struttura a griglia continua
Di conseguenza, una parte del materiale attivo non può partecipare al processo di produzione di energia e la capacità diminuisce, portando alla fine della vita della batteria.
I produttori di celle al piombo cercano di mitigare questo problema con l’inclusione di elementi di lega che aumentano la resistenza alla corrosione delle leghe di piombo. Alcuni di questi costituenti di lega sono arsenico (As) e argento (Ag) in percentuali frazionarie. Di regola, la quantità di As sarà di circa 0,2% e Ag di circa 0,03-0,05% nelle leghe positive.
Caricabatterie - significato di accettazione della corrente
L’accettazione della corrente è dettata dal design della cella. Per esempio, una batteria di Ah simile assemblata con un numero maggiore di piastre (cioè le piastre saranno più sottili), può accettare una corrente di carica più alta a causa della maggiore superficie. Per le procedure dettagliate per misurare le efficienze di carica delle singole piastre, si rimanda i lettori a un articolo di K. Peters. [8]
L’accettazione della carica della piastra negativa è maggiore di quella della piastra positiva (Vedi Figura 1) che è principalmente dovuta alla sua struttura più grossolana, più aperta e con pori che ammette facilmente la diffusione dell’acido all’interno della piastra. Il positivo comincia ad essere sovraccaricato al 70-80% SOC, a seconda di diversi fattori di progettazione. Alcuni fattori interni di progettazione parametrica sono la struttura dei pori, la superficie reale, ecc. Altri parametri esterni sono la corrente di carica in ampere, la temperatura dell’elettrolito, ecc.
L’accettazione della carica della piastra negativa è più alta ed entra nella regione di sovraccarico in un periodo relativamente più tardivo, 90% SOC [8. K. Peters, A.I. Harrison, W.H. Durant, Power Sources 2. Research and Development in Non-mechanical Electrochemical Power Sources, Pergamon Press, New York, USA, 1970, pp. 1-16].
[9. A.M. Hardman, Journal of Power Sources Vol. 23, anno 1988, pagina, 128].

Ad un certo punto, tuttavia, le reazioni secondarie iniziano all’elettrodo negativo, principalmente la riduzione dello ione idrogeno (protone) a idrogeno gassoso per semplice trasferimento di elettroni (che avviene a potenziali molto più bassi di -350 mV che è il potenziale negativo di piastra reversibile, valore E°.), a circa -0,6 a 0,95 V:
2H+ + 2e- →H2 ↑
Una di queste importanti impurità che si accumulano sulla piastra negativa è l’antimonio (Sb), che si deposita a causa del fenomeno chiamato antimonio-migrazione nelle celle che contengono una quantità relativamente maggiore di antimonio nelle griglie. Anche se l’antimonio è un componente essenziale della lega della griglia per la maggior parte delle celle al piombo, ha un impatto negativo sulle prestazioni della cella.
Durante la fase di corrosione della carica (verso la fine della carica di ogni ciclo), la griglia positiva subisce un attacco anodico e l’antimonio passa in soluzione come ioni Sb5+, una parte dei quali viene assorbita dal materiale attivo positivo dove promuove l’autoscarica a causa della formazione locale della cella. Il resto dell’antimonio così dissolto si deposita come Sb3+ sulla superficie del catodo (la superficie negativa della piastra) (“migrazione dell’antimonio”) e a causa del suo potenziale di idrogeno inferiore a quello del piombo, causa un’evoluzione prematura dell’idrogeno. Più tardi, durante copiosi periodi di evoluzione del gas, l’antimonio può, in condizioni favorevoli, essere rilasciato in una certa misura come gas stibina (SbH3), quando si combina con i protoni.
In condizioni favorevoli, una reazione simile con l’arsenico (As) può anche avvenire rilasciando arsina (AsH3), che è un gas velenoso. Pertanto, questo costituente di lega è naturalmente evitato quando le celle sono utilizzate in ambienti chiusi, come un sottomarino.
Termodinamicamente, questo avviene a un potenziale inferiore rispetto alla reazione di carica primaria, ma, come per la generazione di ossigeno all’elettrodo positivo, l’overpotenziale per la generazione di idrogeno sull’elettrodo di piombo è relativamente grande (circa -0,650 V) e quindi la ricarica può essere ampiamente completata prima che l’evoluzione dell’idrogeno inizi completamente.
Questi gas vengono espulsi dalla cella attraverso i fori del tappo di sfiato. Entrambe le piastre sono affette da effetti di impurità sul sovrapotenziale, e quindi non è possibile una ricarica perfettamente efficiente di entrambe le piastre. Per esempio, se si combina il potenziale di reazione dell’evoluzione dell’ossigeno con quello dell’evoluzione dell’idrogeno, abbiamo
1,95 + (-0,95) = 2,9 V per una copiosa evoluzione del gas.
Un altro punto da notare è che secondo le leggi fondamentali, l’acqua dovrebbe decomporsi a 1,23 V e l’ossigeno dovrebbe evolvere su un elettrodo positivo a questo potenziale. Ma questo non è il caso in una cella pratica. Se succede, la stabilità della stessa cella al piombo sarà un problema. Il potenziale positivo standard della piastra (E° = 1,69 V) è circa 0,46V al di sopra della tensione alla quale l’acqua dovrebbe decomporsi (1,23V). La ragione è di nuovo la sovratensione. Cioè, la tensione per l’evoluzione dell’ossigeno sul biossido di piombo in soluzione di acido solforico è molto superiore al valore E° della piastra positiva a 1,95V.
Così la reazione di evoluzione dell’ossigeno sul biossido di piombo in soluzione di acido solforico è inibita, essendo 0,26 V (1,95-1,69 = 0,26) sopra il valore E° della piastra positiva e circa 0,72 V sopra il potenziale di decomposizione dell’acqua (1,95-1,23 = 0,72V) e quindi l’ossigeno non evolve fino al raggiungimento del valore di sovratensione in una soluzione strettamente pura.
Allo stesso modo, l’evoluzione dell’idrogeno sul piombo in soluzione di acido solforico è fortemente inibita a causa del sovrapotenziale dell’idrogeno sul piombo. Questo valore di overpotenziale è circa 0,6 V più negativo ed è al di sotto del potenziale standard dell’elettrodo del piombo in soluzione di acido solforico, E° = -0,35V. Quindi la reazione di evoluzione dell’idrogeno non ostacolerà la carica completa della piastra negativa fino a quando il valore dell’elettrodo non raggiungerà -0,95V in una soluzione rigorosamente pura. Questa è la ragione per cui la piastra negativa ha una migliore efficienza di carica rispetto alla piastra positiva.
Ma, in una cella pratica, questo stadio viene raggiunto molto prima di questa tensione. In effetti, questo 2,9 V non si realizza affatto in una cella pratica, perché le reazioni dovute alle impurità prendono il sopravvento e quindi l’intera evoluzione del gas in volume (H2: O2 = 2:1) è raggiunto a circa 2,6 V. Tuttavia, se la tensione di carica impressa è eccessivamente alta, allora questo valore di 2,9 V può essere raggiunto, in particolare, le batterie in lega senza Sb possono raggiungere un valore di 2,8 V e con celle antimoniali il valore sarà inferiore di 0,2 V, diciamo 2,6 V.
Man mano che i cicli procedono ulteriormente, il valore di gasatura sarà molto ridotto nel caso delle cellule antimoniali, mentre l’altra cella è quasi esente da questo effetto. Questa drastica riduzione è dovuta al fenomeno chiamato “migrazione dell’antimonio” come spiegato prima.
Naturalmente, la differenza di tensione tra le batterie nuove e quelle ciclate aumenta da 250 mV a 400 mV. Questo si traduce nell’incapacità dei materiali attivi di accettare la carica e quasi tutta la corrente genera idrogeno e ossigeno. La figura 3 illustra questo aspetto [10. Hans Tuphorn, Capitolo 17, Figura 17.2 in Battery Technology Handbook, Ed. H.A. Kiehne, seconda edizione, 2003, Marcel Dekker, Inc., New York.]

Come funziona un caricabatterie a 12v?
Per caricare una batteria, il cavo di uscita positivo è collegato al terminale positivo della batteria e così il negativo al terminale negativo. Il caricabatterie viene poi collegato alla rete AC attraverso un modo adeguato.
L’ingresso AC è convertito in DC da un circuito raddrizzatore che ha un trasformatore step-down per convertire alla tensione richiesta. Un raddrizzatore converte il flusso bidirezionale alternato di corrente (AC) in un flusso unidirezionale. Così, mantiene una polarità costante attraverso il carico. Una configurazione di raddrizzatore a ponte è usata per raddrizzare la bassa tensione AC in DC ed è ulteriormente livellata da un condensatore elettrolitico di alto valore (circuito di filtraggio).
Questa corrente continua filtrata è alimentata a un circuito elettronico che regola la tensione in un livello costante e viene applicata alla batteria che richiede una carica,
Il caricatore ha indicatori per la corrente (amperometro), la tensione (voltmetro), e anche in casi speciali un timer e un amperometro.
La batteria è caricata secondo le istruzioni del produttore
Procedura di carica della batteria - Caricabatterie
La batteria che deve essere caricata deve essere pulita accuratamente all’esterno e i terminali, dopo aver rimosso l’eventuale prodotto di corrosione, devono essere ricoperti con un sottile strato di vaselina bianca. Verrà controllato anche il livello degli elettroliti. Il rabbocco non deve essere fatto in questo momento, a meno che il livello non sia sotto l’altezza dei separatori.
Il caricatore destinato a caricare la batteria deve avere specifiche adeguate, come la tensione e la corrente in uscita. Per esempio, una batteria da 12 V ha bisogno di una tensione di uscita C di almeno 18 V. La corrente richiesta dipende dalla capacità della batteria e dal tempo entro il quale la batteria deve essere caricata. Normalmente, una batteria sarà caricata a un decimo di ampere della capacità Ah della batteria. Così, una batteria da 100 ah richiederà almeno 10 ampere di uscita per una ricarica normale. Se deve essere caricato rapidamente, saranno necessari 15 ampere di uscita.
Un ingresso di circa il 110% della capacità è richiesto per una batteria completamente scarica. Ma, se la batteria è già parzialmente carica, dovremmo conoscere il SOC. Qualunque cosa sia, la tensione e il peso specifico sono i due parametri importanti da monitorare per determinare lo stato di carica. Il valore del peso specifico deve essere letto sull’etichetta della batteria. Una batteria completamente carica raggiunge normalmente 16,5 V e più, se è in buone condizioni. Se si tratta di una batteria vecchia, questa tensione non può essere raggiunta facilmente.
Questo è principalmente dovuto alle reazioni secondarie come l’evoluzione di gas dovuta all’elettrolisi dell’acqua nell’elettrolita e agli effetti di riscaldamento dovuti alle resistenze già accumulate a causa del solfato di piombo accumulato.
La batteria è posta su un materiale isolante come un foglio di gomma o un banco di legno. Il cavo del caricatore deve avere una capacità di trasporto di corrente adeguata. Normalmente, un filo di rame quadrato di 1 mm può trasportare in modo sicuro 3 ampere di corrente continua (DC). Dopo essersi assicurati che il caricabatterie sia in posizione off, i cavi del caricabatterie saranno collegati ai rispettivi terminali, cioè, positivo con positivo e negativo con negativo. La tensione, il peso specifico e le letture della temperatura saranno registrate in un foglio di registro, un modello del quale è dato qui sotto:
Modello di registrazione della carica della batteria

Le letture devono essere registrate ogni ora.
Le letture del cadmio indicheranno se una particolare piastra ha raggiunto la piena carica o meno. L’elettrodo di riferimento al cadmio è un’asta di cadmio isolata con un filo di rame saldato all’estremità superiore. L’estremità inferiore sarà immersa nell’elettrolita, in modo che tocchi appena il liquido, e non deve entrare in contatto con le piastre o altre parti di piombo all’interno.
Per una piastra positiva completamente carica, la lettura del cadmio sarà di 2,4 V e più e per la piastra negativa, meno 0,2 V e meno.
Tabella 4
Reazioni nella cella al piombo-acido e le corrispondenti letture del potenziale del cadmio
Letture del potenziale di cadmio
| Reazioni | Valori potenziali | Letture di cadmio |
|---|---|---|
| Potenziale di evoluzione dell'ossigeno 2 H2O → O2 + 4 H+ + 4e- | 1,95 a 2,00 V | 2.00 - (-0.4) = 2.4 V |
| Potenziale standard dell'elettrodo della piastra positiva PbO2/PbSO4/H2SO4 | 1.69 V | [1.69 - (-0.4) = 2.09 V] |
| Fine dello scarico della piastra positiva | 1,40 a 1,5 V |
1.40 - (-0.4) = 1.8 V 1.50 - (-0.4) = 1.9 V |
| Potenziale standard dell'elettrodo dell'idrogeno (SHE) 2H+ + 2e- → H2 | 0.00 V | 0.00 V |
| Fine della scarica della piastra negativa | -0,15, -0,20, -0,25 V (per diverse densità di corrente) | -0.15 - (-0.4) = 0.25 V -0.20 - (-0.4) = 0.20 V -0.25 - (-0.4) = 0.15 V |
| Potenziale dell'elettrodo standard della piastra negativa Pb/PbSO4/H2SO4 | -0.35 V | [-0.35 - (-0.4) = 0.05 V] |
| Elettrodo di riferimento al cadmio Valore E° Cd/Cd2+ | -0.40 V | -0.40 V |
| Potenziale di evoluzione dell'idrogeno- 2H+ + 2e- →H2 (Per una cella commerciale) | -0.60 V | -0.60 - (-0.4) = -0.20 |
| Potenziale di evoluzione dell'idrogeno 2H+ + 2e- →H2 Per una cella sperimentale pura | -0.95 V | -0.95 - (-0.4) = -0.55 |
Principio di funzionamento di un caricabatterie
Alla fine della carica, una batteria da 12 V può raggiungere una tensione terminale di 16,5 e più. Dopo aver mantenuto la tensione del terminale a questo livello per un’ora, la carica può essere terminata. Quando la batteria si avvicina ai 16 anni. 0 V, si può aggiungere acqua approvata, se necessario.
Verso la fine della carica, si osserverà una forte gassificazione dalla batteria. Nessuna fiamma aperta deve essere portata vicino alla stanza di ricarica. I gas si evolvono nel rapporto della loro combinazione, cioè idrogeno 2 parti e ossigeno 1 parte. Quindi, se si permette a questi gas di accumularsi nell’area di ricarica senza un’adeguata ventilazione, è probabile che una scintilla o una fiamma aperta accenda i gas e che questi si combinino con violenza esplosiva, danneggiando la batteria e i suoi dintorni e ferendo anche le persone vicine.
Il limite inferiore per la miscela esplosiva di idrogeno nell’aria è del 4,1%, ma, per motivi di sicurezza, l’idrogeno non dovrebbe superare il 2% in volume. Il limite superiore è il 74%. L’esplosione pesante avviene con violenza quando la miscela contiene il rapporto stechiometrico di questi gas (2 parti di idrogeno a 1 di ossigeno). Questa condizione si ottiene all’interno di una batteria sovraccarica con tappi di sfiato ben avvitati al coperchio. Quindi si consiglia di tenere i tappi di sfiato allentati sopra i fori di sfiato e di non avvitarli strettamente.
Diversi metodi di ricarica delle batterie e diversi tipi di caricabatterie
Anche se ci sono vari metodi per caricare le celle piombo-acido, tutti hanno un obiettivo comune di convertire i prodotti di reazione, cioè il solfato di piombo su entrambe le piastre nei rispettivi materiali attivi, PbO2 sull’elettrodo positivo e Pb sull’elettrodo negativo.
2 PbSO4 + 2H2O→ PbO2 + Pb + 2H2SO4
Esiste un certo numero di varianti nei regimi di tariffazione. Ma in tutti questi metodi, solo due principi di base sono utilizzati: i metodi di carica a corrente costante e a tensione costante. I diversi metodi disponibili combinano questi due principi per raggiungere i loro obiettivi.
La selezione del metodo appropriato di ricarica dipende dal tipo, dal design e dalle condizioni di servizio e dal tempo disponibile per la ricarica. Tutti questi metodi di ricarica usano molti metodi per controllare e finire il processo di ricarica.
Questi metodi possono essere classificati nei seguenti:
Tabella 5
Classificazione dei metodi di diversi caricabatterie & metodi di ricarica della batteria
Diversi metodi di ricarica della batteria
| Metodi basati sulla corrente costante (CC) | Metodi basati sulla tensione costante (CV o CP) | Metodi combinati | Carica conica | Metodi speciali |
|---|---|---|---|---|
| Metodo di ricarica CC a passo singolo | Metodo a tensione costante | Metodo CC-CV | Metodo di carica conica a passo singolo |
1. Carica iniziale 2. Onere di perequazione 3. Carica di opportunità 4. Carica controllata dal gas 5. Carica di mantenimento 6. Carica di spinta 7. Carica a impulsi 8. Ricarica veloce o rapida |
| Metodo di ricarica CC a due fasi | Metodo CV limitato alla corrente o modificato | Metodo di carica conica a due fasi |
Passo singolo Metodo di carica a corrente costante (metodo CC) Caricabatterie
Quando la ricarica deve essere terminata in poco tempo e quando l’utente vuole conoscere l’ingresso in termini di Ah, si può utilizzare il metodo di ricarica a corrente costante. La carica a corrente costante è preferita quando è nota l’uscita precedente, in modo che il 5-10% di sovraccarico può essere efficace per riportare la batteria al 100% SOC. Questo assicurerà anche che l’input corretto sia dato in modo che la vita della batteria non sia influenzata negativamente da un sovraccarico eccessivo. Un tempo di ricarica normale per questo metodo è di 15-20 ore.
In questo metodo, la corrente è mantenuta costante durante tutto il periodo di carica.
Si raccomanda una corrente di carica dal 5 al 10 % della capacità di 20 ore.
Per compensare l’aumento del back emf della batteria durante la carica, la corrente di carica deve essere mantenuta costante variando la resistenza in serie utilizzata o aumentando la tensione del trasformatore. Di solito, la resistenza in serie viene variata per mantenere costante la corrente.
Questo metodo è il più semplice e meno costoso per la ricarica. Ma ha lo svantaggio di una minore efficienza di carica. Questo è dovuto a una certa potenza dissipata nella resistenza e anche in parte alla corrente usata per dividere l’acqua una volta che la batteria raggiunge i 2,5 V per cella. La batteria inizia a produrre gas quando viene caricata a circa il 70-75% di carica. Questo metodo di carica si traduce sempre in una leggera sovraccarica e in una gassificazione vigorosa soprattutto alla fine della carica.
Un’immagine generalizzata per il metodo di carica a corrente costante è data dalla figura 5. Le caratteristiche di carica sono riportate nella figura 6


Metodo di carica a corrente costante in due fasi Caricabatterie
Nel metodo di carica a corrente costante in due fasi vengono utilizzati due tassi di carica, il tasso iniziale e il tasso finale. Il tasso di finitura è normalmente la metà del tasso di partenza. Il tasso di finitura inizia quando la batteria comincia a sviluppare gas. Questo è generalmente un metodo preferito impiegato per la carica al banco delle batterie. La caratteristica di carica può essere vista nella figura 7 [11. P G Balakrishnan, Batterie al piombo, Scitech Publications (India) Pvt. Ltd., Chennai, 2011, pagina 12.8].

Metodi di carica a tensione costante o potenziale Caricabatterie
Il metodo di carica a tensione o potenziale costante (CV o CP) impiega una tensione sorgente che viene mantenuta ad un livello costante per tutto il periodo di carica. Di solito, questa tensione sarà tra 2,25 e 2,4 V per cella.
Questo metodo è il metodo raccomandato per caricare celle e batterie VRLA (valve-regulated lead-acid). Non ci si deve preoccupare della profondità di scarica (DOD) della scarica precedente quando si carica una batteria VRLA con il metodo CV. Le batterie VRLA possono essere caricate senza effetti negativi utilizzando la tensione di carica CV raccomandata dal produttore. Quasi tutti i produttori di VRLAB raccomandano una corrente di avviamento da 0,25 a 0,30 C ampere.
Cioè, per una batteria da 100 Ah, si può selezionare una corrente iniziale di 25-30 ampere. La corrente più alta è usata per caricare batterie molto scariche, mentre quella più bassa per una batteria normalmente scarica. L’effetto di una tensione di carica più bassa è che l’aumento della temperatura sarà minore rispetto a una batteria caricata con una corrente più alta, ma il tempo impiegato per una carica completa sarà maggiore.
Alla fine della carica, la tensione della batteria raggiunge la parità con la tensione impressa e la corrente di carica si riduce a un valore molto basso. Universalmente, la corrente alla fine può raggiungere un valore di 2 a 4 mA per ogni Ah della capacità della batteria. A 2,25-2,3 V per cella, non si osserva alcuna evoluzione di gas nelle batterie fabbricate correttamente. Tuttavia, il gas sarà evidente a 2,4 V per cella. Il volume di gas evoluto a 2,4 V per cella è di circa 1000 ml in 40-50 minuti per 6V/1500 Ah VRLAB
Secondo la clausola 6.1.a. del Japanese Industrial Standard, JIS 8702-1:1998, la durata della carica sarà di circa 16 ore o fino a quando la corrente non cambierà di più del 10 % della corrente di 20 ore (I20) in due ore consecutive [JIS 8702-1:1998]. Per esempio, se la capacità di 20 ore di una batteria (indipendentemente dalla tensione della batteria) è di 60 Ah20, allora la carica sarebbe stata completata se la corrente non cambia di più di 300 mA (cioè, I20 = 60 Ah /20 A = 3 A. Pertanto, 0,1 di I20 = 0.3A)
I dettagli della carica CP delle batterie VR sono mostrati nelle figure
L’efficienza di carica è migliore del metodo a corrente costante. Il demerito di questo metodo è che richiede una tensione stabilizzata ad un alto scarico di corrente, che è costoso. Questo metodo è usato per il funzionamento fluttuante delle celle stazionarie per applicazioni di telecomunicazione e UPS.


Carica a potenziale costante modificata - Caricabatterie
Nelle applicazioni industriali, tale metodo viene utilizzato quando il circuito di carica è parte integrante del sistema. Esempi sono le automobili, l’UPS, ecc. Una resistenza in serie per limitare la corrente è inclusa nel circuito, il cui valore è mantenuto fino al raggiungimento di una tensione prestabilita. In seguito, la tensione viene mantenuta costante fino a quando la batteria è chiamata a svolgere il suo compito per fornire corrente di avviamento, energia di emergenza, ecc.
La scelta della resistenza in serie fissa dipende dal numero di celle nelle batterie e dalla loro capacità in ampere-ora e dalla durata disponibile per la carica. La tensione applicata è mantenuta costante a circa 2,6-2,65 volt per cella.
Man mano che la carica procede, la corrente di carica inizia a scendere da un valore iniziale. Quando la tensione sale gradualmente fino a 2,35-2,40 volt per cella, la tensione di gas tende a salire rapidamente e quindi la corrente di carica scende più rapidamente.
La carica a potenziale costante modificata è comune per le batterie deep-cycling come le batterie da trazione. Le fabbriche normalmente impiegano un profilo di tempo fisso di scaricamento-caricamento, come ad esempio 6 ore di funzionamento del carrello elevatore a forca per una profondità di scaricamento (DOD) dell’80% e una ricarica di 8 ore. Il caricatore è impostato per la tensione di gas e la corrente di avviamento è limitata a 15-20 A per 100 Ah. La corrente comincia a diminuire a tensione costante fino al tasso di finitura di 4,5 a 5 A per 100 Ah, che viene poi mantenuto fino alla fine della carica. Il tempo di carica totale è controllato da un timer.
Ci sono caricabatterie che hanno le disposizioni per mantenere le batterie collegate ad esso anche dopo il completamento della carica per mantenere le batterie in condizioni di carica completa. Questo si ottiene fornendo brevi periodi di ricarica rinfrescante ogni 6 ore per mantenere la sua condizione
I dettagli sono riportati nella figura 12 [12. Special Issue on Lead-Acid Batteries, J. Power Sources 2(1) (1977/1978) 96-98]

Metodi combinati (metodi CC-CV) - Caricabatterie
In questo metodo la carica a corrente costante e a potenziale costante sono combinate insieme. Questo metodo è anche conosciuto come metodo di carica (IU) (I per la corrente e U per la tensione). Nel periodo iniziale di carica, la batteria viene caricata in modalità corrente costante fino a quando la batteria raggiunge la tensione di gas e poi viene commutata in modalità potenziale costante. Questo metodo elimina l’effetto deleterio del metodo di carica a corrente costante alla fine della carica.
Le caratteristiche di carica di questo metodo sono mostrate nella Figura 11 a destra.

Carica del cono - Caricabatterie
Il significato di taper è quello di scendere verso il basso. Come il termine indica chiaramente, la corrente viene lasciata ridurre da un valore più alto a uno più basso, fissando la tensione di carica iniziale a circa 2,1 V per cella e terminando a 2,6 V per cella. Il rapporto dei valori di corrente a queste tensioni è chiamato valore di conicità.
Così, un caricatore con un’uscita di 50 A a 2,1 V per cella e 25 A a 2,6 V per cella, è descritto come avente una caratteristica di conicità di 2:l.
Ci sono metodi di carica conica a un passo e metodi di carica conica a due passi
Carica conica a passo singolo - Caricabatterie
In questo tipo di carica, la corrente si assottiglia da un valore iniziale più alto a uno più basso di tasso finale, che di solito è circa il 4-5% della capacità di tasso di 20 ore della batteria. La gassificazione è un fenomeno necessario poiché aiuta ad equalizzare il gradiente di densità dell’elettrolita. cioè, neutralizza il fenomeno della stratificazione. Quindi, il tasso di finitura è fissato a un valore sufficientemente alto per permettere che questo processo avvenga e allo stesso tempo non corroda indebitamente le griglie positive. Qui, la tensione di uscita del caricatore è impostata a circa 2,7 volt per cella inizialmente e viene fatta scendere a circa 2,1-2,2 volt per cella alla fine del periodo di carica.
La corrente di carica viene fatta diminuire lentamente fino al raggiungimento della tensione di gassificazione (circa 2,4 V per cella) (SOC = 75-80%) e poi diminuisce ad un ritmo più veloce. Normalmente, il rapporto di conicità è fissato a 2:1 o a 1,7 a 1. Il tempo necessario per il completamento della carica è di circa 12 ore. Il periodo di carica dopo il raggiungimento della tensione di gassificazione è controllato incorporando un dispositivo di temporizzazione che inizia a funzionare quando la tensione di gassificazione è raggiunta.
Il periodo di ricarica può essere ridotto a 8 o 10 ore, ma la corrente di avviamento deve essere migliorata, il che non può essere fatto senza considerare l’aspetto economico e l’accessibilità del consumatore.

Le caratteristiche di carica della carica conica a passo singolo sono mostrate nella Figura 12

Carica conica a due fasi - Caricabatterie
Questo metodo di carica è simile alla carica conica a passo singolo, tranne per il fatto che il tempo totale di carica si riduce a circa 8-10 ore. Poiché la batteria è in grado di accettare la carica a un ritmo più veloce quando è profondamente scarica, viene impiegata una corrente elevata nella prima fase fino a quando la batteria raggiunge la fase di gassificazione. Quasi il 70-80% degli ampere-ora da restituire alla batteria viene dato alla batteria nella prima fase ad un ritmo più veloce e gli ampere-ora rimanenti vengono alimentati nella seconda fase.
Le caratteristiche di carica di una batteria da 12V, 500 Ah con carica conica a passo singolo sono mostrate nella Figura 13
I metodi di carica conica sono più popolari per caricare le batterie da trazione che sono normalmente molto scariche. Gli operatori di flotte di veicoli elettrici, per esempio furgoni per la consegna della posta, veicoli per la consegna del latte, richiedono sofisticati caricabatterie per ottenere le migliori prestazioni possibili dalle batterie e per proteggere il grande investimento di denaro coinvolto.
Carica iniziale
Una nuova batteria al piombo-acido ha bisogno di essere attivata e questo processo di carica per la prima volta è chiamato carica di riempimento iniziale. La batteria è riempita con la quantità necessaria di elettrolita ed è completamente carica prima di essere inviata per la spedizione. Normalmente questa carica iniziale è fatta con un metodo di carica a corrente costante a bassa corrente per un lungo periodo fino a quando la batteria raggiunge una tensione di 16,5 V o più per essere completamente carica.
Al giorno d’oggi, questo processo è diventato superfluo, dato che abbiamo batterie caricate in fabbrica pronte all’uso o batterie caricate a secco che richiedono solo l’aggiunta di elettrolita.
Onere di perequazione
Equalizzazione della carica Le differenze da cellula a cellula sono un fatto da accettare. Non ci sono due cellule che possono essere uguali in tutti gli aspetti. Le differenze nei pesi dei materiali attivi, le piccole variazioni nel peso specifico dell’elettrolita, la porosità degli elettrodi, ecc. sono alcune delle differenze. A causa di queste ragioni, ogni cella di una batteria ha le proprie caratteristiche; ognuna richiede una quantità di carica leggermente diversa. Equalizzare la carica una volta ogni tanto allontana la fine della vita della batteria. Le batterie automobilistiche da 12V sono fluttuanti a 14,4V. Una batteria completamente carica richiede una tensione di 16,5 V, che non viene mai realizzata in servizio a bordo del veicolo.
Quindi la carica di equalizzazione (chiamata anche carica al banco) è necessaria per prolungare la vita di una batteria automobilistica. Così, una batteria che riceve una carica di banco periodica ogni sei mesi può sopravvivere alle batterie che non ricevono la carica di banco, almeno di 10-12 mesi. La frequenza e la portata delle cariche di equalizzazione devono essere discusse con il produttore della batteria. Con i caricatori pre-programmati, una “carica di equalizzazione” è talvolta disponibile tramite un interruttore che fornisce una bassa corrente continua utilizzata per stabilizzare la tensione e la densità relativa dell’elettrolito delle cellule.
Allo stesso modo, anche le batterie dell’alimentazione di emergenza UPS e le batterie dei carrelli elevatori richiedono tali cariche di equalizzazione. Una batteria usata in un inverter viene caricata solo fino a 13,8-14,4 V. Come detto prima, questo non è sufficiente per equilibrare lo squilibrio tra le celle di una batteria. Queste batterie, se vengono caricate periodicamente, sopravvivono più a lungo.
Le batterie devono essere sottoposte a una carica di equalizzazione ogni sei mesi. Ma le batterie di trazione utilizzate nelle batterie dei carrelli elevatori devono essere sottoposte a una carica di equalizzazione una volta ogni sesto o undicesimo ciclo, a seconda che le batterie siano nuove o invecchiate. Le batterie più recenti possono essere sottoposte a una carica di equalizzazione una volta ogni 11 cicli e quelle più vecchie ogni6 cicli. Se le batterie ricevono regolarmente cariche complete ogni giorno, la frequenza delle cariche di equalizzazione può essere ridotta a10 e20 cicli. Una carica di equalizzazione deve essere terminata quando le celle non mostrano ulteriori aumenti di tensione e letture di peso specifico per un periodo di 2 o 3 ore.
Leggi un articolo dettagliato su Carica di perequazione qui.
Carica di opportunità
Quando un veicolo elettrico fuori strada o su strada viene utilizzato intensamente, la connessione a un caricabatterie durante le pause e altri brevi periodi di riposo può anche aiutare a estendere il turno di lavoro effettivo del veicolo e quindi ridurre i tempi di inattività dei veicoli elettrici. La ricarica di opportunità è il termine dato a tale ricarica parziale durante la pausa pranzo o il periodo di riposo.
Queste cariche di opportunità tendono a ridurre la vita delle batterie. La batteria conta tale carica e la successiva scarica come un ciclo superficiale. Per quanto possibile, le spese di opportunità dovrebbero essere evitate. La carica normale fornisce da 15 a 20 A per 100Ah di capacità, mentre le cariche di opportunità forniscono correnti leggermente più alte di 25 A per 100Ah di capacità. Ne risulta una temperatura più alta e accelera la corrosione delle griglie positive. E quindi la vita sarà ridotta.
Carica controllata dal gas
La conducibilità termica dell’idrogeno gassoso evoluto è usata per monitorare la corrente di carica. Il gas idrogeno, un ottimo refrigerante, è usato per raffreddare un elemento riscaldato. Il cambiamento di resistenza dell’elemento riscaldante è usato per regolare la corrente. Un termistore può anche essere usato per regolare la corrente. A volte, l’effetto di riscaldamento dovuto alla ricombinazione dell’idrogeno gassoso e dell’ossigeno gassoso evoluti nella cella su un catalizzatore adatto è usato per azionare un interruttore termico per regolare la corrente.
Carica di mantenimento
In una carica continua, il caricabatterie equalizza le perdite dovute all’autoscarica e alla scarica intermittente. Una carica di mantenimento compensa l’autoscarica. Le due modalità di funzionamento sono caratterizzate da tensioni terminali costanti:
Carica di mantenimento da 2,20 a 2,25 V per cella
Carica continua da 2,25 a 2,35 V per cella
A seconda dell’età e delle condizioni della batteria, una densità di corrente da 40 a 100 mA/100 Ah di capacità nominale può essere necessaria durante la carica di mantenimento (carica di mantenimento).
La corrente di carica continua dipende in larga misura dal profilo di carico. Le batterie con carica di mantenimento devono essere ricaricate dopo ogni interruzione di corrente. Lo stesso vale per le batterie in carica continua dopo carichi non programmati.
Aumentare la carica
Si ricorre alla carica boost quando una batteria scarica deve essere utilizzata in caso di emergenza, quando non sono disponibili altre batterie e il SOC non è sufficiente per il lavoro di emergenza. Così, una batteria al piombo-acido può essere caricata a correnti elevate a seconda del tempo disponibile e del SOC della batteria. Dal momento che i caricatori veloci sono disponibili al giorno d’oggi, la ricarica rapida è familiare oggi. Normalmente questi caricatori boost iniziano la carica a 100A e si assottigliano fino a 80A. La cosa più importante è che la temperatura non deve superare i 48-50oC.
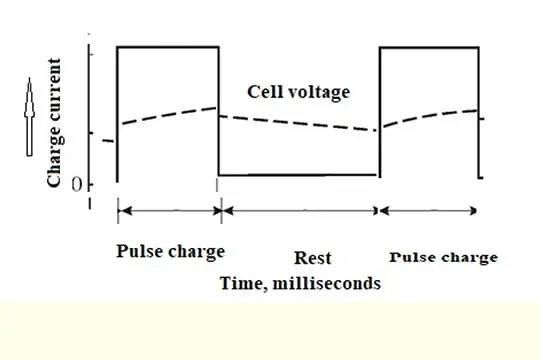
Carica a impulsi
Cos’è la carica a corrente pulsata?
La carica viene effettuata per una durata molto breve, cioè la corrente on-time in millisecondi (ms), e segue un periodo di inattività (off-time in ms). A volte una scarica può anche precedere la carica a impulsi.
Una tecnica a corrente pulsata è stata applicata per la ricarica rapida di celle al piombo-acido automobilistiche. Si è giunti alle seguenti conclusioni:
- La tecnica della corrente pulsata può esercitare effetti molto vantaggiosi.
- Migliora il tasso di ricarica.
- Ha un effetto benefico sulle prestazioni del ciclo di vita delle batterie piombo/acido, specialmente quando si usa un tempo di accensione superiore a 100 ms.
- Inoltre, questa tecnica può anche ringiovanire le cellule che sono state sottoposte a cicli di carica a corrente costante.
- Il tempo di ricarica può essere ridotto di un ordine di grandezza, cioè da ~10 ore a ~1 ora
- La durata del ciclo può essere aumentata di un fattore da tre a quattro.
- L’applicazione di una carica a corrente pulsata a una batteria ciclata (capacità = 80% valore iniziale) può evocare un recupero della capacità della batteria.
- La perdita prematura della capacità si verifica in entrambe le celle Pb-Sb e Pb-Ca-Sn ad alti tassi di scarica con una carica a corrente costante.
Per maggiori dettagli, i lettori possono fare riferimento all’articolo di Lam e altri riportato sopra.
Le celle sottomarine sono state oggetto di carica a impulsi [14. Melvyn James, Jock Grummett, Martin Rowan e Jeremy Newman, Journal of Power Sources 162 (2006) 878-883 879]. Gli autori hanno concluso che
- La capacità può essere migliorata con la carica a impulsi. Questo miglioramento della capacità
è stato drammatico per le cellule relativamente nuove. Ma per le celle più vecchie (4-5 anni) erano necessari 15 o più cicli di carica a impulsi prima di ottenere miglioramenti della capacità.
- Le cellule più vecchie avevano subito una grave solfatazione, che richiede più cicli per rompersi.
- Alcune solfatazioni sono impossibili da invertire.
- L’uso della carica a impulsi ha anche indicato che la carica di gas poteva essere sostanzialmente ridotta.
- L’evoluzione del gas si riduce con l’aumento della frequenza degli impulsi. Questo è più pronunciato con l’evoluzione dell’ossigeno, che è un fattore importante per le batterie sottomarine che soffrono di corrosione della piastra positiva poiché l’ossigeno si evolve dalla piastra positiva durante la carica del gas.
- Dopo l’applicazione della carica a impulsi a una cella, gli effetti benefici rimangono anche se si riprendono le routine di carica convenzionali.
Un tipico programma di carica a impulsi è mostrato qui sotto:
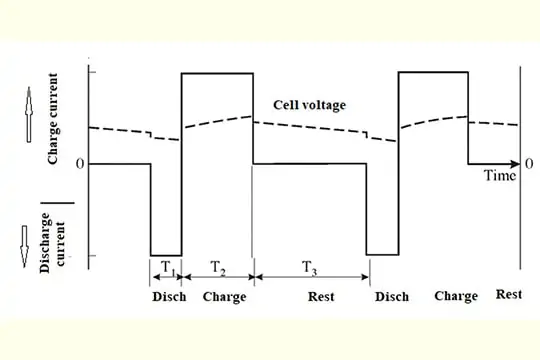
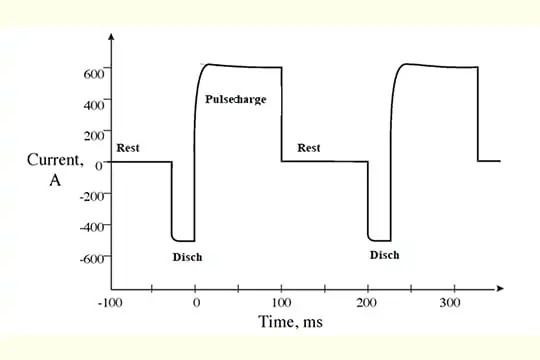
L’applicazione della carica a impulsi può aiutare a prevenire l’accumulo di solfatazione nel tempo. Può essere in grado di ridurre l’accumulo di solfatazione nelle celle con una carica e una manutenzione adeguate se la carica a impulsi viene utilizzata fin dall’inizio. Un accumulo di solfatazione già avvenuto non può essere invertito con questo metodo. Se le celle sono costantemente equalizzate o sovraccaricate, questo danneggia le celle, riducendone la capacità e la vita. Microtex raccomanda di testare regolarmente il peso specifico delle vostre batterie per sapere quanto tempo dureranno, identificare eventuali celle deboli o guaste e confermare il loro stato di carica. I seguenti passi possono essere seguiti in caso di accumulo di solfatazione o di squilibrio della carica.
Ricarica veloce o rapida - Caricabatterie
Venticinque anni fa, si credeva che le batterie al piombo-acido non dovessero essere caricate a tassi elevati perché il materiale attivo positivo sarebbe stato danneggiato irreparabilmente. Si credeva che la carica veloce avrebbe portato a livelli eccessivi di corrosione della rete e di gassificazione, con conseguente fallimento precoce e rapido delle batterie VRLA.
La carica rapida si sta dimostrando non solo un risparmio di tempo e di energia, ma elimina anche i gas e riduce la manutenzione. La carica rapida è stata proposta per la prima volta da Kordesch nel 1972 per le celle Ni-Cd sigillate, [17. K. Kordesch, J. Electrochem. Soc., 113 (1972) 1053] e successivamente sviluppata nel 1993 da Norvik Technologies in Canada per le batterie VRLA.
Il loro Minitcharger™ ha dimostrato che la ricarica di batterie Ni-Cd molto scariche può essere ottenuta in 5-10 minuti [18. J.K. Nor, U.S. Patent 5,202,617(1993)].
Nella prima parte degli anni ’90, Valeriote, Nor, e Ettel di Cominco, Canada, hanno fatto avanzare questa tecnologia alle batterie convenzionali piombo-acido [19. E.M. Valeriote, J. Nor, V.A. Ettel, Proc. Fifth International Lead-Acid Battery Seminar, Vienna, VA, USA, 17-19 aprile 1991, pp 93-122]. Nel 1994, Valeriote, Chang e Jochim dimostrarono che il processo era adatto anche per batterie VRLA a piastre sottili [M. Valeriote, T.G. Chang, D.M. Jochim, Proc. della9th Annual Battery Conference on Applications and Advances, Long Beach, CA, USA, gennaio 1994, pp. 33-38].
Dall’inizio degli anni novanta questa tecnica è stata applicata a batterie di trazione di tutti i tipi [20. K. Nor e J.L. Vogt, Proc. 13th Annual Battery Conference on Application and Advances, 13-16 gennaio 1998, Long Beach, CA, 191-197].
Gli effetti di una carica molto veloce sui seguenti due tipi di batterie ibride piombo/acido deep-cycling sono stati studiati nel 1994 usando un MinitchargerÔ (Norvik Traction Inc., Canada) [21. T.G. Chang, E.M. Valeriote e D.M. Jochim, J. Power Sources 48 (1994) 163-175].
- Le batterie ibride allagate (denominate “AP” in questo lavoro) avevano griglie positive fatte da una lega antimoniale del 4,7% e griglie negative del tipo espanso fatte da una lega alto-calcio-basso-stagno (Pb- 0,1 wt.% Ca-0,3wt.% Sn). Il peso del PAM era di ~800 g, e il NAM ~ 540 g in ogni cella. Era del tipo a scarica profonda e aveva una capacità di 80 Ah20, 54,4 Ah5 e 50,9 Ah3)
- Le batterie regolate da valvole con griglie positive fuse per gravità sono state realizzate con una lega a basso contenuto di antimonio (Pb -1.5wt. % Sb-0.3wt. % Sn (Questa batteria indicata come batterie “ST” in questo lavoro). La configurazione era 5P + 6N. Le griglie negative sono state fuse in lega Pb-O.12wt.%Ca-O.4wt.%. Queste batterie erano destinate ad applicazioni di deep-cycling. Le capacità delle batterie erano 54,5 Ah5 e 52,5 Ah3
Si è scoperto che sia il tasso di ricarica di 5 minuti/50% che quello di 15 minuti/80% potrebbero essere raggiunti, nel caso di una batteria allagata, con un aumento di temperatura abbastanza accettabile. Dopo una profondità di scarica dell’80%, la fonte dominante di calore era ohmica durante il primo 40% della carica restituita a tassi molto elevati, 300 A (da 5 a 6 C3 ampere). Le temperature erano distribuite in modo non uniforme all’interno della batteria. In seguito, la polarizzazione non ohmica è diventata progressivamente più importante. Per la batteria ibrida a ricombinazione, il ciclo dell’ossigeno è una fonte sostanziale di calore durante le ultime fasi della carica, in particolare rispetto alle precedenti batterie non antimoniali che sono state studiate [21 T.G. Chang, E.M. Valeriote e D.M. Jochim, J. Power Sources 48 (1994) 163-175].
Carica rapida di batterie allagate e VRLA
Tabella 6.
[21. T.G. Chang, E.M. Valeriote e D.M. Jochim, J. Power Sources 48 (1994) 163-175].
| Batteria allagata | Batteria regolata a valvola | |
|---|---|---|
| 5-min/50% di ricarica e 15-min/80% di ricarica | Sì | Sì |
| Aumento della temperatura | Accettabile | Accettabile |
| Fonte di calore | Ohmico (fino al 40% della carica) | Il ciclo dell'ossigeno è una fonte sostanziale di calore durante le fasi successive della carica |
| Carica | caricato a una tensione costante senza resistenza di 2,45 V/cella (14,7 V/batteria) | caricato a una tensione costante senza resistenza di 2,45 V/cella (14,7 V/batteria) |
| Corrente | Da 250 a 300 A (da 5 a 6 C3 ampere) | Da 250 a 300 A (da 5 a 6 C3 ampere) |
| Nei 3 minuti iniziali | 1 V superiore al VRB | |
| Riduzione corrente | Ha iniziato a scendere dal livello di 300-A dopo 3 minuti di carica | Ha iniziato a scendere dal livello di 300-A dopo 3 minuti di carica |
| Temperatura | Riscaldamento ohmico più elevato e un tasso di aumento della temperatura molto più alto; ha iniziato a diminuire dopo 4 minuti | La corrente ha iniziato a diminuire solo dopo 4 minuti di carica, ed è stata superiore a quella del tipo allagato per tutto il resto del periodo di carica. |
| Quando la corrente della batteria VR è diminuita, il tasso di aumento della temperatura è diventato maggiore. Dopo 6 minuti, anche se la temperatura continuava a salire, il tasso di aumento ha cominciato a diminuire. La temperatura ha iniziato un lento declino solo dopo circa 20 minuti di carica; con la stessa tensione costante senza resistenza, la batteria VR ha accettato una corrente maggiore, che ha generato ancora più calore. L'energia spesa nel ciclo dell'ossigeno è completamente (100%) convertita in calore, in confronto a circa il 40% per la sola decomposizione dell'acqua. |
Figura 17. In carica: Vref=2,45 V/cella; corrente, I, =3OO A max; DOD = 80%. [21. T.G. Chang, E.M. Valeriote e D.M. Jochim, J. Power Sources 48 (1994) 163-175.]
Confronto tra la ricarica rapida di batterie allagate e VRLA.

Tabella 7. Durata della batteria con MinitCharger
[22. K. Tomantschger, E.V. Valeriote, J.S. Klarchuk, T.G. Chang, M.J. Dewar, V. Ferrone e D.M. Jochim, Proc. 13 Il Conferenza annuale della batteria sull’applicazioneand Advances, January 13-16, 1998, Long Beach, CA, 173-178.]
| Tipo di batteria | Durata del ciclo della batteria | ||
|---|---|---|---|
| Caricabatterie convenzionale | MinitCharger | Fonte | |
| Celle Ni-Cd, tipo A | 500 | 1400 | INCO(1989) |
| Celle Ni-Cd, tipo B | 450 | 1900 | INCO(1996) |
| Celle Ni-MH, tipo A | 400 | 1600 | INCO (1996) |
| Celle Ni-MH, tipo B | 1500 | Oltre 4000 | INCO (1996) |
| Batteria al piombo per trazione, tipo VRLA | 250 | 1500 | COMINCO (1997) |
Anche Chang e Jochim hanno ottenuto risultati simili. Hanno sottoposto le batterie 12V VRLA (tipo avvolto a spirale) a test di carica convenzionale e cicli di carica rapida [21. T.G. Chang, E.M. Valeriote e D.M. Jochim, J. Power Sources 48 (1994) 163-175. 23. Chang, T.G., Jochim, D.M., J. Power Sources, 91 (2000) 177-192]. La durata del ciclo era di 250 cicli per il regime di carica convenzionale e di 1000 cicli per il regime di carica rapida.
La carica molto veloce è stata accolta con grande successo e ha portato a una maggiore durata. Un sondaggio ha dimostrato che il team di ricerca Cominco [ 22. K. Tomantschger, E.V. Valeriote, J.S. Klarchuk, T.G. Chang, M.J. Dewar, V. Ferrone, e D.M. Jochim, Proc. 13il Annual Battery Conference on Application and Advances, January 13-16, 1998, Long Beach, CA, 173-178.] ha condotto un’indagine e il team ha scoperto che trenta varietà di batterie al piombo disponibili in commercio sono in grado di essere ricaricate al 50% in 5 minuti, all’80% in 15 minuti e al 100% in 30 minuti. A questo proposito, le prestazioni di VRLAB sono migliori delle batterie SLI allagate.
I materiali attivi positivi convenzionalmente caricati sono caratterizzati da particelle più grandi e da numerosi grandi pori. Nelle piastre a carica rapida non sono state osservate grandi particelle, pori o vuoti. Le piastre caricate convenzionalmente mostravano 2m2/g di superficie di PAM e quelle caricate ad alta corrente mostravano un valore di superficie di 3m2/g anche dopo 900 cicli [22. K. Tomantschger, E.V. Valeriote, J.S. Klarchuk, T.G. Chang, M.J. Dewar, V. Ferrone, and D.M. Jochim, Proc. 13th Annual Battery Conference on Application and Advances, 13-16 gennaio 1998, Long Beach, CA, 173-178].
Il PAM in quest’ultimo caso si è espanso solo lentamente e di conseguenza è stata esercitata meno pressione sul separatore e sulla piastra negativa, riducendo così il rischio di corti “soak through” nei separatori e l’addensamento del NAM. L’effetto drammatico della carica veloce è che sottoponendo a test del ciclo di vita 12V/50Ah VR LAB avvolto a spirale (quando testato sotto regimi di carica di 10 ore e 15 minuti) le batterie caricate convenzionalmente potrebbero dare solo 250 cicli (all’80% della capacità iniziale) mentre quelle sotto regime di carica veloce potrebbero dare circa quattro volte più cicli.
Immagini al SEM di PAM e NAM di piastre convenzionali e a carica rapida

Un risultato simile è stato ottenuto nei lavori di P. T. Moseley [Journal of Power Sources 73 _1998. 122-126] ALABC-CSIRO Project No. AMC-009). La ricarica ad alta velocità delle batterie VRLA ripristina il materiale attivo positivo in una forma ad alta superficie caratterizzata da un abito aghiforme e quando la batteria viene ricaricata a tassi inferiori il materiale attivo positivo forma particelle più grandi.

Diagramma del caricabatterie



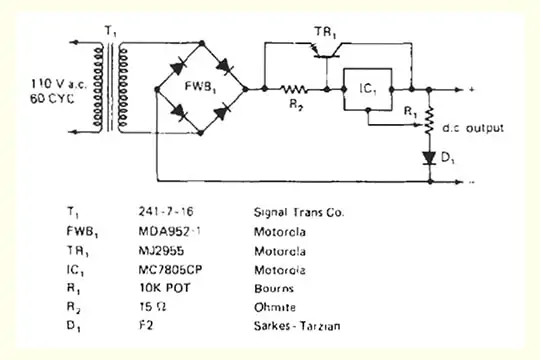

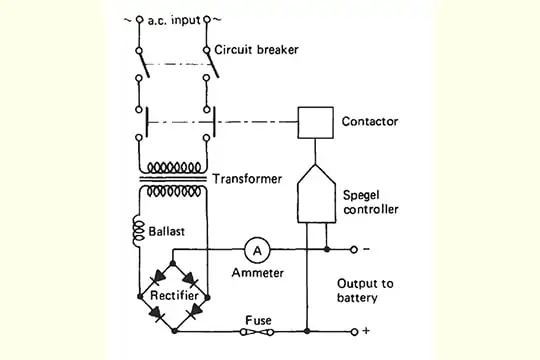

Per quanto tempo si può lasciare un caricabatterie su una batteria?
Questo dipende da due fattori:
- Se il caricatore è sotto tensione o no?
- C’è una disposizione per dare una carica rinfrescante intermittente nel caricatore?
Se il caricabatterie è spento, probabilmente non c’è alcun danno nel lasciare la batteria collegata al caricabatterie, a condizione che non ci sia un malfunzionamento di qualsiasi parte della carica, come un collegamento errato dei fili AC che portano al caricabatterie.
Tuttavia, se il caricatore è acceso, la batteria dovrebbe essere preferibilmente scollegata in modo che gli effetti deleteri del sovraccarico non riducano la durata della batteria.
Nel caso in cui ci sia una disposizione per dare una carica intermittente di rinfresco nel caricatore, si può lasciare la batteria collegata al caricatore. Questo aiuterà a mantenere la batteria in una condizione di carica completa e può essere utilizzato ogni volta che la batteria è necessaria.
Come funziona un caricabatterie per auto?
Il sistema elettrico automobilistico è costituito dai seguenti componenti:
Il sistema di avviamento, illuminazione e accensione (sistema SLI) ha componenti/attrezzature sia meccaniche che elettriche che lavorano all’unisono per far girare il motore e mantenere il veicolo in buon funzionamento.
I componenti principali sono:
- Interruttore di accensione
- La batteria di 12V o 24 V.
- Motore d’avviamento (o motore di avviamento) in corrente continua a coppia elevata con componenti associati
- Disposizione alternatore-raddrizzatore
- Controllori o regolatori di tensione (relè cut-out e cut-in)
Quando il conducente accende l’interruttore di accensione, una forte corrente scorre dalla batteria al motorino di avviamento attraverso un circuito di controllo e il motorino di avviamento può far girare le ruote e così il veicolo comincia a muoversi.
Lo scopo di un motorino d’avviamento è quello di aiutare il motore a raggiungere una certa velocità in modo che possa funzionare. Lo starter aiuta quindi il motore a raggiungere la velocità prevista per far funzionare l’auto. Una volta fatto, lo starter non è più utile e quindi si spegne.
Nel caricabatterie automatico, un circuito sensore di tensione è incorporato per rilevare la tensione della batteria sotto carica. Il caricatore si spegne automaticamente quando la tensione della batteria raggiunge il livello ottimale richiesto.
La corrente scorre lungo un unico cavo dal terminale positivo della batteria al componente da alimentare, e di nuovo alla batteria attraverso il corpo metallico dell’auto (che è fatto la terra, il terminale negativo della batteria è collegato al corpo dell’auto). Il corpo è collegato al terminale di terra (terminale negativo) della batteria con un cavo spesso.
La corrente fornita dalla batteria al motorino d’avviamento è da 3 a 4 volte la capacità della batteria, da 150 a 400 ampere). Cioè, la batteria fornisce una corrente di 3C a 4C ampere al motorino di avviamento. Pertanto, il cavo che trasporta questa corrente dovrebbe essere adeguatamente progettato per la minima caduta di tensione. Le due funzioni principali del sistema d’accensione dell’automobile sono di produrre abbastanza tensione in modo che possa facilmente creare una scintilla per bruciare la miscela aria/combustibile e in secondo luogo esercita il controllo sulla tempistica della scintilla e la trasmette al cilindro adatto. Un tipico sistema di accensione di un’automobile produce una tensione compresa tra 20000 e 50000 volt da una fonte di 12 volt.
La dimensione della batteria varia con la capacità dell’auto. Così, per una piccola auto come Maruti 800 o Alto, si usa una batteria da 12V/33 Ah, mentre per un camion Tata o Benz si usa una batteria da 12V o 24 V/180 Ah.
Un sistema di ricarica dell’automobile genera generalmente una tensione tra 13,5 e 14,4 volt quando il motore è in funzione. Produce corrente elettrica per far funzionare le luci dell’automobile, i sistemi musicali, il riscaldamento, il sistema elettrico del motore. Molto tempo fa, i generatori di corrente continua erano usati nelle automobili. All’inizio degli anni 60, il sistema alternatore-raddrizzatore sostituì il generatore a corrente continua a causa dei suoi vantaggi sull’altro. Ma con i progressi in campo elettrico ed elettronico, tutte le auto usano un alternatore-raddrizzatore (la corrente alternata viene generata e convertita in corrente continua).
Nei motori ad accensione comandata, è necessario un dispositivo per accendere la miscela aria-carburante compressa alla fine della corsa di compressione. Il sistema di accensione soddisfa questo requisito. È una parte del sistema elettrico che porta la corrente elettrica alla tensione richiesta alla candela che genera la scintilla al momento giusto. Consiste in una batteria, un interruttore, una bobina di accensione del distributore, candele e il cablaggio necessario.
Un motore ad accensione per compressione, cioè un motore diesel non richiede alcun sistema di accensione, perché l’autoaccensione della miscela carburante-aria avviene quando il diesel viene iniettato nell’aria compressa ad alta temperatura alla fine della corsa di compressione.
Per evitare che la batteria si scarichi, i produttori impiegano un regolatore di tensione / Cut-Out. Collega/scollega il generatore dalla batteria.
Quando l’uscita del generatore è inferiore alla tensione della batteria, allora disconnette il generatore dalla batteria. Al contrario, quando l’uscita è più alta, collega il generatore di nuovo alla batteria. In questo modo, impedisce alla batteria di scaricarsi alle basse velocità del motore. Quando la tensione del terminale della batteria raggiunge circa 14,0-14,4 V. il relè di disattivazione disconnette la batteria dal circuito di carica.
Posso avviare l'auto con il caricabatterie collegato?
Se non si può avviare il veicolo con la batteria esistente, si può fornire una tensione continua appropriata da un caricatore collegando i cavi del caricatore come se fossero i terminali di un’altra batteria simile. Questo è proprio come avviare un veicolo con il jump-start. Bisogna prendere le dovute precauzioni prima di fare questo lavoro. Bisogna cercare l’aiuto di un professionista.
Quali sono i migliori caricabatterie in base all'applicazione?
Caricabatterie inverter
Gli inverter sono dispositivi elettrici/elettronici che convertono la corrente continua dalle batterie alla corrente alternata per alimentare le esigenze delle case o dei piccoli stabilimenti. Il raddrizzatore svolge la funzione inversa. Cioè il raddrizzatore converte la corrente alternata in corrente continua. La corrente continua è il tipo di corrente elettrica necessaria per caricare la batteria e per far funzionare alcuni dispositivi.
Gli inverter domestici hanno normalmente una o due batterie da 12 V a seconda delle esigenze di potenza delle singole case.
Uninterrupted Power Supply (UPS) è un dispositivo simile, ma il ritardo tra l’interruzione dell’alimentazione di rete e la ripresa da parte dell’UPS è immediato (zero-time delay), mentre in un inverter il ritardo è di 10-20 millisecondi. In alcune unità di produzione e banche, questo ritardo si tradurrà in un’enorme perdita e imbarazzo per i clienti e i banchieri. Per esempio, in un computer desktop domestico, lo schermo si oscura quando è collegato a un inverter, mentre non si sente l’interruzione di corrente nel caso di un UPS.
Come sappiamo bene, se le batterie vengono caricate a tensioni superiori a 14,4 V per una batteria da 12 V, dalle batterie si sprigionano odiosi fumi maleodoranti e indesiderati odori di uova marce, oltre alla formazione di prodotti di corrosione intorno ai terminali e ai connettori, Quindi, queste batterie non possono raggiungere tensioni di carica superiori a circa 14,0 V e il valore di regolazione preferito è 13,8 V. A causa della tensione di carica ridotta, si riduce anche la perdita di acqua dovuta all’elettrolisi, con conseguenti lunghi intervalli tra due rabbocchi con acqua approvata. E un raddrizzatore a onda piena con filtri è una buona aggiunta.
Caricabatterie per auto
Il sistema elettrico dell’automobile si occupa della ricarica della batteria SLI di bordo. Come discusso in carica modificata a potenziale costante, il sistema ha una resistenza inclusa in serie per mantenere la corrente di picco iniziale entro il limite consentito. La tensione massima di carica è da 14,0 a 14,4 V per una batteria da 12 V. La batteria SLI, essendo una batteria a ciclo superficiale, riceve la carica ogni volta che la tensione scende a un livello predeterminato.
Per la ricarica, la batteria è collegata allo statore dell’alternatore attraverso un dispositivo elettronico chiamato diodo, che permette un flusso di solo in una direzione, cioè la corrente dallo statore alla batteria e non nella direzione inversa quando l’alternatore è al minimo.
Pertanto, impedisce la scarica indesiderata del pacco batterie.
Il relè di arresto agisce come un interruttore tra il sistema di carica e la batteria quando l’alternatore non sta generando alcuna corrente. Impedisce lo scarico della batteria nel caso in cui il generatore non funzioni o funzioni a velocità molto basse.
L’aggiunta periodica di acqua è un requisito di manutenzione nelle versioni precedenti delle batterie. Ma, le batterie avanzate hanno bassi livelli di gas e l’aggiunta di acqua è quasi eliminata, o una volta in 12 a 18 mesi.
Caricabatterie per applicazioni fisse
Una batteria fissa è la fonte di alimentazione di emergenza in diverse installazioni, dove l’interruzione dell’alimentazione anche per una frazione di secondo non è tollerabile. Le grandi installazioni di batterie che sono chiamate solo per un tempo molto breve a fornire energia sono chiamate alimentazioni stazionarie o di standby o di emergenza. Vengono utilizzati nelle utility, nei quadri elettrici e in altri ambienti industriali. Tali batterie sono utilizzate per fornire energia per il periodo iniziale fino a quando potrebbero avviare un generatore in modo che possa assumere la funzione.
Anche se ci sono diversi tipi di batterie al piombo-acido (batterie a piastre piatte, batterie Planté, batterie a piastre coniche, ecc.) e batterie al nichel-cadmio (Ni-Cd) disponibili per questa applicazione, la maggior parte degli utenti preferisce batterie stazionarie tubolari di tipo allagato, in particolare, il tipo OPzS, per questo scopo.
La caratteristica più importante di un banco di batterie stazionarie è la fornitura immediata di energia della batteria in caso di un normale guasto alla rete. Per questo motivo la batteria deve essere sempre in una condizione di piena carica pronta all’uso. Pertanto, il sistema di ricarica acquista importanza. La sua affidabilità è molto importante.
Queste batterie sono caricate in modo fluttuante a potenziale costante. Sono disponibili in gruppi di tensione di 24, 48, 72, 120 e 130 V. La capacità può variare da 40 Ah a qualche migliaio di ampere ora.
Da 6 a 50 ampere DC. Gli allarmi integrati sono inclusi per l’alta tensione CC, la bassa tensione CC, il guasto di terra positivo e negativo e la fine della scarica. Il caricabatterie industriale ha controlli digitali e un display LCD. Un certo numero di caratteristiche di sicurezza sono incluse come la protezione del filo su tutti i terminali di campo e la protezione completa dell’ingresso AC e dell’uscita DC
Semplici linee guida per l'acquisto di un caricabatterie
Le seguenti sono le linee guida per la scelta di un caricabatterie:
- Conoscere la tensione della batteria da caricare. Per una cella al piombo, per ogni cella, sono necessari 3 volt per una carica soddisfacente e normale. Così, per una batteria da 12 V, comprate un caricatore con un’uscita di 20 V DC ai terminali.
- Venendo ai dettagli in ampere (cioè la corrente): dall’etichetta della batteria, scoprite la capacità della batteria. Se la capacità è di 100 Ah con un tasso di 10 ore, allora è sufficiente una corrente del 10%. Quindi, si suggerisce un caricatore da 10 A. Ma si può anche optare per un caricatore da 15 A; allora il costo sarà più alto. Il vantaggio è che la batteria può essere caricata in un tempo inferiore. Le batterie possono assorbire correnti più elevate nei periodi iniziali. Quindi, si può caricare a 15 A per il primo 50% di ingresso e poi ridurre la corrente al 10% normale %.
- Il caricabatterie può essere dotato di un voltmetro e di un amperometro digitale o analogico. Una funzione aggiuntiva sarebbe un misuratore di Ah digitale. Inoltre, può essere aggiunta una protezione contro l’inversione di polarità. Questo proteggerà sia la batteria che il caricatore.
- Un raddrizzatore a onda intera con filtri è buono per ottenere una maggiore durata delle batterie. Un tale caricatore produrrà basse ondulazioni AC e quindi la corrosione delle griglie positive e l’aumento di temperatura dell’elettrolito durante la carica saranno minori.
- Per riassumere, per una batteria da 12 V/100 Ah, un caricabatterie valutato a 20V/10 ampere con contatori digitali e filtri con raddrizzamento a onda piena e protezione contro l’inversione di polarità è un buon acquisto.
Caricabatterie per treni
[Riferimenti: Manuale su 25 kW/4.5kW raddrizzatore elettronico cum unità di regolazione (ERRU) di SG TL &AC allenatori,) settembre 2019. “Servizi generali: Illuminazione dei treni”, da Institution of Railway Electrical Engineers (IREE), Governo dell’India, Ministero delle Ferrovie, settembre 2010].
Ovunque si vada l’elettricità è necessaria e le carrozze ferroviarie non sono esenti da luci e ventilatori. Per i pullman con aria condizionata (AC), è necessaria una buona quantità di elettricità per far funzionare le unità di condizionamento montate all’interno del pullman.
Uno dei metodi convenzionali per generare elettricità è l’uso di alternatori azionati dagli assi delle carrozze ferroviarie con una batteria di sufficiente capacità ampere-ora collegata in parallelo per alimentare l’energia alla carrozza in condizioni di bassa tensione. Questi tipi di allenatori sono chiamati allenatori “Autogeneranti (SG)”.
In queste carrozze SG, le unità raddrizzatrici e regolatrici (RRU) controllate da amplificatori magnetici sono utilizzate inizialmente per convertire l’uscita AC dell’alternatore in DC e regolare/controllare la tensione DC generata attraverso la regolazione della corrente di campo dell’alternatore. Questo impedisce anche il flusso inverso di corrente dalla batteria all’alternatore durante i periodi di non generazione.
Questa corrente continua rettificata e regolata è usata per far funzionare le varie apparecchiature elettriche e gli accessori all’interno dell’autobus e per caricare le batterie.
Le batterie al piombo della capacità di 110 V / 120 Ah10 sono disposte da unità monoblocco a 3 celle nelle carrozze a scartamento largo (B.G.) in scatole underslung. Quattro numeri di scatole di terminali di alimentazione di emergenza per la carrozza B.G. e un numero per la carrozza M.G. è fornito su ogni parete terminale per l’interconnessione della carrozza alla carrozza adiacente per ricevere il potere, nel caso la generazione viene a mancare.
Una morsettiera di emergenza numerica è fornita centralmente su ogni lato del sottotelaio per facilitare la ricarica della batteria da una fonte esterna. (Per esempio, quando il treno è inattivo sui binari del raccordo ferroviario). Per le carrozze BG AC, vengono utilizzati alternatori brushless da 18 kW / 25 kW. Due di questi alternatori sono usati in AC-2 Tier /AC-3 Tier / Chair Cars e solo un alternatore è usato nella First AC coach. Le batterie con capacità di 800 / 1100 Ah a 10 h sono utilizzate in I AC / AC-2 Tier / AC-3 Tier/chair car di B.G. Coaches.
Anche se il primo treno in India viaggiò per 34 km con 400 persone il16 aprile 1883 da Bori Bunder (ora rinominato Mumbai CST) a Thane, il sistema di illuminazione del treno (TL) attraverso la dinamo azionata dall’asse pioniere di M/s. J. Stone & Co. arrivò alle ferrovie indiane solo nel 1930. Dinamo / alternatori brushless guidati dall’asse attraverso cinghie piatte / a ‘V’, forniscono il carico quando il treno è in movimento e caricano le batterie. Le batterie alimentano il carico quando il treno è inattivo sulle piattaforme e altrove.
I seguenti sistemi per l’illuminazione dei treni sono attualmente in uso –
1) Sistema azionato dall’asse che lavora su un’alimentazione di 110 V DC.
2) Mid on generation con 415 V, 3 Fase generazione AC 110 V utilizzo.
3) Fine della generazione con generazione a 3 fasi 415 V e utilizzo di AC 110 V
4) Fine della generazione con generazione a 3 fasi 750 V e utilizzo di AC 110 V
Tutti i pullman in costruzione hanno solo un sistema a 110 V. Le carrozze che funzionano con sistemi a 24 V sono già state convertite in un sistema a 110 V.
I valori nominali standard ai terminali di uscita DC dell’ERRU per diverse potenze dell’alternatore sono riportati di seguito:
(i) 25 kW, 130V, 193A
(ii) 4,5 kW 128,5V 35A
ERRU è montato nel sottotelaio dell’allenatore e progettato per lavorare in modo soddisfacente in una temperatura che va da -5 gradi a 55 gradi C e 98% di umidità relativa. È anche progettato per lavorare in una zona molto polverosa, per resistere alle vibrazioni di servizio e agli urti di manovra.
La trasmissione della potenza avviene tramite cinghie trapezoidali. In totale 12 Nos. (6 su ogni lato) e 4 Nos. (solo un lato) di dimensioni C-122 sono forniti su alternatori AC e TL rispettivamente. La velocità dell’alternatore varia da 0 a 2500 RPM. Il diametro della ruota della carrozza è di 915 mm quando è nuova e di 813 mm quando è completamente consumata, il diametro della ruota nuova deve essere considerato per fare i calcoli della velocità del treno in km/h corrispondente alla velocità di entrata e alla velocità minima per la piena uscita (MFO) dell’alternatore.
Le caratteristiche di uscita del raddrizzatore elettronico con regolatore (ERRU) (sia 25 kW che 4,5 kW) sono riportate di seguito:
La tensione di uscita DC a vuoto è di 135 V massimo, che può essere impostata a 128 ± 0,5 V, 97 A (per batterie da 1100 e 650 Ah) e 128 ± 0,5, 19 A per batterie da120 Ah ) a 1500 giri/min (a metà strada tra la velocità minima e massima), la regolazione della tensione è ± 2 %, rendimento 95% (minimo). L’ondulazione di tensione è mantenuta entro il 2% %. La variazione di carico è da 10 A a 193 A a velocità da 400 giri/min a 2500 giri/min (per batterie da 1100 e 650 Ah) e da 350 giri/min a 2500 giri/min (batterie da 120 Ah).
Per le batterie di capacità superiore, la tensione al 15% di sovraccarico è di 120 V (minimo) a 222 A, la corrente è limitata a 230 A (massimo). Per una batteria da 120 Ah, la tensione al sovraccarico di 40 A è fissata a 115 V (minimo).
Il limite di corrente di carica della batteria è di 220 A per una batteria da 1100 Ah, 130 A per una batteria da 650 Ah e 24 A per una batteria da 120 Ah (massimo). Gli ultimi due parametri possono essere impostati dall’Universal Voltage Controller (UVC) e dal Coach Indication Panel (CIP).
Per l’EERU da 4,5 kW, la variazione di carico sarà da 1 A a 37,5 A a 350 RPM a 2500 rpm. La tensione al sovraccarico di 40 A è di 115 V (minimo), la corrente è limitata a 43A (massimo).
Possiamo vedere che la corrente di carica è 1100/220 = 5; 650/130= 5 e 120/24 = 5. Cioè la corrente di carica è limitata per tutte queste batterie è di C/5 ampere, la tensione massima è di 128 V. (cioè il 16% sopra l’OCV del banco di batterie).
Per maggiori dettagli sugli schemi a blocchi per l’Overall Coach, il cablaggio sarà come il seguente diagramma e lo schema a blocchi del sistema Alternatore-ERRU, il link dato sotto può essere riferito:
Caricabatterie di trazione
Le prestazioni e la durata delle batterie dei carrelli elevatori sono influenzate dal caricabatterie di trazione e dai metodi di ricarica utilizzati. Il caricabatterie per carrelli elevatori deve essere selezionato in conformità con la tensione e gli Ah delle batterie.
Un buon caricabatterie per carrelli elevatori
- Dovrebbe limitare l’aumento di temperatura durante la carica
- Senza sovraccaricare indebitamente, il caricatore deve smettere di fornire corrente alla batteria al momento giusto
- Dovrebbe avere un sistema di carica di equalizzazione (cioè, ricarica a correnti più alte).
- In caso di situazioni pericolose, deve essere previsto un dispositivo di autospegnimento.
- Dovrebbe essere programmabile tramite microprocessore o un PC.
- In alcuni caricatori, l’agitazione dell’aria attraverso sottili tubi d’aria nelle celle è anche fornita.
La gamma di tensione di carica varia da 24 V a 96 V.
La corrente dipende dalla capacità della batteria, che va da 250 Ah a 4000 Ah
Metodi di ricarica della batteria di trazione
Carica conica a passo singolo: Il caricatore inizia il suo lavoro a circa 16A/100Ah e la corrente si assottiglia man mano che la tensione della cella aumenta. Quando la tensione della cella raggiunge i 2,4V/cella, la corrente si riduce a 8A/100 Ah e poi raggiunge il tasso finale di 3 o 4 A/100 Ah. La ricarica viene spenta da un timer. Può richiedere circa 11-13 ore (fattore di ingresso Ah 1,20) per batterie scariche all’80% senza agitazione dell’aria.
La differenza nel tempo di carica è dovuta alla variazione della corrente di partenza, cioè, se la corrente di partenza è di 16 A/100 Ah, la durata è minore e se è di 12A/100Ah, la durata è maggiore. Con il dispositivo di agitazione dell’aria, la durata si riduce a 9-11 ore (fattore di ingresso Ah 1,10).
Carica conica a due fasi (modalità CC-CV-CC): È un miglioramento rispetto al metodo precedente. Il caricabatterie inizia con una corrente superiore di 32 A / 100 Ah. Quando la tensione delle celle raggiunge i 2,4 V per cella, il caricatore passa automaticamente alla modalità conica e la corrente continua a diminuire fino a raggiungere i 2,6 V per cella e la corrente passa a un tasso finale di 3 a 4 A/100 Ah e continua per 3 a 4 ore. Possono essere necessarie circa 8-9 ore (fattore di ingresso Ah 1,20) per batterie scariche all’80% senza agitazione dell’aria. Con il dispositivo di agitazione dell’aria, la durata si riduce a 7-8 ore (fattore di ingresso Ah 1,10).
Carica di batterie VRLA gelate: (modalità CC-CV-CC):
Il caricatore inizia con una corrente di 15 A / 100 Ah. Quando la tensione delle celle raggiunge i 2,35 V per cella, il caricatore passa automaticamente alla modalità conica e il caricatore va in modalità CV alla stessa tensione. Questo richiede un massimo di 12 ore. Il passo CV è mantenuto costante finché la corrente di carica scende a un valore limitato di 1,4 A/ 100 Ah. La seconda fase può durare alcune ore, al massimo 4 ore. Questa durata dipende dalla durata della prima fase.
Caricabatterie ad alta frequenza per carrelli elevatori
I caricatori esistenti sono generalmente di due tipi: ferro-risonanti e raddrizzatori controllati al silicio (SCR). Sono più convenienti, ma sono anche meno efficienti.
Caricabatterie che incorporano dispositivi di potenza switching ad alta frequenza, ad esempio, il MOSFET (Metal Oxide Semiconductor Field-effect Transistor) e l’IGBT (Isolated Gate Bipolar Transistor) operano a frequenze molto più alte delle frequenze di linea (da pochi kHz a un paio di centinaia di kHz). Al contrario, i MOSFET e gli IGBT, con la loro capacità full-on/off, possono essere controllati con precisione in qualsiasi momento per permettere a un caricatore di produrre l’uscita desiderata. Gli SCR sono dispositivi semicontrollati con uno spegnimento incontrollabile.
I caricatori HF funzionano come alimentatori a commutazione, il che significa che accendono e spengono gli interruttori elettronici ad alte frequenze (50-170 kHz).
I vantaggi di questa tecnologia HF includono:
| Caricabatterie ad alta frequenza | |
|---|---|
| Fino a 170 kHz Alta frequenza | Le perdite da conversione sono inferiori |
| Efficienza di carica migliorata (dall'87 al 95%) | Costo energetico inferiore (fino al 20%) grazie al risparmio energetico |
| Corrente di ondulazione AC ridotta | Maggiore durata grazie al minore aumento della temperatura. Minori costi di manutenzione grazie alle minori perdite d'acqua |
| È universalmente adattabile | Le batterie allagate, AGM e al gel possono essere tutte caricate senza alcun sovraccarico o sottocarico. |
| Dimensioni ridotte, peso inferiore e maggiore risparmio di spazio | Ha un ingombro ridotto e può essere facilmente montato a bordo |
| Tali caricatori sono disponibili in diverse gamme, da caricatori per batterie da 24 V a 80 V con una corrente di carica da 40 a 300 A. | |
Caricabatterie per applicazioni di batterie per miniere sotterranee
Le batterie delle miniere sotterranee sono principalmente batterie al piombo-acido a ciclo profondo. La tensione tipica varia tra 48 e 440 V, e la capacità varia da 700 Ah a 1550 Ah.
La ricarica di queste batterie è simile a quella delle batterie da trazione. Le batterie sono caricate a
2,6 V inizialmente con una corrente di 21 A a 17 A per 100 Ah e infine 4,5 A per 100 Ah come tasso di finitura. La ricarica può essere completata in 6-8 ore.
Le batterie sono conformi a IS 5154:2013 Parte 1 (IEC 60254-2006)
Caricabatterie marino
Le batterie per applicazioni marine possono essere classificate in due tipi. Le batterie di avviamento hanno piastre più sottili e sono in grado di fornire grandi raffiche di potenza per un breve periodo. L’altro tipo è una batteria a ciclo profondo usata per altre applicazioni marine come accessori elettronici, un trolling motor e apparecchi elettrici ed elettronici a bordo. Inoltre, le batterie a doppia funzione funzionano sia come batterie SLI che come batterie a ciclo profondo. Si usano caricatori specifici per batterie specifiche. La modalità CC-CV dovrebbe essere usata sulle batterie al piombo VR.
Ci sono anche caricatori che possono caricare fino a quattro batterie simultaneamente. Si possono caricare tutti i tipi di batterie marine, le batterie VR (sia AGM che gel) e le batterie allagate a bassa manutenzione.
Dato che le batterie e i caricabatterie sono usati nelle barche, devono rimanere asciutti e avere un’ampia ventilazione. Dovrebbero anche essere impermeabili, antiurto e resistenti alle vibrazioni e, se necessario, completamente sigillati. Inoltre, dovreste assicurarvi che i caricabatterie abbiano una funzione di protezione contro l’inversione di polarità e capacità a prova di scintilla.
Caricabatterie per applicazioni solari
A causa delle variazioni dell’irradiazione solare, l’uscita dei pannelli SPV fluttua. Di conseguenza, un inseguitore digitale del punto di massima potenza (MPPT) è collegato tra il pannello SPV e la batteria per garantire un processo di carica senza preoccupazioni. Un MPPT è un convertitore elettronico DC to DC progettato per ottimizzare la corrispondenza tra il campo solare (pannelli fotovoltaici) e il banco batterie. Rileva l’uscita DC dai pannelli solari, la cambia in AC ad alta frequenza e scende ad una diversa tensione e corrente DC per soddisfare esattamente i requisiti di potenza delle batterie. Il vantaggio di avere un MPPT è spiegato di seguito.
La maggior parte dei pannelli fotovoltaici sono costruiti per un’uscita da 16 a 18 volt, anche se la tensione nominale del pannello SPV è di 12 V. Ma una batteria da 12 V nominali può avere una tensione effettiva da 11,5 a 12,5 V (OCV) a seconda dello stato di carica (SOC). In condizioni di carica, una componente extra di tensione deve essere fornita alla batteria. Nei normali regolatori di carica, la potenza extra prodotta dal pannello SPV viene dissipata come calore, mentre un MPPT rileva i requisiti della batteria e dà una potenza maggiore se il pannello SPV produce una potenza maggiore. Così, lo spreco, il sottocarico e il sovraccarico sono evitati usando un MPPT.
La temperatura influisce sulle prestazioni del pannello SPV. Quando la temperatura aumenta, l’efficienza del pannello SPV diminuisce. (Nota: quando il pannello SPV è esposto a una temperatura più alta, la corrente prodotta dal pannello SPV aumenterà, mentre la tensione diminuirà. Poiché la diminuzione della tensione è più veloce dell’aumento della corrente, l’efficienza del pannello SPV diminuisce). Al contrario, a temperature più basse, l’efficienza aumenta. A temperature inferiori a 25°C (che è la temperatura delle condizioni di prova standard(STC), l’efficienza aumenta. Ma l’efficienza si bilancerà nel lungo periodo.




