Pengisi Daya Baterai - mengisi baterai asam timbal
Baterai dapat didefinisikan sebagai perangkat elektrokimia yang dapat mengubah energi kimia dalam bahan aktifnya menjadi energi listrik. Jika reaksi yang mengarah pada pengubahan satu bentuk energi menjadi bentuk energi yang lain bersifat reversibel, maka kita memiliki sel yang dapat diisi ulang atau sekunder atau penyimpanan. Sel-sel tersebut dapat diisi ulang berulang kali setelah setiap pelepasan untuk membalikkan arah reaksi. Agar baterai dapat memberikan masa pakai yang dimaksudkan, baterai harus menerima pengisian daya yang tepat bila diperlukan.
Sel-sel dengan reaksi ireversibel disebut sel primer.
Baterai timbal-asam terdiri dari elektroda positif dan negatif yang dipisahkan oleh film isolasi yang disebut separator. Larutan asam sulfat encer digunakan sebagai elektrolit. Bahan aktif positif adalah timbal dioksida (PbO2) dan bahan aktif negatif adalah timbal.
Sebelum kita mempelajari detail Pengisi Daya Baterai, perlu dipahami secara singkat beberapa hal yang terkait dengan baterai.
Ampere adalah satuan untuk arus (yang didefinisikan sebagai aliran elektron yang kontinu). Ketika satu coulomb (atau satu ampere-detik) bergerak melewati suatu titik dalam satu detik, arus didefinisikan sebagai 1 ampere.
Tegangan dapat diambil sebagai kekuatan pendorong bagi elektron untuk mengalir dalam konduktor elektronik dan satuannya adalah volt. Ketika 1 ampere-sekon memiliki energi 1 joule, kita katakan bahwa ia memiliki beda potensial listrik 1 volt.
Kedua istilah ini dapat disamakan dengan tangki air di atas gedung. Semakin tinggi tangki air, semakin tinggi kekuatan yang dengannya air akan mengalir. Demikian pula, semakin besar diameter pipa yang membawa air dari tangki ke titik pengguna, semakin tinggi volume air yang diterima pengguna. Air yang mengalir di dalam pipa dapat dibandingkan dengan laju aliran air.
Ampere jam (Ah) adalah jumlah listrik, dan itu adalah produk dari arus dan waktu.
1 Ah = 1 A * 1 jam.
Watt (W) adalah daya, dan merupakan produk dari arus dan volt. Satuan yang lebih tinggi adalah kW (= 1000 W).
mega watt, MW (=1000 kW) dan Giga watt, GW (satu miliar W (1.000.000.000 Watt).1 W = 1 A * 1 V = VA.
Energi (Wh) adalah jumlah daya yang disuplai dalam satuan waktu. Satuan yang lebih tinggi adalah kWh (= 1000 Wh)
megawatt-jam, MWh (= 1000 kWh) dan Giga Watt-jam, GWh (=(satu miliar Wh (1.000.000.000 Watt-jam).
Unit GW digunakan untuk merujuk ke output dari pembangkit listrik besar. GWh digunakan untuk merujuk pada kapasitas produksi industri baterai kendaraan listrik (EV) besar dan sistem penyimpanan baterai berkapasitas besar Wh = 1 W* 1 h = 1 Wh
Dalam bahasa baterai, baterai dapat dikatakan memiliki 1200 Wh (atau 1,2 kWh) jika tegangannya 12 dan kapasitasnya dalam Ah adalah 100.
12 V * 100 Ah = 1200 Wh atau 1,2 kWh.
Daya yang disuplai oleh satuan massa baterai disebut daya spesifik dan satuannya adalah W per kg.
Daya spesifik r = W/kg dan kW/kg.
Demikian pula, energi yang disuplai oleh satuan massa baterai disebut energi spesifik dan satuannya adalah Wh per kg.
Energi spesifik = Wh / kg dan kWh / kg. (Juga ditulis sebagai Wh kg-1)
Demikian pula, daya yang disuplai oleh satuan volume baterai disebut kerapatan daya dan satuannya adalah W per liter.
Kepadatan daya = W / liter dan kW / liter.
Energi yang disuplai oleh satuan volume baterai disebut kerapatan energi dan satuannya adalah Wh per liter.
1 W = 1 J per detik
Kerapatan energi = Wh / liter dan kWh / liter. (Juga ditulis sebagai WL -1 atau W l -1 )
Reaksi pelepasan muatan sel timbal-asam adalah:
Pb (NP) + PbO 2 (PP) + 2H 2 SO 4 Debit ⇔ Muatan PbSO 4 (PP) + PbSO 4 (NP) + 2H 2 O (Mendekati PP)
Catatan: NP = pelat negatif = anoda selama pelepasan = donor elektron selama pelepasan. PP = pelat positif = katoda selama pelepasan = akseptor elektron selama pelepasan
Peran elektroda akan terbalik selama pengisian; anoda akan berperilaku sebagai katoda dan sebaliknya. Akseptor elektron sekarang akan melepaskan elektron dan donor akan menerimanya.
Istilah energi bebas termodinamika adalah ukuran kerja yang dapat diambil dari suatu sistem. Dalam kasus sel galvanik, pekerjaan listrik dilakukan melalui pergerakan partikel bermuatan karena interaksi kimia antara reaktan untuk menghasilkan resultan (produk).
Oleh karena itu, energi diberikan dalam G , perubahan energi bebas Gibb , yang mewakili jumlah maksimum energi kimia yang dapat diekstraksi dari proses konversi energi.
Jika E adalah ggl (gaya gerak listrik atau tegangan atau potensial) sel dan proses yang terjadi (yaitu, pelepasan sel timbal-asam ), dikaitkan dengan lewatnya n Faraday ( F ) per mol reaktan dari satu elektroda ke elektroda lainnya, maka kerja listrik yang dilakukan oleh sel diberikan sebagai nFE . Peningkatan energi bebas yang sesuai sama dengan kerja listrik yang dilakukan pada sistem. Karena itu,
G = nFE atau
G = -nFE atau
-ΔG° = nFE°
(dalam kondisi standar; E° mengacu pada potensial elektroda standar atau tegangan sel standar).
persamaan Gibbs
(Apa yang dimaksud dengan kondisi standar? : 25°C atau Celcius (298.1°K atau Kelvin), tekanan 1 bar, dan aktivitas (yang dapat diambil kira-kira sebagai nilai konsentrasi) dari spesi yang bereaksi, Pb 2+ , adalah satu).
Persamaan ini disebut persamaan Gibbs.
Persamaan Gibbs menghubungkan tegangan sel dengan perubahan energi bebas (DG). Jika reaksi terjadi secara spontan (misalnya pelepasan sel timbal-asam ), G negatif (energi dibebaskan) dan ggl positif yaitu, muatan nF akan mengalir secara spontan ke arah yang diasumsikan dalam reaksi sel.
Di sisi lain, jika G positif, memungkinkan sistem untuk melakukan fenomena elektrolisis (yaitu, selama pengisian sel timbal-asam ).
EMF sel
Ggl sel adalah properti termodinamika intensif yaitu, tidak tergantung pada massa reaktan dan ukuran sel. Sifat intensif (berlawanan dengan sifat ekstensif ) tidak bergantung pada massa reaktan dan oleh karena itu ukuran baterai. Apakah Anda memiliki beberapa miligram atau beberapa kilogram bahan, sistem akan menunjukkan tegangan yang sama dan tidak dapat ditingkatkan dengan meningkatkan massa bahan. Potensial elektroda individu adalah sifat elektrokimia yang melekat dari bahan elektroda itu, dan seseorang tidak dapat mengubah nilainya dalam kondisi yang sama.
Contoh untuk sifat intensif adalah tegangan elektroda dan sel; di sisi lain, sifat ekstensif tergantung pada jumlah zat, misalnya massa, volume, energi, ampere hour dan watt hour. Jadi, 4,5 gram bahan aktif timbal dioksida dalam sel timbal-asam akan menghasilkan satu ampere jam (Ah) secara teoritis, tetapi jika Anda memiliki 45 gram, itu akan menghasilkan sepuluh kali Ah. Jadi, ini adalah properti yang luas; bur dalam kedua kasus potensi elektroda akan sama, yaitu, 1,69 V. Argumen serupa dapat diajukan untuk bahan aktif timbal dan asam sulfat.
Potensial sel standar (E°) terkait dengan perubahan energi bebas standar (DG°) seperti yang diberikan di atas.
Ggl sel timbal-asam dapat ditentukan dari ekspresi
Gº produk – Gº reaktan
Dimana G° mengacu pada energi bebas standar pembentukan spesi yang bereaksi.
Energi bebas pembentukan standar
Tabel 1
Energi bebas pembentukan standar, G° spesies kimia yang berpartisipasi dalam reaksi sel
( Hans Bode, Baterai Asam Timbal, John Wiley, New York, 1977, Lampiran IV, hlm. 366. )
| Reaktan/Produk | Nilai Numerik (k kal mol−1 ) |
|---|---|
| PbO2 | -52.34 |
| Pb | 0 |
| H2SO4 | -177.34 |
| PbSO4 | -193.8 |
| H2O | -56.69 |
Reaksi keseluruhan ditulis sebagai
Pb + PbO 2 + 2H 2 SO 4 2PbSO 4 + 2H 2 O E° = 2,04 V.
G° = Gº produk – Gº reaktan
Dengan mengganti nilai masing-masing dari (yang kita dapatkan dari Standard Textbooks, misalnya, [1. Hans Bode, Lead-Acid Batteries, John Wiley, New York, 1977, Appendix IV, p. 366 ]
= [2 ( 193 . 89) + 2 ( 56 . 69) ] [ 0 ( 52 . 34) + 2 ( 177 . 34)]
= 94 . 14 kkal mol 1
= 94 . 14 kkal mol 1 × 4 . 184 kJ mol 1 ( untuk mengubah kkal ke kJ kalikan dengan 4,184)
= 393 . 88 kJ per mol
E° = -ΔG°/nF
= ( 393 . 88 × 1000) / 2 × 96485
= 2 . 04 V untuk sel timbal-asam
Tegangan sel standar dari sel timbal-asam adalah 2,04 V
dan reaksi sel keseluruhan atau total dari sel timbal-asam ditulis sebagai:
Pelepasan Pb + PbO 2 + 2H 2 SO 4⇔Pengisian PbSO 4 (PP) + PbSO 4 ( NP) + 2H 2 O (Mendekati PP)
Sebelum kita masuk ke rincian pengisian dan pemakaian sel timbal-asam, kita harus memiliki pengetahuan tentang istilah-istilah tertentu yang digunakan dalam Elektrokimia.
Kita telah mengetahui pengertian syarat baku .
Ketika kita mengganggu reaksi sel (apakah dalam arah maju atau mundur), kita mengatakan sel dalam kondisi terganggu dan tidak dalam kondisi setimbang.
Setiap kali sistem elektrokimia terganggu, akan selalu ada perbedaan dari potensial standar. Jadi, jika sel timbal-asam dipaksa ke arah pelepasan tegangan sel berkurang dengan nilai tertentu, yang tergantung pada besarnya arus. Semakin tinggi nilai saat ini, semakin banyak penyimpangan dari nilai standar.
Sekarang tegangan sel akan menjadi
E Disch = E° – V.
Nilai E Disch akan lebih rendah dari E°.
Sebaliknya, jika sel dipaksa ke arah sebaliknya (yaitu, mode pengisian), tegangan sel akan meningkat dengan nilai tertentu yang sekali lagi tergantung pada besarnya arus.
E Ch = E° + V.
Nilai V disebut tegangan lebih atau potensial lebih dan dilambangkan dengan simbol .
Nilai V akan negatif untuk reaksi pelepasan dan positif untuk reaksi muatan.
Fenomena kematian atau peningkatan tegangan sel ini disebut polarisasi dan elektroda dikatakan dalam keadaan terpolarisasi.
Jadi, kita tulis ulang persamaannya sebagai berikut:
E Disch = E° – .
E Ch = E° + .
Jadi terlihat bahwa selama debit
E Disch< E° dan
Selama pengisian
E Ch> E°.
Apa alasan penyimpangan tegangan ini?
Ada beberapa penyebab penyimpangan ini:
- Rugi karena resistansi internal (IR) (η ohmik )
- Polarisasi aktivasi akibat transfer muatan pada kedua elektroda pada saat dimulainya proses t .
- Polarisasi konsentrasi karena penipisan elektrolit dan spesies lain yang berpartisipasi (η c ).
Kerugian akibat polarisasi IR dapat dikurangi dengan menggunakan pengumpul arus elektroda dan elektrolit yang memiliki konduktivitas yang lebih baik. Pemisah dengan resistansi yang lebih rendah juga akan membantu.
Polarisasi aktivasi terkait dengan transfer pembawa muatan melintasi batas fase elektroda dan proses ini disebut sebagai reaksi transfer. Tegangan lebih transfer karena reaksi transfer muatan pada dua elektroda dapat sangat dikurangi dalam elektroda baterai dengan memiliki struktur berpori yang kompatibel. Yang terakhir meningkatkan luas permukaan internal yang sebenarnya (luas permukaan BET, yang mencakup area pori-pori, retakan, dan celah) sebagai lawan dari luas permukaan yang diperoleh dengan perkalian dimensi, panjang, dan lebar) yang tersedia untuk reaksi.
Kepadatan arus
Hal ini pada gilirannya mengurangi kerapatan arus (yaitu, ampere per cm persegi). Dengan demikian, pelat dengan porositas agregat 40% akan menyebabkan kerugian yang lebih tinggi karena polarisasi aktivasi daripada pelat dengan porositas 50%.
Polarisasi konsentrasi (η c) akan lebih banyak jika produk reaksi (timbal sulfat dan molekul air, dalam kasus sel timbal-asam) tidak dipindahkan dari permukaan elektroda untuk memberi jalan bagi reaktan baru (misalnya ion timbal dari elektroda dan ion sulfat dari elektrolit dalam kasus sel timbal-asam). ηc akan lebih jelas menjelang akhir reaksi pelepasan. Di dalam sel, pengangkutan ion dilakukan dengan difusi dan migrasi .
Difusi disebabkan oleh perbedaan konsentrasi, sedangkan migrasi disebabkan oleh gaya medan listrik.
Difusi dapat terjadi di sebagian besar elektrolit atau pemisah: karena ion dihasilkan pada satu elektroda dan dikonsumsi di elektroda lain, ion harus bergerak di antara elektroda.
Ini juga terjadi pada elektroda berpori saat reaksi elektrokimia berlangsung. Produk reaksi dapat bergerak dalam massa aktif ke lokasi akhir mereka dengan difusi.
Bagian dari total arus yang dibawa oleh spesies ionik tertentu (partikel bermuatan) oleh migrasi adalah fungsi dari nomor transferensi mereka. Dalam elektrolit biner, disosiasi menjadi kation dan anion, bilangan transferensi dihubungkan oleh persamaan:
C + A = 1,
di mana C + A menunjukkan jumlah transpor kation dan anion.
Bilangan transferensi bergantung pada konsentrasi ion dan suhu. Dalam larutan garam biner mereka hampir mendekati 0,5. Jadi kedua spesies ionik berbagi sama dalam konduktivitas ionik.
Penyimpangan yang signifikan terjadi pada asam kuat dan basa karena mobilitas ion yang lebih tinggi dari proton (H + ) dan ion hidroksil (OH – ). Nilai untuk asam sulfat elektrolit baterai (terurai menjadi H + dan HSO 2- 4 ) dan kalium hidroksida (terurai menjadi K + dan OH – ) diberikan di bawah ini. 4
H + = 0 . 9; HSO4 2- = 0 . 1; K + = 0 . 22; OH- = 0 . 78
Bilangan transferensi adalah ukuran seberapa besar konsentrasi ion tertentu dipengaruhi oleh migrasi akibat aliran arus. Nilai yang lebih kecil menunjukkan pengaruh yang lebih kecil pada proses migrasi dan nilai yang lebih tinggi menunjukkan pengaruh yang lebih besar pada proses migrasi.
2. D. Berndt, dalam Buku Pegangan Teknologi Baterai, Ed. HA Kiehne, Edisi Kedua, 2003, Marcel Dekker, Inc., New York, Tabel 1.2.
3. JS Newman. Sistem Elektrokimia. Tebing Englewood: Prentice-Hall, 1991, hal 255.
4. SU Falk, AJ Salkind. Baterai Penyimpanan Alkali. New York: John Wiley & Sons, 1969, hal 598
Untuk memperjelas, kita harus memahami bagaimana reaksi pelepasan berlangsung. Segera setelah terminal baterai terhubung ke peralatan konsumsi, elektron mulai mengalir dari pelat negatif ke terminal positif melalui sirkuit eksternal. Di dalam sel, adalah tugas partikel bermuatan untuk menjaga aliran arus. Partikel bermuatan adalah proton (H + ) dan ion bisulfat (HSO¯4).
Selama pelepasan, ion negatif HSO¯4 (dalam hal ini, ion bisulfat dari elektrolit asam sulfat yang berdisosiasi sebagai H + dan HSO¯4) bergerak menuju pelat negatif. Ion negatif ini digabungkan dengan bahan aktif, Pb, menghasilkan, timbal sulfat, PbSO 4 . Reaksi ini juga menghasilkan ion hidrogen bermuatan positif yang disebut proton) yang bermigrasi. Dua elektron yang dilepaskan sebagai hasil reaksi anodik dari bahan aktif timbal, mencapai terminal positif melalui sirkuit eksternal.
Lempeng negatif atau reaksi setengah sel negatif: Pb + HSO¯4 Pb 2+ + SO4 2- +H + + 2e – E°= -0,35 V
Ion timbal bivalen dan ion sulfat segera bergabung membentuk timbal sulfat dan terdeposit pada pelat negatif sebagai timbal sulfat.
Sejauh ini, kita telah melihat gambaran reaksi pelat negatif.
Sekarang mari kita lihat apa yang terjadi secara bersamaan pada pelat positif.
Elektron dari pelat negatif, setelah mencapai terminal positif, bereaksi dengan bela diri aktif positif, PbO 2 , untuk membentuk timbal sulfat dan dua molekul air.
Lempeng positif atau reaksi setengah sel positif: PbO 2 + 3H + + HSO¯4 + 2e – Pb 2+ + SO 4 2- + 2H 2 O E° = 1,69 V
Ion timbal bivalen (Pb 2+ ) dan ion sulfat ( ) segera bergabung membentuk timbal sulfat dan terdeposit pada pelat positif sebagai timbal sulfat.
Mekanisme disolusi-deposisi atau disolusi-presipitasi
Jenis reaksi ini, di mana timbal dan timbal dioksida larut sebagai ion timbal dan segera disimpan sebagai timbal sulfat pada elektroda masing-masing, terjadi melalui mekanisme disolusi-deposisi atau disolusi-presipitasi.
Sekarang dengan menggabungkan dua reaksi setengah sel, kita mendapatkan
Lempeng negatif atau reaksi setengah sel negatif: Pb + HSO¯4 Pb 2+ + SO4 2- +H + + 2e –
Lempeng positif atau reaksi setengah sel positif: PbO 2 + 3H + + HSO¯4 + 2e – Pb 2+ + SO4 2- + 2H 2 O
Keseluruhan atau reaksi total: Pb + PbO 2 + 2H 2 SO 4 Debit⇔Muatan 2PbSO 4 + 2H 2 O
Teori reaksi ini diusulkan oleh Gladstone and Tribe pada tahun 1881, tetapi sel timbal-asam ditemukan pada tahun 1859 oleh Raymond Gaston Planté, Fisikawan Prancis.
JH Gladstone dan A. Tribe, Kimia Akumulator Planté dan Fauré, Alam , 25 (1881) 221 & 461.
JH Gladstone and A. Tribe, Chemistry of Planté and Fauré Accumulators, Nature, 26 (1882) 251, 342 & 602; 27 (1883) 583
Reaksi pelepasan akan berlanjut sampai sekitar setengah dari bahan aktif diubah menjadi timbal sulfat untuk laju pelepasan yang lambat, seperti laju 20 atau 10 jam. Pada saat ini, resistivitas bahan aktif akan meningkat sedemikian rupa sehingga pelepasan lebih lanjut akan menghasilkan penurunan tegangan sel yang sangat cepat. Biasanya, tegangan sel tidak diperbolehkan untuk kurang dari 1,75 V per sel.
Debit dalam di luar 80% depth of discharge (DOD) akan membuat pengisian berikutnya lebih sulit.
Segera setelah timbal larut sebagai ion timbal selama reaksi pelepasan, ia bergabung dengan ion sulfat dan disimpan di pelat negatif. Ion timbal atau molekul timbal sulfat tidak menjauh dari pelat negatif. Hal ini karena kelarutan timbal sulfat dalam larutan asam sulfat encer sangat rendah. Pada orde di atas 1 mg per liter, pengendapan ion timbal bivalen menjadi timbal sulfat akan lebih cepat di tempat-tempat di mana terdapat konsentrasi elektrolit yang tinggi. Saat pelepasan berlangsung lebih jauh, kelarutan timbal sulfat dalam elektrolit meningkat hingga 4 mg per liter.
Hal ini terjadi karena asam menjadi lebih encer karena pelepasan lebih lanjut dan dalam asam encer tersebut, kelarutan timbal sulfat lebih tinggi, hingga 4 mg per liter..
Timbal sulfat yang diendapkan akan terus bertambah hingga berbagai ukuran kristal baik di permukaan maupun retakan dan celah-celah. . Film ini akan terputus-putus dalam struktur. Selama proses pelepasan yang lambat, bentuk struktur sulfat timbal yang terputus ini membantu bagian dalam bahan aktif untuk berpartisipasi dalam reaksi karena memberikan struktur terbuka yang memudahkan masuknya ion. Oleh karena itu, proses pelepasan dapat berlanjut jauh ke bagian dalam pelat.
Sebaliknya, pada tingkat pelepasan yang tinggi, permukaan terhalang oleh produk pelepasan, PbSO 4 , yang membentuk struktur kontinu tanpa putus. Dengan demikian, reaksi lebih lanjut di bagian dalam pelat terhambat dan itulah sebabnya kami tidak dapat memperoleh kapasitas yang diharapkan pada laju pelepasan yang lebih tinggi.
Pengisian baterai timbal-asam
Selama reaksi pengisian, fenomena sebaliknya terjadi, aliran arus dibalik dan oksidasi terjadi
diletakkan pada elektroda positif dan reduksi pada elektroda negatif.
Meja 2
Karakteristik kedua elektroda selama pengisian dan pengosongan
| Elektroda | Pengosongan | Pengisian |
|---|---|---|
| Pelat Negatif |
Timbal Berpori (Sepon) Anoda Melepaskan 2 elektron Pb -2e- → Pb2+ Tegangan berkurang (menjadi kurang positif). Diubah menjadi PbSO4 |
~ 40% Pb + ~ 60% PbSO4 Katoda Menyerap 2 elektron Pb2+ dalam PbSO4 mengambil 2 elektron Tegangan berkurang (menjadi lebih negatif) Dipulihkan menjadi logam Pb H2 berevolusi selama overcharge |
| Piring Positif |
Timbal dioksida berpori Katoda Menyerap 2 elektron Pb4+ (dari PbO2) + 2e- → Pb2+ Tegangan berkurang (menjadi kurang positif). Diubah menjadi PbSO4 |
~ 50% PbO2 + ~50% PbSO4 Anoda Melepaskan 2 elektron Pb2+ dalam PbSO4 menjadi PbO2 Diubah kembali menjadi PbO2 Tegangan meningkat O2 berevolusi selama overcharge |
Gambar 1
Ubah nilai potensial sel timbal-asam selama reaksi pengisian dan pengosongan
Tegangan sel adalah kombinasi dari dua nilai pada setiap tahap fungsi sel galvanik
Jadi
Tegangan sel = Potensial elektroda positif – Potensial elektroda negatif
Karena itu
Tegangan rangkaian terbuka sel timbal-asam atau tegangan keseimbangan = 1,69 – (-0,35) = 2,04 V
Pada atau di dekat akhir pelepasan, tegangan sel, EDisch = 1,50 – (- 0,20) = 1,70 V
Pada atau di dekat akhir pengisian, tegangan sel, ECh = 2,05 – (-0,65) = 2,70 V

Pengisi daya baterai - Koefisien pengisian daya
Baterai isi ulang perlu diisi untuk mendapatkan kembali kapasitas Ah yang dihabiskan pada debit sebelumnya.
Jumlah Ah yang diperlukan untuk membawa baterai ke kondisi terisi penuh sebelumnya dibandingkan dengan output sebelumnya akan menjadi 10 hingga 15% lebih banyak. Rasio input muatan dengan output sebelumnya disebut koefisien muatan
Koefisien muatan = Input Ah / Output sebelumnya Ah = ~ 1,1 hingga 1,2.
Artinya, sekitar 10 sampai 20 % ekstra Ah harus dimasukkan ke dalam untuk mengkompensasi reaksi sekunder, yang dibentuk oleh reaksi overcharge pemisahan air dan reaksi korosi grid. Juga, sebagian kecil akan hilang karena hambatan internal.
Pengisi daya baterai - Efisiensi Pengisian baterai asam timbal
Efisiensi ampere jam
( Efisiensi per jam atau coulombik dan efisiensi energi atau watt-jam )
Dari argumen di atas, dapat dilihat bahwa kita harus mendefinisikan apa yang disebut “efisiensi pengisian”.
Efisiensi ampere jam
Standar India IS 1651 menjelaskan prosedur pengujian sebagai berikut:
- Baterai yang terisi penuh harus mengalami pelepasan pada kecepatan sepuluh jam ke tegangan akhir 1,85 volt per sel.
- Output Ah yang tepat harus dihitung.
- Baterai sekarang diisi ulang dengan jumlah ampere-jam yang sama pada arus yang sama.
- Baterai sekarang mengalami pelepasan kedua seperti sebelumnya.
- Efisiensi Ah (Coulombik)= Ah = Ah yang diberikan selama debit kedua / Masukan Ah.
Efisiensi energi atau watt-jam
Efisiensi watt-jam harus dihitung dengan mengalikan efisiensi ampere-jam yang diperoleh seperti dijelaskan di atas dengan rasio debit rata-rata dan tegangan pengisian ulang.
Efisiensi energi atau watt jam = Wh = Ah * (Tegangan luahan rata-rata / Tegangan rata-rata pengisian)
Efisiensi ampere jam (atau coulombik) pengisian sel timbal-asam dalam kasus input sama dengan 100% dari debit sebelumnya pada tingkat yang sama hampir sama dengan 95% dan efisiensi energi atau watt jam sekitar 85 -90%. Standar India (IS 1651) juga menetapkan efisiensi ampere-jam minimum 90% dan efisiensi watt-jam minimum 75%.
Efisiensi pengisian dibatasi oleh pelat positif daripada pelat negatif. Ketika sekitar tiga perempat dari timbal sulfat pada elektroda positif telah diubah kembali menjadi timbal dioksida dan air tidak dapat berdifusi cukup cepat ke dalam struktur berpori pelat bagian dalam, reaksi sekunder seperti evolusi oksigen terjadi. Untuk beberapa periode waktu, arus pengisian didistribusikan antara proses primer pengubahan PbSO 4 menjadi PbO 2 dan reaksi pengisian berlebih sekunder. Jika pengisian berlanjut untuk waktu yang cukup lama sehingga hampir semua timbal sulfat akan diubah menjadi timbal dioksida, semua arus pengisian berlaku untuk reaksi sekunder.
Tegangan pengisian pengisi daya baterai
Seperti yang dijelaskan sebelumnya
E Ch> E°.
Jadi, kita harus memberikan tegangan yang sedikit lebih tinggi untuk memfasilitasi reaksi ini. Biasanya, pengisi daya yang baik akan dirancang dengan sumber tegangan yang cukup tinggi untuk pengisian daya. Ini adalah aturan praktis yang baik bahwa untuk sel 2 V, seseorang harus menyediakan setidaknya 3 V sehingga sel dapat mencapai muatan penuh dengan mencapai tegangan 2,7 V per sel. Tetapi kita harus mempertimbangkan kerugian pada kabel, dll.
Oleh karena itu untuk baterai 12 V, pengisi daya baterai harus menyediakan setidaknya 18 hingga 20 V.
Jika tegangan ini dikurangi menjadi lebih rendah dari 15 V. maka baterai tidak dapat mencapai kondisi terisi penuh.
Selama pengisian ulang: 2PbSO 4 + 2H 2 O → PbO 2 + Pb + 2H 2 SO 4
Timbal sulfat pada kedua elektroda larut sebagai ion timbal dan segera mengendap sebagai timbal pada pelat negatif dan sebagai PbO2 pada elektroda positif.
Di pelat positif
PbSO 4 + 2H 2 O → PbO 2 + 4H + +SO 4 ²- + 2e –
Elektron bergerak ke pelat negatif untuk reaksi lebih lanjut
Di pelat negatif
PbSO 4 + 2e – → Pb +SO 4 ²-
Karena ion sulfat direproduksi pada kedua pelat, mereka bergabung dengan proton untuk membentuk asam sulfat sehingga berat jenis elektrolit meningkat.
Pelepasan Gas Baterai
Sampai sekarang kita hanya melihat reaksi yang berguna selama proses pengisian. Namun ada beberapa reaksi samping atau reaksi sekunder yang terjadi pada periode overcharge. Dua reaksi sekunder atau samping utama adalah:
- Elektrolisis air dan
- Korosi jaringan positif
Reaksi-reaksi ini dapat direpresentasikan sebagai berikut:
Elektrolisis air
2H 2 O → O 2 + 2H 2 (Pada kedua pelat kelebihan banjir , sel timbal-asam elektrolit)
Oksigen dari pelat positif dan hidrogen dari pelat negatif berkembang dan dibuang ke atmosfer melalui lubang sumbat ventilasi.
Tetapi dalam sel baterai asam timbal yang diatur katup (VRLA), oksigen memang berevolusi, tetapi bukan hidrogen. Oksigen yang berevolusi juga tidak dibiarkan keluar tetapi berdifusi melalui rongga yang tersedia di pemisah alas kaca absorptif (AGM) dan bereaksi dengan bahan aktif negatif untuk meregenerasi molekul air. Ini adalah langkah yang memungkinkan sel VRLA berkembang tanpa diisi air.
2H 2 O → O 2 + 4H+ + 4e – Pada pelat positif sel elektrolit atau VRLA yang kelaparan
Korosi jaringan positif dalam baterai asam timbal
Pada kedua jenis sel timbal-asam korosi grid positif terjadi dengan cara yang sama:
Korosi grid: Pb + 2H 2 O → PbO 2 + 4H + + 4e –
Jika elektroda platina berlapis dibuat katoda, hidrogen berkembang hampir pada reversibel
potensial hidrogen dari larutan. Dengan elektroda lain, misalnya timbal, diperlukan potensial yang lebih negatif
agar reaksi ini terjadi.
Sampai tegangan sel mencapai nilai 2,3 V, ada gas yang diabaikan. Tapi penyerangan dengan gas dimulai pada 2,4 V per sel. Di luar 2,4 V, gas lebih banyak dan karenanya efisiensi pengisian akan berkurang. Pada 2,5 V, gas akan berlebihan, dan suhu elektrolit baterai akan mulai naik. Sekarang ada gas yang cukup untuk memberikan agitasi elektrolit dan berat jenis mulai menyamakan. Saat baterai dalam keadaan idle, berat jenis elektrolit akan sedikit lebih tinggi di bagian bawah daripada di bagian atas. Ini diperparah jika sel-selnya lebih tinggi.
Baterai timbal-asam dapat diisi dengan kecepatan berapa pun yang tidak menyebabkan gas berlebihan, suhu tinggi, dan tegangan sangat tinggi di terminal. Baterai yang benar-benar kosong dapat menyerap tingkat pengisian daya yang tinggi pada awal pengisian tanpa gas dan kenaikan tegangan dan suhu yang cukup besar.
Pada beberapa waktu proses pengisian, ketika hampir semua timbal sulfat telah diubah menjadi timbal dioksida di plat positif, reaksi sekunder lebih dominan. Ini adalah reaksi elektrolisis air dan korosi grid positif, seperti yang diberikan sebelumnya.
Korosi grid positif seperti itu dimulai langsung dari tahap pembentukan (atau dalam kasus pembentukan tabung) dari muatan pertama. Korosi ini adalah aspek yang paling berbahaya bagi kehidupan baterai timbal-asam. Karena korosi grid positif terjadi setiap kali sel memasuki wilayah over charge, bagian dari struktur grid akan diubah menjadi timbal dioksida dan berat grid turun sedikit pada setiap periode korosi. Pada akhirnya, tahap akan tercapai ketika elektron dari situs reaksi di grid tidak dapat melakukan perjalanan ke bus bar, karena tidak tersedianya struktur grid kontinu.
Akibatnya, bagian dari bahan aktif tidak dapat berpartisipasi dalam proses produksi energi dan kapasitasnya menurun, yang mengarah ke akhir masa pakai baterai.
Produsen sel timbal-asam mencoba untuk mengurangi masalah ini dengan memasukkan elemen paduan yang meningkatkan ketahanan korosi dari paduan timbal. Beberapa konstituen paduan tersebut adalah arsenik (As) dan perak (Ag) dalam persentase fraksional. Sebagai aturan, jumlah As akan menjadi sekitar 0,2% dan Ag sekitar 0,03 hingga 0,05% dalam paduan positif.
Pengisi daya baterai - arti penerimaan saat ini
Penerimaan saat ini ditentukan oleh desain sel. Misalnya, baterai Ah serupa yang dirakit dengan jumlah pelat yang lebih banyak (yaitu pelat akan lebih tipis), dapat menerima arus pengisian yang lebih tinggi karena luas permukaan yang ditingkatkan. Untuk prosedur rinci untuk mengukur efisiensi muatan masing-masing pelat, pembaca dirujuk ke artikel oleh K. Peters. [8]
Penerimaan muatan pelat negatif lebih besar daripada pelat positif (Lihat Gambar 1) yang terutama karena strukturnya yang lebih kasar, lebih terbuka dan pori yang dengan mudah menerima difusi asam ke bagian dalam pelat. Positif mulai ditagih berlebihan pada 70–80% SOC, tergantung pada beberapa faktor desain. Beberapa faktor desain parametrik dalam adalah struktur pori, luas permukaan sebenarnya, dll. Parameter eksternal lainnya adalah arus pengisian dalam ampere, suhu elektrolit, dll.
Penerimaan muatan pelat negatif lebih tinggi dan masuk ke wilayah pengisian berlebih pada periode yang relatif lebih lambat, 90% SOC [8. K. Peters, AI Harrison, WH Durant, Sumber Daya 2. Penelitian dan Pengembangan Sumber Daya Elektrokimia Non-mekanis, Pergamon Press, New York, AS, 1970, hlm. 1–16.]
[9. SAYA Hardman, Jurnal Sumber Daya Vol. 23, Tahun 1988, halaman, 128].

Namun, pada titik tertentu, reaksi sekunder dimulai pada elektroda negatif, terutama reduksi ion hidrogen (proton) menjadi gas hidrogen dengan transfer elektron sederhana (terjadi pada potensial yang jauh lebih rendah dari -350 mV yang merupakan potensial reversibel pelat negatif, E° nilai.), sekitar -0,6 hingga 0,95 V:
2H + + 2e → H 2
Salah satu pengotor penting yang terakumulasi pada pelat negatif adalah antimon (Sb), yang diendapkan karena fenomena yang disebut migrasi antimon dalam sel yang mengandung jumlah antimon yang relatif lebih tinggi dalam kisi. Meskipun antimon merupakan komponen penting dari paduan kisi untuk sebagian besar sel timbal-asam, ia memiliki dampak negatif pada kinerja sel.
Selama tahap korosi pengisian (menjelang akhir pengisian setiap siklus), grid positif diserang anodik dan antimon masuk ke dalam larutan sebagai ion Sb 5+ , sebagian diserap oleh bahan aktif positif di mana ia mendorong self-discharge karena pembentukan sel lokal. Sisa antimon yang terlarut diendapkan sebagai Sb 3+ pada permukaan katoda (permukaan pelat negatif) (“migrasi antimon” ) dan karena hidrogennya lebih rendah daripada potensial timbal, hal itu menyebabkan evolusi hidrogen prematur. Kemudian, selama periode evolusi gas yang berlebihan, antimon dapat, dalam kondisi yang menguntungkan, dilepaskan sampai batas tertentu sebagai gas stibin (SbH 3 ), ketika bergabung dengan proton.
Di bawah kondisi yang menguntungkan, reaksi serupa dengan arsenik (As) juga dapat terjadi melepaskan arsin (AsH 3 ), yang merupakan gas beracun. Oleh karena itu, konstituen paduan ini secara alami dihindari di mana sel digunakan dalam lingkungan tertutup, seperti kapal selam.
Secara termodinamika, ini terjadi pada potensial yang lebih rendah daripada reaksi pengisian primer tetapi, seperti pembangkitan oksigen pada elektroda positif, potensi berlebih untuk pembangkitan hidrogen pada elektroda timbal relatif besar (sekitar -0,650 V) sehingga pengisian ulang sebagian besar dapat diselesaikan sebelum evolusi hidrogen dimulai secara penuh.
Gas-gas ini dikeluarkan dari sel melalui lubang sumbat ventilasi. Kedua pelat dipengaruhi oleh efek pengotor pada potensi berlebih, dan dengan demikian pengisian ulang kedua pelat yang sangat efisien tidak mungkin dilakukan. Misalnya, jika Anda menggabungkan potensi reaksi evolusi oksigen dengan evolusi hidrogen, kami memiliki:
1,95 + (-0,95) = 2,9 V untuk evolusi gas yang berlebihan.
Hal lain yang perlu diperhatikan adalah bahwa sesuai dengan hukum dasar, air harus terurai pada 1,23 V dan oksigen harus berkembang pada elektroda positif pada potensial ini. Tapi ini tidak terjadi di sel praktis. Jika itu terjadi, stabilitas sel timbal-asam itu sendiri akan menjadi pertanyaan. Potensial pelat positif standar (E° = 1,69 V) adalah sekitar 0,46V di atas tegangan di mana air harus terurai (1,23V). Alasannya lagi-lagi tegangan lebih. Artinya, tegangan untuk evolusi oksigen pada timbal dioksida dalam larutan asam sulfat terletak jauh di atas nilai E° pelat positif pada 1,95V.
Dengan demikian reaksi evolusi oksigen pada timbal dioksida dalam larutan asam sulfat terhambat, menjadi 0,26 V (1,95-1,69 = 0,26) di atas nilai E° pelat positif dan sekitar 0,72 V di atas potensi dekomposisi air (1,95-1,23 = 0,72V) dan maka oksigen tidak berkembang sampai nilai tegangan lebih tercapai dalam larutan murni murni.
Demikian pula, evolusi hidrogen pada timbal dalam larutan asam sulfat sangat terhambat karena kelebihan potensial hidrogen pada timbal. Nilai potensial berlebih ini sekitar 0,6 V lebih negatif dan di bawah potensial elektroda standar timbal dalam larutan asam sulfat, E° = -0,35V. Oleh karena itu reaksi evolusi hidrogen tidak akan menghalangi muatan penuh pelat negatif sampai nilai elektroda mencapai -0,95V dalam larutan yang benar-benar murni. Inilah alasan mengapa pelat negatif memiliki efisiensi pengisian yang lebih baik daripada pelat positif.
Tapi, dalam sel praktis, tahap ini dicapai jauh sebelum tegangan ini. Faktanya, 2,9 V ini sama sekali tidak direalisasikan dalam sel praktis, karena reaksi akibat pengotor lebih dominan dan oleh karena itu evolusi gas penuh berdasarkan volume (H 2 : O 2 = 2:1) dicapai pada sekitar 2,6 V. Namun, jika tegangan pengisian terkesan terlalu tinggi, maka nilai 2,9 V ini dapat dicapai, khususnya, baterai paduan bebas Sb dapat mencapai nilai 2,8 V dan dengan antimonial sel nilainya akan lebih rendah sebesar 0,2 V, katakanlah 2,6 V.
Saat siklus berlangsung lebih jauh, nilai penyerangan dengan gas akan sangat berkurang dalam kasus sel antimonial, sementara sel lain hampir bebas dari efek ini. Penurunan drastis ini disebabkan oleh fenomena yang disebut “migrasi antimon” seperti yang telah dijelaskan sebelumnya.
Secara alami, perbedaan tegangan baterai baru dan baterai daur ulang meningkat dari 250 mV menjadi 400 mV. Ini akan mengakibatkan ketidakmampuan bahan aktif untuk menerima muatan dan hampir semua arus menghasilkan hidrogen dan oksigen. Gambar 3 mengilustrasikan aspek ini [10. Hans Tuphorn, Bab 17, Gambar 17.2 dalam Buku Pegangan Teknologi Baterai, Ed. HA Kiehne, Edisi Kedua, 2003, Marcel Dekker, Inc., New York.]

Bagaimana cara kerja pengisi daya baterai 12v?
Untuk mengisi baterai, kabel keluaran positif terhubung ke terminal positif baterai dan negatif ke terminal negatif. Pengisi daya kemudian dihubungkan ke sumber listrik AC melalui cara yang sesuai.
Input AC diubah menjadi DC oleh rangkaian penyearah yang memiliki transformator step-down untuk diubah menjadi tegangan yang diperlukan. Penyearah mengubah aliran arus bolak-balik dua arah (AC) menjadi aliran searah. Dengan demikian, ia mempertahankan polaritas konstan di seluruh beban. Konfigurasi penyearah jembatan digunakan untuk memperbaiki tegangan rendah AC yang diturunkan menjadi DC dan selanjutnya dihaluskan oleh kapasitor elektrolitik bernilai tinggi (sirkuit penyaringan).
DC yang disaring ini diumpankan ke sirkuit elektronik yang mengatur tegangan ke tingkat yang konstan dan diterapkan ke baterai yang membutuhkan biaya,
Pengisi daya memiliki indikator untuk arus (amperemeter), tegangan (voltmeter), dan juga dalam kasus khusus pengatur waktu dan pengukur ampere-jam.
Baterai diisi sesuai petunjuk pabrikan
Prosedur pengisian baterai - Pengisi Daya Baterai
Baterai yang perlu diisi harus dibersihkan bagian luarnya secara menyeluruh dan terminal, setelah menghilangkan produk korosi, jika ada, harus diberi lapisan tipis Vaseline putih. Tingkat elektrolit juga akan diperiksa. Pengisian ulang tidak perlu dilakukan pada saat ini kecuali jika ketinggiannya berada di bawah ketinggian separator.
Pengisi daya yang dimaksudkan untuk mengisi daya baterai harus memiliki spesifikasi yang memadai, seperti tegangan dan arus keluaran. Misalnya, baterai 12 V membutuhkan tegangan output C minimal 18 V. Arus yang dibutuhkan tergantung pada kapasitas baterai dan waktu pengisian baterai. Biasanya, baterai akan diisi pada 0ne sepersepuluh ampere dari kapasitas Ah baterai. Jadi, baterai 100 ah akan membutuhkan setidaknya 10 ampere output untuk pengisian normal. Jika ingin diisi dengan cepat, diperlukan output 15 ampere.
Input sekitar 110% dari kapasitas diperlukan untuk baterai yang benar-benar kosong. Tapi, jika baterai sudah terisi sebagian, kita harus tahu SOCnya. Apa pun itu, tegangan dan berat jenis adalah dua parameter penting yang harus dipantau untuk menentukan status muatan. Nilai berat jenis harus dibaca dari label pada baterai. Baterai yang terisi penuh biasanya akan mencapai 16,5 V dan lebih, jika dalam kondisi baik. Jika itu adalah baterai yang sudah tua, tegangan ini tidak dapat dengan mudah dicapai.
Ini terutama karena reaksi sekunder seperti evolusi gas karena elektrolisis air dalam elektrolit dan efek pemanasan karena resistensi yang sudah terbentuk karena akumulasi timbal sulfat.
Baterai ditempatkan pada bahan isolasi seperti lembaran karet atau bangku kayu. Kabel pengisi daya harus memiliki kapasitas pembawa arus yang memadai. Biasanya, kawat tembaga persegi 1mm dapat membawa arus searah (DC) 3 ampere dengan aman. Setelah memastikan pengisi daya dalam posisi mati, kabel pengisi daya akan dihubungkan ke terminal masing-masing, yaitu positif ke positif dan negatif ke negatif. Tegangan, berat jenis dan pembacaan suhu akan dicatat dalam lembar log, model yang diberikan di bawah ini:
Templat catatan pengisian baterai

Pembacaan harus dicatat setiap jam.
Pembacaan kadmium akan menunjukkan apakah pelat tertentu telah mencapai muatan penuh atau tidak. Elektroda referensi kadmium adalah batang kadmium terisolasi dengan kawat tembaga yang disolder ke ujung atas. Ujung bawah akan direndam dalam elektrolit, sehingga hanya menyentuh cairan, dan tidak boleh bersentuhan dengan pelat atau bagian timah lainnya di dalamnya.
Untuk pelat positif yang terisi penuh, pembacaan kadmium akan menjadi 2,4 V dan lebih untuk pelat negatif, minus 0,2 V dan kurang.
Tabel 4
Reaksi dalam sel timbal-asam dan pembacaan potensial kadmium yang sesuai
Pembacaan potensial kadmium
| Reaksi | Nilai Potensial | Bacaan Kadmium |
|---|---|---|
| Potensi evolusi oksigen 2 H2O → O2 + 4 H+ + 4e- | 1,95 hingga 2,00 V | 2,00 - (-0,4) = 2,4 V |
| Potensial Elektroda Standar pelat Positif PbO2/PbSO4/H2SO4 | 1,69 V | [1,69 – (-0,4) = 2,09 V] |
| Akhir pelepasan pelat positif | 1,40 hingga 1,5 V |
1,40 – (-0,4) = 1,8 V 1,50 – (-0,4) = 1,9 V |
| Potensi Elektroda Hidrogen Standar (SHE) 2H+ + 2e- → H2 | 0.00 V | 0.00 V |
| Akhir pelepasan pelat negatif | -0,15, -0,20, -0,25 V (Untuk rapat arus berbeda) | -0,15 – (-0,4) = 0,25 V -0,20 – (-0,4) = 0,20 V -0,25 – (-0,4) = 0,15 V |
| Potensial Elektroda Standar pelat Negatif Pb/PbSO4/H2SO4 | -0,35 V | [-0,35 – (-0,4) = 0,05 V] |
| Nilai E° elektroda referensi kadmium Cd/Cd2+ | -0,40 V | -0,40 V |
| Potensi evolusi hidrogen- 2H+ + 2e− →H2 (Untuk sel komersial) | -0,60 V | -0,60 – (-0,4) = -0,20 |
| Potensi evolusi hidrogen 2H+ + 2e− →H2 Untuk sel eksperimental murni | -0,95 V | -0,95 – (-0,4) = -0,55 |
Prinsip kerja pengisi daya baterai
Pada akhir pengisian, baterai 12 V dapat mencapai tegangan terminal 16,5 ke atas. Setelah mempertahankan tegangan terminal pada level ini selama satu jam, pengisian daya dapat dihentikan. Saat baterai mendekati 16. 0 V, air yang disetujui dapat ditambahkan, jika diperlukan.
Menjelang akhir pengisian, gas berat akan diamati dari baterai. Tidak boleh ada api terbuka yang dibawa ke dekat ruang pengisian. Gas-gas berevolusi dalam rasio kombinasi mereka, yaitu hidrogen 2 bagian dan oksigen 1 bagian. Oleh karena itu, jika gas-gas ini dibiarkan menumpuk di area pengisian daya tanpa ventilasi yang memadai, kemungkinan besar percikan atau nyala api akan menyulut gas dan akan bergabung dengan kekerasan eksplosif, merusak baterai dan sekitarnya dan juga melukai orang-orang di sekitarnya. .
Batas bawah campuran hidrogen yang mudah meledak di udara adalah 4,1%, tetapi, untuk alasan keamanan, hidrogen tidak boleh melebihi 2% volume. Batas atas adalah 74%. Ledakan hebat terjadi dengan kekerasan ketika campuran mengandung rasio stoikiometrik dari gas-gas ini (2 bagian hidrogen dengan 1 oksigen). Kondisi ini diperoleh di dalam baterai yang pengisian dayanya berlebihan dengan sumbat ventilasi yang disekrup rapat ke penutupnya. Oleh karena itu, disarankan untuk menjaga sumbat ventilasi tetap longgar di atas lubang ventilasi dan tidak mengencangkannya dengan kencang.
Berbagai Metode pengisian baterai dan Berbagai jenis pengisi daya baterai
Meskipun ada berbagai metode pengisian sel timbal-asam, semuanya memiliki satu tujuan yang sama untuk mengubah produk reaksi, yaitu timbal sulfat pada kedua pelat menjadi bahan aktif masing-masing, PbO 2 pada elektroda positif dan Pb pada elektroda negatif. .
2 PbSO 4 + 2 H 2 O → PbO 2 + Pb + 2 H 2 SO 4
Ada sejumlah varian dalam rezim pengisian. Tetapi dalam semua metode ini, hanya dua prinsip dasar yang digunakan: metode pengisian arus konstan dan tegangan konstan. Beberapa metode yang tersedia menggabungkan dua prinsip ini untuk mencapai tujuannya.
Pemilihan metode pengisian yang tepat tergantung pada jenis, desain dan kondisi layanan dan waktu yang tersedia untuk pengisian. Semua metode pengisian ini menggunakan banyak metode untuk mengontrol dan menyelesaikan proses pengisian.
Metode-metode ini dapat diklasifikasikan menjadi berikut:
Tabel 5
Klasifikasi metode pengisi daya baterai & metode pengisian baterai yang berbeda
Metode pengisian baterai yang berbeda
| Metode berbasis arus konstan (CC) | Metode berbasis tegangan konstan (CV atau CP) | Metode kombinasi | Pengisian lancip | Metode khusus |
|---|---|---|---|---|
| Metode pengisian CC satu langkah | Metode Tegangan Konstan | metode CC-CV | Metode pengisian lancip satu langkah |
1. Biaya awal 2. Biaya pemerataan 3. Peluang pengisian 4. Pengisian yang dikendalikan gas 5. Pengisian tetesan 6. Tingkatkan pengisian daya 7. Pengisian pulsa 8. Pengisian cepat atau cepat |
| Metode pengisian CC dua langkah | Metode CV terbatas saat ini atau dimodifikasi | Metode pengisian lancip dua langkah |
Satu langkah Metode pengisian berbasis arus konstan (metode CC) Pengisi baterai
Ketika pengisian ulang diperlukan untuk diselesaikan dalam waktu singkat dan ketika pengguna ingin mengetahui input dalam hal Ah, metode pengisian arus konstan dapat digunakan. Pengisian arus konstan lebih disukai ketika output sebelumnya diketahui, sehingga pengisian berlebih 5-10% dapat efektif untuk mengembalikan baterai ke SOC 100%. Ini juga akan memastikan bahwa input yang benar diberikan sehingga masa pakai baterai tidak terpengaruh oleh pengisian yang berlebihan. Waktu pengisian ulang normal untuk metode ini adalah 15 hingga 20 jam.
Dalam metode ini, arus dijaga konstan selama periode pengisian.
Direkomendasikan arus pengisian 5 hingga 10% dari kapasitas 20 jam.
Untuk mengimbangi kenaikan ggl belakang baterai saat pengisian, arus pengisian harus dijaga konstan baik dengan memvariasikan resistansi seri yang digunakan atau dengan meningkatkan tegangan transformator. Biasanya, resistansi seri divariasikan untuk menjaga agar arus tetap konstan.
Metode ini adalah metode pengisian yang paling sederhana dan lebih murah. Tetapi memiliki kelemahan efisiensi biaya yang lebih rendah. Hal ini disebabkan oleh beberapa daya yang dihamburkan dalam resistansi dan juga sebagian karena arus yang digunakan untuk membelah air setelah baterai mencapai 2,5 V per sel. Baterai mulai mengeluarkan gas saat baterai diisi hingga sekitar 70 hingga 75%. Metode pengisian ini selalu menghasilkan sedikit pengisian berlebih dan gas yang berlebihan terutama pada akhir pengisian.
Gambaran umum untuk metode pengisian arus konstan diberikan Gambar 5 . Karakteristik pengisian diberikan pada Gambar 6


Metode pengisian arus konstan dua langkah Pengisi baterai
Dua laju pengisian, laju awal dan laju akhir, digunakan dalam metode pengisian arus konstan dua langkah. Tingkat penyelesaian biasanya setengah dari tingkat awal. Tingkat penyelesaian dimulai ketika baterai mulai mengeluarkan gas. Ini umumnya merupakan metode yang disukai yang digunakan untuk pengisian baterai di bangku. Karakteristik pengisian dapat dilihat pada Gambar 7 [11. PG Balakrishnan, Baterai Penyimpanan Timbal, Publikasi Scitech (India) Pvt. Ltd., Chennai, 2011, halaman 12.8].

Tegangan konstan atau metode pengisian potensial Pengisi daya baterai
Metode pengisian tegangan atau potensial konstan (CV atau CP) menggunakan tegangan sumber yang dipertahankan pada tingkat konstan selama periode pengisian. Biasanya, tegangan ini akan berada di antara 2,25 dan 2,4 V per sel.
Metode ini adalah metode yang direkomendasikan untuk pengisian sel dan baterai valve-regulated lead-acid (VRLA). Seseorang tidak perlu khawatir tentang kedalaman debit (DOD) dari debit sebelumnya saat mengisi baterai VRLA dengan metode CV. Baterai VRLA dapat diisi daya tanpa efek merugikan dengan menggunakan tegangan pengisian CV yang direkomendasikan pabrikan. Hampir semua pabrikan VRLAB merekomendasikan arus awal 0,25 hingga 0,30 C ampere.
Artinya, untuk baterai 100 Ah, arus awal 25 hingga 30 ampere dapat dipilih. Arus yang lebih tinggi digunakan untuk mengisi baterai yang dalam keadaan kosong, sedangkan arus yang lebih rendah digunakan untuk baterai yang habis secara normal. Efek dari tegangan pengisian yang lebih rendah adalah bahwa kenaikan suhu akan lebih sedikit dibandingkan dengan baterai yang diisi, dengan arus yang lebih tinggi, tetapi waktu yang dibutuhkan untuk pengisian penuh akan lebih lama.
Pada akhir pengisian, tegangan baterai mencapai paritas dengan tegangan terkesan arus pengisian mengecil ke nilai yang sangat rendah. Secara universal, arus pada ujungnya dapat mencapai nilai 2 hingga 4 mA untuk setiap Ah kapasitas baterai. Pada 2,25 hingga 2,3 V per sel, tidak ada evolusi gas yang diamati pada baterai yang dibuat dengan benar. Namun, gas akan terlihat jelas pada 2,4 V per sel. Volume gas yang berkembang pada 2,4 V per sel adalah sekitar 1000 ml dalam 40-50 menit untuk VRLAB 6V/1500 Ah
Menurut Klausul 6.1.a. Standar Industri Jepang, JIS 8702-1:1998, durasi pengisian akan sekitar 16 jam atau sampai arus tidak berubah lebih dari 10% dari arus laju 20 jam (I 20 ) ampere dalam dua jam berturut-turut[JIS 8702-1:1998] . Misalnya, jika kapasitas baterai 20 jam (terlepas dari tegangan baterainya) adalah 60 Ah20 , maka pengisian akan selesai jika arus tidak berubah lebih dari 300 mA (yaitu, I20 = 60 Ah /20 A = 3 A. Oleh karena itu, 0,1 dari I20 = 0.3A)
Rincian pengisian CP baterai VR ditunjukkan pada Gambar
Efisiensi pengisian lebih baik daripada metode arus konstan. Kekurangan dari metode ini adalah membutuhkan tegangan yang stabil pada aliran arus yang tinggi, yang mahal. Metode ini digunakan untuk operasi float sel stasioner untuk aplikasi telekomunikasi dan UPS.


Pengisian potensial konstan yang dimodifikasi - Pengisi daya baterai
Dalam aplikasi industri, metode seperti itu digunakan di mana sirkuit pengisian merupakan bagian integral dari sistem. Contohnya adalah mobil, UPS dll. Resistansi seri untuk membatasi arus termasuk dalam rangkaian, yang nilainya dipertahankan sampai tegangan preset tercapai. Setelah itu tegangan dipertahankan konstan sampai baterai dipanggil untuk melakukan tugasnya untuk memasok arus start, daya darurat, dll.
Pilihan resistansi seri tetap tergantung pada jumlah sel dalam baterai dan kapasitas ampere-jamnya dan pada durasi yang tersedia untuk pengisian. Tegangan yang diberikan dijaga konstan sekitar 2,6 hingga 2,65 volt per sel.
Saat pengisian berlangsung, arus pengisian mulai turun dari nilai awal. Ketika tegangan naik secara bertahap hingga 2,35-2,40 volt per sel, tegangan gas cenderung naik dengan cepat dan karenanya arus pengisian turun pada tingkat yang lebih cepat.
Muatan potensial konstan yang dimodifikasi adalah umum untuk baterai siklus dalam seperti baterai traksi. Pabrik biasanya menggunakan profil waktu pengisian-pengosongan tetap seperti pengoperasian truk fork lift selama 6 jam hingga kedalaman pelepasan (DOD) 80% dan pengisian ulang periode 8 jam. Pengisi daya diatur untuk tegangan gas dan arus awal dibatasi hingga 15 hingga 20 A per 100 Ah. Arus mulai lancip pada tegangan konstan ke tingkat akhir 4,5 hingga 5 A per 100 Ah, yang kemudian dipertahankan hingga akhir pengisian. Total waktu pengisian dikendalikan oleh pengatur waktu.
Ada pengisi baterai yang memiliki ketentuan untuk menjaga baterai tetap terhubung bahkan setelah pengisian selesai untuk menjaga baterai dalam kondisi terisi penuh. Hal ini dicapai dengan memberikan waktu singkat untuk mengisi ulang setiap 6 jam untuk mempertahankan kondisinya
Rinciannya diberikan pada Gambar 12 [ 12. Edisi Khusus Baterai Asam Timbal, J. Sumber Daya 2 (1) (1977/1978) 96-98]

Metode kombinasi (metode CC-CV) - Pengisi daya baterai
Dalam metode ini pengisian arus konstan dan potensial konstan digabungkan bersama. Metode ini juga dikenal sebagai metode pengisian (IU) (I untuk arus dan U untuk tegangan). Pada periode awal pengisian, baterai diisi pada mode arus konstan sampai baterai mencapai tegangan gas dan kemudian dialihkan ke mode potensial konstan. Metode ini menghilangkan efek merusak dari metode pengisian arus konstan pada akhir pengisian.
Karakteristik pengisian dari metode ini ditunjukkan pada Gambar 11 di sebelah kanan.

Pengisian lancip - Pengisi daya baterai
Arti kata lancip adalah menuruni. Seperti yang ditunjukkan oleh istilah dengan jelas, arus dibiarkan berkurang dari nilai yang lebih tinggi ke nilai yang lebih rendah, dengan menetapkan tegangan pengisian awal sekitar 2,1 V per sel dan berakhir pada 2,6 V per sel. Rasio nilai arus pada tegangan ini disebut sebagai nilai lancip.
Jadi, pengisi daya dengan keluaran 50 A pada 2,1 V per sel dan 25 A pada 2,6 V per sel, digambarkan memiliki karakteristik lancip 2:l.
Ada metode pengisian lancip satu langkah dan metode pengisian lancip dua langkah
Pengisian lancip satu langkah - Pengisi daya baterai
Dalam jenis pengisian ini, arus berkurang dari nilai awal yang lebih tinggi ke tingkat penyelesaian yang lebih rendah, yang biasanya sekitar 4 hingga 5% dari kapasitas kecepatan baterai 20 jam. Gassing adalah fenomena yang diperlukan karena membantu menyamakan gradien densitas elektrolit. yaitu, menetralkan fenomena stratifikasi. Oleh karena itu, tingkat penyelesaian ditetapkan pada nilai yang cukup tinggi untuk memungkinkan proses ini terjadi dan pada saat yang sama tidak terlalu merusak kisi-kisi positif. Di sini, tegangan keluaran pengisi daya diatur sekitar 2,7 volt per sel pada awalnya dan dibuat turun menjadi sekitar 2,1 hingga 2,2 volt per sel pada akhir periode pengisian.
Arus pengisian dibuat untuk mengurangi secara perlahan sampai tegangan gas (sekitar 2,4 V per sel) tercapai (SOC = 75 sampai 80%) dan mengecil pada tingkat yang lebih cepat setelahnya. Biasanya, rasio lancip ditetapkan pada 2:1 atau pada rasio 1,7 banding 1. Waktu yang dibutuhkan untuk menyelesaikan pengisian adalah sekitar 12 jam. Periode pengisian setelah voltase penyerangan gas tercapai dikendalikan dengan memasukkan perangkat pengatur waktu yang mulai beroperasi ketika voltase penyerangan gas tercapai.
Periode pengisian dapat dikurangi menjadi 8 hingga 10 jam, tetapi arus awal harus ditingkatkan, yang tidak dapat dilakukan tanpa pertimbangan ekonomi yang terlibat dan keterjangkauan konsumen.

Karakteristik pengisian single step taper charging ditunjukkan pada Gambar 12

Pengisian lancip dua langkah - Pengisi daya baterai
Metode pengisian ini mirip dengan pengisian lancip satu langkah kecuali fakta bahwa total waktu pengisian berkurang menjadi sekitar 8 hingga 10 jam. Karena baterai mampu menerima muatan pada tingkat yang lebih cepat ketika baterai benar-benar habis, arus yang tinggi digunakan pada langkah pertama hingga baterai mencapai tahap pengosongan gas. Hampir 70 hingga 80% jam ampere yang akan dikembalikan ke baterai diberikan ke baterai pada langkah pertama dengan kecepatan yang lebih cepat dan ampere-jam yang tersisa diumpankan pada langkah kedua.
Karakteristik pengisian baterai 12V, 500 Ah dengan pengisian lancip satu langkah ditunjukkan pada Gambar 13
Metode pengisian lancip lebih populer untuk mengisi baterai traksi yang biasanya sangat kosong. Operator armada kendaraan listrik, misalnya van pengiriman pos, kendaraan pengiriman susu, memerlukan pengisi daya baterai yang canggih untuk mendapatkan kinerja terbaik dari baterai dan untuk melindungi investasi uang tunai yang besar.
Biaya awal
Baterai timbal-asam yang baru perlu diaktifkan dan proses pengisian ini untuk pertama kalinya disebut pengisian pengisian awal. Baterai diisi dengan jumlah elektrolit yang diperlukan dan terisi penuh sebelum dikirim untuk pengiriman. Biasanya pengisian awal ini dilakukan dengan metode pengisian arus konstan pada arus rendah untuk waktu yang lama sampai baterai mencapai tegangan 16,5 V atau lebih untuk terisi penuh.
Saat ini, proses ini menjadi berlebihan karena kita mendapatkan baterai yang diisi dari pabrik yang siap digunakan atau baterai yang diisi ulang yang hanya membutuhkan penambahan elektrolit.
Biaya pemerataan
Menyamakan muatan Sel ke sel perbedaan adalah fakta yang harus diterima. Tidak ada dua sel yang bisa sama dalam semua aspek. Perbedaan berat bahan aktif, variasi kecil dalam berat jenis elektrolit, porositas elektroda, dll adalah beberapa perbedaan. Karena alasan ini, setiap sel dalam baterai memiliki karakteristiknya sendiri; masing-masing membutuhkan jumlah biaya yang sedikit berbeda. Menyamakan biaya sesekali membuat akhir masa pakai baterai menjauh. Baterai otomotif 12V diapungkan pada 14.4V. Baterai yang terisi penuh membutuhkan level tegangan 16,5 V, yang tidak pernah direalisasikan dalam layanan di dalam kendaraan.
Oleh karena itu equalizing charge (juga disebut bench charging) diperlukan untuk memperpanjang umur baterai otomotif. Jadi, baterai yang menerima pengisian bangku secara berkala setiap enam bulan dapat hidup lebih lama dari baterai yang tidak menerima pengisian bangku, setidaknya 10-12 bulan. Frekuensi dan tingkat penyetaraan biaya harus didiskusikan dengan pabrikan baterai. Dengan pengisi daya yang telah diprogram sebelumnya, ‘pengisian penyetaraan’ terkadang tersedia melalui sakelar yang menyediakan arus rendah terus-menerus yang digunakan untuk menstabilkan tegangan dan kerapatan relatif elektrolit sel.
Demikian pula, baterai catu daya darurat UPS dan baterai truk forklift juga memerlukan biaya pemerataan tersebut. Baterai yang digunakan dalam inverter hanya diisi hingga 13,8 hingga 14,4 V. Seperti yang dikatakan sebelumnya, ini tidak cukup untuk menyamakan ketidakseimbangan antar sel dalam baterai. Baterai ini, jika diberi muatan pemerataan berkala, akan bertahan lebih lama.
Baterai harus diberi biaya penyetaraan setiap enam bulan. Tetapi baterai traksi yang digunakan dalam baterai forklift harus diberi muatan pemerataan setiap siklus keenam atau kesebelas, tergantung pada apakah baterai baru atau lama. Baterai yang lebih baru dapat diberi muatan pemerataan setiap 11 siklus dan baterai yang lebih lama setiap 6 siklus . Jika baterai menerima muatan penuh secara teratur setiap hari, frekuensi muatan pemerataan dapat dikurangi menjadi siklus ke – 10 dan ke – 20. Muatan pemerataan harus dihentikan bila sel tidak menunjukkan peningkatan lebih lanjut dalam pembacaan tegangan dan berat jenis selama periode 2 sampai 3 jam.
Baca artikel rinci tentang biaya Ekualisasi di sini.
Pengisian peluang
Di mana kendaraan listrik off-road atau on-road dioperasikan secara intensif, mencolokkan ke pengisi daya selama istirahat dan waktu istirahat singkat lainnya juga dapat membantu memperpanjang shift kerja efektif kendaraan dan dengan demikian mengurangi waktu henti EV. Opportunity charging adalah istilah yang diberikan untuk pengisian parsial tersebut selama waktu makan siang atau istirahat.
Biaya peluang seperti itu cenderung mengurangi masa pakai baterai. Baterai menghitung pengisian dan pengosongan berikutnya sebagai satu siklus dangkal. Sedapat mungkin biaya peluang harus dihindari. Pengisian normal menyediakan 15 hingga 20 A per kapasitas 100Ah, sedangkan biaya peluang memberikan arus yang sedikit lebih tinggi yaitu 25 A per kapasitas 100Ah. Ini menghasilkan suhu yang lebih tinggi dan mempercepat korosi pada grid positif. Dan karenanya kehidupan akan berkurang.
Pengisian yang dikendalikan gas
Konduktivitas termal dari gas hidrogen yang dikembangkan digunakan untuk memantau arus pengisian. Gas hidrogen, pendingin yang sangat baik digunakan untuk mendinginkan elemen yang dipanaskan. Perubahan resistansi elemen pemanas digunakan untuk mengatur arus. Termistor juga dapat digunakan untuk mengatur arus. Kadang-kadang, efek pemanasan karena rekombinasi gas hidrogen dan gas oksigen yang berkembang di dalam sel melalui katalis yang sesuai digunakan untuk mengoperasikan sakelar panas untuk mengatur arus.
Pengisian tetesan
Dalam pengisian terus menerus, pengisi daya menyamakan kerugian karena pengosongan sendiri dan pengosongan terputus-putus. Biaya pemeliharaan mengkompensasi self-discharge. Dua mode operasi dicirikan oleh tegangan terminal konstan:
Biaya perawatan 2,20 hingga 2,25 V per sel
Pengisian terus menerus 2,25 hingga 2,35 V per sel
Tergantung pada usia dan kondisi baterai, kerapatan arus 40 hingga 100 mA/100 Ah kapasitas nominal mungkin diperlukan selama pengisian daya (trickle charge).
Arus muatan kontinu sangat bergantung pada profil beban. Baterai pada biaya pemeliharaan harus diisi ulang setelah setiap pemadaman listrik. Hal yang sama berlaku untuk baterai yang terus diisi setelah beban yang tidak direncanakan.
Tingkatkan pengisian daya
Boost charging terpaksa dilakukan ketika baterai yang kosong diperlukan untuk digunakan dalam keadaan darurat ketika tidak ada baterai lain yang tersedia dan SOC tidak cukup untuk pekerjaan darurat. Dengan demikian, baterai timbal-asam dapat diisi pada arus tinggi tergantung pada waktu yang tersedia dan SOC baterai. Karena pengisi daya cepat tersedia saat ini, pengisian daya tambahan sudah tidak asing lagi saat ini. Biasanya pengisi daya penguat seperti itu mulai mengisi daya pada 100A dan mengecil hingga 80A. Yang terpenting suhunya tidak boleh melebihi 48-50 o C.
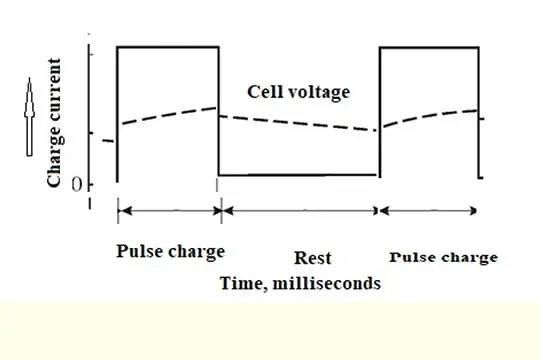
Pengisian pulsa
Apa itu pengisian arus berdenyut?
Pengisian dilakukan untuk durasi yang sangat singkat yaitu, saat ini on-time dalam milidetik (ms), dan periode idle mengikuti (off-time dalam ms). Terkadang pelepasan juga dapat mendahului pengisian pulsa.
Teknik arus berdenyut telah diterapkan untuk pengisian cepat sel timbal-asam otomotif. Kesimpulan berikut telah tiba di:
- Teknik arus berdenyut dapat memberikan efek yang sangat menguntungkan.
- Ini meningkatkan tingkat pengisian ulang.
- Ini memiliki manfaat pada kinerja siklus-masa pakai baterai timbal/asam, terutama bila digunakan tepat waktu lebih dari 100 ms.
- Selain itu, teknik ini juga dapat meremajakan sel yang telah disiklus dengan pengisian arus konstan.
- Waktu pengisian ulang dapat dikurangi dengan urutan besarnya, yaitu dari ~10 jam menjadi ~1 jam
- Siklus hidup dapat ditingkatkan dengan faktor tiga sampai empat.
- Penerapan pengisian arus berdenyut ke baterai yang didaur ulang (kapasitas = 80% nilai awal) dapat membangkitkan pemulihan kapasitas baterai.
- Kehilangan kapasitas prematur terjadi pada sel Pb-Sb dan Pb-Ca-Sn pada tingkat pelepasan yang tinggi dengan pengisian arus konstan.
Untuk lebih jelasnya, pembaca dapat merujuk ke artikel oleh Lam dan lainnya yang diberikan di atas.
Sel-sel bawah laut telah menjadi subjek pengisian pulsa [14. Melvyn James, Jock Grummett, Martin Rowan dan Jeremy Newman, Jurnal Sumber Daya 162 (2006) 878–883 879]. Para penulis telah menyimpulkan bahwa
- Kapasitas dapat ditingkatkan dengan pengisian pulsa. Peningkatan kapasitas ini
dramatis untuk sel yang relatif baru. Tetapi untuk sel yang lebih tua (4–5 tahun) 15 atau lebih siklus pengisian pulsa diperlukan sebelum peningkatan kapasitas diperoleh.
- Semakin tua sel mengalami sulphation parah, yang membutuhkan lebih banyak siklus untuk memecah.
- Beberapa sulfat tidak mungkin untuk dibalik.
- Penggunaan pengisian pulsa juga menunjukkan bahwa biaya penyerangan dengan gas beracun dapat dikurangi secara substansial.
- Evolusi gas berkurang dengan meningkatnya frekuensi denyut nadi. Ini lebih jelas dengan evolusi oksigen, yang merupakan faktor penting untuk baterai kapal selam yang mengalami korosi pelat positif karena oksigen berevolusi dari pelat positif selama pengisian gas.
- Setelah penerapan pengisian pulsa ke sel, efek menguntungkan tetap ada meskipun rutinitas pengisian konvensional dilanjutkan.
Program pengisian pulsa tipikal ditunjukkan di bawah ini:
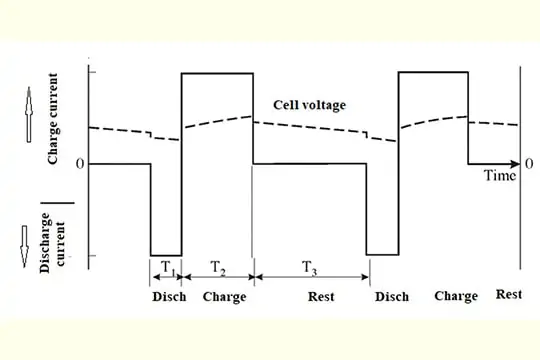
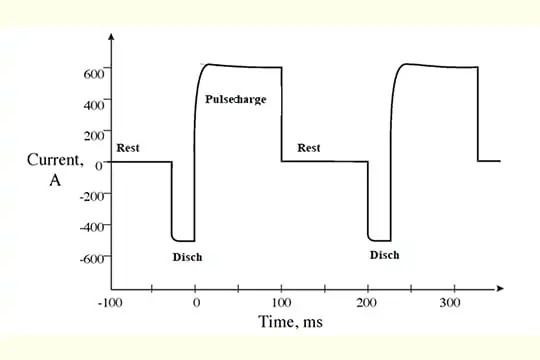
Penerapan pengisian pulsa dapat membantu mencegah pembentukan sulfat dari waktu ke waktu. Mungkin dapat mengurangi penumpukan sulfat dalam sel dengan pengisian dan perawatan yang tepat jika pengisian pulsa digunakan sejak awal. Akumulasi sulfat yang sudah terjadi tidak dapat dibalik dengan metode ini. Jika sel terus-menerus disamakan atau ditagih berlebihan, ini merusak sel, mengurangi kapasitas dan umurnya. Microtex merekomendasikan untuk menguji berat jenis baterai Anda secara teratur untuk mengetahui berapa lama baterai akan bertahan, mengidentifikasi sel yang lemah atau gagal, dan mengonfirmasi status pengisian daya. Langkah-langkah berikut dapat diikuti jika terjadi penumpukan sulfat atau ketidakseimbangan muatan.
Pengisian cepat atau cepat - Pengisi daya baterai
Dua puluh lima tahun yang lalu, diyakini bahwa baterai timbal-asam tidak boleh diisi dengan kecepatan tinggi karena bahan aktif positif akan rusak secara permanen. Diyakini bahwa pengisian cepat akan menghasilkan tingkat korosi jaringan dan gas yang berlebihan, yang mengakibatkan kegagalan awal dan cepat baterai VRLA.
Pengisian cepat terbukti tidak hanya menghemat waktu dan energi, tetapi juga menghilangkan penggunaan gas beracun dan mengurangi perawatan. Pengisian cepat pertama kali diusulkan oleh Kordesch pada tahun 1972 untuk sel Ni-Cd yang disegel, [17. K. Kordesch, J. Elektrokimia. Soc., 113 (1972) 1053] kemudian dikembangkan pada tahun 1993 oleh Norvik Technologies di Kanada untuk baterai VRLA.
Minitcharger™ mereka membuktikan bahwa pengisian ulang baterai Ni-Cd yang habis dalam dapat dicapai dalam 5 hingga 10 menit [18. JK Nor, Paten AS 5.202.617 (1993)].
Pada bagian pertama tahun 1990-an, Valeriote, Nor, dan Ettel dari Cominco, Kanada, mengembangkan teknologi ini ke baterai timbal-asam konvensional [19. EM Valeriote, J.Nor, VA Ettel, Proc. Seminar Baterai Asam Timbal Internasional Kelima, Wina, VA, AS, 17-19 April 1991, hlm 93-122]. Pada tahun 1994, Valeriote, Chang, dan Jochim membuktikan bahwa proses ini juga cocok untuk baterai VRLA pelat tipis [ M. Valeriote, TG Chang, DM Jochim, Proc. dari Konferensi Baterai Tahunan ke- 9 tentang Aplikasi dan Kemajuan, Long Beach, CA, AS, Januari 1994, hlm. 33-38 ] .
Sejak awal tahun sembilan puluhan teknik ini telah diterapkan pada semua jenis baterai traksi [20. K. Nor dan JL Vogt, Proc. Konferensi Baterai Tahunan ke- 13 tentang Aplikasi dan Kemajuan, 13-16 Januari 1998, Long Beach, CA, 191-197].
Efek pengisian sangat cepat pada dua jenis baterai timbal/asam hibrid siklus dalam berikut ini dipelajari pada tahun 1994 menggunakan MinitchargerÔ (Norvik Traction Inc., Kanada) [21. TG Chang, EM Valeriote dan DM Jochim, J. Sumber Daya 48 (1994) 163-175].
- Baterai hibrida yang dibanjiri (disebut sebagai “AP” dalam karya ini) memiliki kisi-kisi positif yang terbuat dari paduan antimonial 4,7% dan kisi-kisi negatif dari jenis yang diperluas yang terbuat dari paduan tinggi-kalsium-rendah-timah (Pb- 0,1 wt.% Ca -0,3wt.% Sn). Berat PAM adalah ~800 g, dan NAM ~ 540 g di setiap sel. Itu adalah tipe pelepasan dalam dan memiliki kapasitas 80 Ah 20 , 54,4 Ah 5 dan 50,9 Ah 3 )
- Baterai yang diatur katup dengan kisi-kisi positif cor gravitasi dibuat dari paduan antimon rendah (Pb -1.5wt. % Sb-0.3wt. % Sn (Baterai ini disebut sebagai baterai “ST” dalam pekerjaan ini). Konfigurasinya adalah 5P + 6N Grid negatif dicetak dari paduan Pb-O.12wt. %Ca-O.4wt.% Sn. Baterai ini dimaksudkan untuk aplikasi siklus dalam. Kapasitas baterai adalah 54,5 Ah5 dan 52,5 Ah 3
Ditemukan bahwa tingkat pengisian ulang 5-menit/50% dan 15-menit/80%-isi ulang dapat dicapai, dalam kasus baterai yang kebanjiran, dengan kenaikan suhu yang cukup dapat diterima. Setelah kedalaman pelepasan 80%, sumber panas yang dominan adalah ohmik selama 40% pertama muatan yang dikembalikan dengan kecepatan yang sangat tinggi, 300 A (5 hingga 6 C 3 ampere). Suhu didistribusikan secara tidak merata di dalam baterai. Setelah ini, polarisasi non-ohmik menjadi semakin penting. Untuk baterai rekombinasi hibrida, siklus oksigen merupakan sumber panas yang substansial selama tahap pengisian selanjutnya, terutama dibandingkan dengan baterai non-antimonial sebelumnya yang telah diselidiki [21 TG Chang, EM Valeriote and DM Jochim, J. Power Sumber 48 (1994) 163-175].
Pengisian cepat baterai yang kebanjiran dan VRLA
Tabel 6.
[21. TG Chang, EM Valeriote dan DM Jochim, J. Sumber Daya 48 (1994) 163-175].]
| Baterai kebanjiran | Baterai yang diatur katup | |
|---|---|---|
| Tarif pengisian ulang 5 menit/50% dan pengisian ulang 15 menit/80% | Ya | Ya |
| Kenaikan suhu | Dapat diterima | Dapat diterima |
| Sumber panas | Ohmik (biaya hingga 40%) | Siklus oksigen adalah sumber panas yang substansial selama tahap pengisian selanjutnya |
| Pengisian | diisi pada tegangan bebas hambatan konstan 2,45 V/sel (14,7 V/baterai) | diisi pada tegangan bebas hambatan konstan 2,45 V/sel (14,7 V/baterai) |
| Saat ini | 250 hingga 300 A (5 hingga 6 C3 ampere) | 250 hingga 300 A (5 hingga 6 C3 ampere) |
| Dalam 3 menit awal | 1 V lebih tinggi dari VRB | |
| Pengurangan arus | Mulai menurun dari level 300-A setelah 3 menit pengisian daya | Mulai menurun dari level 300-A setelah 3 menit pengisian daya |
| Suhu | Pemanasan ohmik yang lebih tinggi dan tingkat kenaikan suhu yang jauh lebih tinggi; mulai berkurang setelah 4 menit | Arus mulai menurun hanya setelah 4 menit pengisian, dan itu lebih tinggi dari itu untuk jenis banjir selama sisa periode pengisian. |
| Ketika arus untuk baterai VR menurun, laju kenaikan suhu menjadi lebih besar. Setelah 6 menit, meskipun suhu masih naik, laju kenaikan mulai menurun. Suhu mulai menurun perlahan hanya setelah sekitar 20 menit pengisian; dengan tegangan bebas hambatan konstan yang sama, baterai VR menerima arus yang lebih tinggi, yang menghasilkan lebih banyak panas. Energi yang dihabiskan untuk siklus oksigen sepenuhnya (100%) diubah menjadi panas, dibandingkan dengan sekitar 40% untuk dekomposisi air saja. |
Gambar 17. Pengisian: V ref = 2,45 V/sel; Arus, I, =3OO A maks; DO = 80%. [21. TG Chang, EM Valeriote dan DM Jochim, J. Sumber Daya 48 (1994) 163-175.]
Perbandingan pengisian cepat baterai yang kebanjiran dan baterai VRLA.

Tabel 7. Daya Tahan Baterai dengan MinitCharger ®
[22. K.Tomanschger, EV Valeriote, JS Klarchuk, TG Chang, MJ Dewar, V. Ferrone, dan DM Jochim, Proc. 13Konferensi Baterai Tahunan tentang Aplikasi dan Kemajuan, 13-16 Januari 1998, Long Beach, CA, 173-178. ]
| Jenis baterai | Siklus Hidup Baterai | ||
|---|---|---|---|
| Pengisi daya baterai konvensional | MinitCharger® | Sumber | |
| Sel Ni-Cd, tipe A | 500 | 1400 | INCO(1989) |
| Sel Ni-Cd, tipe B | 450 | 1900 | INCO(1996) |
| Sel Ni-MH, tipe A | 400 | 1600 | INCO (1996) |
| Sel Ni-MH, tipe B | 1500 | Lebih dari 4000 | INCO (1996) |
| Baterai Traksi asam timbal, tipe VRLA | 250 | 1500 | COMINCO (1997) |
Chang dan Jochim juga mendapatkan hasil yang serupa. Mereka menggunakan baterai VRLA 12V (tipe luka spiral) untuk uji siklus pengisian daya konvensional dan pengisian cepat [21. TG Chang, EM Valeriote dan DM Jochim, J. Sumber Daya 48 (1994) 163-175. 23. Chang, TG, Jochim, DM, J. Sumber Daya, 91 (2000) 177-192]. Siklus hidup adalah 250 siklus untuk rezim pengisian konvensional dan 1000 siklus untuk rezim pengisian cepat.
Pengisian sangat cepat telah bertemu dengan sukses besar dan menghasilkan kehidupan yang lebih tinggi. Sebuah survei menunjukkan bahwa Tim Riset Cominco [ 22. K. Tomanschger, EV Valeriote, JS Klarchuk, TG Chang, MJ Dewar, V. Ferrone, dan DM Jochim, Proc. 13th Konferensi Baterai Tahunan tentang Aplikasi dan Kemajuan, 13-16 Januari 1998, Long Beach, CA, 173-178.] melakukan survei dan tim menemukan bahwa tiga puluh jenis baterai asam timbal yang tersedia secara komersial mampu diisi ulang hingga 50% dalam 5 menit, 80% dalam 15 menit, dan 100% dalam 30 menit. Dalam hal ini, kinerja VRLAB lebih baik daripada baterai SLI yang kebanjiran.
Bahan aktif positif bermuatan konvensional dicirikan oleh partikel yang lebih besar dan banyak pori-pori besar. Dalam pelat bermuatan cepat tidak ada partikel besar, pori-pori atau rongga yang diamati. Pelat bermuatan konvensional menunjukkan luas permukaan PAM 2 m 2 /g dan pelat bermuatan pada arus tinggi menunjukkan nilai luas permukaan 3 m 2 /g bahkan setelah 900 siklus [22. K. Tomanschger, EV Valeriote, JS Klarchuk, TG Chang, MJ Dewar, V. Ferrone, dan DM Jochim, Proc. Konferensi Baterai Tahunan ke- 13 tentang Aplikasi dan Kemajuan, 13-16 Januari 1998, Long Beach, CA, 173-178 ] .
PAM dalam kasus terakhir hanya berkembang perlahan dan akibatnya lebih sedikit tekanan yang diberikan pada separator dan pelat negatif, sehingga mengurangi risiko korslet “merendam” di separator dan densifikasi NAM. Efek dramatis dari pengisian cepat adalah bahwa pada pengujian siklus hidup 12V/50Ah luka spiral VR LAB (ketika diuji di bawah rezim pengisian 10 jam dan 15 menit) baterai yang diisi secara konvensional hanya dapat memberikan 250 siklus (hingga 80% dari kapasitas awal) sedangkan mereka yang berada di bawah rezim pengisian cepat dapat memberikan siklus sekitar empat kali lebih banyak.
Gambar SEM dari PAM & NAM dari pelat konvensional dan cepat terisi

Hasil serupa juga diperoleh dalam karya PT Moseley [Journal of Power Sources 73 _1998. 122–126] Proyek ALABC-CSIRO No. AMC-009). Pengisian baterai tingkat tinggi dari baterai VRLA mengembalikan bahan aktif positif dalam bentuk luas permukaan tinggi yang dicirikan oleh kebiasaan seperti jarum dan ketika baterai diisi ulang pada tingkat yang lebih rendah, bahan aktif positif membentuk partikel yang lebih besar.

Diagram pengisi daya baterai



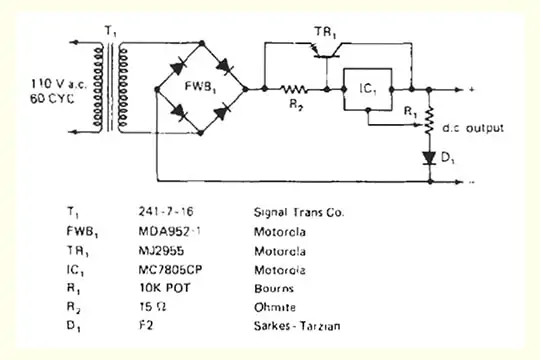

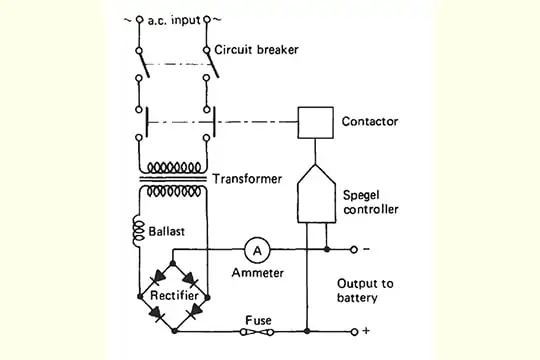

Berapa lama Anda bisa meninggalkan pengisi daya baterai di baterai?
Ini tergantung pada dua faktor:
- Apakah pengisi daya hidup atau tidak?
- Apakah ada ketentuan untuk memberikan biaya refresh intermiten di charger?
Jika pengisi daya dimatikan, mungkin tidak ada salahnya membiarkan baterai tetap terhubung ke pengisi daya, asalkan tidak ada bagian pengisi daya yang rusak, seperti sambungan kabel AC yang salah yang mengarah ke pengisi daya.
Namun, jika pengisi daya dihidupkan, baterai sebaiknya dicabut sehingga efek merusak dari pengisian daya yang berlebihan tidak mengurangi masa pakai baterai.
Jika ada ketentuan untuk memberikan pengisian daya yang terputus-putus di pengisi daya, Anda dapat membiarkan baterai tetap terhubung ke pengisi daya. Ini akan membantu menjaga baterai dalam kondisi terisi penuh dan dapat digunakan kapan saja baterai diperlukan.
Bagaimana cara kerja pengisi daya baterai mobil?
Sistem kelistrikan otomotif terdiri dari komponen-komponen berikut:
Sistem starter, penerangan, dan pengapian (sistem SLI) memiliki komponen/peralatan mekanik dan elektrik yang bekerja secara bersamaan untuk menghidupkan mesin dan menjaga kendaraan tetap beroperasi dengan baik.
Komponen utamanya adalah:
- Saklar pengapian
- Baterai 12V atau 24V.
- Motor DC Starter torsi tinggi (atau motor Cranking) dengan komponen terkait
- Pengaturan alternator-rectifier
- Pengontrol atau regulator Tegangan (Relai pemutus dan pemutus)
Ketika pengemudi menyalakan kunci kontak, arus besar mengalir dari baterai ke motor starter melalui sirkuit kontrol dan motor starter dapat memutar roda sehingga kendaraan mulai bergerak.
Tujuan dari motor starter adalah untuk membantu mesin mencapai kecepatan tertentu sehingga dapat bekerja. Oleh karena itu, starter membantu mesin mencapai kecepatan yang diinginkan untuk menjalankan mobil. Setelah selesai, starter tidak lagi berguna dan mati.
Dalam pengisi daya baterai otomatis, sirkuit sensor tegangan dimasukkan untuk merasakan tegangan baterai yang sedang diisi. Pengisi daya dimatikan secara otomatis ketika tegangan baterai mencapai tingkat optimal yang diperlukan.
Arus mengalir di sepanjang kabel tunggal dari terminal positif baterai ke komponen yang dialiri daya, dan kembali ke baterai melalui bodi logam mobil (yang dijadikan bumi, terminal negatif baterai terhubung ke bodi mobil). Tubuh terhubung ke terminal bumi (terminal negatif) baterai dengan kabel tebal.
Arus yang disuplai baterai ke motor starter adalah 3 sampai 4 kali kapasitas baterai, 150 sampai 400 ampere). Artinya, baterai mensuplai arus 3C hingga 4C ampere ke motor starter. Oleh karena itu, kabel yang membawa arus ini harus dirancang secara memadai untuk penurunan tegangan yang paling kecil. Dua fungsi utama dari sistem pengapian mobil adalah untuk menghasilkan tegangan yang cukup sehingga dapat dengan mudah membuat percikan api untuk membakar campuran udara/bahan bakar dan kedua menjalankan kontrol atas waktu percikan dan mengirimkannya ke silinder yang tepat. Sistem pengapian mobil yang khas menghasilkan tegangan di suatu tempat antara 20.000 volt dan 50.000 volt dari sumber 12 volt.
Ukuran baterai bervariasi dengan kapasitas mobil. Jadi, untuk mobil kecil seperti Maruti 800 atau Alto digunakan aki 12V/33 Ah, sedangkan untuk truk Tata atau Benz 12V atau 24 V/180 Ah digunakan aki.
Sistem pengisian mobil umumnya menghasilkan tegangan antara 13,5 dan 14,4 volt saat mesin bekerja. Ini menghasilkan arus listrik untuk mengoperasikan lampu mobil, sistem musik, pemanas, sistem kelistrikan mesin. Dahulu, generator DC digunakan di mobil. Pada awal tahun 60-an, sistem alternator-rectifier menggantikan generator DC karena kelebihannya dibandingkan yang lain. Tetapi dengan kemajuan listrik dan elektronik, semua mobil menggunakan pengaturan penyearah alternator (AC dihasilkan dan diubah menjadi DC.)
Pada mesin penyalaan bunga api, diperlukan suatu alat untuk menyalakan campuran udara-bahan bakar terkompresi pada akhir langkah kompresi. Sistem pengapian memenuhi persyaratan ini. Ini adalah bagian dari sistem kelistrikan yang membawa arus listrik pada tegangan yang diperlukan ke busi yang menghasilkan percikan pada waktu yang tepat. Ini terdiri dari baterai, sakelar, koil penyalaan distributor, busi, dan kabel yang diperlukan.
Mesin penyalaan kompresi, yaitu mesin diesel tidak memerlukan sistem pengapian apa pun, karena penyalaan sendiri campuran bahan bakar-udara terjadi ketika solar diinjeksikan ke dalam udara tekan pada suhu tinggi pada akhir langkah kompresi.
Untuk mencegah baterai terkuras, pabrikan menggunakan pengatur tegangan / Cut-Out. Menghubungkan/memutuskan generator dari baterai.
Ketika output generator lebih rendah dari tegangan baterai, maka generator terputus dari baterai. Sebaliknya, ketika output lebih tinggi, itu menghubungkan generator kembali ke baterai. Dengan demikian, ini mencegah baterai dari pemakaian pada kecepatan mesin yang lambat. Ketika tegangan terminal baterai mencapai sekitar 14,0 hingga 14,4 V. relai pemutus memutuskan baterai dari sirkuit pengisian.
Bisakah saya menyalakan mobil dengan pengisi daya baterai terpasang?
Jika seseorang tidak dapat menghidupkan kendaraan dengan baterai yang ada, tegangan DC yang sesuai dapat disuplai dari pengisi daya dengan memasang kabel pengisi daya seolah-olah itu adalah terminal baterai lain yang serupa. Ini seperti menghidupkan kendaraan dengan cara jump-start. Tindakan pencegahan yang tepat harus diambil sebelum melakukan pekerjaan ini. Bantuan dari seorang profesional harus dicari.
Apa pengisi daya terbaik berdasarkan aplikasi?
Pengisi Daya Baterai Inverter
Inverter adalah perangkat listrik/elektronik yang mengubah DC dari baterai menjadi AC untuk memasok kebutuhan rumah atau perusahaan kecil. Penyearah melakukan fungsi sebaliknya. Yaitu penyearah mengubah AC menjadi DC. DC adalah jenis arus listrik yang diperlukan untuk mengisi baterai dan mengoperasikan beberapa perangkat.
Inverter rumah biasanya memiliki satu atau dua baterai 12 V tergantung pada kebutuhan daya masing-masing rumah.
Uninterrupted Power Supply (UPS) adalah perangkat serupa, tetapi jeda waktu antara kegagalan daya utama dan dimulainya kembali UPS adalah segera (zero-time delay), sedangkan pada inverter waktu tunda adalah 10-20 milidetik. Di beberapa unit produksi dan bank, penundaan ini akan mengakibatkan kerugian besar dan memalukan bagi nasabah dan bankir. Misalnya, di komputer desktop rumah, layar akan mati saat terhubung ke inverter, sementara Anda tidak merasakan pemadaman listrik dalam kasus UPS.
Seperti yang kita ketahui dengan baik jika baterai diisi pada tegangan yang lebih tinggi dari 14,4 V per 12 V baterai, asap berbau busuk dan bau telur busuk yang tidak diinginkan akan keluar dari baterai, selain dari pembentukan produk korosi di sekitar terminal dan konektor. yang dapat membuat pengguna tidak nyaman, Oleh karena itu, baterai ini tidak diperbolehkan untuk mencapai tegangan pengisian daya lebih dari sekitar 14,0 V dan nilai pengaturan yang disukai adalah 13,8 V. Karena tegangan pengisian yang berkurang, kehilangan air karena elektrolisis juga berkurang, menghasilkan interval yang lama antara dua pengisian ulang dengan air yang disetujui. Dan penyearah gelombang penuh dengan filter adalah tambahan yang bagus.
Pengisi baterai untuk mobil
Sistem kelistrikan mobil menangani pengisian baterai SLI onboard. Seperti yang dibahas di bawah pengisian yang dimodifikasi, pengisian potensial konstan, sistem memiliki resistansi yang disertakan secara seri untuk menjaga arus lonjakan awal dalam batas yang diizinkan. Tegangan pengisian maksimum adalah 14,0 hingga 14,4 V untuk baterai 12 V. Baterai SLI menjadi baterai siklus dangkal menerima muatan setiap kali tegangan turun ke tingkat yang telah ditentukan.
Untuk pengisian, baterai dihubungkan ke stator alternator melalui alat elektronik yang disebut dioda, yang memungkinkan aliran hanya dalam satu arah, yaitu arus dari stator ke baterai dan tidak dalam arah sebaliknya ketika alternator idle. .
Oleh karena itu, ini mencegah pelepasan baterai yang tidak diinginkan.
Relai pemutus bertindak sebagai pemutus arus antara sistem pengisian dan baterai ketika alternator tidak menghasilkan arus apa pun. Ini mencegah pemakaian baterai jika generator tidak bekerja atau berjalan pada kecepatan yang sangat rendah.
Penambahan air secara berkala merupakan persyaratan perawatan pada baterai versi sebelumnya. Tapi, baterai canggih memiliki tingkat gas yang rendah dan penambahan air hampir dihilangkan, atau sekali dalam 12 hingga 18 bulan.
Pengisi daya baterai untuk aplikasi stasioner
Baterai stasioner adalah sumber catu daya darurat di beberapa instalasi, di mana pemutusan catu daya bahkan untuk sepersekian detik tidak dapat ditoleransi. Instalasi baterai besar yang dipanggil hanya untuk waktu yang sangat singkat untuk memasok daya disebut catu daya stasioner atau siaga atau darurat. Mereka digunakan dalam utilitas, switchgear, dan lingkungan industri lainnya. Baterai tersebut digunakan untuk menyediakan daya untuk periode awal sampai mereka dapat menghidupkan generator sehingga dapat mengambil alih fungsi tersebut.
Meskipun ada beberapa jenis baterai timbal-asam (baterai pelat datar, baterai Planté, baterai pelat kerucut, dll.) dan baterai nikel-kadmium (Ni-Cd) yang tersedia untuk aplikasi ini, sebagian besar pengguna lebih memilih baterai stasioner tabung tipe banjir. , khususnya, jenis OPzS, untuk tujuan ini.
Fitur yang paling penting dari bank baterai stasioner adalah pasokan langsung daya baterai dalam kasus kegagalan listrik normal. Karena itu baterai harus selalu dalam kondisi siap pakai terisi penuh. Oleh karena itu, sistem pengisian menjadi penting. Keandalannya sangat penting.
Baterai ini terisi penuh dengan mode potensial konstan. Mereka datang dalam kelompok tegangan 24, 48, 72, 120 dan 130 V. Kapasitas dapat berkisar dari 40 Ah hingga beberapa ribu ampere jam.
6 sampai 50 amp DC. Alarm internal disertakan untuk tegangan DC tinggi, tegangan DC rendah, gangguan ground positif dan negatif, dan pengosongan akhir. Pengisi daya baterai industri memiliki kontrol digital dan layar LCD. Sejumlah fitur keselamatan disertakan seperti perlindungan kabel di semua terminal medan dan perlindungan input AC dan output DC penuh
Panduan sederhana untuk membeli pengisi daya baterai
Berikut ini adalah panduan untuk memilih pengisi daya baterai:
- Ketahui tegangan baterai yang akan diisi. Untuk sel timbal-asam, untuk setiap sel, diperlukan 3 volt untuk pengisian yang memuaskan dan normal. Jadi, untuk baterai 12 V, beli pengisi daya dengan output DC 20 V di terminal.
- Datang ke rincian ampere (yaitu, arus): dari label baterai, cari tahu kapasitas baterai. Jika kapasitasnya 100 Ah pada kecepatan 10 jam, maka keluaran arus 10% sudah cukup. Jadi, pengisi daya 10 A disarankan. Tetapi Anda juga dapat menggunakan pengisi daya 15 A; maka biayanya akan lebih tinggi. Keuntungannya adalah baterai dapat diisi dalam waktu yang lebih singkat. Baterai dapat menyerap arus yang lebih tinggi pada periode awal. Jadi, Anda dapat mengisi daya pada 15 A untuk input 50% pertama dan kemudian mengurangi arus menjadi normal 10 %.
- Pengisi daya dapat dilengkapi dengan voltmeter dan ammeter digital atau analog. Fasilitas tambahannya adalah Ah meter digital. Juga, perlindungan polaritas terbalik dapat ditambahkan. Ini akan melindungi baterai dan pengisi daya.
- Penyearah gelombang penuh dengan filter bagus untuk mendapatkan masa pakai baterai yang lebih lama. Pengisi daya seperti itu akan menghasilkan riak AC yang rendah sehingga korosi pada kisi positif dan kenaikan suhu elektrolit selama pengisian akan lebih rendah.
- Untuk meringkas, untuk baterai 12 V/100 Ah, pengisi daya dengan nilai 20V/10 ampere dengan meter digital dan filter dengan penyearah gelombang penuh dan perlindungan polaritas terbalik adalah pembelian yang baik.
Pengisi baterai untuk kereta api
[Referensi: Handbook on 25 kW/4.5kW electronic rectifier cum regulator unit (ERRU) of SG TL &AC coach,) September 2019. “Layanan Umum: Penerangan Kereta”, oleh Institution of Railway Electrical Engineers (IREE), Pemerintah India, Kementerian Perkeretaapian, September 2010.]
Ke mana pun Anda pergi, listrik diperlukan dan gerbong kereta api tidak terkecuali untuk mengoperasikan lampu dan kipas angin. Untuk gerbong berpendingin udara (AC), cukup banyak listrik yang dibutuhkan untuk menjalankan unit pendingin udara yang dipasang di dalam gerbong.
Salah satu metode konvensional untuk menghasilkan listrik adalah dengan menggunakan alternator yang digerakkan oleh as roda gerbong kereta api dengan baterai berkapasitas ampere-jam yang cukup terhubung paralel untuk memasok daya ke gerbong selama kondisi tegangan rendah. Jenis pelatih ini disebut pelatih “Self-Generating (SG)”.
Dalam pelatih SG ini, Rectifier cum Regulator Units (RRUs) yang dikendalikan penguat magnetik digunakan pada awalnya untuk mengubah output AC alternator menjadi DC dan mengatur / mengontrol tegangan DC yang dihasilkan melalui pengaturan arus medan alternator. Ini juga mencegah aliran balik arus dari baterai ke alternator selama periode non-generasi.
Daya DC yang diperbaiki dan diatur ini digunakan untuk mengoperasikan berbagai peralatan dan aksesori listrik di dalam pelatih dan untuk mengisi baterai.
Baterai asam timbal dengan kapasitas 110 V / 120 Ah 10 disusun dari unit monoblok 3 sel di pelatih pengukur luas (BG) di kotak underslung. Empat nomor kotak terminal umpan darurat untuk BG dan satu nomor untuk pelatih MG disediakan di setiap dinding ujung untuk menghubungkan pelatih ke pelatih yang berdekatan untuk menerima daya, jika pembangkitan gagal.
Satu kotak terminal darurat nomor disediakan secara terpusat di setiap sisi rangka bawah untuk memfasilitasi pengisian baterai dari sumber eksternal. (Misalnya, ketika kereta berhenti di peron persimpangan Kereta Api). Untuk pelatih BG AC, alternator tanpa sikat 18 kW / 25 kW digunakan. Dua alternator tersebut digunakan di AC-2 Tier /AC-3 Tier / Chair Cars dan hanya satu alternator yang digunakan di bus AC Pertama. Baterai berkapasitas 800 / 1100 Ah pada rating 10 jam digunakan di mobil I AC / AC-2 Tier / AC-3 Tier/kursi dari BG Coaches.
Meskipun kereta api pertama di India menempuh 34 km dengan 400 orang pada tanggal 16 April 1883 dari Bori Bunder (sekarang dinamai Mumbai CST) ke Thane, sistem penerangan kereta api (TL) melalui dinamo yang digerakkan poros dipelopori oleh M/s. J. Stone & Co. datang ke Indian Railways hanya pada tahun 1930. Dinamo / alternator brushless yang digerakkan dari poros melalui sabuk datar / ‘V’, memasok beban saat kereta sedang bergerak dan mengisi baterai. Baterai memasok beban saat kereta berhenti di peron dan di tempat lain.
Sistem penerangan kereta api berikut ini sedang digunakan –
1) Sistem penggerak gandar bekerja pada suplai DC 110 V.
2) Generasi pertengahan dengan 415 V, 3 Fasa generasi AC 110 V pemanfaatan.
3) Pembangkitan akhir dengan pembangkitan 3 Fasa 415 V dan pemanfaatan AC 110 V
4) Pembangkitan akhir dengan pembangkitan 3 Fasa 750 V dan pemanfaatan AC 110 V
Semua gerbong yang sedang dibangun hanya memiliki sistem 110 V. Bus yang dioperasikan dalam sistem 24 V telah diubah menjadi sistem 110 V.
Peringkat standar di terminal keluaran DC ERRU untuk peringkat yang berbeda dari alternator diberikan di bawah ini:
(i) 25 kW, 130V, 193A
(ii) 4,5 kW 128.5V 35A
ERRU dipasang di rangka bawah pelatih dan dirancang untuk bekerja dengan baik dalam suhu mulai dari -5 derajat hingga 55 derajat C dan kelembaban relatif 98%. Ini juga dirancang untuk bekerja di area yang sangat berdebu, untuk menahan getaran servis dan guncangan shunting.
Transmisi daya melalui V-belt. Total 12 No. (6 di setiap sisi) dan 4 no. (hanya satu sisi) dari ukuran C-122 disediakan masing-masing pada alternator AC dan TL. Kecepatan alternator bervariasi dari 0 hingga 2500 RPM. Diameter roda gerbong adalah 915 mm saat baru dan 813 mm saat aus sepenuhnya, diameter roda baru harus dipertimbangkan untuk membuat perhitungan kecepatan kereta dalam km/jam sesuai dengan kecepatan potong dan Kecepatan Minimum untuk Output Penuh (MFO) kecepatan alternator.
Karakteristik output dari unit pengatur penyearah elektronik (ERRU) (baik 25 kW dan 4,5 kW) diberikan di bawah ini:
Tegangan keluaran DC tanpa beban adalah maksimum 135 V, yang dapat diatur pada 128 ± 0,5 V, 97 A (untuk baterai 1100 dan 650 Ah ) dan 128 ± 0,5, 19 A untuk baterai 120 Ah ) pada 1500 rpm (di tengah antara kecepatan minimum dan maksimum), pengaturan tegangan menjadi ± 2 %, efisiensi 95% (minimum). Riak tegangan dijaga dalam 2 %. Variasi beban 10 A sampai 193 A pada kecepatan 400 rpm sampai 2500 rpm (untuk baterai 1100 dan 650 Ah) dan 350 RPM sampai 2500 rpm (baterai 120 Ah).
Untuk baterai berkapasitas lebih tinggi, tegangan pada kelebihan 15% adalah 120 V (minimum) pada 222 A, arus dibatasi hingga 230A (maksimum). Untuk baterai 120 Ah, tegangan pada kelebihan beban 40 A diatur pada 115 V (minimum).
Batas arus pengisian baterai adalah 220 A untuk baterai 1100 Ah, 130 A untuk baterai 650 Ah dan 24 A untuk baterai 120 Ah (maksimum). Dua parameter terakhir dapat diatur dari Universal Voltage Controller (UVC) serta dari Coach Indication Panel (CIP).
Untuk EERU 4,5 kW, variasi beban akan menjadi 1 A hingga 37,5 A pada 350 RPM hingga 2500 rpm. Tegangan pada beban lebih 40 A adalah 115 V (minimum), arus dibatasi hingga 43A (maksimum).
Kita dapat melihat bahwa arus pengisian adalah 1100/220 = 5; 650/130= 5 dan 120/24 = 5. Artinya arus pengisian dibatasi untuk semua baterai ini adalah C/5 ampere, tegangan maksimum menjadi 128 V. (yaitu, 16% di atas OCV bank baterai).
Untuk lebih jelasnya diagram blok untuk The Overall Coach, pengkabelan akan seperti diagram berikut dan Diagram Blok Sistem Alternator-ERRU, tautan yang diberikan di bawah ini dapat dirujuk:
Pengisi daya baterai traksi
Kinerja dan masa pakai baterai Forklift dipengaruhi oleh pengisi daya baterai traksi dan metode pengisian yang digunakan. Pengisi daya baterai forklift harus dipilih sesuai dengan tegangan dan Ah baterai.
Pengisi daya baterai Forklift yang bagus
- Harus membatasi kenaikan suhu saat mengisi daya
- Tanpa pengisian yang berlebihan, pengisi daya harus berhenti memasok arus ke baterai pada waktu yang tepat
- Harus memiliki fasilitas biaya pemerataan (yaitu, pengisian pada arus yang lebih tinggi).
- Dalam kasus situasi berbahaya, fasilitas auto-shut-off harus disediakan.
- Harus dapat diprogram melalui mikroprosesor atau PC.
- Di beberapa pengisi daya, agitasi udara melalui pipa udara tipis di dalam sel juga disediakan.
Rentang tegangan pengisian bervariasi dari 24 V hingga 96 V.
Arus tergantung pada kapasitas baterai, yang berkisar antara 250 Ah hingga 4000 Ah
Metode pengisian daya baterai traksi
Pengisian lancip satu langkah: Pengisi daya mulai bekerja pada sekitar 16A/100Ah dan arus mengecil saat voltase sel naik. Ketika tegangan sel mencapai 2,4V/sel, arus mengecil menjadi 8A/100 Ah dan kemudian mencapai tingkat akhir 3 hingga 4 A/100 Ah. Pengisian daya dimatikan oleh timer. Mungkin diperlukan sekitar 11 hingga 13 jam (faktor input Ah 1,20) untuk baterai yang habis 80% tanpa pengadukan udara.
Perbedaan waktu pengisian disebabkan oleh variasi arus start, yaitu jika arus start 16 A/100 Ah, durasinya lebih kecil dan jika 12A/100Ah durasinya lebih lama. Dengan fasilitas pengadukan udara, durasinya dikurangi menjadi 9 hingga 11 jam (faktor input Ah 1.10).
Pengisian lancip dua langkah (mode CC-CV-CC): Ini merupakan peningkatan dari metode sebelumnya. Pengisi daya dimulai dengan arus yang lebih tinggi dari 32 A / 100 Ah. Ketika tegangan sel mencapai 2,4 V per sel, pengisi daya secara otomatis beralih ke mode lancip dan arus terus meruncing hingga 2,6 V per sel tercapai dan arus menuju tingkat akhir 3 hingga 4 A/100 Ah dan berlanjut selama 3 hingga 4 jam. Mungkin diperlukan waktu sekitar 8 hingga 9 jam (faktor input Ah 1,20) untuk baterai yang habis 80% tanpa pengadukan udara. Dengan fasilitas pengadukan udara, durasinya dikurangi menjadi 7 hingga 8 jam (faktor input Ah 1.10).
Pengisian baterai VRLA Gel: (mode CC-CV-CC):
Pengisi daya dimulai dengan arus 15 A / 100 Ah. Ketika tegangan sel mencapai 2,35 V per sel, pengisi daya secara otomatis beralih ke mode lancip dan pengisi daya masuk ke mode CV pada tegangan yang sama. Ini membutuhkan waktu maksimal 12 jam. Langkah CV dipertahankan konstan selama arus muatan turun ke nilai terbatas 1,4 A/100 Ah. Fase kedua dapat berlangsung selama beberapa jam, maksimal 4 jam. Durasi ini tergantung pada durasi fase pertama.
Pengisi daya baterai forklift frekuensi tinggi
Charger yang ada umumnya ada dua jenis: ferro-resonant dan silicon controlled rectifier (SCR). Mereka lebih terjangkau, tetapi mereka juga kurang efisien.
Pengisi daya baterai yang menggabungkan perangkat daya switching frekuensi tinggi, misalnya, MOSFET (Transistor Efek Medan Semikonduktor Logam Oksida) dan IGBT (Transistor Bipolar Gerbang Terisolasi) beroperasi pada frekuensi yang jauh lebih tinggi daripada frekuensi saluran (beberapa kHz hingga beberapa ratus kHz). Sebaliknya, MOSFET dan IGBT, dengan kemampuan hidup/mati penuh, dapat dikontrol dengan tepat setiap saat untuk memungkinkan pengisi daya menghasilkan keluaran yang diinginkan. SCR adalah perangkat setengah terkontrol dengan turn-off yang tidak terkendali.
Pengisi daya HF berfungsi sebagai catu daya switching, yang berarti mereka menghidupkan dan mematikan sakelar elektronik pada frekuensi tinggi (50-170 kHz).
Keunggulan teknologi HF ini antara lain:
| Pengisi daya baterai frekuensi tinggi | |
|---|---|
| Frekuensi Tinggi hingga 170 kHz | Kerugian dari konversi lebih rendah |
| Peningkatan efisiensi pengisian daya (87 hingga 95%) | Biaya energi lebih rendah (hingga 20%) karena penghematan energi |
| Mengurangi arus riak AC | Hidup lebih lama karena kenaikan suhu yang lebih rendah. Biaya perawatan yang lebih rendah karena kehilangan air yang lebih rendah |
| Ini dapat disesuaikan secara universal | Baterai yang kebanjiran, AGM, dan gel semuanya dapat diisi tanpa pengisian yang berlebihan atau pengisian yang kurang. |
| Ukuran lebih kecil, bobot lebih ringan, dan lebih hemat tempat | Ini memiliki ruang kaki yang lebih kecil dan dapat dengan mudah dipasang di pesawat |
| Pengisi daya tersebut tersedia dalam rentang yang berbeda dari pengisi daya untuk baterai 24 V hingga 80 V dengan arus pengisian 40 hingga 300 A. | |
Pengisi daya baterai untuk aplikasi baterai penambangan bawah tanah
Baterai pertambangan bawah tanah terutama baterai timbal-asam siklus dalam. Tegangan tipikal berkisar antara 48 dan 440 V, dan kapasitas berkisar dari 700 Ah hingga 1550 Ah.
Pengisian baterai ini mirip dengan pengisian baterai traksi. Baterai diisi pada
2,6 V awalnya dengan arus 21 A hingga 17 A per 100 Ah dan akhirnya 4,5 A per 100 Ah sebagai kecepatan akhir. Pengisian daya dapat diselesaikan dalam 6 hingga 8 jam.
Baterai sesuai dengan IS 5154:2013 Bagian 1 (IEC 60254-2006)
Pengisi baterai laut
Baterai untuk aplikasi kelautan dapat diklasifikasikan menjadi dua jenis. Baterai starter memiliki pelat yang lebih tipis dan mampu menghasilkan ledakan daya yang besar untuk waktu yang singkat. Jenis lainnya adalah baterai siklus dalam yang digunakan untuk aplikasi kelautan lainnya seperti aksesori elektronik, motor trolling, dan peralatan listrik dan elektronik onboard. Selain itu, baterai fungsi ganda berfungsi sebagai baterai SLI dan baterai siklus dalam. Pengisi daya khusus digunakan untuk baterai tertentu. Mode CC-CV harus digunakan pada baterai asam timbal VR.
Ada juga charger yang bisa mengisi hingga empat baterai secara bersamaan. Semua jenis baterai laut, baterai VR (baik AGM dan gel) serta baterai banjir perawatan rendah dapat diisi.
Karena baterai dan pengisi daya digunakan di kapal, baterai dan pengisi daya harus tetap kering dan memiliki ventilasi yang cukup. Mereka juga harus tahan air, tahan goncangan dan tahan getaran dan jika perlu disegel sepenuhnya. Selain itu, Anda harus memastikan pengisi daya memiliki fitur perlindungan polaritas terbalik dan kemampuan anti percikan.
Pengisi daya baterai untuk aplikasi surya
Karena variasi penyinaran matahari, output panel SPV berfluktuasi. Hasilnya, pelacak titik daya maksimum digital (MPPT) terhubung antara panel SPV dan baterai untuk memastikan proses pengisian daya tanpa khawatir. MPPT adalah konverter DC ke DC elektronik yang dirancang untuk mengoptimalkan kecocokan antara panel surya (panel PV) dan bank baterai. Ini merasakan output DC dari panel surya, mengubahnya menjadi AC frekuensi tinggi dan turun ke tegangan dan arus DC yang berbeda agar sesuai dengan kebutuhan daya baterai. Manfaat memiliki MPPT dijelaskan di bawah ini.
Sebagian besar panel PV dibuat untuk output 16 hingga 18 volt, meskipun peringkat tegangan nominal panel SPV adalah 12 V. Tetapi baterai 12 V nominal mungkin memiliki rentang tegangan aktual 11,5 hingga 12,5 V (OCV) tergantung pada keadaan muatan (SOC). Dalam kondisi pengisian, komponen tegangan ekstra harus dikirim ke baterai. Dalam pengontrol muatan normal, daya ekstra yang dihasilkan oleh panel SPV dihamburkan sebagai panas, sementara MPPT merasakan kebutuhan baterai dan memberikan daya yang lebih tinggi jika daya yang lebih tinggi dihasilkan oleh panel SPV. Dengan demikian, pemborosan, undercharge dan overcharge dihindari dengan menggunakan MPPT.
Suhu mempengaruhi kinerja panel SPV. Ketika suhu naik, efisiensi panel SPV menurun. (Catatan: Ketika panel SPV terkena suhu yang lebih tinggi, arus yang dihasilkan oleh panel SPV akan meningkat, sedangkan tegangan akan berkurang. Karena penurunan tegangan lebih cepat daripada kenaikan arus, efisiensi panel SPV menurun.). Sebaliknya, pada suhu yang lebih rendah, efisiensi meningkat. Pada suhu lebih rendah dari 25 °C (yang merupakan suhu kondisi uji standar ( STC ), efisiensi meningkat. Tetapi efisiensi akan seimbang dalam jangka panjang.




