லித்தியம் அயன் பேட்டரி எவ்வாறு செயல்படுகிறது
லெட் ஆசிட் பேட்டரிகள் பழைய தொழில்நுட்பம் என்பது பொது களத்தில் உள்ள கருத்து. லித்தியம் அயன் பேட்டரி வேறுபட்ட கருத்தைக் கொண்டுள்ளது, இது நவீனமானது, தூய்மையானது, இது 3 அல்லது 4 மடங்கு ஆற்றல் அடர்த்தி மற்றும் நீண்ட சுழற்சி ஆயுளைக் கொண்டுள்ளது. இவை அனைத்திலும், 150 ஆண்டு பழமையான லெட் ஆசிட் தொழில்நுட்பம் என்ன சாத்தியமான நன்மைகளை அட்டவணையில் கொண்டு வர முடியும்? உண்மையில், எல்லாம் தோன்றுவது போல் இல்லை, சந்தைப்படுத்தல் உரிமைகோரல்களில் பயன்படுத்தப்படும் தரவுகளின் தலைப்புச் செய்திகளைப் பாருங்கள், பின்னர் சிறிது பொது அறிவு, அடிப்படை ஆராய்ச்சி மற்றும் சில அடிப்படை அறிவியலைப் பயன்படுத்துங்கள். உண்மையான கதை வித்தியாசமாக இருப்பதை நீங்கள் காண்பீர்கள்.
முதல் தவறான கருத்து அளவு மற்றும் குறிப்பிட்ட ஆற்றல் அடர்த்தி பற்றியது. 4 முதல் 5 மடங்குகளின் தலைப்பு மதிப்புகள் குறிப்பிட்ட ஆற்றல் அடர்த்தி மற்றும் குறைந்த எண்ணிக்கையிலான லித்தியம் அயன் பேட்டரி வேதியியல் ஆகியவற்றுடன் மட்டுமே தொடர்புடையது, அவற்றில் சில இன்னும் வணிகப் பயன்பாட்டில் இல்லை. படம். 2 லித்தியம் அயன் பேட்டரி கலங்களுக்கான பல கேத்தோட்களை ஒப்பிடுகிறது, இவை பாதுகாப்பான Li-FePO4 வேதியியலுக்கு சுமார் 100Wh/kg முதல் நிக்கல்-கோபால்ட்-அலுமினியம் ஆக்சைடு மாறுபாட்டிற்கு 200Wh/kg வரை இருக்கும். லீட் ஆசிட் பேட்டரி வரைபடம் கீழே கொடுக்கப்பட்டுள்ளது:


இந்த மதிப்புகள் ஒற்றை செல் நிலைக்கு மட்டுமே பொருந்தும், பேக் அல்லது சேவை நிலையில் அல்ல. படம். 3 செல் மற்றும் சிஸ்டம் மட்டத்தில் வெவ்வேறு பேட்டரி வேதியியலின் ஆற்றல் அடர்த்தியைக் காட்டுகிறது. அனைத்து இணைப்புகள், குளிரூட்டல், பாதுகாப்பு மற்றும் பேட்டரி மேலாண்மை கருவிகளுடன் முழுமையாக நிறுவப்பட்டால், லித்தியம் அயன் பேட்டரி செல்களின் ஆற்றல் அடர்த்தி நடைமுறையில் பாதியாகக் குறைக்கப்படுகிறது.
குறிப்பிட்ட ஆற்றல் அடர்த்தியின் 3 முதல் 5 மடங்கு செல் நிலை நன்மை 2 முதல் 3 மடங்கு வரை குறைக்கப்படுகிறது. லித்தியம் கேத்தோடு வேதியியலைச் சார்ந்து, சில பயன்பாடுகளில் முழுமையாக நிறுவப்பட்ட பேட்டரி அமைப்பிற்கான லித்தியம் அயன் பேட்டரிகள் மற்றும் லெட் ஆசிட் பேட்டரிகள் ஆற்றல் அடர்த்தி ஆகியவற்றுக்கு இடையே உள்ள சமநிலையை நாம் பார்க்க முடியும்.
மற்றொரு காரணி, சுழற்சி வாழ்க்கை, குழப்பத்திற்கு ஒரு ஆதாரமாகும். லித்தியம் அயன் பேட்டரி திறன் அதன் பெயர்ப்பலகை மதிப்பீட்டில் 80% க்குக் கீழே குறைவதற்கு முன்பு எத்தனை சுழற்சிகளைச் செய்ய முடியும்? இரண்டா, மூவாயிரமா? அட்டவணை 1 செயல்திறன் மற்றும் சுழற்சி வாழ்க்கைக்கான வெவ்வேறு லி-அயன் கேத்தோடு பொருட்களின் சுருக்கத்தை வழங்குகிறது.
லீட் ஆசிட் பேட்டரி வேதியியலின் நன்மைகள்
பேட்டரிகள் விசித்திரமான சாதனங்கள். யாரும் அவர்களை விரும்பவில்லை, ஆனால் அனைவருக்கும் அவை தேவை. தேவைப்படும் போது மட்டுமே அவை வாங்கப்படுகின்றன. பேட்டரிகளுக்கான உள்ளூர் மாலுக்கு ஜன்னல் கடைக்குச் செல்ல எத்தனை பேர் திட்டமிட்டுள்ளனர்? அவை வெறுக்கத்தக்க கொள்முதல் மற்றும் முற்றிலும் தேவைப்படும் போது மட்டுமே வாங்கப்படுகின்றன. ஒரு நல்ல விற்பனையாளர் உங்களிடம் பணம் இருந்தால் இரண்டு ஜோடி காலணிகள், இரண்டு கார்கள் மற்றும் இரண்டு வீடுகளை விற்கலாம், ஆனால் அவர் உங்களுக்கு இரண்டு SLI ஆட்டோமொபைல் பேட்டரிகளை விற்க முடியாது. சோலார் பேனலுக்கான சோலார் பேட்டரி , எலக்ட்ரிக் பைக் அல்லது யுபிஎஸ் மற்றும் இன்வெர்ட்டர் பேட்டரி பேக்அப் சிஸ்டம் அல்லது ஃபோர்க்லிஃப்ட்களுக்கான இழுவை பேட்டரி என நீங்கள் பேட்டரியை வாங்கும்போது, அதைப் பற்றி மேலும் தெரிந்து கொள்ள வேண்டாமா?
லெட் ஆசிட் பேட்டரிகள் எவ்வாறு வேலை செய்கின்றன, வகைகள் மற்றும் மாதிரிகள் இடையே உள்ள வேறுபாடுகள் என்ன, வெவ்வேறு வேதியியல் எப்படி? அவை விலை உயர்ந்ததாக இருக்கலாம். வணிக அல்லது உள்நாட்டு பயன்பாட்டில், ஈய அமில பேட்டரியை மாற்றுவதன் ஆயுள் மற்றும் செலவு என்ன? உங்களுக்கு தேவையான அளவு, கிடைக்கும் இடம், லீட் ஆசிட் பேட்டரியின் ஆற்றல் திறன் மற்றும் ரீசார்ஜ் நேரம்? பின்னர், பாதுகாப்பு, அகற்றல் மற்றும் கார்பன் தடம் ஆகியவற்றின் மறைக்கப்பட்ட செலவுகள் உள்ளன. இந்தக் கட்டுரை லீட் ஆசிட் பேட்டரிகளை லித்தியம் அயன் பேட்டரியுடன் ஒப்பிடுகிறது மற்றும் இந்த இரண்டு வேதியியலுடனும் தொடர்புடைய பல தவறான கருத்துக்களைக் குறிக்கிறது.
எந்த லித்தியம் அயன் பேட்டரி சிறந்தது
| கத்தோட் பொருள் | குறுகிய பெயர் | பெயரளவு மின்னழுத்தம் | குறிப்பிட்ட ஆற்றல் Wh/kg (செல்) | சுழற்சி வாழ்க்கை | கருத்துகள் |
|---|---|---|---|---|---|
|
லித்தியம் கோபால்ட் ஆக்சைடு (LiCoO2) |
LCO | 3.6 | 150-200 | 500-1000 | போர்ட்டபிள் சாதனங்கள் - அதிக கட்டணம் வசூலித்தால் வெப்ப ரன்வே |
| லித்தியம் மாங்கனீஸ் ஆக்சைடு (LiMn2O4) | LMO | 3.7 | 100-150 | 300-700 | சக்தி கருவிகள், மருத்துவ சாதனங்கள் - LCO ஐ விட பாதுகாப்பானது |
| லித்தியம் நிக்கல் மாங்கனீஸ் கோபால்ட் ஆக்சைடு (LiNiMnCO2) | என்எம்சி | 3.6/3.7 | 150-220 | 1000-2000 | மின்-பைக்குகள், EV, தொழில்துறை - உயர் சுழற்சி வாழ்க்கை |
| லித்தியம் இரும்பு பாஸ்பேட் (LiFePO4) | LFP | 3.2 | 90-120 | 1000-2000 | EV, SLI, Leisure - அனைத்து லித்தியம் அயன் பேட்டரி இரசாயனங்களில் பாதுகாப்பானது |
| லித்தியம் நிக்கல் கோபால்ட் அலுமினியம் ஆக்சைடு (LiNiCoAlO2) | NCA | 3.6 | 200-260 | 500 | தொழில்துறை, EV பவர்டிரெய்ன் (டெஸ்லா) TR இல் 150C, CL 500 |
| லித்தியம் டைட்டனேட் (Li4Ti5O12) | LTO | 2.4 | 50-80 | யுபிஎஸ், சோலார், ஈவி பவர்டிரெய்ன் (ஹோண்டா, மிட்சுபிஷி). CL 3000-7000 - மிகவும் பாதுகாப்பானது |
காணக்கூடியது போல, அனைத்தும் 800 முதல் 2000 சுழற்சி வரம்பிற்குள் அடங்கும். ஒப்பிடுகையில், நன்கு வடிவமைக்கப்பட்ட லெட் ஆசிட் பேட்டரி 1600 சுழற்சிகளுக்கு மேல் 80% DOD வரை எளிதாக அடைய முடியும். உரிமையின் விலையைக் கருத்தில் கொள்ளும்போது இவை அனைத்தும் எவ்வாறு சேர்க்கப்படுகின்றன? இது லீட்-ஆசிட் பேட்டரியின் விலையான அடுத்த கட்டத்திற்கு நம்மைக் கொண்டுவருகிறது. லீட்-ஆசிட் பேட்டரியுடன் ஒப்பிடும்போது லித்தியம்-அயன் பேட்டரியின் விலை எவ்வளவு? லித்தியம் அயன் பேட்டரி உற்பத்தி ஆலையின் விலை? இயற்கையாகவே, லித்தியம் அயன் பேட்டரி விலை அதிகம் ஆனால் எவ்வளவு அதிகம். மீண்டும், இது கருதப்படும் அளவைப் பொறுத்தது. லி-அயன் விலைகள் வீழ்ச்சியடைந்து வருவதாகவும், இப்போது ஈய அமிலத்தை விட 2-3 மடங்கு வரம்பில் இருப்பதாகவும் செய்திக்குறிப்புகள் நமக்குச் சொல்லும்.
உண்மையில்? லித்தியம் அயன் பேட்டரி மற்றும் லெட் ஆசிட் பேட்டரிகள் இரண்டிற்கும் வணிக ரீதியாகக் கிடைக்கும் 12V மற்றும் 100 Ah இன் ஓய்வுநேர பேட்டரிகளின் விலைகளைப் பெறுவதற்கான சமீபத்திய UK இணையத் தேடலின் சராசரி விலைகள்:
லித்தியம் அயன் பேட்டரி $960 அல்லது $800/kwh
லீட் ஆசிட் பேட்டரி $215 அல்லது $180/kwh
வெளிப்படையாக, லித்தியம் அயன் பேட்டரியின் ஆயுள் அதே மதிப்பைப் பெறுவதற்கு ஈய அமில பேட்டரிக்கு சமமான 4 மடங்கு அதிகமாக இருக்க வேண்டும். நாம் பார்த்தபடி, இது அப்படி இல்லை.


எல்லா சந்தர்ப்பங்களிலும், சிறந்த சார்ஜ் ஏற்று மற்றும் நீண்ட சுழற்சி ஆயுளைக் கொடுக்க பெரிய லீட்-அமில பேட்டரி பொருத்தப்பட்டாலும், லீட்-அமில பேட்டரி கட்டுமானம் மிகவும் செலவு குறைந்ததாக இருந்தது. இந்த எடுத்துக்காட்டில், பயன்பாடு இந்தியாவில் தொலைத்தொடர்பு கோபுரமாக இருந்தது. இதே கொள்கை பெரும்பாலான பயன்பாடுகள் மற்றும் புவியியல் ஆகியவற்றில் உண்மையாக உள்ளது, மேலும் குளிர் காலநிலையில். மற்ற தவறான கருத்து என்னவென்றால், லி-அயன் ஒரு தூய்மையான தொழில்நுட்பம் மற்றும் ஈய-அமிலத்தை விட குறைவான மாசுபடுத்தும். வெவ்வேறு பேட்டரி வேதியியலுக்கான தொட்டில் இருந்து வாயில் உமிழ்வு படம் கொடுக்கப்பட்டுள்ளது. 5 மற்றும் 6.
இந்த எண்ணிக்கை பேட்டரி உற்பத்திக்கான செயல்பாடுகளின் எல்லையைக் காட்டுகிறது. மூலப்பொருட்களைப் பிரித்தெடுத்தல் மற்றும் கொண்டு செல்வதில் இருந்து அனைத்து செயலாக்கப் படிகளிலும் பேட்டரிகள் அனுப்பத் தயாராக இருக்கும் இடம் வரை.
அட்டவணை 2 என்பது வெவ்வேறு ஆயுட்காலங்களில் வேலை செய்யும் லித்தியம் அயன் பேட்டரி மற்றும் லெட் ஆசிட் பேட்டரியைப் பயன்படுத்துவதன் பொருளாதாரத்தை ஒப்பிடும் நிஜ வாழ்க்கைச் சூழ்நிலையாகும்.
| விலை பொருள் | தினசரி இயங்கும் செலவு USD | தினசரி இயங்கும் செலவு USD |
|---|---|---|
| 3 ஆண்டுகள் | லீட் ஆசிட் பேட்டரி | லித்தியம் அயன் பேட்டரி |
| பணமதிப்பு நீக்கம் | 8.30 | 16.90 |
| டீசல் (வழங்கப்பட்டது) | 15.50 | 15.50 |
| பராமரிப்பு | 2.46 | 2.46 |
| மின்சாரம் | 1.47 | 1.47 |
| பேட்டரி சார்ஜிங் | 0.65 | 0.50 |
| மொத்த நாள்/மாதம் | 28.38/851 | 36.83/1105 |
| 6 வருடம் | ||
| பணமதிப்பு நீக்கம் | 5.86 | 8.46 |
| டீசல் | 15.50 | 15.50 |
| பராமரிப்பு | 2.46 | 2.46 |
| மின்சாரம் | 1.47 | 1.47 |
| பேட்டரி சார்ஜிங் | 0.54 | 0.50 |
| மொத்த நாள்/மாதம் | 25.83/775 | 28.39/852 |
ஆர்கோன் நேஷனல் லேபரேட்டரீஸின் இந்தத் தரவு, லித்தியம் அயன் பேட்டரிகளுக்கான மூலப்பொருட்களைப் பிரித்தெடுத்தல் மற்றும் கொண்டு செல்வது உள்ளிட்ட மொத்த உற்பத்தி செயல்முறையானது ஈய அமில மதிப்பை விட 4 மடங்கு அதிகமாக இருப்பதைக் காட்டுகிறது. பொருட்களை பிரித்தெடுப்பது குறித்து, கோபால்ட் மற்றும் மாங்கனீசு மற்றும் லித்தியம் போன்ற அடிப்படை கேத்தோடு பொருட்கள் வழங்கப்படுவது முற்றிலும் உறுதியாகவில்லை. பிரித்தெடுத்தல் மற்றும் மீட்பு செயல்முறைகள் உள்ளன, ஆனால் தேவைகள் கணிசமாக அதிகரித்தால் சுரங்கங்கள் மற்றும் உற்பத்தி தளங்களின் எண்ணிக்கை விநியோகத்தை கட்டுப்படுத்தலாம். புவி-அரசியல் வரைபடம் இந்த பொருட்களின் சில ஆதாரங்களுக்கான நிச்சயமற்ற தன்மையையும் முன்னறிவிக்கிறது.
லித்தியம் அயன் பேட்டரிகள் மறுசுழற்சி செய்யக்கூடியவை
இந்த இரசாயனங்களின் மறுசுழற்சி மற்றும் பாதுகாப்பு முக்கியமான காரணிகள். லீட் ஆசிட் பேட்டரிகளில் உள்ள அனைத்து கூறுகளும் 100% மறுசுழற்சி செய்யப்படுகின்றன என்பது அறியப்படுகிறது, அதேசமயம் லித்தியம் அயன் பேட்டரியை மறுசுழற்சி செய்வதற்கான வணிக செயல்முறைகள் எதுவும் இல்லை. Li, Co, Mn போன்ற அதிக விலையுயர்ந்த கூறுகள் மொத்த லித்தியம் அயன் பேட்டரியில் ஒரு சிறிய பகுதியே என்பதை நீங்கள் கருத்தில் கொள்ளும்போது இந்த நிலைமை புரிந்துகொள்ளத்தக்கது. உதாரணமாக, லித்தியம் மொத்த செல் எடையில் 4% ஆகும். லித்தியம் அதிக வினைத்திறன் கொண்டது (அதன் உயர் ஆற்றல் அடர்த்தியின் அடிப்படை) என்ற வெளிப்படையான உண்மையை இதனுடன் சேர்க்கவும், இது கழிவுகளிலிருந்து பிரித்தெடுப்பதை விலை உயர்ந்ததாக ஆக்குகிறது.
அதன் கட்டுமானத்தில் பல்வேறு பொருட்களுடன் சிக்கலான கூடுதல் காரணி தொழில்நுட்ப ரீதியாகவும் பொருளாதார ரீதியாகவும் மறுசுழற்சி கடினமாக்குகிறது. முடிவு? இந்த பேட்டரிகளை மறுசுழற்சி செய்வதற்கு எந்த வணிக ஊக்கமும் இல்லை. இந்த காரணத்திற்காக, மறுசுழற்சி வசதிகள் இன்னும் முன்னோடி கட்டத்தில் உள்ளன மற்றும் பெரும்பாலும் அரசாங்க நிதியுதவியுடன் உள்ளன.
தற்போது, ஸ்கிராப் செய்யப்பட்ட லித்தியம் அயன் பேட்டரியின் பெரும்பாலானவை, அவற்றின் மறுசுழற்சியை கட்டாயப்படுத்துவதற்கான தொழில்நுட்ப முன்னேற்றம் அல்லது சட்டத்திற்காக காத்திருக்கின்றன. பிந்தையது செயல்படுத்தப்பட்டால், இறுதியில் நுகர்வுக்கு ஒரு செலவு இருக்கும். இது லீட் ஆசிட் பேட்டரி வகைகளுடன் ஒப்பிடும்போது லி-அயன் கலத்தின் விலையை மேலும் அதிகரிக்கும்.
லித்தியம் அயன் பேட்டரி வெடிக்க முடியுமா?
இறுதியாக, எங்களுக்கு பாதுகாப்பு உள்ளது. கையடக்க எலக்ட்ரானிக் சாதனங்கள் மற்றும் மின்சார வாகனங்களில் கூட லி-அயன் பேட்டரியைப் பயன்படுத்துவது எங்களுக்குத் தெரியும் என்பதால், எங்கள் அறிவுக்கு எந்த லெட் ஆசிட் பேட்டரி பயன்பாடுகளும் பாதுகாப்பு திரும்பப் பெறவில்லை. படம். இந்த கட்டுரையை எழுதும் நேரத்தில், சில வாரங்களுக்கு முன்பு இங்கிலாந்தில் ஒரு புதிய கலப்பின வால்வோவுக்கு என்ன நடந்தது என்பதை 7 காட்டுகிறது. இந்நிலையில் அதன் லித்தியம் அயன் பேட்டரிகள் சார்ஜ் செய்யும் போது தீப்பிடித்தது.
லித்தியம் அயன் பேட்டரி எரிகிறது
படம் 7 வால்வோ ஹைப்ரிட் மின்சார வாகனத்தில் லி-அயன் பேட்டரியால் ஏற்பட்ட தீ: ஏப்ரல் 2018-யுகே குடியிருப்பு


இந்த வீடியோவில் லித்தியம் பேட்டரியால் ஏற்பட்ட மிக சமீபத்திய தீ விபத்தை காட்டுகிறது. செல்களில் ஏற்றத்தாழ்வு மற்றும் முறையற்ற BMS காரணமாக இருக்கலாம்.
லித்தியம் அயன் பேட்டரிகள் சேமிக்கப்பட்டாலும் அல்லது கொண்டு செல்லப்பட்டாலும் கூட, ஆபத்தான தீ விபத்துகள் ஏற்படுகின்றன. இந்த சந்தர்ப்பங்கள் அரிதாக இருந்தாலும், அவை ஒப்புக் கொள்ளப்பட வேண்டும், மேலும் பொருத்தமான பாதுகாப்பு உபகரணங்கள் மற்றும் பேட்டரி மேலாண்மை மென்பொருள் நிறுவப்பட வேண்டும். உதாரணமாக நியூயார்க் தீயணைப்புத் துறையானது லித்தியம் அயன் பேட்டரிகளில் ஏற்படும் தீயை எவ்வாறு சமாளிப்பது என்பதைத் தீர்மானிக்கும் பணியில் உள்ளது. உலகெங்கிலும் இருக்கும் லித்தியம் அயன் பேட்டரிகளுக்கான பாதுகாப்பு நடவடிக்கைகள் மறுபரிசீலனை செய்யப்பட வேண்டும் என்று இது வலுவாக பரிந்துரைக்கும்.
நியூயார்க் தீயணைப்புத் துறையின் பார்வை பின்வருமாறு:
செய்திக் கட்டுரை மேற்கோள்: AWS பயன்பாட்டு இயக்கி நவம்பர் 15, 2016 “தீ மிகப்பெரிய பிரச்சனை அல்ல,” ரோஜர்ஸ் கூறினார். தீயணைப்பு வீரர்கள் தீயை சமாளிக்க பயிற்சி பெற்றவர்கள், ஆனால் அவர்கள் என்ன கையாளுகிறார்கள் என்பதை அவர்கள் தெரிந்து கொள்ள வேண்டும். லி-அயன் பேட்டரிகள் நச்சு அமிலங்கள் மற்றும் எரியக்கூடிய நீராவிகளை வெளியிடும். அந்த நீராவிகளில் சில தீயால் நுகரப்படுகின்றன, ஆனால் அவை இல்லையென்றால், அவை தீப்பிடித்து அல்லது தீயணைப்பு வீரர்களுக்கு ஒரு பிரச்சனையாக இருக்கலாம். “பிந்தைய அறுவை சிகிச்சைக்கு” என்ன நடக்கும் என்பது மிகப்பெரிய பிரச்சனை, அதாவது தீ அணைக்கப்பட்ட பிறகு. ஒரு பேட்டரி மூடப்பட்டாலும், அது 72 மணிநேரம் வரை மீண்டும் எரியக்கூடும் என்று ரோஜர்ஸ் கூறினார். -லெப்டினன்ட். நியூயார்க்கின் அபாயகரமான பொருட்கள் செயல்பாட்டுப் பிரிவின் பால் ரோஜர்ஸ் தீயணைப்புத் துறை”
லித்தியம் அயன் பேட்டரியா அல்லது லீட் ஆசிட் பேட்டரியா?
லித்தியம் அயன் பேட்டரி நிச்சயமாக ஈய அமிலத்தை விட சிறந்த செயல்திறன் பண்புகளைக் கொண்டுள்ளது. இருப்பினும், பாதுகாப்பு மற்றும் நிர்வாகத் தேவைகளுடன் தொடர்புடைய கூடுதல் வன்பொருளால் இந்த நன்மைகள் கடுமையாகக் குறைக்கப்படுகின்றன. நிகர முடிவு என்னவென்றால், லெட் ஆசிட் பேட்டரிகள் தனித்துவமான நன்மைகளைக் கொண்டுள்ளன, குறிப்பாக எடை அல்லது சார்ஜ் ஏற்றுக்கொள்ளுதல் ஆகியவற்றால் கட்டுப்படுத்தப்படாத பயன்பாடுகளைக் கருத்தில் கொள்ளும்போது. லெட் ஆசிட் பேட்டரி உற்பத்தி ஆலையின் குறைந்த ஆரம்ப விலை; ஈய அமிலத்தின் குறைந்த கொள்முதல் விலை மற்றும் குறைந்த கடனீட்டுச் செலவு ஆகியவை அதன் குறைந்த சுற்றுச்சூழல் தாக்கம் மற்றும் உள்ளார்ந்த பாதுகாப்புடன் இணைந்து பின்வரும் நன்மைகளை வழங்குகிறது:
- குறைந்த கொள்முதல் விலை. விலை லி-அயன் சமமான கால் பங்கு ஆகும். பெரும்பாலான பயன்பாடுகளில் குறைந்த செயல்பாட்டுச் செலவுகள் உரிமையின் மொத்தச் செலவைக் குறைக்கும்.
- மறுசுழற்சி. கிட்டத்தட்ட 100% லீட் ஆசிட் பேட்டரி பொருட்கள் மறுசுழற்சி செய்யப்படுகின்றன. ஸ்க்ராப் மதிப்பு பேட்டரி பொருள் செலவில் 20% வரை கூடுதல் வருவாயை வழங்க முடியும். லித்தியம் பேட்டரிகள் மறுசுழற்சி செய்வதற்கான உள்கட்டமைப்பு அல்லது வணிக செயல்முறை இல்லை
- பாதுகாப்பு. லித்தியம் அயன் பேட்டரியை விட ஈய அமிலத்தின் வேதியியல் இயல்பாகவே பாதுகாப்பானது
- நிலைத்தன்மை. ஈய அமிலத்திற்கான பல நன்கு நிறுவப்பட்ட ஆதாரங்கள் உள்ளன, குறிப்பாக மறுசுழற்சி வசதிகளிலிருந்து. லித்தியம் மற்றும் பிற கேத்தோடு பொருட்கள் அரசியல் ரீதியாக உணர்திறன் வாய்ந்த பகுதிகளிலிருந்து வழங்கப்படலாம். தற்போதைய உலகளாவிய பொருட்கள் பிரித்தெடுத்தல் மற்றும் உற்பத்தி திறன் ஆகிய இரண்டும் லித்தியம் அயன் பேட்டரியின் உற்பத்தியில் விரைவான அதிகரிப்புக்கு ஆதரவளிக்காது.
- கார்பன் தடம். லீட் ஆசிட் பேட்டரி தயாரிப்பில், லித்தியம் அயன் பேட்டரிகளில் மூன்றில் ஒரு பங்கு கார்பன் தடம் பதிக்க தொட்டில் உள்ளது.
லித்தியம் அயன் பேட்டரி நிறுவனங்கள் வரைந்த படத்தை விட வித்தியாசமான படம். ஆற்றல் அடர்த்தியில் ஈய அமிலம் ஒரு குறைபாட்டைக் கொண்டுள்ளது என்று வாதிட முடியாது என்றாலும், உண்மை என்னவென்றால், ஈய-அமில பேட்டரி இன்னும் பல பயன்பாடுகளில் மிகவும் பாதுகாப்பான, போட்டி மற்றும் பேட்டரி தொழில்நுட்பத்தின் சிறந்த தேர்வாக உள்ளது.
லித்தியம் அயன் பேட்டரி என்றால் என்ன
கேத்தோடு மற்றும் அனோட் பொருட்கள்: 1990களில் நிக்கல்-மெட்டல் ஹைட்ரைடு (Ni-MH) செல்கள் விரும்பப்பட்டாலும், உலகின் முதல் வணிக லித்தியம் அயன் ரிச்சார்ஜபிள் பேட்டரி தயாரிப்பு 1991 இல் சோனி கார்ப்பரேஷன் மூலம் வெளியிடப்பட்டது. அதிக ஆற்றல் உள்ளடக்கத்துடன், நிறை மற்றும் அளவு இரண்டிலும், இந்த பேட்டரி சிறந்த குறைந்த வெப்பநிலை பண்புகள், சுமை பண்புகள் மற்றும் சுழற்சி பண்புகளை வழங்கியது. இதன் விளைவாக, இது விரைவாக சந்தையைக் கைப்பற்றியது மற்றும் ஆடியோ மற்றும் வீடியோ உபகரணங்கள், தனிப்பட்ட கணினிகள், கையடக்க தொலைபேசிகள் மற்றும் பிற சிறிய சாதனங்களுக்கு இன்றியமையாத சக்தியாக மாறியது.
இன்றைய மேம்பட்ட பேட்டரி தொழில்நுட்பம், ஃபோர்டு மோட்டார் கோ. ஆய்வகத்தில் கும்மர் மற்றும் சக பணியாளர்களால் சோடியம் β-அலுமினா எனப்படும் NaAl 11 O 17 என்ற திடநிலையின் உயர் அயனி கடத்துத்திறனைக் கண்டுபிடித்ததன் மூலம் தொடங்கியது. [1. Olof Ramsrtomstrom, வேதியியலுக்கான நோபல் பரிசு, 2019 வேதியியலுக்கான நோபல் பரிசு பற்றிய அறிவியல் பின்னணி; 2. YFY யாவ் மற்றும் JT கும்மர், J. Inorg. அணு செம். 29, 2453 (1967)].
இது திடப்பொருட்களில் உள்ள அயனி போக்குவரத்து உண்மையில் மிக வேகமாக இருக்கும் என்பதையும், அது பல்வேறு புதிய தொழில்நுட்பங்களுக்கு வழிவகுக்கும் என்பதையும் உணர வழிவகுத்தது. சிறிது நேரத்திற்குப் பிறகு, ஃபோர்டு ஆராய்ச்சியாளர்கள், எதிர்மறை மின்முனையில் உருகிய சோடியம் மற்றும் சோடியம்-கடத்துதலுடன் நேர்மறை மின்முனையாக கந்தகத்தில் சோடியத்தின் உருகிய கரைசலைப் பயன்படுத்தி, முற்றிலும் புதிய வகை பேட்டரியை உருவாக்க, அதிக மின்கடத்தா திட எலக்ட்ரோலைட்டைப் பயன்படுத்தலாம் என்று காட்டினார்கள். இடையே திட மின்பகுளி [N. வெபர் மற்றும் ஜேடி கும்மர், ப்ரோக். வருடாந்திர சக்தி ஆதாரங்கள் conf. 21, 37 (1967) ].
எதிர்பார்த்தது போலவே, ஒத்த லித்தியம் அமைப்புகளின் சாத்தியக்கூறுகள் விரைவில் பரிசீலிக்கப்பட்டது, ஏனென்றால் அதற்கு சமமான லித்தியம் செல் சோடியம் கலத்தை விட அதிக மின்னழுத்தங்களை உருவாக்க வேண்டும் என்று அங்கீகரிக்கப்பட்டது. கூடுதலாக, லித்தியம் சோடியத்தை விட குறைவான எடையைக் கொண்டுள்ளது, மற்றொரு நன்மை.
எலிமெண்டல் லித்தியம் அதன் குறைந்த உருகுநிலை காரணமாக, பயன்படுத்த முடியவில்லை. மாறாக, திடமான லித்தியம் கலவைகள், முதன்மையாக Li/Si மற்றும் Li/Al அமைப்புகள், ஆய்வு செய்யப்பட்டன [ RA Huggins, J. Power Sources 81–82, 13 (1999)].
அந்த நேரத்தில் பல பொருட்கள் நேர்மறை மின்முனை எதிர்வினைகளாக ஆய்வு செய்யப்பட்டன, FeS அல்லது FeS 2 இன் பயன்பாட்டிற்கு அதிக கவனம் செலுத்தப்பட்டது. லித்தியத்துடன் எதிர்வினையின் போது, இந்த பொருட்கள் மறுசீரமைப்பு எதிர்வினைகளுக்கு உட்படுகின்றன, ஆரம்ப கட்டங்கள் மறைந்து புதியவை உருவாகின்றன .டிஆர் விசர்ஸ், இசட். டோம்சுக் மற்றும் ஆர்.கே ஸ்டூனென்பெர்க், ஜே. எலக்ட்ரோகெம். Soc. 121, 665 (1974)].
லித்தியம் அயன் பேட்டரி எப்போது கண்டுபிடிக்கப்பட்டது?
பேராசிரியர் விட்டிங்ஹாம் அத்தகைய பொருட்களில் மின் வேதியியல் இடைக்கணிப்பை ஆராய்ந்தார் மற்றும் 1973 இல் பேட்டரிகளில் உள்ள மின்முனைகள் போன்ற பொருட்களை முன்மொழிந்தார். இந்த வேலை 1976 இல் வேலை செய்யும், ரிச்சார்ஜபிள் பேட்டரியில் விளைந்தது. வெற்றிகரமான செல் லித்தியம் உலோகத்தை அனோடாகவும், டைட்டானியம் சல்பைடு (TiS 2 ) கேத்தோடாகவும், லித்தியம் ஹெக்ஸாஃப்ளூரோபாஸ்பேட் ( LiPF 6 ) ப்ரோபிலீன் கார்பனேட்டில் (PC) எலக்ட்ரோலைட்டாக கரைப்பானாகவும் ஆனது. இந்த நம்பிக்கைக்குரிய ஆய்வுகள் பேட்டரிகளில் உள்ள மின்முனைகள் போன்ற பொருட்களில் மின் வேதியியல் இடைச்சேர்க்கையை ஆராய விட்டிங்ஹாமை ஊக்கப்படுத்தியது. 1976 இல் வேலை செய்யும், ரிச்சார்ஜபிள் பேட்டரி பின்னர் நிரூபிக்கப்பட்டது
[(a)Whittingham, MS எலக்ட்ரோஇன்டர்கலேஷன் இன் டிரான்சிஷன்-மெட்டல் டிசல்பைட்ஸ். ஜே. செம். Soc., Chem. கம்யூனிஸ்ட். 1974, 328–329.] (எக்ஸான் ஆராய்ச்சி மற்றும் பொறியியல் நிறுவனத்துடன்).
(b)Whittingham, MS Batterie à Base de Chalcogenures. பெல்ஜிய காப்புரிமை எண். 819672, 1975.
(c)விட்டிங்காம், MS மின் ஆற்றல் சேமிப்பு மற்றும் இடைக்கணிப்பு வேதியியல். அறிவியல் 1976, 192 (4244), 1126–1127.
ஆனால் வெற்றி குறுகிய காலமே இருந்தது. மீண்டும் மீண்டும் சைக்கிள் ஓட்டும்போது, உலோக லித்தியம் சைக்கிள் ஓட்டும்போது உலோக மேற்பரப்பில் டென்ட்ரைட்டுகளை உருவாக்குகிறது, இதன் விளைவாக குறுகிய சுற்றுகள் ஏற்படுகின்றன.
இந்த சிக்கல் மாற்று தீர்வுகளுக்கான புதிய தேடலுக்கு உத்வேகம் அளித்தது மற்றும் “அயன் பரிமாற்ற செல்” உள்ளமைவு (“ராக்கிங் நாற்காலி” என்றும் அழைக்கப்படுகிறது) செல்கள், இரண்டு மின்முனைகளும் அயனிகளுக்கு இடமளிக்கும் வகையில் முன்மொழியப்பட்டது.
ஒரு நேர்மறை மின்முனைப் பொருளில் ஆரம்பத்தில் லித்தியம் இருந்தால், முதல் சார்ஜிங்கின் போது சில அல்லது அனைத்து லித்தியமும் அகற்றப்பட்டால், செல் திறனை உருவாக்குகிறது. எனவே, ஏற்கனவே லித்தியம் இருந்தால், சுமார் 3Vக்கு மேல் உள்ள ஆற்றல்களில் லித்தியத்துடன் வினைபுரியும் நேர்மறை மின்முனைப் பொருட்கள் இருக்க முடியும், மேலும் இந்த லித்தியத்தை மின்-வேதியியல் முறையில் பிரித்தெடுக்க முடியும்.
லித்தியம் அயன் பேட்டரியை கண்டுபிடித்தவர் யார்?
இந்த அணுகுமுறை, லித்தியம் ஏற்கனவே உள்ள பொருட்களின் பயன்பாட்டை உள்ளடக்கியது, முதலில் பேராசிரியர் குட்எனஃப் மூலம் நிரூபிக்கப்பட்டது. 1980 இல் Li1−xCoO2 இல் தயாரிக்கப்பட்ட லித்தியம் மற்றும் அவற்றிலிருந்து மின்வேதியியல் ரீதியாக லித்தியத்தை நீக்கும் பொருட்களின் முதல் எடுத்துக்காட்டுகள்.
[கே. மிசுஷிமா, பிசி ஜோன்ஸ், பிஜே வைஸ்மேன் மற்றும் ஜேபி குட்எனஃப், மேட்டர். ரெஸ். காளை. 15, 783 (1980)] மற்றும் Li1−xNiO2
[JB Goodenough, K. Mizushima மற்றும் T. Takada, Jpn. J. Appl. இயற்பியல் 19 (சப்பிள். 19-3), 305 (1980)]
அனோட் வளர்ச்சிக்கு இணையாக, உலோக லித்தியத்தை விட அதிக திறன் கொண்ட அனோட்களுடன் இணைந்து உயர் செல் emf ஐப் பெறுவதற்கு சிறந்த கேத்தோடு பொருட்கள் தேடப்பட்டன. 1979/1980 இல் ஜான் பி. குட்எனஃப் மற்றும் ஆக்ஸ்போர்டில் அவரது சக ஊழியர்களுடன் ஒரு திருப்புமுனை ஏற்பட்டது.
UK, பல்கலைக்கழகம், LixCoO2, MX2 வகையின் மற்றொரு இடைக்கணிக்கப்பட்ட உலோக சால்கோஜெனைடு, ஒரு கேத்தோடு பொருளாகச் செயல்படும் என்பதைக் கண்டறிந்தது.
[குட்னஃப், ஜேபி; மிசுஷிமா, கே. ஃபாஸ்ட் அயன் கண்டக்டர்கள். அமெரிக்க காப்புரிமை எண். 4,357,215, 1982].
[மிசுஷிமா, கே.; ஜோன்ஸ், பிசி; வைஸ்மேன், PJ; Goodenough, JB LixCoO2 (0<x<-1): ஒரு புதியது
உயர் ஆற்றல் அடர்த்தி கொண்ட பேட்டரிகளுக்கான கத்தோட் பொருள். மேட்டர். ரெஸ். காளை. 1980, 15 (6), 783–789].
பொருளின் அமைப்பு Li ஐ ஒத்ததாக இருந்ததுx TiS2 கோபால்ட் டை ஆக்சைடுக்கு இடையே வான் டெர் வால்ஸ் இடைவெளிகளுடன் (CoO2 ) லித்தியம் அயனிகளை அதிக லட்டு விரிவாக்கம் இல்லாமல் பிணைக்கக்கூடிய அடுக்குகள். குட்எனஃப் தர்க்கம் செய்த போது X இல் MX2 என்பது ஒரு சிறிய எலக்ட்ரோநெக்டிவ் உறுப்பு ஆகும், இதன் விளைவாக ஏற்படும் கேஷன் அப்டேக் செயல்முறையானது ஒரு பெரிய எதிர்மறை இலவச ஆற்றல் மாற்றம் மற்றும் உயர் செல் மின்னழுத்தத்துடன் (ΔG = -nFE) தொடர்புடையதாக இருக்கும். X ஆக்ஸிஜனுடன், நிலைமை குறிப்பாக நம்பிக்கைக்குரியதாகக் கருதப்பட்டது, மேலும் லித்தியம் அயனிகள் நெருக்கமான நிரம்பிய ஆக்சிஜன் வரிசைகளில் போதுமான அளவு மொபைல் இருக்க முன்மொழியப்பட்டது.
தர்க்கம் சரியானது என்று நிரூபிக்கப்பட்டது, மேலும் CoO2 பொருள் Li+/Li உடன் ஒப்பிடும்போது ~4 முதல் 5 V வரை மிக உயர்ந்த திறனைக் காட்டியது. ப்ரோப்பிலீன் கார்பனேட்டில் உள்ள லித்தியம் டெட்ராபுளோரோபோரேட் (LiBF4) கொண்ட எலக்ட்ரோலைட் மூலம் இந்த வழக்கில் மின்வேதியியல் ஆய்வுகள் மேற்கொள்ளப்பட்டன.
இந்த கண்டுபிடிப்பு லித்தியம் உலோகத்தை விட அதிக ஆற்றல் கொண்ட அனோட் பொருட்களைப் பயன்படுத்த உதவியது, மேலும் பொருத்தமான கார்பனேசிய பொருட்களைத் தேடுகிறது. கிராஃபைட்டின் மின் வேதியியல் இடைச்சேர்க்கையின் சிக்கலைத் தீர்ப்பதில் உள்ள சிக்கலைக் கருத்தில் கொண்டு, அதற்குப் பதிலாக பிற விருப்பங்கள் ஆராயப்பட்டன.
லித்தியம் அயன் பேட்டரி எங்கே கண்டுபிடிக்கப்பட்டது?
1985 ஆம் ஆண்டில் அகிரா யோஷினோ (அசாஹி கேசி கார்ப்பரேஷனின்) தலைமையிலான ஜப்பானிய குழு நீராவி-கட்டத்தில் வளர்ந்த கார்பன் ஃபைபர்களையும் (VGCF) பின்னர் வெப்ப-சிகிச்சையளிக்கப்பட்ட பெட்ரோலியம் கோக்கையும் கண்டுபிடித்தபோது ஒரு முன்னேற்றம் ஏற்பட்டது. பிந்தைய பொருள் படிக (கிராஃபிடிக்) மற்றும் படிகமற்ற களங்களின் கலவையைக் கொண்டிருப்பதாக அறியப்பட்டது, மேலும் ஆராய்ச்சியாளர்கள் குறிப்பிட்ட அளவு படிகத்தன்மையுடன் குறிப்பாக நிலையான, ஆனால் அதிக செயல்திறன் கொண்ட குணங்களை அடையாளம் காண முடியும்.
[அகிரா யோஷினோ, லி-அயன் பேட்டரியின் பிறப்பு, அங்கேவாண்டே கட்டுரைகள், ஆங்கேவ்., செம். Int. எட்., 2012 , 51, 5798-5800]
இந்த பயனுள்ள அனோட் பொருட்கள் மூலம், யோஷினோ அயன் பரிமாற்ற செல் கட்டமைப்பின் அடிப்படையில் திறமையான, வேலை செய்யும் லித்தியம்-அயன் பேட்டரியை உருவாக்கினார். இவ்வாறு அடையாளம் காணப்பட்ட கார்பனேசியப் பொருள் அனோடாகப் பயன்படுத்தப்பட்டது மற்றும் குட்எனஃப் இன் லிக்ஸ்கோஓ2 பொருள் (பொதுவாக சிறிய அளவு தகரம் கொண்டது) கேத்தோடாகப் பயன்படுத்தப்பட்டது. பாலிஎதிலீன் அல்லது பாலிப்ரோப்பிலீன் கொண்ட பிரிப்பான் அடுக்குகள் பயன்படுத்தப்பட்டன மற்றும் எலக்ட்ரோலைட் புரோபிலீன் கார்பனேட்டில் (பிசி) லித்தியம் பெர்குளோரேட் (LiClO4) ஆனது.
யோஷினோ இந்த பேட்டரியின் பாதுகாப்பை 1986 இல் பேட்டரியின் மீது எடையைக் குறைத்து நிரூபித்தார். லித்தியம் மெட்டல் அனோடைப் பயன்படுத்தும் பேட்டரிகள் வன்முறையாக செயல்படும் அதேசமயம் தீ அல்லது வெடிப்புகள் எதுவும் ஏற்படவில்லை.

படம் 8. 1986 இல் யோஷினோ தனது லி-அயன் பேட்டரி மூலம் முதல் பாதுகாப்பு சோதனைகளை மேற்கொண்டார்.
A) ஒரு இரும்பு கட்டி பேட்டரியுடன் மோதும் தருணம்
B) மோதலுக்குப் பிறகு லி-அயன் பேட்டரியின் முன்மாதிரி
சி) மோதலுக்குப் பிறகு மெட்டாலிக் லி அனோட் பேட்டரி
[Credit: Akira Yoshino, The Birth of Li-Ion Battery, Angewandte Essays, Angew., Chem. Int. எட்., 2012, 51, 5798-5800 ]
இந்த கண்டுபிடிப்புகள் மற்றும் வளர்ச்சிகள் இறுதியில் வணிக லித்தியம் பேட்டரியை வெளியிட வழிவகுத்தது
1991 இல். மேலும் வளர்ச்சியுடன், Li-ion பேட்டரி 1991 இல் சோனியால் வணிகமயமாக்கப்பட்டது மற்றும் 1992 இல் Asahi Kasei மற்றும் Toshiba ஆகியவற்றின் கூட்டு முயற்சியால் ஆனது.
[நிஷி, ஒய்., லித்தியம் அயன் இரண்டாம் நிலை பேட்டரிகளின் வளர்ச்சி. செம். ரெக். 2001, 1, 406–413]
மின்கலமானது பெட்ரோலியம் கோக்-அடிப்படையிலான அனோட் பொருள், LixCoO2 கேத்தோடாகவும், மற்றும் ப்ரோபிலீன் கார்பனேட்டில் (PC) லித்தியம் ஹெக்ஸாஃப்ளூரோபாஸ்பேட் (LiPF6) கொண்ட நீர்-இலவச எலக்ட்ரோலைட்டாகவும் அமைந்தது. சார்ஜிங் மின்னழுத்தம் அதிகமாக இருந்தது (4.1 V வரை), பதிவுசெய்யப்பட்ட குறிப்பிட்ட ஆற்றல் ~80 Wh/kg மற்றும் ஆற்றல் அடர்த்தி ~200 Wh/ லிட்டர்.
அந்த நேரத்தில் சந்தையில் இருந்த மற்ற பேட்டரிகளுடன் ஒப்பிடுகையில், லித்தியம் பேட்டரி விரைவில் மிகவும் போட்டித்தன்மையுடன் மாறியது மற்றும் வரவிருக்கும் மொபைல் புரட்சிக்கு வழி வகுத்தது.
அதே நேரத்தில், கிராஃபைட் உண்மையில் பொருத்தமான எலக்ட்ரோலைட் கலவையுடன் இணைந்து பயன்படுத்தப்படலாம் என்று கண்டறியப்பட்டது. [Fong R, Sacken U von, Dahn JR, Nonaqueous Electrochemical Cells ஐப் பயன்படுத்தி கார்பன்களில் லித்தியம் இண்டர்கலேஷன் பற்றிய ஆய்வுகள். ஜே. எலக்ட்ரோகெம். Soc. 1990, 137 (7), 2009–2013]
எத்திலீன் கார்பனேட்டைக் கொண்ட கரைப்பான்களைப் பயன்படுத்துவதன் மூலம், அதன் அதிக உருகுநிலை காரணமாக பொதுவாகப் புறக்கணிக்கப்பட்டது, சார்ஜ்/டிஸ்சார்ஜ் சுழற்சியின் போது கிராஃபைட் மின்முனையின் மேற்பரப்பில் ஒரு திட எலக்ட்ரோலைட் இடைநிலை (SEI) உருவாக்கப்பட்டது, இதனால் கார்பன் பொருள் உரிதல் மற்றும் சிதைவு ஆகியவற்றிலிருந்து பாதுகாக்கப்படுகிறது. . [Peled, E. தி எலக்ட்ரோகெமிக்கல் பிஹேவியர் ஆஃப் அல்காலி மற்றும் அல்கலைன் எர்த் மெட்டல்ஸ் இன் நோனாக்வஸ் பேட்டரி சிஸ்டம்ஸ், தி சாலிட் எலக்ட்ரோலைட் இன்டர்ஃபேஸ் மாடல். ஜே. எலக்ட்ரோகெம். Soc. 1979, 126 (12), 2047–2051.
இந்த கண்டுபிடிப்பு பேட்டரி சமூகத்தால் விரைவாக ஏற்றுக்கொள்ளப்பட்டது, மேலும் அனோட் பொருளாக கிராஃபைட்டை அடிப்படையாகக் கொண்ட அடுத்த தலைமுறை லித்தியம்-அயன் பேட்டரி உருவாக்கப்பட்டது. இந்த அனோட் பொருள் மூலம், 4.2 V இன் சார்ஜிங் மின்னழுத்தங்களைக் கொண்ட பேட்டரிகள் விரைவில் உற்பத்தி செய்யப்பட்டன, இதன் விளைவாக ஆற்றல் அடர்த்தி ~400 Wh/லிட்டர்.
லித்தியம்-அயன் பேட்டரியின் வளர்ச்சி இந்த முக்கியமான கண்டுபிடிப்புகளுடன் நின்றுவிடவில்லை, ஆனால் பல மேம்பாடுகள் மற்றும் மாற்றுகள் பின்னர் அறிவிக்கப்பட்டுள்ளன. எடுத்துக்காட்டாக, குறிப்பிட்ட பேட்டரி பயன்பாடுகளில் பயன்படுத்த புதிய கேத்தோடு பொருட்கள் தொடர்ந்து அடையாளம் காணப்பட்டுள்ளன, மேலும் இதுபோன்ற இரண்டு பொருட்கள் Goodenough இன் குழுவிலிருந்து தோன்றியவை: ஸ்பைனல் பொருள் Li1-xMn2O4 மற்றும் ஆலிவின் பொருள் LixFePO4 (LFP).
[பதி, ஏகே; நஞ்சுண்டசாமி, கே.எஸ். குட்எனஃப், ரிச்சார்ஜபிள் லித்தியம் பேட்டரிகளுக்கான நேர்மறை-எலக்ட்ரோடு பொருட்களாக JB பாஸ்போ-ஆலிவின்கள். ஜே. எலக்ட்ரோகெம். Soc. 1997, 144, 1188–1194.
தாக்கரே, எம்எம்; டேவிட், WIF; புரூஸ், பிஜி; குட்எனஃப், மாங்கனீசு ஸ்பைனல்களில் ஜேபி லித்தியம் செருகல். மேட்டர். ரெஸ். காளை. 1983, 18, 461–472].
பிந்தைய பொருள் LixCoO2 ஐ விட Li+/Liக்கு எதிராக சற்றே குறைந்த திறனால் வரையறுக்கப்பட்டுள்ளது, ஆனால் அதிக நிலைப்புத்தன்மையைக் கொண்டுள்ளது மற்றும் அதிக சார்ஜிங் விகிதங்களில் பயன்படுத்தப்படலாம். பல மின்முனை பொருட்கள் மற்றும் எலக்ட்ரோலைட் அமைப்புகளும் கண்டுபிடிக்கப்பட்டுள்ளன, இது சமுதாயத்தின் நலனுக்காக எப்போதும் மேம்படுத்தப்பட்ட ஆற்றல் சேமிப்பு பொருட்களுக்கு வழிவகுத்தது.
மின்சார வாகனங்களில் எந்த வகையான பேட்டரி பயன்படுத்தப்படுகிறது?
இப்போதெல்லாம், பெரும்பாலான EVகள் Li-ion பேட்டரிகளைப் பயன்படுத்துகின்றன. முன்னதாக, Ni-MH மற்றும் லீட்-அமில பேட்டரிகள் பயன்படுத்தப்பட்டன, ஆனால் அதிக குறிப்பிட்ட ஆற்றல் மற்றும் அதிக ஆற்றல் அடர்த்தி மதிப்புகளைக் கொண்ட Li-ion பேட்டரிகளின் வருகையால் அவற்றின் பயன்பாடு மெதுவாகக் குறைந்தது. லீட் ஆசிட் பேட்டரிகளின் குறிப்பிட்ட ஆற்றல் சுமார் 40-50 Wh/kg ஆகும், Li-ion பேட்டரியில் 150 Wh/kg உள்ளது. லீட்-அமில பேட்டரிகளுக்கான ஆற்றல் அடர்த்தி மதிப்பு 80-100 Wh/லிட்டராக உள்ளது, அதே சமயம் Li-ion பேட்டரி 250 Wh/லிட்டருக்கு அதிகமாக உள்ளது.
சமீபத்திய டெஸ்லா பேட்டரி பேக்குகளில் (2019-2020) பயன்படுத்தப்பட்டவை போன்ற நிக்கல்-கோபால்ட்-அலுமினியம் (NCA) கத்தோட்கள் மற்றும் சிலிக்கான்/கிராஃபைட் கலவை அனோட்கள் கொண்ட உருளை செல்கள் தோராயமாக 270 Wh/kg மற்றும் 650 Wh/லிட்டரை எட்டியுள்ளன. சியோன் பவர் மூலம் Licerion எனப்படும் புதிய தொழில்நுட்பம் 500 Wh/kg குறிப்பிட்ட ஆற்றல் மற்றும் 1000 Wh/L ஆற்றல் அடர்த்தி மற்றும்> 0.4 Ah வளர்ச்சி கலங்களில் 450 சுழற்சிகள்.
சிறிய பேட்டரிகளுக்கு, நாம் Wh அடிப்படையில் பேசுகிறோம். அதிக திறன் அமைப்புகளுக்கு, kWh அலகு பயன்படுத்தப்படுகிறது. Wh மதிப்பை 103 ஆல் வகுத்தால் kWh ஐக் கொடுக்கும்.
இவ்வாறு 850 Wh = 850/1000 = 0.850 kWh.
இன்றைய EV பேட்டரியில் பயன்படுத்தப்படும் செல்கள் 140 -170 Wh/kg என்ற பெயரளவிலான குறிப்பிட்ட ஆற்றலை எட்டும். இதன் விளைவாக வரும் பேட்டரி பேக்கின் குறிப்பிட்ட ஆற்றல் பொதுவாக 30 முதல் 40 சதவீதம் குறைவாக அல்லது 80 -120 Wh/kg ஆகும். பல தொடர்கள் மற்றும் இணையான இணைக்கும் தடங்கள், BMS மற்றும் வெப்ப மேலாண்மை அமைப்பு (குளிர்ச்சி அல்லது வெப்பமாக்கல்) காரணமாக குறைப்பு ஏற்படுகிறது. 2019 இல், செல் அல்லாத கூறுகளின் பேக் சதவீதம் சுமார் 28% ஆகக் குறைந்துள்ளது.
இப்போது வரை, செல்கள் முதலில் தொகுதிகளாக வைக்கப்பட்டு பின்னர் பேக்களாக வைக்கப்படுகின்றன. இரண்டும் தற்கால ஆம்பெரெக்ஸ் டெக்னாலஜி கோ. லிமிடெட், சீனா ( CATL) மற்றும் டெஸ்லா அவர்கள் தொகுதிகளை அகற்றிவிட்டு செல்களை நேரடியாக பேக்குகளில் வைக்க முடிவு செய்துள்ளனர். CATL ஏற்கனவே அவ்வாறு செய்துள்ளது மற்றும் அதை செல்-டு-பேக் தொழில்நுட்பம் என்று அழைக்கிறது. இது பற்றிய தகவல்கள் குறைவாக இருந்தாலும், குறிப்பிட்ட ஆற்றலை 10-15% அதிகரிக்கலாம் மற்றும் தொகுதி பயன்பாட்டை 15-20% மேம்படுத்தலாம் என்று நிறுவனம் கூறுகிறது. மொத்தத்தில், இது பேட்டரி பேக்குகளுக்கு தேவையான பாகங்களை 40% குறைக்கும் என்று கூறப்படுகிறது. [https://cleantechnica.com/2020/02/18/how-catl-lithium-iron-phosphate-batteries-could-be-leading-to-100-kwh-tesla-model-3/]
லித்தியம் பேட்டரியின் பெயர்
சர்வதேச மின் தொழில்நுட்ப ஆணையம் (IEC) மற்றும் இந்திய தரநிலை நிறுவனம் ஆகியவை லித்தியம்-அயன் கலங்களின் வேதியியல் மற்றும் அளவை விவரிக்க ஒரு பொதுவான பதவியை நிறுவியுள்ளன.
[ கையடக்க பயன்பாடுகளுக்கான இரண்டாம் நிலை லித்தியம் செல்கள் மற்றும் பேட்டரிகள், சர்வதேச மின் தொழில்நுட்ப ஆணையம், IEC 61960-1 மற்றும் IEC 61960-2 மற்றும் IS 16047: 2012 ].
எழுத்துக்கள் வேதியியல் மற்றும் வடிவ காரணியைக் குறிக்கின்றன, அதே நேரத்தில் எண்கள் செல்லின் இயற்பியல் பரிமாணங்களைக் குறிப்பிடுகின்றன. முதல் எழுத்து பொது வேதியியலை விவரிக்கிறது, இரண்டாவது எழுத்து குறிப்பிட்ட கேத்தோடு வேதியியலைக் குறிக்கிறது மற்றும் மூன்றாவது எழுத்து வடிவத்தைக் குறிக்கிறது.
முதல் எழுத்து: நான் – லித்தியம்-அயன் வேதியியல்
இரண்டாவது எழுத்து: சி-கோபால்ட், எஃப்-இரும்பு, எஃப்பி – இரும்பு பாஸ்பேட், என்-நிக்கல், எம்-மாங்கனீஸ், எம்பி-மாங்கனீஸ் பாஸ்பேட், டி-டைட்டானியம், வி-வெனடியம் மற்றும் x – மற்றவை.
மூன்றாவது எழுத்து: ஆர்- உருளை, பி-பிரிஸ்மாடிக்
பின் வரும் முதல் இரண்டு எண்கள் விட்டத்தை மிமீ என்றும், கடைசி மூன்று மிமீ உயரத்தை பத்தில் ஒரு பங்கு என்றும் குறிப்பிடுகின்றன. இவ்வாறு, ICR19/66 என்று குறிப்பிடப்பட்ட செல் என்பது ஒரு லித்தியம் அயன் செல் ஆகும், இது கோபால்ட் கேத்தோடு விட்டம் கொண்டது.> 18 மிமீ மற்றும் ≤ 19 மிமீ மற்றும் அதிகபட்ச ஒட்டுமொத்த உயரம்> 65 மிமீ மற்றும் ≤ 66 மிமீ.
ப்ரிஸ்மாடிக் செல்களுக்கு, ஆரம்ப எழுத்துக்கள் ஒரே பொருளைக் கொண்டுள்ளன, ஆனால் முதல் இரண்டு எண்கள் மிமீ அகலத்தைக் குறிக்கின்றன, அடுத்த இரண்டு எண்கள் மிமீ உயரம் மற்றும் கடைசி இரண்டு எண்கள் மிமீ நீளம். எனவே, செல் பதவி IMP9/35/150 அதிகபட்ச தடிமன் கொண்ட மாங்கனீசு கேத்தோடு கலத்துடன் கூடிய பிரிஸ்மாடிக் லித்தியம் அயன் கலத்தை விவரிக்கிறது. > 8 மிமீ மற்றும் ≤ 9 மிமீ மற்றும் அதிகபட்ச அகலம் > 34 மிமீ மற்றும் ≤ 35 மிமீ மற்றும் அதிகபட்ச ஒட்டுமொத்த உயரம் > 149 மிமீ மற்றும் ≤ 150 மிமீ.
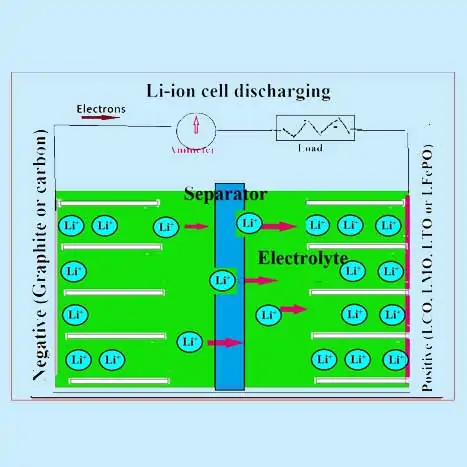
லித்தியம் அயன் பேட்டரி எப்படி வேலை செய்கிறது?
லித்தியம் அயன் பேட்டரி எவ்வாறு தயாரிக்கப்படுகிறது
அணு எண் 3 கொண்ட லித்தியம் உலோகம், 0.534 g/cc அடர்த்தி, மிகக் குறைந்த நிலையான குறைப்பு திறன் (Li + /Li ஜோடி -3.05 V vs. SHE) மற்றும் 3860 Ah/kg (2061 mAh/cc) என்ற தத்துவார்த்த குறிப்பிட்ட திறன் கொண்டது அனைத்து உலோகங்களிலும் குறைந்த எடை, அதிக மின்னழுத்தம் மற்றும் அதிக ஆற்றல் அடர்த்தி. (அணு எண் 82, அடர்த்தி 11.29 g/cc, 257.8 Ah/kg இன் கோட்பாட்டு குறிப்பிட்ட திறன் மற்றும் -0.35V vs. SHE இன் நிலையான குறைப்பு திறன் ஆகியவற்றுடன் ஒப்பிடுக).
லித்தியம் அயன் பேட்டரி - செயலில் உள்ள பொருட்கள்
நேர்மறை மின்முனையின் செயலில் உள்ள பொருட்கள் LiCoO2 அல்லது LiMnO2 அல்லது LiFePO4 போன்ற கலப்பு ஆக்சைடுகளில் ஏதேனும் ஒன்று. எதிர்மறை மின்முனையானது முக்கியமாக கிராஃபைட் மற்றும் உருவமற்ற கார்பன் கலவைகள் ஆகும். ஒரு கரிம எலக்ட்ரோலைட் (LIPF6 போன்ற உப்பைக் கடத்தும் ஒரு பிரிந்த லித்தியம் கொண்டது) பயன்படுத்தப்படுகிறது. ஒரு பாலிப்ரோப்பிலீன் (PP) அல்லது பாலிதீன் (PE) அல்லது கலப்பு பிரிப்பான் பயன்படுத்தப்படுகிறது. லித்தியம் அயனிகள் சார்ஜ் மற்றும் டிஸ்சார்ஜ் செய்யும் போது லித்தியம்-அயன் பேட்டரிகளின் மின்முனைகளுக்கு இடையே முன்னும் பின்னுமாக இடம்பெயர்ந்து கீழே விவரிக்கப்பட்டுள்ளபடி செயலில் உள்ள பொருட்களில் ஒன்றிணைக்கப்படுகின்றன:

படம் 9. லித்தியம் அயன் கலத்தின் வெடித்த காட்சி
கடன்: Zhang Z., Ramadass P. (2012) Lithium-Ion Battery Systems and Technology. இல்: மேயர்ஸ் RA (eds) என்சைக்ளோபீடியா ஆஃப் சஸ்டைனபிலிட்டி சயின்ஸ் அண்ட் டெக்னாலஜி. ஸ்பிரிங்கர், நியூயார்க், NY, pp 6124. http s://doi.org/10.1007/978-1-4419-0851-3_663
லித்தியம் அயன் பேட்டரி எவ்வாறு சார்ஜ் செய்யப்படுகிறது
ஒரு லித்தியம் அயன் கலத்தில் (LIB) வெளியேற்றும் செயல்பாட்டின் போது, அனோடில் இருந்து லித்தியம் அயனிகள் எலக்ட்ரோலைட்டிற்குள் பிரிக்கப்படுகின்றன (அல்லது பிரித்தெடுக்கப்படுகின்றன) . அனோடில் இருந்து கேத்தோடிற்கு அயனிகளின் இந்த இயக்கம் வெளிப்புற சுற்றுகளில் பாயும் எலக்ட்ரான்களின் வெளியீட்டோடு சேர்ந்துள்ளது. லித்தியம் அயனிகள் கேத்தோடில் இருந்து நகர்ந்து எலக்ட்ரோலைட் வழியாக நேர்மின்முனையில் ஒன்றிணைக்கும் சார்ஜிங் செயல்பாட்டின் போது தலைகீழ் செயல்முறை நிகழ்கிறது. வணிக எல்ஐபிகள் பொதுவாக LiCoO 2 , LiMn 2 O 4 மற்றும் LiFePO 4 போன்ற மாறுதல் உலோக ஆக்சைடுகளைப் பயன்படுத்துகின்றன.
எலக்ட்ரானிக் கடத்துத்திறனை மேம்படுத்துவதற்கும், எலக்ட்ரோடு பொருளின் சிறந்த ஒட்டுதலை அடைவதற்கும், பத்து முதல் இருபது சதவீதம் கடத்தும் கார்பன் மற்றும் 5-10 பாலிமெரிக் பைண்டர்களான பாலிவினைலைடின் டிஃப்ளூரைடு ( %–10% ) மற்றும் பாலிடெட்ராஃப்ளூரோஎத்திலீன் (பிடிஎஃப்இ) ஆகியவையும் செயலில் உள்ள பொருட்களுடன் சேர்க்கப்படுகின்றன. நேர்மின்வாயில் பொருள் ஒரு செப்பு மின்னோட்ட சேகரிப்பான் மீது பூசப்பட்டு, தேவைப்பட்டால் கார்பன் மற்றும் PVDF ஐ கடத்துகிறது.
இரண்டு மின்முனைகளும் ஒரு நுண்துளை பிரிப்பான் (பாலிஎதிலீன் அல்லது பாலிப்ரோப்பிலீன் ஃபிலிம் தடிமன் 10-20 µm) எலக்ட்ரோலைட் கரைசலில் ஊறவைக்கப்படுகின்றன (LiPF6 ஒரு கரிம கரைப்பானில்). பிரிப்பான் மற்றும் எலக்ட்ரோலைட் கரைசல் இரண்டும் சிறந்த அயனி கடத்துத்திறனைக் கொண்டிருக்க வேண்டும். செல் பொதுவாக ஜெல்லிரோல் பாணியில் ஒரு உலோக உறையில் இரண்டு மின்முனைகளுக்கு இடையில் எலக்ட்ரோலைட்-டிப் பிரிப்பான் மூலம் புனையப்படுகிறது. ஒரு LIB இன் திட்டவட்டமானது புள்ளிவிவரங்களில் காட்டப்பட்டுள்ளது, அங்கு வழக்கமான கட்டணம் மற்றும் வெளியேற்ற செயல்முறைகள் காட்டப்படுகின்றன.
லித்தியம்-அயன் (லி-அயன்) ரிச்சார்ஜபிள் பேட்டரிகள் லித்தியம் அயனிகளின் (Li + ) (விருந்தினர் இனங்கள்) அல்லது லித்தியம் செருகும் கலவைகள் எனப்படும் ஹோஸ்ட் மேட்ரிக்ஸில் (நேர்மறை மற்றும் எதிர்மறை மின்முனை செயல்படும் பொருட்கள்) ஒரு மீளக்கூடிய செருகல்/பிரித்தல் ஆகியவற்றைப் பயன்படுத்துகின்றன. செயல்முறைகள் ஏற்படும். லித்தியம் அயன் பேட்டரிகள் ராக்கிங் நாற்காலி பேட்டரிகள் என்று குறிப்பிடப்படுகின்றன, ஏனெனில் லித்தியம் அயனிகள் செல் சார்ஜ் மற்றும் டிஸ்சார்ஜ் செய்யப்படும்போது நேர்மறை மற்றும் எதிர்மறை மின்முனைகளுக்கு இடையில் முன்னும் பின்னுமாக “ராக்” செய்கின்றன.
நேர்மறை செயலில் உள்ள பொருள் பொதுவாக லித்தியம் கோபால்ட் ஆக்சைடு (LiCoO 2 ) போன்ற அடுக்கு அமைப்பைக் கொண்ட உலோக ஆக்சைடு அல்லது லித்தியம் மாங்கனீசு ஆக்சைடு (LiMn 2 O 4 ) போன்ற சுரங்கப்பாதை அமைப்பைக் கொண்ட ஒரு பொருள், பெரும்பாலும் அலுமினிய மின்னோட்ட சேகரிப்பாளரில் உள்ளது. . எதிர்மறை செயலில் உள்ள பொருள் பொதுவாக ஒரு கிராஃபிடிக் கார்பன் ஆகும், மேலும் ஒரு அடுக்கு பொருள், பெரும்பாலும் செப்பு மின்னோட்ட சேகரிப்பான் மீது. சார்ஜ்-டிஸ்சார்ஜ் செயல்பாட்டில், லித்தியம் அயனிகள் செயலில் உள்ள பொருட்களின் அணு அடுக்குகளுக்கு இடையில் உள்ள இடைவெளியில் இருந்து செருகப்படுகின்றன அல்லது பிரித்தெடுக்கப்படுகின்றன.
நீர் அல்லாத எலக்ட்ரோலைட்டுகள் அல்லது ஆர்கானிக் எலக்ட்ரோலைட்டுகள் லித்தியம் செல்களில் பயன்படுத்தப்படுகின்றன.
லித்தியம்-அயன் பேட்டரிகளுக்கான பிரிப்பான்கள் பாலியோலின் மைக்ரோபோரஸ் பிலிம்கள் பாலிஎதிலீன் (PE) மற்றும் பாலிப்ரோப்பிலீன் (PP) ஆகும்.

லித்தியம் அயன் பேட்டரியில் மின்வேதியியல் செல் எதிர்வினைகள்
ஒரு பொதுவான லித்தியம் அயன் கலத்தில், பின்வரும் பொதுவான எதிர்வினைகள் ஏற்படுகின்றன.
நேர்மறை மின்முனை எதிர்வினை:
LiMO 2 ⇔ Li 1-x MO 2 + x Li + + xe –
எதிர்மறை மின்முனை எதிர்வினை:
C + y Li + + ye – ⇔ Li y C
மொத்த செல் எதிர்வினை:
LiMO 2 + x/y C ⇔ x/y Li y C + Li 1-x MO 2
M = Co, Mn, Ni, Ti, போன்ற உலோகங்கள்.
பொதுவாக x என்பது 0.5 மற்றும் y என்பது 0.16, எனவே x/y என்பது 3 ஆகும். [ஜெஃப் டான் மற்றும் கிராண்ட் எம். எர்லிச். “லித்தியம் அயன் பேட்டரிகள்”, லிண்டனின் கையேடு பேட்டரிகள், 4 வது பதிப்பு, தாமஸ் பி. ரெட்டி (பதிப்பு), மெக்ரா
எலக்ட்ரோலைட் மற்றும் சாலிட்-எலக்ட்ரோலைட் இன்டர்ஃபேஸ் (SEI)
முன்பு குறிப்பிட்டபடி, நீர் அல்லாத மின்பகுளிகள் அல்லது கரிம எலக்ட்ரோலைட்டுகள் லித்தியம் செல்களில் பயன்படுத்தப்படுகின்றன. லி-செல்கள் ஒப்பீட்டளவில் அதிக மின்னழுத்தத்தில் இயங்குகின்றன, ஒரு கலத்திற்கு 4.2 V வரை. லித்தியம் ஹெக்ஸாபுளோரோபாஸ்பேட் (LiPF6), லித்தியம் ஹெக்ஸாபுளோரோ ஆர்சனேட் (LiAsF6), லித்தியம் டெட்ராஃப்ளூரோபோரேட் (LiBF4), லித்தியம் பெர்குளோரேட் (LiClO4), லித்தியம் ட்ரைஃப்ளூரோமெத்தேன்சல்ஃபோனேட் (Lithium trifluoromethanesulphonate. (LiClO4), லித்தியம் ட்ரைபுளோரோமெத்தேன்சுல்ஃபோனேட் (Lithium trifluoromethanesulphonate.(LiboriFloox) , உண்மையான எலக்ட்ரோலைட்டுகள் (எலக்ட்ரோலைட் உப்புகளைத் தக்கவைத்தல்), அத்தகைய அதிக மின்னழுத்தத்தில் நிலையான பொருத்தமான கரைப்பான்கள் தேவைப்படுகின்றன. இத்தகைய கரைப்பான்களில் பெரும்பாலானவை உயர் மின்கடத்தா மாறிலிகளைக் கொண்டுள்ளன, எளிதாக அயனி விலகல் மற்றும் அதிக செறிவூட்டப்பட்ட லி-அயனிகளின் இருப்பை எளிதாக்குகின்றன. இத்தகைய கரைப்பான்கள் லி அயனிகளின் நிலையான இருப்புக்கான தீர்வு உறைகளாகவும் செயல்படுகின்றன, இதனால் எதிர் அயனிகளின் செல்வாக்கு குறைகிறது.
அதிக மின்கடத்தா மாறிலிகளைக் கொண்டிருப்பதன் தீமை என்னவென்றால், அவை அதிக பாகுத்தன்மை மதிப்புகளைக் கொண்டிருப்பதால் அயனிகளின் இயக்கம் பலவீனமடைகிறது . குறைந்த அயனி கடத்துத்திறனைக் கடக்க, குறைந்த பிசுபிசுப்பு கரைப்பான்கள் பொதுவாக அதிக பிசுபிசுப்பு கரைப்பான்களுடன் கலக்கப்படுகின்றன. ஆனால், குறைந்த பிசுபிசுப்பான கரைப்பான்கள் குறைந்த அயனி விலகலைக் கொண்டிருப்பதால், கலவையானது நல்ல அயனி கடத்துத்திறன் மற்றும் நல்ல இயக்கம் இரண்டையும் கொண்டிருக்கும் வகையில் உகந்த கலவை விகிதத்தைத் தாக்குவது கட்டாயமாகிறது. நீர் அல்லாத கரைப்பான்களாக, டைமெத்தில் கார்பனேட் (டிஎம்சி), டைதில் கார்பனேட் (டிஇசி) மற்றும் எத்தில் மெத்தில் கார்பனேட் (இஎம்சி) போன்ற குறைந்த பிசுபிசுப்பான நேரியல் அல்கைல் கார்பனேட்டுகளுடன் எத்திலீன் கார்பனேட் (EC) கலவைகள் வணிக ரீதியாக கிடைக்கும் LIB களில் பயன்படுத்தப்படுகின்றன.
அப்ரோடிக் கரைப்பான்கள் ஈதர்கள், எஸ்டர்கள் மற்றும் அல்கைல் கார்பனேட்டுகள்: அவை டைதில் ஈதர் (DEE), டெட்ராஹைட்ரோஃபுரான் (THF), டையாக்சோலேன், எத்திலீன் கார்பனேட் (EC), ப்ரோப்பிலீன் கார்பனேட் (PC), டைமெத்தில் கார்பனேட் (DMC), டைத்தில் கார்பனேட் (DEC), எத்தில் மெத்தில் கார்பனேட் (EMC), மெத்தில் ஃபார்மேட், γ-பியூட்டிரோலாக்டோன் (BL), மெத்தில் அசிடேட், அசிட்டோனிட்ரைல் (AN), டைமெதில் சல்பாக்சைடு (DMSO), டைமெதில்ஃபார்மமைடு (DMF), மெத்தில் குளோரைடு, நைட்ரோமெத்தேன் போன்றவை.)
திரவ எலக்ட்ரோலைட்டுகள் என்பது ஒன்று அல்லது அதற்கு மேற்பட்ட கரிம கரைப்பான்களில் உள்ள லித்தியம் உப்பின் கரைசல்கள், பொதுவாக கார்பனேட்டுகள்.
கிராஃபைட்டை அனோடாகப் பயன்படுத்த வேண்டுமானால், ப்ரோப்பிலீன் கார்பனேட்டை (PC) எலக்ட்ரோலைட்டாகப் பயன்படுத்த முடியாது, ஏனெனில் முந்தையது கிராஃபைட் மேற்பரப்பில் சிதைகிறது; EC அல்லது LiBOB) Li bisoxalato borate இன் சிறிய சேர்க்கைகள் இல்லாமல் தனியாகப் பயன்படுத்தப்படும் பிசி, கிராஃபைட் மின்முனைகளில் சிதைவை ஏற்படுத்தலாம், ஏனெனில் அது லித்தியத்துடன் இணைந்து, உரிதல் ஏற்படுகிறது.
எலக்ட்ரோலைட் மாறாதது (சார்ஜ் செய்யும் போது எலக்ட்ரோலைட்டை விட்டு வெளியேறும் அதே எண்ணிக்கையிலான அயனிகள் நுழைகின்றன
வெளியேற்றம்). எலக்ட்ரோலைட் உப்பு பொதுவாக கரிம கார்பனேட் கரைப்பான்களில் கரைக்கப்படுகிறது. ஒவ்வொரு உற்பத்தியாளருக்கும் எத்திலீன் கார்பனேட் (EC) ஒரு பொதுவான பிரிவாக இருக்கும் கரைப்பான்களின் வெவ்வேறு கலவையைக் கொண்டுள்ளது.
சாலிட்-எலக்ட்ரோலைட் இன்டர்ஃபேஸ் (SEI) அடுக்கு உருவாக்கம் என்பது எலக்ட்ரோலைட்டுகளால் செய்யப்படும் மற்றொரு முக்கியமான செயல்பாடு ஆகும். ஒரு கார உலோகம் ஒரு பேட்டரி எலக்ட்ரோலைட்டில் மூழ்கும்போது, அல்லது எதிர்மறை ஆற்றல் கார்பனுக்கு அல்லது எலக்ட்ரோலைட்டில் மூழ்கியிருக்கும் ஒரு மந்த மின்முனைக்கு பயன்படுத்தப்படும்போது, ஒரு SEI உருவாகத் தொடங்குகிறது.
SEI அடுக்கு கரைசலுடன் உலோகத்துடன் தொடர்பு கொள்ளும்போது உடனடியாக உருவாகிறது, எலக்ட்ரோலைட் கூறுகளின் கரையாத மற்றும் ஓரளவு கரையக்கூடிய குறைப்பு தயாரிப்புகளைக் கொண்டுள்ளது. SEI என்பது பேட்டரியின் பாதுகாப்பு, ஆற்றல் திறன், லித்தியம் வைப்புகளின் உருவவியல், அடுக்கு ஆயுள் மற்றும் சுழற்சி ஆயுளை தீர்மானிக்கும் முக்கிய காரணியாகும். அனோடில் நல்ல ஒட்டுதலும் முக்கியமானது.
மேலே வலியுறுத்தப்பட்டபடி, அனோடின் கரைதல் அல்லது அரிப்பை நிறுத்தினால் மட்டுமே நடைமுறை முதன்மை அல்லது இரண்டாம் நிலை கார அல்லது கார-பூமி மின்கலங்களை உருவாக்க முடியும். எனவே, எலக்ட்ரோலைட் ஒரு கரையாத திட-எலக்ட்ரோலைட் இடைநிலையை உருவாக்க லித்தியத்துடன் (அல்லது அல்காலி-மெட்டல் அனோடுடன்) விரைவாக வினைபுரியும் குறைந்தபட்சம் ஒரு SEI முன்னோடியைக் கொண்டிருக்கும் வகையில் வடிவமைக்கப்பட வேண்டும். உப்பு அயனிகளின் குறைப்பு தயாரிப்புகள் பொதுவாக LiF, LiCl மற்றும் Li 2 O போன்ற கனிம சேர்மங்களாகும், அவை மின்முனையின் மேற்பரப்பில் படிகின்றன. கரைப்பான் குறைக்கப்படுவதைத் தொடர்ந்து Li 2 CO 3 மற்றும் ஓரளவு கரையக்கூடிய செமி கார்பனேட்டுகள் மற்றும் பாலிமர்கள் போன்ற கரையாத SEI கூறுகள் உருவாகின்றன.
கார்பன் மின்முனையைப் பொறுத்தவரை, SEI உருவாகும் மின்னழுத்தமானது கார்பனின் வகை, அதன் மேற்பரப்பின் வினையூக்கி பண்புகள் (சாம்பலின் உள்ளடக்கம், படிக விமானத்தின் வகை, அடித்தளத்திலிருந்து விளிம்பு விமான விகிதம்), வெப்பநிலை, கரைப்பான்கள், உப்புகள் மற்றும் அசுத்தங்கள் மற்றும் தற்போதைய அடர்த்தியின் செறிவு மற்றும் வகைகள். லித்தியம்-அயன் பேட்டரியின் முதல் சார்ஜில், SEI உருவாவதற்கு முக்கியமாக தேவைப்படும் “மீளமுடியாத திறன் இழப்பு” (Q IR ) எனப்படும் திறன் இழப்பு உள்ளது.
SEI உருவாவதற்கு கூடுதலாக, Q IR ஆனது கரையக்கூடிய குறைப்பு தயாரிப்புகளின் (Q SP ) உருவாக்கத்துடன் தொடர்புடைய திறன் இழப்பால் ஏற்படலாம்.
பேட்டரியின் நீண்ட சுழற்சி ஆயுளுக்கு மாசு இல்லாத SEI அவசியம். அதிக விகிதத்தில் சைக்கிள் ஓட்டும் போது மற்றும் வெளியேற்றத்தின் அதிக ஆழத்தில் இது இன்னும் முக்கியமானது.
லித்தியம் ஹெக்ஸாபுளோரோபாஸ்பேட் (LiPF6) மற்றும் லித்தியம் ஹெக்ஸாபுளோரோஅர்செனேட் (LiAsF6) கரைசல்களில் உள்ள SEI மற்ற உப்புகளின் கரைசல்களுடன் ஒப்பிடும்போது அதிக எதிர்ப்பாற்றலைக் கொண்டுள்ளது. இது LiPF6 மற்றும் LiAsF6 எலக்ட்ரோலைட்டுகளில் உள்ள லித்தியம் அனோடின் உயர் இடைமுக மின்மறுப்புக்கு வழிவகுக்கும் இனங்கள்-கட்டுப்படுத்தப்பட்ட எதிர்ப்பிற்கு பங்களிக்கும் எதிர்ப்பாற்றல் மாற்றங்கள் காரணமாகும். கூடுதலாக, Li2CO3 லித்தியம்-சைக்கிளிங் செயல்திறனை மேம்படுத்துவதற்கான சிறந்த செயலற்ற முகவர்களில் ஒன்றாகக் கூறப்படுகிறது [J Electrochem Soc.,164 (7) A1703-A1719 (2017)].
லித்தியம் அயன் பேட்டரிகளுக்கான பிரிப்பான்கள்
லித்தியம்-அயன் பேட்டரிகளுக்கான பிரிப்பான்கள் பாலியோல்ஃபின் மைக்ரோபோரஸ் பிலிம்கள் மற்றும் பொதுவாக ஒரே மாதிரியாக வரையப்பட்ட பாலிஎதிலீன் (PE) மற்றும் பாலிப்ரோப்பிலீன் (PP), இருமுனையாக வரையப்பட்ட PE அல்லது மல்டிஆக்சியில் வரையப்பட்ட PP/PE/PP ஆகும்.
லித்தியம் அயன் பேட்டரியில் செயல்படும் பொருட்களுக்கான மூலப்பொருட்கள்
லித்தியம் அயன் பேட்டரிகள் வெவ்வேறு கேத்தோடு பொருட்களைப் பயன்படுத்துகின்றன. டைட்டானியம்-நியோபியம் ஆக்சைடு அனோட்கள், Li-Si அலாய் போன்ற சிலவற்றைத் தவிர, அனோட் மாறாமல் கார்பன் அடிப்படையிலானது. பின்வரும் அட்டவணை மற்றும் படம் இந்த பேட்டரிகளில் பயன்படுத்தப்படும் பல்வேறு வேதியியல் பற்றி சில யோசனைகளை வழங்குகிறது.

படம் 12. லித்தியம் அயன் பேட்டரிகளுக்கான சில தற்போதைய மற்றும் எதிர்கால மின்முனை வேதியியல் விருப்பங்களின் சுருக்கம். Li(Si) இன் முன்மொழியப்பட்ட திறன், பொருளின் கோட்பாட்டுத் திறனில் 50% ஆகும், இது சில நேர்மறை மின்முனைப் பொருட்களுக்குக் காணப்படுவது போன்றது.
[கடன்: Yu Miao, Patrick Hynan, Annette von Jouanne, and Alexandre Yokochi, Energies 2019, 12, 1074; doi:10.3390/en12061074]
அட்டவணை 1.
வெவ்வேறு கேத்தோடு பொருட்கள் கொண்ட லித்தியம் அயன் செல்களின் சிறப்பியல்புகள்
| கத்தோட் பொருள் | லி-நி-கோ-அல் (NCA) | லி-நி-எம்என்-கோ (என்எம்சி) | Li-MnO2 (LMO) | லி-அயர்ன் பாஸ்பேட் (LFP) | லி டைட்டனேட் (LTO) | லி கோபால்ட் ஆக்சைடு (LCO) |
|---|---|---|---|---|---|---|
| ஒரு கலத்தின் பெயரளவு மின்னழுத்தம் (V) | 3.6 | 3.65 (2.7-4.2) | 3.8 | 3.25 (2-3.6) | 3.2 | 3.6 |
| கோட்பாட்டு குறிப்பிட்ட ஆற்றல் (Wh/kg) | 279 | 256 | 148 | 128 (373) | 293 (175) | 274 (370) (x=0.5) |
| கேத்தோட்களுக்கான குறிப்பிட்ட திறன் (Ah/Kg) பொட்டன்ஷியல் vs Li/Li+ (V) | 180-200 (3.8) | 200 | 148 (4.1) | 150-170 (3.45) | 175 | 274 (3.9) (x=0.5) |
| கேத்தோட்களுக்கான குறிப்பிட்ட ஆற்றல் (Wh/Kg) | 680-760 | 610-680 | 410-492 548 | 518-587 544 | -- | 546 |
| பாதுகாப்பு | பாதுகாப்பான | மிதமான | பாதுகாப்பானது | உயர் | மிகவும் நல்லது | மிதமான |
லித்தியம் அயன் பேட்டரியில் உள்ள கத்தோட் பொருட்கள்
நேர்மறை மின்முனை பொருளின் தேர்வு சார்ந்து பல தேவைகளை கேத்தோடு பொருட்கள் பூர்த்தி செய்ய வேண்டும்.
- அதிக திறன் வழங்க, இந்த பொருட்கள் தயாரிக்கப்பட்டது போன்ற லித்தியம் ஒரு பெரிய அளவு இணைக்க வேண்டும்.
- மேலும், நீண்ட சுழற்சி வாழ்க்கை, உயர் ஆம்பியர் மணிநேர செயல்திறன் மற்றும் அதிக ஆற்றல் திறன் ஆகியவற்றை அனுமதிக்க பொருட்கள் சிறிய கட்டமைப்பு மாற்றத்துடன் தலைகீழாக ஒன்றிணைக்க வேண்டும்.
- உயர் செல் மின்னழுத்தம் மற்றும் அதிக ஆற்றல் அடர்த்தியை அடைய, லித்தியம் பரிமாற்ற எதிர்வினை லித்தியத்துடன் ஒப்பிடும்போது அதிக ஆற்றலில் நிகழ வேண்டும்.
- அதிக விகித கட்டணம் மற்றும் வெளியேற்ற செயல்முறைகளை எளிதாக்க, பொருளில் மின்னணு கடத்துத்திறன் மற்றும் லித்தியம் அயன் இயக்கம் அதிகமாக இருக்க வேண்டும்.
- நேர்மறை மின்முனைப் பொருள் எலக்ட்ரோலைட்டில் கரைந்துவிடக் கூடாது மற்றும் மலிவு விலையில் கிடைக்க வேண்டும். செலவைக் குறைக்க, குறைந்த செலவில் மலிவான பொருட்களிலிருந்து தயாரிப்பது விரும்பப்படுகிறது
LiFePO 4 இந்த விதிக்கு விதிவிலக்கு. LiFePO 4 இல், நானோமீட்டர் துகள் அளவைக் கொண்ட எலக்ட்ரோடு துகள்களைப் பயன்படுத்துவதன் மூலம் போதுமான லித்தியம் அயன் போக்குவரத்து அடையப்படுகிறது. [ஜெஃப் டான் மற்றும் கிராண்ட் எம். எர்லிச். “லித்தியம் அயன் பேட்டரிகள்”, லிண்டனின் கையேடு பேட்டரிகள், 4 வது பதிப்பு, தாமஸ் பி. ரெட்டி (பதிப்பு), மெக்ரா ஹில், பக். 26.6, 2011]
லித்தியம் அயன் கலங்களில் உள்ள நேர்மறை செயலில் உள்ள பொருட்கள் (PAM) உற்பத்தியாளரைப் பொறுத்து மாறுபடும். கேத்தோடு பொருட்களை மூன்று பரந்த பிரிவுகளாக வகைப்படுத்தலாம் [ ஆறுமுகம் மந்திரம், இயற்கை தொடர்புகள் (2020) 11:1550]. அவை:
அடுக்கு ஆக்சைடுகள் - லித்தியம் அயன் பேட்டரியில் உள்ள கேத்தோடு பொருட்கள்
பொது வகை LiMO 2 இன் பல ஆக்சைடுகள் (எம் = வெனடியம், குரோமியம், கோபால்ட் மற்றும் நிக்கல்) ஒரு அடுக்கு அமைப்பில் படிகமாக்குகின்றன, இதில் Li + மற்றும் M 3+ அயனிகள் மாற்று [பாறை உப்பு கட்டமைப்பின் பாதைகளை அடுக்கு வரிசையை வழங்குகின்றன. O-Li-OMO இன்.
அடுக்கு ஆக்சைடு கேத்தோடான LiCoO 2 இல், Li + மற்றும் trivalent Co 3+ அயனிகளுக்கு இடையே உள்ள பெரிய மின்சுமை மற்றும் அளவு வேறுபாடுகள் நல்ல கேஷன் வரிசைப்படுத்தலுக்கு இட்டுச் செல்கின்றன, இது லித்தியம் விமானத்தில் வேகமாக இரு பரிமாண லித்தியம்-அயன் பரவல் மற்றும் கடத்துத்திறனை ஆதரிக்க மிகவும் முக்கியமானது.
கத்தோட் பொருட்களுக்கு மிக உயர்ந்த தூய்மை அளவுகள் தேவைப்படுகின்றன மற்றும் தேவையற்ற உலோக அசுத்தங்கள் இல்லாமல் இருக்க வேண்டும் – குறிப்பாக இரும்பு, வெனடியம் மற்றும் கந்தகம்.

படம் 13. ஒரு அடுக்கு கட்டமைப்பின் எளிமைப்படுத்தப்பட்ட திட்டம், இதில் மாற்று ஆக்கிரமிப்பு உள்ளது
நெருக்கமான நிரம்பிய ஆக்சைடு அயனி அடுக்குகளுக்கு இடையே கேஷன் அடுக்குகள்.
[கடன்: ராபர்ட் ஏ. ஹக்கின்ஸ், மேம்பட்ட பேட்டரிகள், பொருட்கள் அறிவியல் அம்சங்கள், ஸ்பிரிங்கர், நியூயார்க், 2009, ப.168]
உயர் மின் மற்றும் லித்தியம்-அயன் கடத்துத்திறனுடன் நல்ல கட்டமைப்பு நிலைத்தன்மையும் நல்ல மீள்தன்மையுடன் வேகமான சார்ஜ்-டிஸ்சார்ஜ் பண்புகளை வழங்குகிறது. இந்த அம்சங்களுடன், LiCoO2 ~4 V இன் உயர் இயக்க மின்னழுத்தத்துடன் இன்றுவரை சிறந்த கத்தோட்களில் ஒன்றாக உள்ளது. LiCoO2 கேத்தோடு தீர்க்கப்பட்டது
1970 களில் தொடரப்பட்ட சல்பைட் கத்தோட்களுடன் தொடர்புடைய இரண்டு முக்கிய சவால்கள். இது இயக்க மின்னழுத்தத்தில் கணிசமான அதிகரிப்பை மட்டும் செயல்படுத்தியது< 2.5 V முதல் ~4 V வரை ஆனால் ஒரு உலோக லித்தியம் அனோடைப் பயன்படுத்த வேண்டிய அவசியம் இல்லாமல் ஒரு கலத்தின் அசெம்பிளி.
ஸ்பைனல் ஆக்சைடுகள் - லித்தியம் அயன் பேட்டரியில் உள்ள கேத்தோடு பொருட்கள்
கேத்தோடின் இரண்டாம் வகுப்பு ஸ்பைனல் LiMn 2 O 4 ஆகும். (பொது சூத்திரம் AB 2 O 4 ஆகும்). இந்த அமைப்பு பொதுவாக கன ஆயத்தொகுப்புகளில் படம்பிடிக்கப்பட்டாலும், இது (111) விமானங்களில் ஆக்சைடு அயனிகளின் இணையான அடுக்குகளைக் கொண்டுள்ளது, மேலும் ஆக்சைடு அயனித் தளங்களுக்கு இடையில் எண்முகமாக ஒருங்கிணைக்கப்பட்ட தளங்கள் மற்றும் டெட்ராஹெட்ரல் ஒருங்கிணைக்கப்பட்ட தளங்கள் இரண்டும் உள்ளன. ஆக்டோஹெட்ரல் தளங்களின் எண்ணிக்கை ஆக்சைடு அயனிகளின் எண்ணிக்கைக்கு சமம், ஆனால் இரண்டு மடங்கு டெட்ராஹெட்ரல் தளங்கள் உள்ளன. முப்பரிமாண கட்டமைப்பு நிலைத்தன்மை மற்றும் உயர் மின் மற்றும் லித்தியம்-அயன் கடத்துத்திறன் ஆகியவை LiCoO 2 உடன் ஒப்பிடும்போது நல்ல மீள்தன்மையுடன் Li 1 – x Mn 2 O 4 க்கு இன்னும் வேகமான சார்ஜ்-டிஸ்சார்ஜ் பண்புகளை வழங்குகின்றன.
LiCoO 2 இலிருந்து LiMn 2 O 4 க்கு செல்வதில் ஒரு முக்கியமான நன்மை என்னவென்றால், மாங்கனீசு Co ஐ விட விலையில் இரண்டு ஆர்டர்கள் குறைவாக இருப்பதால் செலவில் குறிப்பிடத்தக்க குறைப்பு ஆகும். இருப்பினும், LiMn 2 O 4 இல் உள்ள ஒரு முக்கியமான பிரச்சினை, Mn 3 இன் நன்கு அறியப்பட்ட விகிதாச்சாரத்தின் காரணமாக எலக்ட்ரோலைட்டில் H + அயனிகளின் (அமிலத்தன்மை) சுவடு அளவுகள் (பிபிஎம் அளவுகள்) முன்னிலையில், மாங்கனீஸை லேட்டிஸில் இருந்து எலக்ட்ரோலைட்டாகக் கரைப்பது ஆகும். அமிலத்தில் + Mn 4+ மற்றும் Mn 2+ .

படம் 14. டெட்ராஹெட்ரல் மற்றும் ஆக்டோஹெட்ரல் தளங்களில் ஆக்சைடு அயனிகளின் நெருக்கமான (111) விமானங்களுக்கு இடையில் கேஷன்கள் விநியோகிக்கப்படும் ஸ்பைனல் கட்டமைப்பின் திட்டவட்டம் [ கடன்: ராபர்ட் ஏ. ஹக்கின்ஸ், மேம்பட்ட பேட்டரிகள், பொருட்கள் அறிவியல் அம்சங்கள், ஸ்பிரிங்கர், நியூயார்க், 2009, ப.17].
உயர் மின்னழுத்த லித்தியம்-நிக்கல்-மாங்கனீஸ் ஆக்சைடு (LNMO) கேத்தோடு பொருள் அடுத்த தலைமுறை பேட்டரிகளில் நம்பிக்கைக்குரியதாகத் தோன்றுகிறது. ஆனால் எல்என்எம்ஓ-அடிப்படையிலான பேட்டரியின் அழுத்தங்களைக் கையாளக்கூடிய எலக்ட்ரோலைட் இல்லாததே தடுமாற்றம். LNMO கேத்தோட் அடிப்படையிலான பேட்டரி செல்கள் மற்ற உயர் செயல்திறன் கொண்ட லித்தியம் அடிப்படையிலான பேட்டரிகளுக்கு இணையான முடிவுகளை வழங்குகின்றன, ஆனால் கணிசமாக குறைந்த விலையில்.
எவ்வாறாயினும், எலக்ட்ரோலைட் உற்பத்தியாளர்கள் தற்போதைய ஆராய்ச்சி மற்றும் மேம்பாட்டிலிருந்து மிகவும் நம்பிக்கைக்குரிய முடிவுகளைப் பெறுகின்றனர், இது ஒரு கட்டத்தில், எல்என்எம்ஓ பேட்டரி கலத்தில் நன்கு செயல்படும் எலக்ட்ரோலைட்டுகளை விளைவிக்கும். https://blog.topsoe.com/the-cathode-material-for-next-generation-lithium-ion-batteries-is-ready
மிக சமீபத்தில், Ni உள்ளடக்கத்தை அதிகரிப்பது மற்றும் NMC கேத்தோட்களில் கோபால்ட் உள்ளடக்கத்தை குறைப்பது அல்லது நீக்குவது மிகவும் முக்கியத்துவம் வாய்ந்ததாகிறது [ Li, W., Erickson., E. & Manthiram, A. லித்தியம்-அடிப்படையிலான வாகன பேட்டரிகளுக்கான உயர்-நிக்கல் அடுக்கு ஆக்சைடு கத்தோட்கள். , நாட். ஆற்றல் 5, 26 – 24 (2020)].
பாலி-அயன் ஆக்சைடுகள் - லித்தியம் அயன் பேட்டரியில் உள்ள கேத்தோடு பொருட்கள்
ஆக்சைடுகளின் மூன்றாம் வகுப்பு பாலியானியன் ஆக்சைடுகள் ஆகும். Fe 2 (MoO 4 ) 3 மற்றும் Fe 2 (WO 4 ) 3 போன்ற பாலியானியன் ஆக்சைடுகள் Li 2 Fe 2 (MoO 4 ) 3 அல்லது Li 2 Fe 2 ( 2 (MoO 4 ) 3 (Li 2 Fe 2 ) கொடுக்க ஒரு ஃபார்முலா யூனிட்டிற்கு இரண்டு லித்தியம் அயனிகளின் மீளக்கூடிய செருகல் / பிரித்தெடுத்தல் ஆகியவை கண்டறியப்பட்டன. WO 4 ) 3 இரசாயன மற்றும் மின் வேதியியல் முறைகள் மூலம்
[மந்திரம், A., Goodenough, JB லித்தியம் Fe 2 (MO 4 ) 3 கட்டமைப்பில் செருகுதல்: M = W ஐ M = Mo உடன் ஒப்பிடுதல். ஜே. சாலிட் ஸ்டேட் கெம். 71, 349– 360 (1987)].
மந்திரம் மற்றும் குட்எனஃப் படைப்புகளின் அடிப்படையில்,
[ மந்திரம் , ஏ ஜே. சாலிட் ஸ்டேட் கெம். 71, 349–360 (1987). மந்திரம் , ஏ ஜே. பவர் சோர்ஸ் 26, 403–406 (1989).]
லித்தியம் கொண்ட பாஸ்பேட்டுகளை கேத்தோட்களாக ஆராய்வது, ஒலிவின் LiFePO 4 ஐ ஒரு கேத்தோடாக அடையாளம் காண வழிவகுத்தது [பதி, AK, Nanjundaswamy, KS & Goodenough, JB Phospho-Olivines ரிச்சார்ஜபிள் லித்தியம் பேட்டரிகளுக்கு நேர்மறை மின்முனைப் பொருட்கள். ஜே. எலக்ட்ரோகெம். Soc. 144, 1188-1194 (1997] 1997 இல்.
ஆனால், பாலியனியன் ஆக்சைடு வகுப்பு மோசமான மின்னணு கடத்துத்திறனால் பாதிக்கப்படுகிறது. [ ஆறுமுகம் மந்திரம், நேச்சர் கம்யூனிகேஷன்ஸ் (2020) 11:1550].
லித்தியம் கொண்ட பாஸ்பேட்டுகளை கேத்தோட்களாக ஆராய்வது, ஒலிவின் LiFePO 4 ஐ ஒரு கேத்தோடாக அடையாளம் காண வழிவகுத்தது [பதி, AK, Nanjundaswamy, KS & Goodenough, JB Phospho-Olivines ரிச்சார்ஜபிள் லித்தியம் பேட்டரிகளுக்கு நேர்மறை மின்முனைப் பொருட்கள். ஜே. எலக்ட்ரோகெம். Soc. 144, 1188-1194 (1997] 1997 இல்.
ஆனால், பாலியனியன் ஆக்சைடு வகுப்பு மோசமான மின்னணு கடத்துத்திறனால் பாதிக்கப்படுகிறது. [ ஆறுமுகம் மந்திரம், நேச்சர் கம்யூனிகேஷன்ஸ் (2020) 11:1550].
கத்தோட் பொருட்களின் உற்பத்தி - லித்தியம் அயன் பேட்டரி
முன்னதாக, லித்தியம் உலோக ஆக்சைடு கேத்தோடு கலவைகள் லித்தியம் கார்பனேட் மற்றும் தேர்ந்தெடுக்கப்பட்ட உலோகத்தின் உப்பு ஆகியவற்றிலிருந்து கரைசலில் நிகழ்த்தப்பட்ட தொடர்ச்சியான இரசாயன மாற்று எதிர்வினைகள் மூலம் தயாரிக்கப்பட்டன. விரும்பிய தயாரிப்பு துரிதப்படுத்தப்பட்டு தெளிக்கப்பட்டு உலர்த்தப்படுகிறது.
LiCoO 2 முதலில் படத்தில் குறிப்பிடப்பட்டுள்ள வழக்கமான தொகுப்பு முறையால் தயாரிக்கப்பட்டது . ட்ரைகோபால்ட் டெட்ராக்சைடு (Co 3 0 4 ) மற்றும் லித்தியம் கார்பனேட் (Li 2 CO 3 ) ஆகியவை நன்கு கலக்கப்பட்டன, அதைத் தொடர்ந்து சுமார் 950ºC வெப்பநிலையில் காற்று ஓட்டத்தில் சுணக்கம் செய்யப்பட்டது. இருப்பினும், இந்த முறையின் மூலம், LiCoO 2 இன் கரடுமுரடான துகள்களைத் தயாரிப்பது மிகவும் கடினமாக இருந்தது மற்றும் 1-3 pm விட்டம் கொண்ட நுண்ணிய துகள்களை மட்டுமே பெற முடியும்.
ஃபைன் ஆக்டிவ் எலக்ட்ரோடு பொருட்கள் பாதுகாப்புக் கண்ணோட்டத்தில் விரும்பத்தக்கவை அல்ல. வெளிப்புற ஷார்ட் சர்க்யூட் அல்லது நசுக்குதல் போன்ற துஷ்பிரயோகங்களின் போது, பெரிய குறிப்பிட்ட பரப்பளவைக் கொண்ட நுண்ணிய துகள்கள் ஒரே நேரத்தில் எளிதில் வினைபுரியும் மற்றும் அனைத்து செல் ஆற்றலும் வெப்பநிலை அதிகரிப்புடன் மிகக் குறுகிய நேரத்திற்குள் திடீரென வெளியிடப்படுகிறது. மிக மோசமான நிலையில், செல் தீப்பிடிக்கலாம் [யோஷியோ நிஷி, லித்தியம் அயன் பேட்டரிகளில், எம். வக்கிஹாரா மற்றும் 0. யமமோட்டோ (எடி.). பக்கம் 192-193].
லித்தியம் அயன் பேட்டரி எவ்வாறு தயாரிக்கப்படுகிறது? பாய்வு விளக்கப்படம்
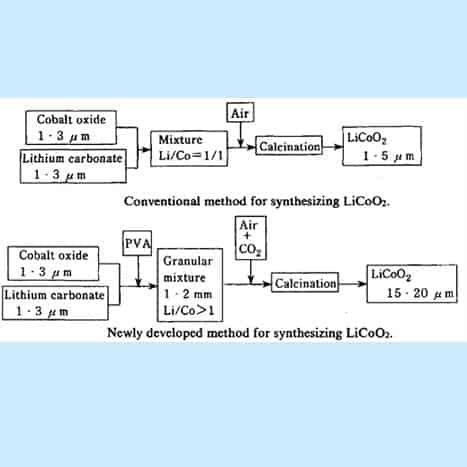
படம் 15. Li-CoO 2 ஐ உருவாக்குவதற்கான பாய்வு விளக்கப்படம்
[கடன்: Yoshio Nishi, Lithium ion Batteries இல், M. Wakihara மற்றும் 0. Yamamoto (Eds.). பக்கம் 192-193].
பெரிய துகள் அளவு கொண்ட லித்தியம் கோபால்டைட்டை ஒருங்கிணைக்கும் ஒரு மேம்படுத்தப்பட்ட செயல்முறை: முதல் புள்ளி, சிறிய அளவு PVA பிசின் மூலப்பொருட்களின் கலவையில் (Co 3 0 4 மற்றும் Li 2 CO 3 ) சேர்த்து சிறுமணித் துகள்களை உருவாக்குகிறது. . தகுந்த அளவு C0 2 வாயுவைக் கொண்ட காற்றோட்டத்தில் துகள்களைத் துடைப்பதன் மூலம், சராசரியாக 20pm விட்டம் கொண்ட லித்தியம் கோபால்டைட் துகள்கள் ஒருங்கிணைக்கப்படுகின்றன. இரண்டாவது புள்ளி, மூலப் பொருட்களில் லித்தியம் கார்பனேட்டை (Li 2 CO 3 ) சற்றே அதிகமாகப் பயன்படுத்துகிறோம், எனவே மூலப் பொருட்களில் Li/Co அணு விகிதம் ஒன்றுக்கு அதிகமாக உள்ளது. இந்த செயல்முறை கரடுமுரடான துகள்களைப் பெறுவதற்கும் சாதகமானது, மேலும் இதன் விளைவாக வரும் LiCoO 2 சிறிய அளவு எஞ்சியிருக்கும் Li 2 CO 3 ஐக் கொண்டுள்ளது.
முதல் புள்ளி, சிறிய அளவு PVA பிசின், மூலப்பொருட்களின் (Co304 மற்றும் Li 2 CO 3 ) கலவையில் ஒரு கிரானுலேட்டருடன் சிறுமணித் துகள்களை உருவாக்குகிறது. லித்தியம் கோபால்ட் ஆக்சைடை சின்டரிங் செய்வதன் மூலம் லித்தியம் கார்பனேட் Li 2 CO 3 மற்றும் கோபால்ட் ஆக்சைடு, Co 3 O 4 அல்லது மெட்டாலிக் கோபால்ட் ஆகியவற்றின் ஸ்டோச்சியோமெட்ரிக் கலவையை 600-800 டிகிரி செல்சியஸில் அதிக வெப்பநிலையில் சுடுவதன் மூலம் உடனடியாக தயாரிக்கலாம். பல மணிநேரங்களுக்கு 900°C, அனைத்தும் ஆக்ஸிஜன் வளிமண்டலத்தின் கீழ்.
750-900 டிகிரி செல்சியஸ் வரை லித்தியம் ஹைட்ராக்சைடுடன் நீரேற்றப்பட்ட ஆக்சைடைக் கணக்கிடுவதன் மூலமும் இதைப் பெறலாம்.
மூன்றாவது முறை லித்தியம் அசிடேட், கோபால்ட் அசிடேட் மற்றும் சிட்ரிக் அமிலம் ஆகியவற்றை சம மோலார் அளவுகளில், நீர் கரைசலில் பயன்படுத்துகிறது. 80 டிகிரி செல்சியஸ் வெப்பம் கலவையை ஒரு பிசுபிசுப்பான வெளிப்படையான ஜெல் ஆக மாற்றுகிறது. உலர்ந்த ஜெல் பின்னர் தரையில் மற்றும் 550 ° C க்கு படிப்படியாக வெப்பப்படுத்தப்படுகிறது. (https: //en.wikipedia.org/wiki/Lithium_cobalt_oxide).
சில பொதுவான எடுத்துக்காட்டுகள்: சோல்-ஜெல் முறை
ஒரு சோல்-ஜெல் செயல்பாட்டில், எதிர்வினைகளின் அக்வஸ் கரைசல்கள் மற்றும் செலேட்டிங் ஏஜென்ட் கரைசல் ஆகியவை கலக்கப்படுகின்றன. கரைப்பானின் மெதுவான ஆவியாதல் ஒரு சோலை உருவாக்குகிறது மற்றும் சோலின் மிதமான வெப்பம் ஒரு ஜெல்லை உருவாக்குகிறது. பிந்தையது விரும்பிய பொருளைப் பெற பொருத்தமான வெப்பநிலையில் கணக்கிடப்படுகிறது.
எடுத்துக்காட்டு 1.
பல்வேறு சிக்கலான முகவர்களிடமிருந்து LiCoO 2 இன் தொகுப்பு: கோபால்ட் நைட்ரேட் ஹெக்ஸா ஹைட்ரேட் (Co(NO 3 ) 2 .6H 2 O, மற்றும் லித்தியம் நைட்ரேட், அன்ஹைட்ரஸ் LiNO 3 ஆகியவை பயன்படுத்தப்படும் உப்புகள். சிட்ரிக் அமிலம், அன்ஹைட்ரஸ் (C 3 H 4 OH(COOH) 3 , கிளைசின், (H 2 NCH 2 COOH); ஸ்டார்ச் (வணிக கார்ன் ஸ்டார்ச் மற்றும் ஜெலட்டின்) ஆகிய நான்கு வெவ்வேறு சிக்கலான முகவர்களைப் பயன்படுத்தி ஜெல் தயாரிக்கப்பட்டது.
Li:Co = 1.1:1 என்ற விகிதத்தில் 20 மில்லி தண்ணீரில் LiNO 3 மற்றும் Co(NO 3 ) 2 .6H 2 O ஆகியவற்றைக் கொண்ட ஐந்து கரைசல்கள் தயாரிக்கப்படுகின்றன. ஒவ்வொரு தீர்வுக்கும் ஒரு குறிப்பிட்ட சிக்கலான முகவர் சேர்க்கப்படுகிறது: ( i ) சிட்ரிக் அமிலம் (4.611 கிராம்) 5 மில்லி தண்ணீரில் நீர்த்தப்படுகிறது; ( ii ) கிளைசின் (1.501 கிராம்); ( iii ) ஸ்டார்ச் (1.250 கிராம்); ( iv ) ஜெலட்டின் (3.500 கிராம்) மற்றும் ( v ) வெற்று சோதனை.
முதல் நான்கு தீர்வுகள் 70 முதல் 80 டிகிரி செல்சியஸ் வெப்பநிலையில் ஒரு கிளிசரின் குளியலில் ஜெல் உருவாகும் வரை சூடேற்றப்பட்டன. ஒவ்வொரு ஜெல்லிங் ஏஜெண்டிற்கும் இந்த செயல்முறையின் நேரம் வேறுபட்டது: ( i ) சிட்ரிக் அமிலம் (5 மணி நேரம்), ( ii ) கிளைசின் (3 மணி நேரம்), ( iii ) ஸ்டார்ச் (1 மணி நேரம்), ( iv ) ஜெலட்டின் (3 மணி நேரம்) . அனைத்து மாதிரிகளுக்கும் படிகப் பொடிகளின் உற்பத்தி இரண்டு நிலைகளில் மஃபிள் உலைகளில் செய்யப்பட்டது: முதலில் பொருட்களை 300 ° C வெப்பநிலையில் 20-30 நிமிடங்கள் சுடவும், பின்னர் 700 ° C க்கு 24 மணிநேரத்திற்கு சூடாக்கவும். [புருனோ ஜிஏ ஃப்ரீடாஸ் மற்றும் பலர், ஜே. பிரேஸ். செம். Soc. 28, 11, நவம்பர் 2017].
எடுத்துக்காட்டு 2.
சோல்-ஜெல் முறையால் தயாரிக்கப்பட்டது
LiNO3 முதலில் சிட்ரிக் அமிலக் கரைசலில் கரைக்கப்படுகிறது. LiNi 0.7 – 𝑥 M 𝑥 Co 0.3 O2 (0 ⩥ 0.1), முறையே. சிட்ரிக் அமிலத்தின் அளவு Co, Ni மற்றும் Mg இன் மொத்த மோலார் அளவுக்கு சமம். பின்னர், Co(Ac)2 4H2O, Ni(NO3)2 6H2O மற்றும் Mg(NO3)2 6H2O ஆகியவை கலவையில் சேர்க்கப்பட்டன. முழு கலவையும் நீர் குளியல் மூலம் 80∘C இல் சூடுபடுத்தப்பட்டது. வெப்பமூட்டும் செயல்பாட்டின் போது, மழைப்பொழிவு இல்லாமல் ஒரு தெளிவான, இளஞ்சிவப்பு தீர்வு உருவாகிறது. இறுதியாக, தெளிவான தீர்வு மெதுவாக உலர்த்தப்பட்டு ஜெல் ஆக மாறியது. ஜெரோஜெல் உலர்த்தப்பட்டு, அரைக்கப்பட்டு, பின்னர் 120 டிகிரி செல்சியஸ் வெப்பநிலையில் 12 மணிநேரத்திற்கு அடுப்பில் சூடாக்கப்பட்டது.
ஜெல் முன்னோடி காற்றில் 500 டிகிரி செல்சியஸ் வெப்பநிலையில் 6 மணிநேரம் கணக்கிடப்பட்டு, ஒரு குழாய்-உலையில் அறை வெப்பநிலையில் குளிர்விக்கப்பட்டது. பொடிகளைப் பெறுவதற்கு வெப்ப-சிகிச்சை செய்யப்பட்ட பொருட்கள் ஒரு அகேட் மோர்டரில் அரைக்கப்பட்டன. பின்னர் தூள் 12 மணி நேரம் 800 ° C இல் கணக்கிடப்பட்டது. கேத்தோட்களை உருவாக்குவதற்கு, தயாரிக்கப்பட்ட பொருட்கள் முதலில் அசிட்டிலீன் கருப்பு மற்றும் பாலிவினைலைடின் ஃவுளூரைடு (80: 8:12 எடை) 𝑁-மெத்தில் பைரோலிடோனில் (NMP) கலக்கப்பட்டன. பெறப்பட்ட குழம்பு அல் ஃபாயிலில் பூசப்பட்டு 80 o C வெப்பநிலையில் 18 மணிநேரத்திற்கு உலர்த்தப்பட்டது. . [ ஹைலாங் ஜாங், மெட்டீரியல் அறிவியல் மற்றும் பொறியியல் தொகுதி 2014, கட்டுரை ஐடி 746341, ]

படம் 16. லித்தியம் மாங்கனேட்டைத் தயாரிப்பதற்கான சோல்-ஜெல் செயல்முறைக்கான பாய்வு விளக்கப்படம்
( கடன்: YS Lee, YK Sun and KS, Nahm, Solid State Ionics 109 (1998) 285 வழங்கியது, M. Pasquali, S. Passerini மற்றும் G Pistoia, லித்தியம் பேட்டரிகள், அறிவியல் மற்றும் தொழில்நுட்பத்தில், பதிப்பு. GA நஸ்ரி மற்றும் ஜி. பிஸ்டோயா, ஸ்பிரிங்கர், நியூயார்க், (2009), ப. 318)
லித்தியம் அயன் பேட்டரியில் அனோட் பொருட்கள் உற்பத்தி
மேம்படுத்தப்பட்ட ஆற்றல் மற்றும் ஆற்றல் அடர்த்தி கொண்ட LIB களுக்கு வழிவகுக்கும் ஊக்கமளிக்கும் பாதையானது, நல்ல சுழற்சி வாழ்க்கை மற்றும் பாதுகாப்பு கவலைகள் இல்லாததுடன், அதிக திறன் மற்றும் ஆனோடில் லி-அயனிகளின் பரவலை எளிதாக்கக்கூடிய பொருத்தமான நேர்மின்முனைப் பொருட்களைத் தேர்ந்தெடுப்பதாகும்.
முன்னோடி பொருட்களின் அடிப்படையில், கார்பன் அனோட்களை கீழே கொடுக்கப்பட்டுள்ளபடி பல வகைகளாக வகைப்படுத்தலாம்.
முன்னோடி பொருள் மற்றும் செயலாக்க அளவுருக்கள் உற்பத்தி செய்யப்படும் கார்பனின் தன்மையை தீர்மானிக்கின்றன. அதிக வெப்பநிலையில் (2000 முதல் 3000 டிகிரி செல்சியஸ் வரை) சிகிச்சை மூலம் கிராஃபிடைஸ் செய்யக்கூடிய பொருட்கள் மென்மையான கார்பன்கள் என்று அழைக்கப்படுகின்றன.
கிராஃபிடைசேஷனில், அதிகரிக்கும் வெப்பநிலையுடன் டர்போஸ்ட்ராடிக் கோளாறு படிப்படியாக அகற்றப்பட்டு, பொருளின் திரிபு விடுவிக்கப்படுகிறது [டி. ஜெங், ஜேஎன் ரீமர்ஸ் மற்றும் ஜேஆர் டான், இயற்பியல் ரெவ். பி 51 , 734 (1995)] 3000 டிகிரி செல்சியஸ் வெப்பநிலையில் சிகிச்சையளிக்கப்பட்டாலும், பினாலிக் பிசினிலிருந்து தயாரிக்கப்பட்டது போன்ற கடினமான கார்பன்களை உடனடியாக கிராஃபிடைஸ் செய்ய முடியாது. கோக்-வகைப் பொருட்கள் சுமார் 1000°C இல் தயாரிக்கப்படுகின்றன, பொதுவாக ஒரு நறுமண பெட்ரோலியம் முன்னோடியிலிருந்து [ஜெஃப் டான் மற்றும் கிராண்ட் எம். எர்லிச். “லித்தியம் அயன் பேட்டரிகள்”, லிண்டனின் கையேடு பேட்டரிகள், 4 வது பதிப்பு, தாமஸ் பி. ரெட்டி (பதிப்பு), மெக்ரா ஹில், பக். 26., 2011]

படம் 17. கார்பன் அனோட் பொருட்கள் முன்னோடி வகைப்பாடு
[கடன்: ஜெஃப் டான் மற்றும் கிராண்ட் எம். எர்லிச். “லித்தியம் அயன் பேட்டரிகள்”, லிண்டனின் கையேடு பேட்டரிகள், 4 வது பதிப்பு, தாமஸ் பி. ரெட்டி (பதிப்பு), மெக்ரா ஹில், பக். 26., 2011]
கோரிபார்டி LIB இன் ஆனோட் பொருட்களை லித்தியத்துடன் அவற்றின் எதிர்வினை பொறிமுறையைப் பொறுத்து மூன்று வகைகளாகப் பிரிக்கிறது [ சுப்ரமணியம் கோரிபார்ட்டி, எர்மன்னோ மியேல், பிரான்செஸ்கோ டி ஏஞ்சலிஸ், என்ஸோ டி ஃபேப்ரிசியோ, ரெமோ ப்ரோயெட்டி சக்காரியா, கிளாடியோ காபிக்லியா, ஜே பவர் சோர்சஸ் 257 (2014) 421-443]
இடைக்கணிப்பு/இடையிடல் குழு
இந்த வகை அனோடில் கார்பனேசியஸ் மற்றும் டைட்டானியம் ஆக்சைடு பொருட்கள் அடங்கும். இடைக்கணிப்புப் பாதையின் மூலம் நிகழும் சேமிப்புத் திறன் மேற்பரப்புப் பகுதி, உருவவியல், படிகத்தன்மை மற்றும் அதன் நோக்குநிலை ஆகியவற்றுடன் நெருக்கமாக தொடர்புடையது. மென்மையான கார்பன்கள் பொதுவாக நன்கு ஏற்றுக்கொள்ளப்பட்டு பேட்டரி துறையில் பயன்படுத்தப்படுகின்றன. மென்மையான கார்பன் மிகவும் முதிர்ந்த தொழில்நுட்பம் என்று பார்க்கப்பட்டது, அதே நேரத்தில் கடினமான கார்பன் ஒரு சுவாரஸ்யமான மாற்று தீர்வை வழங்கக்கூடும், குறிப்பாக மின்சார வாகனத் துறை போன்ற அதிக திறன் தேவைப்படும் பயன்பாடுகளுக்கு. டைட்டானியம் ஆக்சைடு அனோட்கள் ஏற்கனவே சில பேட்டரி தொழிற்சாலைகளால் பயன்படுத்தப்படுகின்றன.


கிராபீனும் விரிவாக மதிப்பாய்வு செய்யப்பட்டது. குறிப்பாக, அவற்றின் மின் பண்புகள் இந்தப் பொருளை ஹைப்ரிட் கிராபெனின்/மெட்டல் அனோட்களுக்கு ஏற்றதாக ஆக்குகிறது (உதாரணமாக SnO2 மற்றும் Fe2O3 உடன் கிராபெனின்). கார்பன் நானோ-குழாய்கள் (CNT கள்) அவற்றின் மிகவும் சுவாரஸ்யமான கல்வி முடிவுகளுக்கு குறிப்பிடத்தக்கவை, இருப்பினும் உற்பத்தி செலவு எதிர்காலத்தில் பேட்டரி துறையில் அனோட் செயலில் உள்ள பொருளாக அவற்றின் பயன்பாட்டிற்கு தடையாக இருக்கலாம்.


இருப்பினும், பெரிய EV பேட்டரிகளுக்கு, குறைந்த விலை கிராஃபைட்டுகள் பொதுவாக விலைக் கருத்தில் கொள்ளப்படுகின்றன.
இரண்டாவது பிரிவில், Si, Ge, SiO, SnO2 போன்ற கலவைப் பொருட்கள் விவரிக்கப்பட்டுள்ளன. இந்த பொருட்கள் ஒரு அலாய்/டி-அலாய் எலக்ட்ரோகெமிக்கல் பொறிமுறையில் லித்தியத்துடன் வினைபுரிவதன் மூலம் முந்தைய குழுவுடன் ஒப்பிடும்போது பெரிய திறன்களையும் அதிக ஆற்றல் அடர்த்தியையும் வழங்க முடியும். இருப்பினும், இந்த செயல்முறை பெரிய அளவிலான விரிவாக்கத்தைக் குறிக்கிறது, இது சைக்கிள் ஓட்டும்போது கணிசமான திறன் இழப்பை ஏற்படுத்துகிறது. மொத்த பரிமாணங்களில் இருந்து நானோ அளவிற்கான குறைப்பு, கடத்தும் மெட்ரிக்ஸுடன் இணைந்து சிக்கலான கட்டமைப்புகளை உணர்தல் ஆகியவற்றுடன், மேலே குறிப்பிடப்பட்ட சிக்கல்களை சமாளிக்கவும் ஒட்டுமொத்த நேர்மின்முனை செயல்திறனை மேம்படுத்தவும் முன்மொழியப்பட்டது.
சிலிக்கான் மற்றும் SnO2 மற்றும் கார்பனுடன் அவற்றின் கலவை ஆகியவை எதிர்கால லித்தியம் பேட்டரிகளில் பயன்பாடுகளுக்கு மிகவும் நம்பிக்கைக்குரிய பொருட்களாகும், இருப்பினும், அனோட் பொருட்களாக அவற்றின் வெகுஜன உற்பத்திக்கு மலிவான வழி இன்னும் அவசியம். மறுபுறம், Ge, அதன் மின்வேதியியல் பண்புகள் மற்றும் சிறந்த சோதனை ஆய்வக முடிவுகளுக்கு ஆர்வமாக இருந்தாலும், பூமியின் மேலோட்டத்தில் ஏராளமாக இருக்கும் உறுப்புகளின் ஐம்பதாவது தரவரிசையின் குறைபாட்டால் பாதிக்கப்படுகிறது. எனவே, லித்தியம் பேட்டரி தொழில்நுட்ப வெகுஜன பயன்பாட்டுக்கு இது ஒரு நல்ல விருப்பமாக இல்லை.
மூன்றாவது குழுவில், மாற்று எதிர்வினை பாணியில் லித்தியத்துடன் வினைபுரியும் பொருட்கள் விவரிக்கப்பட்டுள்ளன. குறிப்பாக, உலோக ஆக்சைடுகள் / பாஸ்பைடுகள் / நைட்ரைடுகள் / சல்பைடுகள் கருதப்பட்டன. இருப்பினும், மோசமான திறன் தக்கவைப்பு மற்றும் பெரிய சாத்தியமான ஹிஸ்டெரிசிஸ் காரணமாக இந்த பொருட்கள் இன்னும் பெரிய வணிக லித்தியம் பேட்டரி சந்தையில் இருந்து வெகு தொலைவில் உள்ளன. எனவே, மேலே அடையாளம் காணப்பட்ட சிக்கல்களைத் தீர்க்க இந்தப் பொருட்களின் பல்வேறு நானோ-கட்டமைக்கப்பட்ட வடிவங்களும் ஆராயப்பட்டுள்ளன.
லித்தியம் பேட்டரிகளுக்கான அடுத்த தலைமுறை அனோட் பொருட்களைப் பொறியியலுக்கு நானோ தொழில்நுட்பம் நிச்சயமாக ஒரு வலிமையான அணுகுமுறையாகும். வணிக எல்ஐபிகளில், குறிப்பாக EV பயன்பாடுகளுக்கு, விவரிக்கப்பட்ட பொருட்களை பயனுள்ள அனோட்களாகப் பயன்படுத்த, இன்னும் ஆராய்ச்சிப் பணிகள் தேவைப்படுகின்றன. உண்மையில், நானோமயமாக்கப்பட்ட பொருட்களின் பெரிய அளவிலான தொகுப்புக்கான மலிவான புனையமைப்பு செயல்முறைகளை உருவாக்குவதன் மூலம் அதிக ஆற்றல் மற்றும் அதிக ஆற்றல் அடர்த்தி இரண்டையும் அடைவது அவசியம். மேலும், எலக்ட்ரோடு/எலக்ட்ரோலைட் இடைமுகத்தில் உள்ள எலக்ட்ரான் போக்குவரத்து பண்புகளுடன் லித்தியம் மற்றும் விவரிக்கப்பட்ட பொருட்களின் நானோமயமாக்கப்பட்ட வடிவங்களுக்கு இடையேயான தொடர்புகளை ஆளும் வழிமுறைகளின் விசாரணை, நானோ தொழில்நுட்பத்தால் வடிவமைக்கப்பட்ட அடுத்த தலைமுறை ஆனோட் செயலில் உள்ள பொருட்களின் வடிவமைப்பிற்கு மிகவும் முக்கியமானது. .
தற்போது லித்தியம் செல்களில் பயன்படுத்தப்படும் எதிர்மறை மின்முனைகள் கார்பனின் வடிவங்களில் ஒன்றில் லித்தியத்தின் திடமான கரைசலை உள்ளடக்கியது. லித்தியத்தின் உருகுநிலைக்கு மேலான வெப்பநிலையில் செயல்படும் லித்தியம் செல்கள், தனிம லித்தியத்திற்கு பதிலாக உலோகக் கலவைகளைப் பயன்படுத்த வேண்டும். இவை பொதுவாக பைனரி அல்லது மும்மை உலோக கட்டங்களாகும். சுற்றுப்புற வெப்பநிலையில் கார்பன்களுக்குப் பதிலாக உலோகக் கலவைகளைப் பயன்படுத்துவதற்கான சாத்தியக்கூறுகளில் தற்போதைய ஆர்வமும் அதிகரித்து வருகிறது, மின்முனையின் அளவைக் குறைக்கும் நோக்கத்துடன், அத்துடன் கணிசமாக அதிகரித்த திறனை அடைகிறது. [Robert A. Huggins, Advanced Batteries, Materials Science Aspects, Springer, New York, 2009, p.123].
கிராஃபைட் ஆம்போடெரிக் ஆகும், மேலும் கிராபெனின் அடுக்குகளுக்கு இடையில் கேஷன்கள் அல்லது அயனிகள் அதில் செருகப்படலாம். கேஷன்கள் செருகப்படும் போது, புரவலன் கிராஃபைட் அமைப்பு எதிர்மறை மின்னூட்டத்தைப் பெறுகிறது. கேஷன் எடுத்துக்காட்டுகள் லி + , கே + , ஆர்பி + மற்றும் சிஎஸ் + . அயனிகள் செருகப்படும் போது, ஹோஸ்ட் கிராஃபைட் அமைப்பு நேர்மறை மின்னூட்டத்தைப் பெறுகிறது, மேலும் அயனி எடுத்துக்காட்டுகள் Br – ,SO2 – , SbF6 –
கார்பனில் கார உலோகங்கள் செருகப்படுவது முதன்முதலில் 1926 இல் நிரூபிக்கப்பட்டது . ஃப்ரெடன்ஹேகன் மற்றும் ஜி. கேடன்பாக், இசட். அனோர்க். Allg. செம். 158, 249 (1926)] மற்றும் லித்தியம்-கார்பன்களின் வேதியியல் தொகுப்பு 1955 இல் நிரூபிக்கப்பட்டது. [ D. Guerard, A. Heold, Carbon 13, 337 (1975 )]. எக்ஸ்ரே ஃபோட்டோமிஷன் ஸ்பெக்ட்ரோஸ்கோபி சோதனைகள், செருகப்பட்ட லித்தியம் அதன் எலக்ட்ரானை கார்பனுக்கு விட்டுக்கொடுக்கிறது என்பதைக் காட்டுகிறது, இதனால் கிராஃபைட் கட்டமைப்பின் கார்பன் அடுக்குகளுக்கு இடையில் உள்ள லி + அயனிகளாக கட்டமைப்பைக் காணலாம்.
[GK Wertheim, PMTh.M. வான் அட்டேகம் மற்றும் எஸ். பாசு, சாலிட் ஸ்டேட் கம்யூ. 33, 1127 (1980)]. கிராஃபைட்டில் இனங்களைச் செருகுவதற்கான ஆரம்பகால வேலைகளின் பொதுவான மதிப்பாய்வைக் காணலாம்
[எல்பி ஈபர்ட், கிராஃபைட்டின் இடைக்கணிப்பு கலவைகள், பொருட்கள் அறிவியலின் வருடாந்திர மதிப்பாய்வில்,
தொகுதி. 6, பதிப்பு. RA Huggins மூலம், வருடாந்திர விமர்சனங்கள், பாலோ ஆல்டோ, CA (1976), ப. 181].
நேர்மின்வாயில் பொருளின் தூய்மையின் முக்கிய காரணி, மேற்பரப்பில் உள்ள ஆக்ஸிஜன் கொண்ட உயிரினங்களை அகற்றுவது அவசியம், ஏனெனில் இவை எலக்ட்ரோலைட்டுடன் வினைபுரியும். இந்த எதிர்வினையைத் தடுக்க, உற்பத்தியாளர்கள் கிராஃபைட்டை 1100ºC) குறைக்கும் அல்லது செயலற்ற வளிமண்டலத்தில் சுடுகிறார்கள். இது கிராஃபைட்டுடன் ஒப்பிடும் போது மற்ற பயன்பாடுகளுக்கான விலையை அதிகரிக்கிறது. கார்பன் (90%) அனோட் பேஸ்ட் அல்லது ஸ்லரி செய்ய பல பொருட்களுடன் கலக்கப்படுகிறது. கேத்தோடைப் போலவே, பாலிவினைலைடின் புளோரைடு (PVDF) ஒரு பைண்டராக (-5%) பயன்படுத்தப்படுகிறது, மேலும் கடத்துத்திறனை உறுதிப்படுத்த சிறிய அளவு கார்பன் கருப்பு சேர்க்கப்படுகிறது. கூடுதலாக, n-மெத்தில் பைரோலிடோன் (NMP) ஒரு சீரான கலவையை உருவாக்க பொருட்களை கரைக்க பயன்படுத்தப்படுகிறது. அழுத்தம் சீரான தானிய அளவை உறுதி செய்கிறது (சாண்டி 1999).
லித்தியம் டைட்டனேட் (LTO) மிகவும் ஆர்வமாக உள்ளது. LTO செல்கள் மற்ற வேதியியலைக் காட்டிலும் குறைந்த வெப்பநிலையில் இயங்குகின்றன மற்றும் அதிக ஆற்றல் அடர்த்தியை வழங்குகின்றன. இருப்பினும், அத்தகைய செல்கள் குறைந்த பெயரளவு மின்னழுத்தத்தைக் கொண்டிருக்கின்றன, ஒரு கலத்திற்கு சுமார் 2.2-2.3 V வரம்பில். [Norio Takami, Hiroki Inagaki, Yoshinao Tatebayashi, Hidesato Saruwatari, Keizoh Honda, Shun Egusa, J Power Sources 244 (2013) 469-475]
எலக்ட்ரோடு பொருள், பொதுவாக கிராஃபைட், சார்ஜிங் செயல்பாட்டின் போது 10% விரிவடைகிறது. லித்தியம் அயனிகள் பிரிக்கும்போது கிராஃபைட் அதன் அசல் அளவைப் பெறுகிறது. அலுமினியம் பயன்படுத்தப்பட்டால் லித்தியம் அயனிகள் கிராஃபைட்டுடன் ஒன்றிணைக்கப்படுவது மட்டுமல்லாமல், கடத்தியில் செருகப்படும், இதனால் அலுமினியம்-லித்தியம் கலவை உருவாகிறது. டிஸ்சார்ஜ் செய்யும் போது தலைகீழ் செயல்முறை ஏற்படும். அலுமினியம் சில சுழற்சிகளுக்குப் பிறகு சிதைந்து, தற்போதைய சேகரிப்பாளராக பயனற்றதாக இருக்கும்.
இருப்பினும், எதிர்மறை மின்முனையானது கிராஃபைட்டுக்குப் பதிலாக லித்தியம் டைட்டனேட்டிலிருந்து உருவாக்கப்பட்டால், நிலைமை வியத்தகு முறையில் மாறுகிறது. Li 4 Ti 5 O 12 இன் மின்முனை திறன் கிராஃபைட்டை விட 1.4 V அதிகமாக உள்ளது (செல் மின்னழுத்தம் சுமார் 1.4 V குறைவாக உள்ளது, 3.6 V க்கு எதிராக 2.2 V). இது லித்தியம் அயனிகள் அலுமினியத்துடன் ஒன்றிணைவதைத் தடுக்கும். எனவே, செலவு தொடர்பான மற்றும் எடை தொடர்பான காரணங்களுக்காக தாமிரத்தை விட அலுமினியம் விரும்பப்படுகிறது. Li 4 Ti 5 O 12 அதன் குறைந்த செல் மின்னழுத்தம் காரணமாக முக்கியமாக நிலையான பயன்பாடுகளில் பயன்படுத்தப்படுகிறது. [ Călin Wurm et al., in Lithium-Ion Batteries, Reiner Korthauer (ed), Translated by Michael Wuest et.al., Springer, 2018. pp. 57 ].
லித்தியம் டைட்டனேட்டை உற்பத்தி செய்வதற்கான செயல்முறை: டைட்டானியம் டை ஆக்சைடு மற்றும் லித்தியம் கலவை (இதில் ஏதேனும் ஒன்று: லித்தியம் கார்பனேட், லித்தியம் ஹைட்ராக்சைடு, லித்தியம் நைட்ரேட் மற்றும் லித்தியம் ஆக்சைடு) கலவையானது 670°C மற்றும் 800°C வெப்பநிலையில் முன் வடிகட்டப்படுகிறது. . TiO 2 , மற்றும் Li 2 TiO 3 ஆகியவற்றைக் கொண்ட ஒரு கலவை அல்லது TiO 2 , Li 2 TiO 3 , மற்றும் Li 4 Ti 5 O 12 ஆகியவற்றைக் கொண்ட கலவை பெறப்படுகிறது. கலவை பின்னர் 800 முதல் 950 டிகிரி செல்சியஸ் வெப்பநிலையில் சின்டர் செய்யப்படுகிறது. [Tetsuya Yamawaki et.al., US காப்புரிமை 6,645,673 B2, 2003 Toho Titanium Co., Ltd., Chigasaki க்கு ஒதுக்கப்பட்டது]
தோஷிபாவின் SCiB™ ரீசார்ஜ் செய்யக்கூடிய பேட்டரி (https://www.scib.jp/en/)
SCiB™ பாதுகாப்பு, நீண்ட ஆயுள், குறைந்த வெப்பநிலை செயல்திறன், விரைவான சார்ஜிங், அதிக உள்ளீடு/வெளியீட்டு சக்தி மற்றும் பெரிய பயனுள்ள திறன் ஆகியவற்றை அடைய லித்தியம் டைட்டானியம் ஆக்சைடை (LTO) அதன் அனோடில் பயன்படுத்துகிறது. SCiB™ வாகனம், தொழில்துறை மற்றும் உள்கட்டமைப்பு பயன்பாடுகளில் ஆட்டோமொபைல்கள், பேருந்துகள், இரயில் கார்கள், லிஃப்ட் மற்றும் மின் உற்பத்தி நிலையங்கள் உட்பட பரந்த பயன்பாடுகளைக் கண்டறிந்துள்ளது.
லித்தியம் அயன் பேட்டரி பிரிப்பான் உற்பத்தி
இரண்டு வகையான செயல்முறைகள் உள்ளன: ஈரமான மற்றும் உலர். ஜப்பானிய உற்பத்தியாளர்கள் ஈரமான செயல்முறையைப் பயன்படுத்துகின்றனர், இதில் பாலிமர் எண்ணெயில் கரைக்கப்படுகிறது. எண்ணெய் பின்னர் ஒரு நுண்துளை படலத்தை விட்டு ஆவியாகிறது. அவர்கள் செல்கார்டை உருவாக்க அல்ட்ராஹை மூலக்கூறு எடையின் பாலிமர்களைப் பயன்படுத்துகின்றனர், பாலிமர் கட்டமைப்பைக் கட்டுப்படுத்த, ஊதப்பட்ட பாலிமர் ஃபிலிமின் மூன்று அடுக்குகள் லேமினேட் செய்யப்பட்டு, கீழே வரையப்பட்டு, உருகுநிலைக்குக் கீழே இணைக்கப்படுகின்றன. தாள் பின்னர் போரோசிட்டியைப் பெற விரைவாக நீட்டப்படுகிறது.
இரண்டு வகையான செயல்முறைகள் உள்ளன: ஈரமான மற்றும் உலர். ஜப்பானிய உற்பத்தியாளர்கள் ஈரமான செயல்முறையைப் பயன்படுத்துகின்றனர், இதில் பாலிமர் எண்ணெயில் கரைக்கப்படுகிறது. எண்ணெய் பின்னர் ஒரு நுண்துளை படலத்தை விட்டு ஆவியாகிறது. அவர்கள் செல்கார்டை உருவாக்க அல்ட்ராஹை மூலக்கூறு எடையின் பாலிமர்களைப் பயன்படுத்துகின்றனர், பாலிமர் கட்டமைப்பைக் கட்டுப்படுத்த, ஊதப்பட்ட பாலிமர் ஃபிலிமின் மூன்று அடுக்குகள் லேமினேட் செய்யப்பட்டு, கீழே வரையப்பட்டு, உருகுநிலைக்குக் கீழே இணைக்கப்படுகின்றன. தாள் பின்னர் போரோசிட்டியைப் பெற விரைவாக நீட்டப்படுகிறது.
[Pekala, RW, et al., 2000, “Separators: An Overlooked Opportunity to Enhance Battery Performance?,” 17வது சர்வதேச கருத்தரங்கு மற்றும் முதன்மை மற்றும் இரண்டாம் நிலை பேட்டரிகள் மீதான கண்காட்சி, அடி. லாடர்டேல், ஃப்ளா., மார்ச் 6-9]
இந்த செயல்முறை இயக்க நிலைமைகளுக்கு மிகவும் உணர்திறன் கொண்டது மற்றும் பொருள் தொகுப்புகளுடன் கூட மாறுபடும், எனவே கவனமாகக் கட்டுப்படுத்துவது அவசியம் [லிண்டா கெய்ன்ஸ் மற்றும் ராய் குவென்கா, வாகனங்களுக்கான லித்தியம் அயன் பேட்டரிகளின் விலை, ANL அறிக்கை ANL/ESD-42, மே 2000, பக். 20 ] .
இருப்பினும், EV/HEV செல்களுக்கு பிரிப்பான்களில் தேவைப்படும் கூடுதல் தடிமன் குறைக்கப்பட்ட வலிமையை ஈடுசெய்கிறது. [ஒய். நிஷி, இல்: எம். வக்கிஹாரா, ஓ. யமமோட்டோ (பதிப்பு.), லித்தியம் அயன் பேட்டரிகள், விலே/விசிஎச்/கோடன்ஷா, டோக்கியோ, 1998, ப. 195.
பி. அரோரா, இசட். ஜாங், செம். ரெவ். 104 (2004) 4419].
நல்ல இயந்திர வலிமை, எலக்ட்ரோலைட் ஊடுருவல் போன்ற வழக்கமான பண்புகளுக்கு கூடுதலாக, இந்த மைக்ரோ நுண்துளை பிரிப்பான்கள் செல் துஷ்பிரயோகத்தின் போது ஒரு பாதுகாப்பு பண்புகளைக் காட்டுகின்றன. எடுத்துக்காட்டாக, அதிகப்படியான ஓவர்சார்ஜ் காரணமாக செல் வெப்பநிலை அசாதாரணமாக உயர்ந்தால், எடுத்துக்காட்டாக, உருவாகும் வெப்பம் PE ஐ மென்மையாக்குகிறது மற்றும் படத்தில் உள்ள மைக்ரோபோர்களை மூடுகிறது. இது பிரிப்பான் “பணிநிறுத்தம்” என்று அழைக்கப்படுகிறது. பணிநிறுத்தம் ஏற்பட்டவுடன், மின்முனைகளுக்கிடையேயான அயனி போக்குவரத்து திறம்பட நிறுத்தப்பட்டு மின்னோட்டம் பாய்வதை நிறுத்துகிறது. பிரிப்பான் அதன் பணிநிறுத்தம் வெப்பநிலைக்கு மேல் இயந்திர ஒருமைப்பாட்டை தக்க வைத்துக் கொள்ள முடிந்தால், அது சாதனத்திற்கு ஒரு பாதுகாப்பு விளிம்பை வழங்க முடியும்; இல்லையெனில், மின்முனைகள் நேரடி தொடர்புக்கு வரலாம், வேதியியல் ரீதியாக வினைபுரிந்து, வெப்ப ரன்வேக்கு வழிவகுக்கும்.
இருப்பினும், வெப்ப மந்தநிலை காரணமாக, பணிநிறுத்தத்திற்குப் பிறகும் வெப்பநிலை தொடர்ந்து உயரும். இத்தகைய நிலைமைகளின் கீழ் பிரிப்பான் உருகி மின்முனைகளை சுருக்கி, வன்முறை எதிர்வினைகள் மற்றும் வெப்ப உருவாக்கத்திற்கு வழிவகுக்கும். இந்த நிகழ்வு பிரிப்பானின் “உருகுதல்” அல்லது “முறிவு” என்று அழைக்கப்படுகிறது. எனவே, கலத்தின் பாதுகாப்பை உறுதி செய்வதற்காக, “பணிநிறுத்தம்” மற்றும் “உருகுதல்” வெப்பநிலைகளுக்கு இடையிலான வேறுபாடு முடிந்தவரை பெரியதாக இருக்க வேண்டும்.
முழுக்க முழுக்க உயர் அடர்த்தி பாலிஎதிலினால் செய்யப்பட்ட பிரிப்பான்கள் 135 டிகிரி செல்சியஸ் வெப்பநிலையில் உருகும் மற்றும் இந்த வெப்பநிலைக்கு மேல் இயந்திர ஒருமைப்பாட்டை இழக்கின்றன. இருப்பினும், பாலிப்ரொப்பிலீன் மற்றும் பாலிஎதிலீன் அடுக்குகளை லேமினேட் செய்வதன் மூலம் செய்யப்பட்ட பிரிப்பான்கள் குறைந்தபட்சம் 165 டிகிரி செல்சியஸ் வரை இயந்திர ஒருமைப்பாட்டை பராமரிக்கின்றன, இது பாலிப்ரோப்பிலீனின் உருகும் புள்ளியாகும். அல்ட்ராஹை மூலக்கூறு எடை பாலிஎதிலீன் 135 ° C இல் உருகினாலும், இந்த பொருளிலிருந்து பிரிப்பான்கள் குறைந்தபட்சம் 180 ° C வரை இயந்திர ஒருமைப்பாட்டை தக்கவைத்துக்கொள்கின்றன, ஏனெனில் பொருளின் பாகுத்தன்மை உடல் ஒருமைப்பாட்டை பராமரிக்கிறது.
பணிநிறுத்தம் பிரிப்பான்கள் நம்பகமானவை மற்றும் லித்தியம்-அயன் பேட்டரி உற்பத்தியாளர்கள் தங்கள் தயாரிப்புகளில் தங்கள் ஒருங்கிணைப்பை அதிகளவில் தேர்வு செய்கின்றனர். மிகவும் பொதுவான பணிநிறுத்தம் பிரிப்பான்கள் அதிக மூலக்கூறு எடை பாலிப்ரோப்பிலீன் மற்றும் சூப்பர்-ஹை மூலக்கூறு எடை பாலிஎதிலினுடன் கலக்கப்படுகின்றன. இங்கே, பாலிஎதிலினின் தனித்துவமான பணிநிறுத்தம் பண்பு உயர்ந்த வெப்பநிலையில் பாலிப்ரொப்பிலீனின் உயர் இயந்திர ஒருமைப்பாட்டுடன் சாதகமாக இணைக்கப்பட்டுள்ளது. பணிநிறுத்தம் மீள முடியாதது என்பதால், ஒருமுறை செயல்படுத்தப்பட்டால், இந்த பிரிப்பான்கள் செல்களை நிரந்தரமாக சேதப்படுத்தும். [பி.ஜி.பாலகிருஷ்ணன், ஆர். ரமேஷ், டி. பிரேம் குமார் , ஜே. பவர் சோர்ஸ். 155 (2006) 401–414]
லித்தியம் அயன் பேட்டரியில் உள்ள மற்ற பொருட்கள்
அலுமினியம், நிக்கல் மற்றும் காப்பர் ஃபாயில்கள், s tyrene-butadiene copolymer (SBR) போன்ற பைண்டர்கள் மற்றும் p ஒலிவினைலைடின் ஃவுளூரைடு (PVDF), எலக்ட்ரோலைட்டுகள் மற்றும் கரைப்பான்கள், கேத்தோடு கடத்தும் சேர்க்கைகள், பிரிப்பான் போன்ற பிற பொருட்கள் உள்ளன.
லித்தியம் அயன் பேட்டரியின் நன்மைகள் மற்றும் வரம்புகள் - லித்தியம் அயன் செல் உற்பத்தி
அனோட் மற்றும் கேத்தோடு எடை விகிதம்
செல் செயல்பாட்டின் போது லித்தியம் உலோகம் உருவாகாமல் இருப்பது மிகவும் முக்கியம். உலோகத்தின் படிவு டென்ட்ரைட்டுகளை உருவாக்குகிறது, இது கலத்தை உட்புறமாக சுருக்குகிறது. சார்ஜிங் மற்றும் செல் சமநிலையின் போது மின்னழுத்த கட்டுப்பாடு இந்த சிக்கலை மிக பெரிய அளவில் குறைக்க உதவுகிறது. லித்தியம் படிவைக் கட்டுப்படுத்துவதற்கான முக்கிய முறையானது கலத்தில் உள்ள தனித்தனி தகடுகளின் கேத்தோடு திறனுக்கு நேர்மின்வாயின் விகிதமாகும். நேர்மின்வாயில் மின்முனையானது கேத்தோடைக் காட்டிலும் 10% அதிகப் பயன்படுத்தக்கூடிய திறன் கொண்டது. மின்னோட்டத்தின் போது மின்முனையில் லித்தியம் உலோக படிவு ஏற்படுவதை இது தடுக்கிறது, ஏனெனில் கேத்தோடு கலத்தின் திறனை தீர்மானிக்கிறது. எலக்ட்ரோடு மேற்பரப்பில் லித்தியம் உலோகம் படிந்தால், அது எலக்ட்ரோலைட்டுடன் வினைபுரிந்து வெப்ப ஓட்டத்தைத் தொடங்கலாம்.

படம் 21. லித்தியம் அயன் கலத்தில் அனோட் மற்றும் கேத்தோடு திறன் விகிதம்
( கடன்: Ralph J. Brodd and Kazuo Tagawa, in Advances in Lithium-Ion Batteries, Walter A. van Schalkwijk and Bruno Scrosati (Eds), Kluwer Academic Publishers, New York, pp. 272, 2002.)
லித்தியம் அயன் செல் சட்டசபை செயல்முறைகள்
ஒரு லித்தியம் அயன் பேட்டரிக்கான செல் அசெம்பிளி செயல்முறைகளுக்கு, செயலில் உள்ள பொருளுடன் பூசப்பட்ட நேர்மறை மற்றும் எதிர்மறை எலக்ட்ரோடு பங்குகளை பூசும்போது துல்லியம் மற்றும் துல்லியம் தேவைப்படுகிறது. பூச்சு செயல்முறை உயர் திறன், உயர் நம்பகத்தன்மை தயாரிப்பு உறுதி ஒரு முக்கிய உறுப்பு ஆகும். பூச்சுகள் தரமற்றதாக இருந்தால், குறைந்த செயல்திறன் கொண்ட பேட்டரிகள் மட்டுமே தயாரிக்கப்படும். செயலில் உள்ள வெகுஜனத்தை தயாரிப்பதில் ஆரம்ப படிகள் முடிவை தீர்மானிக்கின்றன.
கோஹன் மற்றும் குடோஃப் [ஈ. கோஹன் மற்றும் ஈ. குடோஃப், நவீன பூச்சு மற்றும் உலர்த்தும் தொழில்நுட்பம், விலே-விசிஎச்,
நியூயார்க், 1992] பூச்சு குழம்பு, தேவையான துல்லியம் மற்றும் பூச்சு வேகம் ஆகியவற்றின் அடிப்படையில், ஒரு குறிப்பிட்ட பயன்பாட்டிற்கான சிறந்த பூச்சு நுட்பத்தை அடைய ஒரு வழிமுறையை விவரிக்கிறது.

படம் 22. அனோட் மற்றும் கேத்தோடு பூச்சு செயல்முறை
( கடன்: ரால்ப் ஜே. ப்ராட் மற்றும் கசுவோ டகாவைன் இன் அட்வான்ஸ் இன் லித்தியம்-அயன் பேட்டரிகள், வால்டர் ஏ. வான் ஷால்க்விஜ்க் மற்றும் புருனோ ஸ்க்ரோசாட்டி (எடிட்ஸ்), க்ளூவர் அகாடமிக் பப்ளிஷர்ஸ், நியூயார்க், பக். 273, 2002.)
லித்தியம் அயன் பேட்டரி தயாரிப்பதற்கான பாய்வு விளக்கப்படம்

படம் 23. லித்தியம் அயன் செல்கள் உற்பத்திக்கான ஓட்ட விளக்கப்படம்
[Ralph J. Brodd and Kazuo Tagawa in Advances in Lithium-Ion Batteries, Walter A. van Schalkwijk and Bruno Scrosati (Eds.), Kluwer Academic Publishers, New York, pp. 271, 2002.]

கடன்: எலக்ட்ரோபீடியா https: //www.mpoweruk.com/battery_manufacturing.htm
படம் 24. மூலப்பொருட்களிலிருந்து மின்முனைகள் தயாரிப்பதற்கான பாய்வு விளக்கப்படம்
லித்தியம் அயன் செல் அசெம்பிளி




லித்தியம் அயன் பேட்டரி உற்பத்தியாளர்கள் செல்களை இணைக்கும்போது பின்வரும் புள்ளிகளை இலக்காகக் கொள்கின்றனர்:
- லித்தியம் அயன் கலத்திற்கான வடிவமைப்புகள் எலக்ட்ரோடு பகுதி முழுவதும் ஒரே மாதிரியான மின்னோட்ட அடர்த்தியை ஏற்படுத்த வேண்டும்.
- செயலில் உள்ள பொருட்களுக்கும் (AM) தற்போதைய சேகரிப்பாளருக்கும் இடையே நல்ல தொடர்பை உறுதிப்படுத்த
- செல்களுக்கு அதிக விகித செயல்திறனை வழங்க பெரிய பரப்பளவு மின்முனைகள் பயன்படுத்தப்படுகின்றன. இது துருவமுனைப்பைக் குறைக்கிறது, அதாவது மின்முனை எதிர்வினைகளின் இயக்கவியல் காரணமாக மின்னழுத்த இழப்புகள் மற்றும் பிரிப்பான் முழுவதும் மின்னழுத்த வீழ்ச்சியைக் குறைக்கிறது.
துளை அமைப்பு மற்றும் கடத்தும் கார்பன்களின் கலவையானது செயலில் உள்ள பொருளின் நல்ல இடை-துகள் தொடர்பை அளிக்கிறது.
செயலில் உள்ள பொருட்கள், கடத்தும் கார்பன் மற்றும் தற்போதைய சேகரிப்பான் ஆகியவற்றுக்கு இடையே நல்ல தொடர்பு அவசியம், செயலில் உள்ள பொருட்களின் முழு பயன்பாட்டிற்கும் மற்றும் அதிக விகித செயல்திறனின் போது நல்ல செயல்திறனுக்கும்.
கோபால்ட் கேத்தோடு கலவை LiCoO2 (ஒரு கருப்பு தூள்) + PVdF பைண்டர் (ஒரு வெள்ளை அரை-படிக புளோரோபாலிமர் தெர்மோபிளாஸ்டிக்) + N-மெத்தில் பைரோலிடோன் (NMP, நிறமற்ற கரிம திரவம்) ஆகியவற்றிலிருந்து ஒரு கரைப்பானாகத் தயாரிக்கப்படுகிறது. LICoO2 கடத்துத்திறன் இல்லாதது, கடத்தும் நீர்த்துப்போகும், எப்போதும் ஒரு கார்பன் கருப்பு, LiCoO2 இன் கடத்துத்திறனை மேம்படுத்த சேர்க்கப்படுகிறது.
பொருட்களின் விகிதம் மற்றும் அளவுகள் செல் வடிவமைப்பு மற்றும் கலவையின் அளவு ஆகியவற்றால் தீர்மானிக்கப்படுகின்றன. பூச்சு கரைப்பான் மற்றும் பைண்டரைச் சேர்ப்பதற்கு முன் கடத்தாத செயலில் உள்ள பொருள் மற்றும் கார்பனை உலர்த்துவதற்கு ஒரு தீவிர கலவை செயல்முறை பயன்படுத்தப்படுகிறது.
AM மற்றும் தற்போதைய சேகரிப்பான் கட்டம் (அலுமினியப் படலம், 20 மிமீ தடிமன்) இடையே மின் தொடர்பு மேம்படுத்தப்படுவதற்கு, கடத்தும் கார்பனின் மெல்லிய படலத்துடன் செயலில் உள்ள பொருளின் துகள்களின் ஒரு சீரான பூச்சு கொடுக்க கலவை உலர்ந்த கலவையாகும். இதனால் AM இன் முழுப் பயன்பாட்டை உறுதி செய்கிறது. பாலிமர் என்எம்பி ஒரு தனி கொள்கலனில் பூச்சு கரைப்பானில் கரைக்கப்படுகிறது. உலர் கலவை கலவை மற்றும் கரைப்பான் கரைசல் பின்னர் ஒரு குழம்பாக இணைக்கப்படுகிறது.
கரைப்பான் சேர்த்தல் பூச்சு செயல்பாட்டிற்கு குழம்பு (அல்லது பெயிண்ட்) பாகுத்தன்மையை சரிசெய்ய பயன்படுத்தப்படுகிறது . பாலிவினைலென்டிபுளோரைடு (PVdF) தேர்வு மற்றும் பைண்டர் ஆகும் கரைப்பான் N-மெத்தில்பைரோலிடினோன் (NMP) ஆகும். கலவை செயல்பாட்டின் குழம்பு சீல் செய்யப்பட்ட கொள்கலன்களில் வைக்கப்படுகிறது, இது பூச்சு நடவடிக்கைகளுக்கு நீர்த்தேக்கம் மற்றும் பரிமாற்ற ஊடகமாக செயல்படுகிறது. பூச்சு தலைக்குச் செல்லும் திரவத்தில் காற்று நுழைவதைத் தவிர்ப்பதற்காக, கியர் பம்ப் அல்லது அதேபோன்ற துல்லியமான பம்ப் மூலம் சேமிப்புக் கொள்கலனில் இருந்து துல்லியமான அளவு பூச்சு குழம்பு செலுத்தப்படுகிறது.
அனோட் கலவையானது கடினமான கார்பன், PVdF பைண்டர் மற்றும் NMP ஆகியவற்றைக் கொண்டு இதே முறையில் தயாரிக்கப்படுகிறது. இந்த கலவை கட்டமாக பயன்படுத்தப்படும் ஒரு செப்புத் தாளில் பூசப்பட்டுள்ளது (10 மிமீ தடிமன்).
அனோட்கள் மற்றும் கேத்தோட்கள் இரண்டிற்கும் சுமார் 100 மிமீ தடிமன் வரை இருபுறமும் பூச்சு செய்யப்படுகிறது. பூச்சு தடிமனைக் குறைப்பதன் மூலம், கலத்தின் ஒரு திட்டவட்டமான தொகுதிக்கு மொத்த பரப்பளவில் அதிகரிப்பு அடையப்படுகிறது. பயன்படுத்தப்படும் கரிம எலக்ட்ரோலைட்டுகள் நீர்நிலைகளுடன் ஒப்பிடும்போது குறைந்த கடத்துத்திறனைக் கொண்டுள்ளன, எனவே இந்த அதிக பரப்பளவு அதிக சக்தி வெளியேற்ற கலத்திற்கு உதவும்.
மின்முனையின் தடிமன் தேவைப்படும் அதிகபட்ச சக்தியைப் பொறுத்தது. லித்தியம் அயன் பேட்டரி உற்பத்தி தொழில்நுட்பத்தின் ஒரு தனித்துவமான அம்சம் என்னவென்றால் , அதே மின்முனை உற்பத்தி தொழில்நுட்பத்துடன் பலவிதமான ஆற்றல்/ஆற்றல் விகித வடிவமைப்புகளை இது அனுமதிக்கிறது. [புரூஸ்லி, நஸ்ரி பக் 651]. ஆனால் பொருத்தமான தற்போதைய சேகரிப்பு மற்றும் டேப்பிங், செல் வடிவம் மற்றும் வடிவமைப்பு ஆகியவை முக்கியம்.
செல் அசெம்பிளி: பூசப்பட்ட படலம் கரைப்பானை ஆவியாக்க அடுப்பு வழியாக செல்கிறது மற்றும் படலத்தில் ஒரு துல்லியமான அளவு செயலில் உள்ள நிறைவை விட்டுச் செல்கிறது. பல பூச்சு கரைப்பான்கள் அபாயகரமானவை என வகைப்படுத்தப்பட்டு வளிமண்டலத்திற்கு வெளியிட முடியாது. செலவு-சேமிப்பு நடவடிக்கையாக, கரைப்பான் பொதுவாக செயல்பாட்டில் மறுபயன்பாட்டிற்காக மீட்டெடுக்கப்படுகிறது. சுற்றுச்சூழல் மாசுபடுவதைத் தவிர்க்க கரைப்பான் எரிக்கப்படலாம்.
பெரும்பாலான லித்தியம் அயன் செல்கள் உருளை வடிவில் உள்ளன. ப்ரிஸ்மாடிக் செல்களுக்கான தனிமங்களைப் பெற ஜெல்லி ரோல் தட்டையானது .
ப்ரிஸ்மாடிக் செல்கள் சிறந்த தொகுதி நிரப்புதலுக்கு சாதகமானவை, ஆனால் சைக்கிள் ஓட்டுதல் அல்லது வயதாகும்போது வீக்கம் ஏற்படுவதற்கு பொறுப்பாகும். உருளை செல் கேன்கள் சிறந்த இயந்திர வலிமை, நல்ல பரிமாண நிலைத்தன்மை மற்றும் தனிமங்களில் சீரான அழுத்தத்தை வழங்குகின்றன.
பூச்சு செயல்பாடு சுருளின் நீளத்துடன் பொருந்தக்கூடிய குறுக்கீடு பூச்சுகளை உருவாக்குகிறது. முறுக்கு இயந்திரங்கள் கேத்தோட்கள் மற்றும் அனோட்கள் மற்றும் பிரிப்பான் (25 மிமீ அல்லது குறைவான தடிமன், பிபி அல்லது பிஇ அல்லது கலப்பு) ஆகியவற்றின் உலர்ந்த ஜம்போ ரோல்களுடன் பயன்படுத்த தானாகவே செயல்படும் வகையில் வடிவமைக்கப்பட்டுள்ளன.
படலங்களின் பூசப்படாத பிரிவில் தாவல்களை வெல்டிங் செய்வதன் மூலம் செயல்பாடுகள் தொடங்குகின்றன. முறுக்கு இயந்திரம் பின்னர் சரியான நீளத்திற்கு துண்டுகளை வெட்டி, ஜெல்லிரோல் பாணியில் ஒரு இறுக்கமான சுருள் அல்லது பாபினில் கலவையான அனோட்-பிரிப்பான்-கேத்தோடை வீசுகிறது. காயத்தின் மையத்தின் விட்டம் அதிகரிக்கும் போது, சுருளின் விட்டத்தில் நெருங்கிய சகிப்புத்தன்மைக்கு விட்டம் அதிகரிக்கும் போது முறுக்கு இயந்திரம் நிலையான பதற்றத்தை பராமரிக்க தானாகவே ஈடுசெய்கிறது. பிரிஸ்மாடிக் செல்களுக்கான நீள்வட்ட காற்று மிகவும் சிக்கலான மற்றும் மெதுவான செயல்முறையாகும்.
முறுக்கு பிறகு, கேனில் செருகப்படுவதற்கு முன், சுருள் உள் ஷார்ட்களுக்காக சரிபார்க்கப்படுகிறது. எஃகு கேன்கள் சுத்தமாகவும், நிக்கல் பூசப்பட்டதாகவும் இருக்க வேண்டும், இதனால் அவை நிலையான மேற்பரப்பை வழங்குகின்றன மற்றும் செல் அசெம்பிளிக்கு முன் அரிப்பைக் குறைக்கும். அனோட் ஈயம் கேனின் அடிப்பகுதியில் பற்றவைக்கப்படுகிறது மற்றும் கேத்தோடு ஈயம் பாதுகாப்பு வென்ட்டில் பற்றவைக்கப்படுகிறது. அரை-அசெம்பிள் கலத்தில் எலக்ட்ரோலைட் சேர்க்கப்படுகிறது. மேல் அட்டையின் crimping மூலம் சட்டசபை முடிந்தது.
சாத்தியமான செல் தவறுகளை முன்கூட்டியே நிராகரிப்பது ஒரு பொருளாதார நடவடிக்கையாகும் மற்றும் கெட்ட செல்கள் மீது அதிக வேலை செய்வதைத் தடுக்கிறது. பாபின் கேனில் செருகப்படுகிறது, இதனால் கேன் தனிமத்தின் கூறுகளை நெருக்கமாக வைத்திருக்க நிலையான அழுத்தத்தை வழங்குகிறது, இதனால் அவற்றுக்கிடையே வெற்றிடங்களுக்கான எந்த வாய்ப்பையும் நீக்குகிறது. சில உற்பத்தியாளர்கள் சுருளின் மையத்தை நிலைப்படுத்த ஒரு மேண்டலைச் செருகலாம்.
அனைத்து செயல்பாடுகளும் உலர்ந்த அறை அல்லது உலர்ந்த பெட்டியில் மேற்கொள்ளப்படாவிட்டால், எலக்ட்ரோலைட் நிரப்புதல் செயல்முறைக்கு முன், செயலில் உள்ள பொருட்களில் உள்ள உறிஞ்சப்பட்ட நீர் வெப்பம் மற்றும் வெற்றிடத்தால் அகற்றப்பட வேண்டும்.
எலக்ட்ரோலைட்டின் துல்லியமான வெற்றிட நிரப்புதல், எலக்ட்ரோலைட் ஊடுருவி மற்றும் பிரிப்பான் மற்றும் எலக்ட்ரோடு கட்டமைப்புகளில் கிடைக்கும் போரோசிட்டியை முழுமையாக நிரப்புவதை உறுதி செய்வதற்காக செய்யப்படுகிறது. துல்லியமான பம்புகள் நல்ல செல் செயல்பாட்டிற்குத் தேவையான எலக்ட்ரோலைட்டின் கணக்கிடப்பட்ட அளவை அளவிடுகின்றன. எப்போதும் அனைத்து உற்பத்தியாளர்களும் LiPF 6 (ஒரு கனிம வெள்ளை படிக கலவை) எலக்ட்ரோலைட் மற்றும் சுழற்சி (EC, எத்திலீன் கார்பனேட்) அல்லது நேரியல் கார்பனேட்டுகள் (DMC, டைமிதில் கார்பனேட், DEC, டைதைல் கார்பனேட், அல்லது EMC, எத்தில்-மெத்தில் கார்பனேட் போன்றவை) பயன்படுத்துகின்றனர். இந்த எலக்ட்ரோலைட் உப்புக்கான கரைப்பான்கள்.
டைமெத்தில் கார்பனேட் (DMC) மற்றும்/அல்லது டைதில் கார்பனேட் (DEC) உடன் எத்திலீன் கார்பனேட் (EC) கரைப்பான் கலவையை அடிப்படையாகக் கொண்ட எலக்ட்ரோலைட்டுகள் பொதுவாக லித்தியம் அயன் பேட்டரிகளுக்கு “4 V” கத்தோட்களுடன் (கோபால்டேட், நிக்கலேட் மற்றும் மாங்கனேட்) இணைந்து பயன்படுத்தப்படுகின்றன. கரைப்பான்களின் உயர் ஆக்சிஜனேற்ற திறன்.
கலத்தை எலக்ட்ரோலைட்டுடன் நிரப்பிய பிறகு, செல் கேனுக்கும் மேல் தட்டுக்கும் இடையில் வைக்கப்பட்டுள்ள பாலிமர் கேஸ்கெட் அல்லது குரோமெட்டின் கட்டுப்படுத்தப்பட்ட சுருக்கத்தால் செல் சீல் செய்யப்படுகிறது. பாலிமர் கேஸ்கெட் முத்திரையின் அழுத்தம் பாலிமரின் மீள் வரம்பிற்குள் வைத்திருக்க கட்டுப்படுத்தப்படுகிறது. மீள் வரம்புகள் மீறப்பட்டால், பாலிமர் குளிர் பாய்கிறது மற்றும் முத்திரையை சமரசம் செய்கிறது.
ஒவ்வொரு உற்பத்தியாளரும் செல்களை மூடுவதற்கு சற்றே வித்தியாசமான இயந்திரக் கட்டுமானத்தைப் பயன்படுத்துகின்றனர், ஆனால் இறுதி முடிவுகள் அடிப்படையில் ஒரே மாதிரியானவை. பொதுவாக, கலத்தின் மேற்பகுதிக்கு அருகில் தோள்பட்டை அல்லது விளிம்பு உருவாகிறது. இது முத்திரைக்கான அடிப்படையாகவும், ஜெல்லிரோலை இடத்தில் வைத்திருக்கவும் மற்றும் அதிர்வு மற்றும் அதிர்ச்சியின் செல்வாக்கின் கீழ் காயம் பாபினின் தொலைநோக்கி அல்லது நிலையை மாற்றுவதைத் தடுக்கவும் உதவுகிறது.
நிலையின் எந்த மாற்றமும் தற்போதைய விநியோகத்தில் மாற்றத்தை ஏற்படுத்துகிறது மற்றும் மோசமான சுழற்சி வாழ்க்கை அல்லது உயர் செயல்திறன் கலங்களில் லித்தியம் முலாம் பூசுகிறது. செல் மேல் தட்டு முத்திரை ஒரு வென்ட், ஒரு நேர்மறை வெப்பநிலை குணகம் உறுப்பு (PTC) மற்றும் தற்போதைய குறுக்கீடு (CID) பாதுகாப்பு சாதனங்களைக் கொண்டுள்ளது. CID மற்றும் PTC ஆகிய இரண்டும் பாதுகாப்பு சாதனங்களாகும் மேல் அசெம்பிளியில் இணைப்பதற்கு முன், ஒவ்வொரு சாதனங்களும் சரியான செயல்பாட்டிற்காக சரிபார்க்கப்படுகின்றன.
முத்திரையைப் பயன்படுத்திய பிறகு, செல்களைக் கழுவி, ஜாக்கெட் மற்றும் லேபிளிடலாம். உற்பத்தி நாள் மற்றும் அனைத்து செல் கூறுகளையும் (எலக்ட்ரோட் பொருட்கள், எலக்ட்ரோலைட், பிரிப்பான் மற்றும் போன்றவை) அடையாளம் காண அவர்களுக்கு ஒரு வரிசை எண் வழங்கப்படுகிறது. திறன் மற்றும் மின்னழுத்தம் பற்றிய தகவல்கள் செல் எண்ணுடன் சேமிக்கப்பட்டு, பேக் அசெம்பிளிக்கான கலங்களை பொருத்த பின்னர் பயன்படுத்தப்படும்.
நீண்ட கால ஹெர்மீடிக் முத்திரைகளை வழங்க, செல்களை கண்ணாடி முதல் உலோக முத்திரைகள் வரை லேசர் வெல்டிங் செய்யலாம். பெரிய செல்கள் மூலம், துஷ்பிரயோக நிலைமைகளின் கீழ் கூட, பாதுகாப்பான செயல்பாட்டை உறுதிப்படுத்த அதிக கவனம் செலுத்தப்பட வேண்டும்.
மேலே உள்ள செயல்முறைகள், கையடக்க மின்னணுவியலில் பயன்படுத்தப்படும் சிறிய சீல் செய்யப்பட்ட செல்களுக்குச் சித்தரிக்கப்பட்டுள்ள நிலையில், ஆற்றல் சேமிப்பு, விண்வெளி மற்றும் EV பயன்பாடுகளுக்கான பெரிய தொழில்துறை பேட்டரிகளுக்கான செயல்முறை அதே பொதுவான அவுட்லைனைப் பின்பற்றுகிறது.
லித்தியம் அயன் பேட்டரி - உருவாக்கம் மற்றும் வயதானது
அசெம்பிள் செய்யப்பட்டதால், லி அயனிகள் அனோட் கார்பனுக்குள் செலுத்தப்படுவதில்லை, அதனால் செல் மின்னழுத்தத்தைக் காட்டாது. ஆரம்ப சார்ஜிங்கின் போது, PAM LiCoO 2 இலிருந்து Li அயனிகளின் ஒரு பகுதி Li 1-x CoO 2 ஆக மாற்றப்படாது, மேலும் இந்த லித்தியம் அயனிகள் கார்பன் அனோடில் (C y ) டோப் செய்யப்பட்டு Li x C y ஆக மாறுகிறது. சார்ஜிங் மின்னழுத்தம் 4.1 முதல் 4.2 V வரை அடையும் போது, x இன் மதிப்பு சுமார் 0.5 ஆகும். (அதாவது, 50 %) LiCoO 2 இலிருந்து 50 % Li பயன்படுத்தப்பட்டதைக் குறிக்கிறது.
கவனிக்க வேண்டிய மற்றொரு அம்சம் என்னவென்றால், டோப் செய்யப்பட்ட லித்தியம் அயனிகளின் ஒரு பகுதி திரும்பாது மற்றும் அனோடில் இருக்கும். இதில், x-dx லித்தியம் அயனிகள் திறனில் பங்களிக்காமல் இருக்கும். இது 10 முதல் 20% மீளமுடியாத லித்தியம் ஆகும், அதாவது ஆரம்ப கட்டணத்தின் செயல்திறன் 80 முதல் 90% ஆகும். இரண்டாவது சுழற்சியில் இருந்து, மீளமுடியாத அளவு அதிகரிக்காது மற்றும் செல் உற்பத்தியாளரால் வடிவமைக்கப்பட்ட 100% திறனைக் காட்டுகிறது.
கழுவுதல் மற்றும் ஜாக்கெட் செய்த பிறகு, ஆனால் உருவாக்கம் செயல்முறை தொடங்கும் முன், அனைத்து செல்களின் மின்னழுத்தம் மற்றும் மின்மறுப்பு ஏதேனும் குறைபாடுள்ள செல்களை வரிசைப்படுத்த பதிவு செய்யப்படுகிறது. பின்னர் செல்கள் முதல் முறையாக சார்ஜ் செய்யப்படுகின்றன
(ஆரம்ப சார்ஜிங் அல்லது உருவாக்கம் சார்ஜிங்). முதல் கட்டணத்தின் நிபந்தனைகள் குறைந்தது இரண்டு காரணங்களுக்காக முக்கியமானவை:
1) திட எலக்ட்ரோலைட் இடைநிலை (SEI) அடுக்கு சாதாரண செல் செயல்பாட்டின் போது எலக்ட்ரோலைட்டுடன் தன்னிச்சையாக வினைபுரிவதிலிருந்து பாதுகாக்க அனோடில் உருவாகிறது , மேலும் 2) இது செயலில் உள்ள பொருட்களுக்கும் எலக்ட்ரோலைட்டுக்கும் இடையே நல்ல மின் தொடர்பை ஏற்படுத்துகிறது. முதல் கட்டணம் செல்களை சார்ஜ் செய்வதற்கான உற்பத்தியாளரின் பரிந்துரைக்கப்பட்ட நடைமுறையைப் பின்பற்றுகிறது, ஆனால் பெரும்பாலும் குறைந்த மின்னோட்டத்தில் தொடங்குகிறது, பின்னர் சார்ஜ் காலத்தின் மூன்றில் ஒரு பங்கு சாதாரண சார்ஜிங் மின்னோட்டத்திற்கு அதிகரிக்கிறது. மின்னழுத்த வரம்புகளுக்குள் மின்னழுத்த வரம்புகளுக்குள் செல்கள் சுழற்சியைத் தொடரலாம் மற்றும் உருவான பிறகு ஒன்று அல்லது இரண்டு சுழற்சிகளுக்கு வெளியேற்றலாம்.
உருவாக்கம் அல்லது சைக்கிள் ஓட்டுதலுக்குப் பிறகு, செல் மின்னழுத்தம் மற்றும் திறன் ஆகியவை செல் தேர்வு செயல்பாட்டில் பின்னர் பயன்படுத்துவதற்காக அளவிடப்பட்டு சேமிக்கப்படும். உற்பத்தியாளரைப் பொறுத்து வயதான காலம் இரண்டு வாரங்கள் முதல் ஒரு மாதம் வரை மாறுபடும். கலங்களின் மின்னழுத்தம் சேமிப்பிற்குப் பிறகு மீண்டும் அளவிடப்படுகிறது. சேமிப்பக காலத்தின் தொடக்கத்திலும் முடிவிலும் உள்ள மின்னழுத்தத்தில் உள்ள வேறுபாடுகள், “மென்மையான-” அல்லது “மைக்ரோ-” குறும்படங்களுடன் செல்களை வரிசைப்படுத்தப் பயன்படுகிறது. உள் குறும்படங்களைக் கொண்ட செல்கள் சேமிப்பிற்குப் பிறகு குறைந்த மின்னழுத்தத்தைக் கொண்டிருக்கும் மற்றும் சாதாரண மின்னழுத்தம் மற்றும் திறன் விநியோகத்திலிருந்து தங்களைப் பிரித்துக் கொள்ளும். உருவான வாயுக்களை அகற்ற, உருவான பிறகு பெரிய செல்களை வெளியேற்றுவது அவசியமாக இருக்கலாம்.
சட்டசபை செயல்முறையின் விரிவான விளக்கத்திற்கு, வாசகர்கள் குறிப்பிடப்படுகிறார்கள்
- கௌரு நகாஜிமா மற்றும் யோஷியோ நிஷி அத்தியாயம் 5 இல்: எலக்ட்ரானிக்ஸிற்கான ஆற்றல் சேமிப்பு அமைப்புகள், எட் டெட்சுயா ஒசாகா மற்றும் மாதவ் தத்தா, கார்டன் மற்றும் ரீச் சயின்ஸ் பப்ளிஷர்ஸ், ஆம்ஸ்டர்டாம், 2000.
- லித்தியம்-அயன் செல் உற்பத்தி செயல்முறைகள், ரால்ப் ஜே. பிராட் மற்றும் கசுவோ டகாவா, அத்தியாயம் 9 இல்: லித்தியம்-அயன் பேட்டரிகளில் முன்னேற்றங்கள், வால்டர் ஏ. வான் ஷால்க்விஜ்க் மற்றும் புருனோ ஸ்க்ரோசட்டி (எடிட்ஸ்), க்ளூவர் அகாடமிக் பப்ளிஷர்ஸ், நியூயார்க், 2023, pp. .
- லித்தியம் பேட்டரிகள், அறிவியல் மற்றும் தொழில்நுட்பம், பதிப்பு. ஜி.ஏ. நஸ்ரி மற்றும் ஜி. பிஸ்டோயா, ஸ்பிரிங்கர், நியூயார்க், 2009.
- Lithium-Ion Batteries, Reiner Korthauer (ed) (2018), Michael Wuest et.al., Springer, 2018 மொழிபெயர்த்தது.
- Kazuo Tagawa மற்றும் Ralph J. Brodd, Lithium-Ion Batteries இல் Lithium-Ion Batteries தயாரிப்பதற்கான உற்பத்தி செயல்முறைகள், Yoshio M., Brodd RJ, Kozawa A. (eds) Springer, New York, NY. https: //doi.org/10.1007/978-0-387-34445-4_8]
- ஜாங் இசட்., ராமதாஸ் பி. (2012) லித்தியம்-அயன் பேட்டரி அமைப்புகள் மற்றும் தொழில்நுட்பம். இல்: மேயர்ஸ் RA (ed) என்சைக்ளோபீடியா ஆஃப் சஸ்டைனபிலிட்டி சயின்ஸ் அண்ட் டெக்னாலஜி. ஸ்பிரிங்கர், நியூயார்க். https: //doi.org/10.1007/978-1-4419-0851-3_663
- லித்தியம்-அயன் பேட்டரி பேக் வடிவமைப்பு வேதியியல், கூறுகள், வகைகள் மற்றும் சொற்களஞ்சியத்தின் கையேடு, ஜான் வார்னர், எல்சேவியர், 2018




