Cách thức hoạt động của pin Lithium ion
Công chúng cho rằng ắc quy axit chì là công nghệ cũ. Pin Lithium ion có một nhận thức khác, nó hiện đại hơn, sạch hơn, có mật độ năng lượng gấp 3 hoặc 4 lần và tuổi thọ chu kỳ dài hơn. Với tất cả những điều này, công nghệ axit chì 150 năm tuổi có thể mang lại những lợi thế nào? Thực ra, tất cả không phải như nó có vẻ, hãy nhìn vào các tiêu đề về dữ liệu được sử dụng trong các tuyên bố tiếp thị, sau đó áp dụng một chút kiến thức thông thường, nghiên cứu cơ bản và một số khoa học thô sơ. Bạn sẽ thấy rằng câu chuyện thực sự là khá khác nhau.
Quan niệm sai lầm đầu tiên liên quan đến mật độ thể tích và năng lượng cụ thể. Các giá trị tiêu đề từ 4 đến 5 lần chỉ liên quan đến mật độ năng lượng cụ thể và một số hạn chế của pin lithium ion, một số trong số đó vẫn chưa được sử dụng cho mục đích thương mại. Quả sung. 2 so sánh một số cực âm cho các tế bào pin lithium ion, chúng dao động từ khoảng 100Wh / kg đối với hóa học Li-FePO4 an toàn nhất đến hơn 200Wh / kg đối với biến thể niken-coban-nhôm oxit. Sơ đồ pin axit chì được cho dưới đây:


Các giá trị này chỉ áp dụng cho mức ô đơn, không áp dụng cho gói hoặc điều kiện trong dịch vụ. Quả sung. 3 cho thấy mật độ năng lượng của các hóa chất pin khác nhau ở cấp độ tế bào và hệ thống. Mật độ năng lượng của các tế bào pin lithium ion thực tế giảm đi một nửa khi được lắp đặt hoàn chỉnh với tất cả các kết nối, thiết bị làm mát, an toàn và quản lý pin.
Lợi thế cấp độ tế bào của 3 đến 5 lần mật độ năng lượng cụ thể được giảm xuống còn 2 đến 3 lần. Phụ thuộc vào hóa học catốt của lithium, chúng ta gần như có thể xem xét sự tương đương giữa pin lithium ion và mật độ năng lượng của pin axit chì cho một hệ thống pin được lắp đặt hoàn chỉnh trong một số ứng dụng.
Yếu tố khác, đó là vòng đời, cũng là một nguồn gây nhầm lẫn. Pin lithium ion có thể thực hiện bao nhiêu chu kỳ trước khi dung lượng giảm xuống dưới 80% mức xếp hạng trên bảng tên của nó? Hai, ba nghìn? Bảng 1 đưa ra tóm tắt về các vật liệu làm catốt Li-ion khác nhau về hiệu suất và vòng đời của chu trình.
Ưu điểm của hóa học pin axit chì
Pin là thiết bị kỳ lạ. Không ai muốn chúng, nhưng mọi người cần chúng. Chúng chỉ được mua khi có nhu cầu. Có bao nhiêu người lên kế hoạch cho một chuyến đi đến trung tâm mua sắm địa phương để mua pin? Chúng là một kiểu mua thù dai và chỉ được mua khi thực sự cần thiết. Một người bán hàng giỏi có thể bán cho bạn hai đôi giày, hai chiếc ô tô và có thể là hai căn nhà nếu bạn có tiền, nhưng anh ta không thể bán cho bạn hai chiếc pin ô tô SLI. Khi bạn mua pin, cho dù pin năng lượng mặt trời cho bảng điều khiển năng lượng mặt trời, cho xe đạp điện hay UPS và hệ thống dự phòng acquy biến tần hay pin kéo cho xe nâng , bạn có muốn biết thêm về nó không?
Pin axit chì hoạt động như thế nào, sự khác biệt giữa các loại và mẫu mã, và các hóa chất khác nhau như thế nào? Chúng có thể đắt tiền. Trong một ứng dụng thương mại hoặc trong nước, hoàn vốn là bao nhiêu, tuổi thọ và chi phí thay thế pin axit chì là bao nhiêu? Kích thước bạn cần, không gian có sẵn, hiệu suất năng lượng của pin axit chì và thời gian sạc lại? Và sau đó, có những chi phí tiềm ẩn về an toàn, thải bỏ và lượng khí thải carbon. Bài báo này so sánh pin axit chì với pin lithium ion và giải quyết nhiều quan niệm sai lầm liên quan đến cả hai loại hóa học này.
Pin lithium ion nào tốt nhất
| Vật liệu catốt | Tên ngắn | Định mức điện áp | Năng lượng riêng Wh / kg (ô) | Chu kỳ cuộc sống | Bình luận |
|---|---|---|---|---|---|
|
Oxit Lithium Coban (LiCoO2) |
LCO | 3.6 | 150-200 | 500-1000 | Thiết bị di động - thoát nhiệt khi sạc quá mức |
| Lithi Mangan Oxit (LiMn2O4) | LMO | 3.7 | 100-150 | 300-700 | Dụng cụ điện, thiết bị y tế - an toàn hơn LCO |
| Lithium Nickel Mangan Coban Oxit (LiNiMnCO2) | NMC | 3.6/3.7 | 150-220 | 1000-2000 | Xe đạp điện, EV, công nghiệp - vòng đời cao |
| Lithium Sắt Phosphate (LiFePO4) | LFP | 3.2 | 90-120 | 1000-2000 | EV, SLI, Leisure - an toàn nhất trong tất cả các hóa chất pin lithium ion |
| Oxit nhôm Lithium Niken Coban (LiNiCoAlO2) | NCA | 3.6 | 200-260 | 500 | Công nghiệp, hệ thống truyền động EV (Tesla) TR ở 150C, CL 500 |
| Lithium Titanate (Li4Ti5O12) | LTO | 2.4 | 50-80 | Bộ lưu điện, năng lượng mặt trời, hệ thống truyền lực EV (Honda, Mitsubishi). CL 3000-7000 - rất an toàn |
Có thể thấy, tất cả đều nằm trong khoảng chu kỳ 800 đến 2000. Trong khi đó, pin axit chì được thiết kế tốt có thể dễ dàng đạt được hơn 1600 chu kỳ đến 80% DOD. Vì vậy, làm thế nào để tất cả những điều này cộng lại khi xem xét chi phí sở hữu? Điều này đưa chúng ta đến điểm tiếp theo là giá pin axit-chì. Giá của pin lithium-ion so với pin axít chì là bao nhiêu? Chi phí nhà máy sản xuất pin Lithium-ion? Đương nhiên, pin lithium ion đắt hơn nhưng nhiều hơn bao nhiêu. Một lần nữa, điều này phụ thuộc vào mức độ đang được xem xét. Các thông cáo báo chí sẽ cho chúng ta biết rằng giá Li-ion đang giảm và hiện đang trong khoảng 2-3 lần so với axit chì.
Có thật không? Giá trung bình trên một tìm kiếm trên internet gần đây của Vương quốc Anh để biết giá của các loại pin giải trí 12V và 100 Ah được bán trên thị trường cho cả pin lithium ion và pin axit chì:
pin lithium ion $ 960 hoặc $ 800 / kwh
Pin axit chì $ 215 hoặc $ 180 / kwh
Rõ ràng, tuổi thọ của pin lithium ion phải gấp 4 lần tuổi thọ của pin axit chì tương đương để có cùng giá trị. Như chúng ta đã thấy, đây không phải là trường hợp.


Trong mọi trường hợp, cấu tạo pin axit-chì tiết kiệm chi phí nhất ngay cả khi lắp pin axit-chì lớn hơn để có khả năng chấp nhận sạc tốt hơn và tuổi thọ chu kỳ dài hơn. Trong ví dụ này, ứng dụng là một tháp viễn thông ở Ấn Độ. Nguyên tắc tương tự cũng đúng trong hầu hết các ứng dụng và khu vực địa lý, hơn thế nữa ở những vùng khí hậu lạnh hơn. Quan niệm sai lầm khác cho rằng Li-ion là một công nghệ sạch hơn và ít gây ô nhiễm hơn axit-chì. Cơ sở dẫn đến sự phát thải ở cổng cho các chất hóa học pin khác nhau được đưa ra trong Hình. 5 và 6.
Hình này cho thấy ranh giới của các hoạt động sản xuất pin. Từ việc khai thác và vận chuyển nguyên liệu thô phải trải qua tất cả các bước xử lý cho đến khi pin sẵn sàng xuất xưởng.
Bảng 2 là một tình huống thực tế so sánh tính kinh tế của việc sử dụng pin lithium ion và pin axit chì hoạt động trong các khoảng thời gian sử dụng khác nhau.
| Mục chi phí | Phí vận hành hàng ngày USD | Phí vận hành hàng ngày USD |
|---|---|---|
| 3 năm | Ắc quy | Pin Lithium ion |
| Khấu hao | 8.30 | 16.90 |
| Diesel (đã giao) | 15.50 | 15.50 |
| Bảo dưỡng | 2.46 | 2.46 |
| Điện lực | 1.47 | 1.47 |
| Sạc pin | 0.65 | 0.50 |
| Tổng ngày / tháng | 28.38/851 | 36.83/1105 |
| 6 năm | ||
| Khấu hao | 5.86 | 8.46 |
| Dầu diesel | 15.50 | 15.50 |
| Bảo dưỡng | 2.46 | 2.46 |
| Điện lực | 1.47 | 1.47 |
| Sạc pin | 0.54 | 0.50 |
| Tổng ngày / tháng | 25.83/775 | 28.39/852 |
Dữ liệu này từ Phòng thí nghiệm Quốc gia Argonne, cho thấy tổng quy trình sản xuất bao gồm khai thác và vận chuyển nguyên liệu thô cho pin lithium ion gấp hơn 4 lần giá trị axit chì. Về việc khai thác nguyên liệu, nguồn cung cấp nguyên liệu catốt cơ bản như coban và mangan và liti không hoàn toàn chắc chắn. Các quy trình khai thác và phục hồi vẫn tồn tại nhưng số lượng mỏ và địa điểm sản xuất có thể hạn chế nguồn cung nếu nhu cầu tăng lên đáng kể. Bản đồ địa chính trị cũng dự đoán sự không chắc chắn đối với một số nguồn tài liệu này.
Pin lithium ion có thể tái chế được không
Khả năng tái chế và độ an toàn của các chất hóa học này là những yếu tố quan trọng. Được biết, hầu hết tất cả các thành phần trong pin axit chì đều được tái chế 100% trong khi không có quy trình thương mại nào để tái chế pin lithium ion. Tình huống này là dễ hiểu khi bạn cho rằng các thành phần đắt tiền hơn của Li, Co, Mn, v.v. chỉ là một phần nhỏ trong tổng số pin lithium ion. Ví dụ, Lithium chiếm khoảng 4% tổng trọng lượng tế bào. Thêm vào đó là sự thật hiển nhiên rằng Lithium có tính phản ứng cao (cơ sở của mật độ năng lượng cao), điều này có thể hiểu là khiến việc chiết xuất từ chất thải trở nên đắt đỏ.
Yếu tố phức tạp cộng thêm với nhiều vật liệu khác nhau trong xây dựng của nó làm cho việc tái chế trở nên khó khăn, cả về mặt kỹ thuật và kinh tế. Kết quả? Đơn giản là không có động cơ thương mại để tái chế những viên pin này. Vì lý do này, các cơ sở tái chế vẫn đang ở giai đoạn thí điểm và chủ yếu do chính phủ tài trợ.
Hiện tại, phần lớn pin lithium ion phế thải được dự trữ để chờ một bước đột phá về công nghệ hoặc luật pháp buộc chúng phải tái chế. Nếu cái thứ hai được thực hiện thì sẽ có một chi phí, cuối cùng là cho người tiêu dùng. Điều này sẽ làm tăng giá của pin Li-ion hơn nữa so với các loại pin axit chì.
Pin lithium ion có thể phát nổ
Cuối cùng, chúng tôi có được sự an toàn. Theo hiểu biết của chúng tôi, không có ứng dụng pin axit chì nào bị thu hồi an toàn như chúng tôi biết như trường hợp pin Li-ion trong các thiết bị điện tử cầm tay và thậm chí cả xe điện. Quả sung. 7 cho thấy những gì đã xảy ra với một chiếc Volvo hybrid mới ở Anh chỉ vài tuần trước, tại thời điểm viết bài này. Trong trường hợp này, pin lithium ion của nó bốc cháy khi đang sạc.
Pin Lithium-ion cháy
Hình 7 Cháy do pin Li-ion trong xe điện hybrid Volvo: Tháng 4 năm 2018-Cư trú tại Vương quốc Anh


Video này cho thấy một vụ cháy gần đây do pin lithium gây ra. Có thể do sự mất cân bằng trong tế bào và BMS không phù hợp.
Ngay cả khi được cất giữ hoặc vận chuyển, pin lithium ion đã là nguyên nhân gây ra các vụ hỏa hoạn nguy hiểm nghiêm trọng. Mặc dù những trường hợp này hiếm khi xảy ra, nhưng chúng phải được thừa nhận và phải cài đặt thiết bị an toàn phù hợp và phần mềm quản lý pin. Ví dụ, cơ quan cứu hỏa New York vẫn đang trong quá trình quyết định cách giải quyết các vụ cháy pin lithium ion. Điều này thực sự gợi ý rằng các biện pháp an toàn hiện có đối với pin lithium ion trên toàn thế giới cần phải được xem xét lại.
Sau đây là quan điểm từ Sở Cứu hỏa New York:
Trích dẫn bài báo: Ổ đĩa tiện ích AWS ngày 15 tháng 11 năm 2016 “Cháy không phải là vấn đề lớn nhất,” Rogers nói. Nhân viên cứu hỏa được đào tạo để đối phó với hỏa hoạn, nhưng họ cần biết những gì họ đang đối phó. Pin Li-ion có thể giải phóng axit độc hại và hơi dễ cháy. Một số hơi trong số đó được tiêu thụ bởi ngọn lửa, nhưng nếu không, chúng có thể bốc cháy hoặc gây khó khăn cho nhân viên cứu hỏa. Vấn đề lớn nhất là những gì xảy ra “hậu vận”, tức là sau khi đám cháy được dập tắt. Rogers cho biết, ngay cả khi pin bị tắt, nó có thể hoạt động trở lại trong tối đa 72 giờ. -T. Sở cứu hỏa Paul Rogers thuộc bộ phận hoạt động vật liệu nguy hiểm của New York ”
Pin Lithium ion hay Pin axit chì?
Pin Lithium ion chắc chắn có đặc điểm hiệu suất tốt hơn axit chì. Tuy nhiên, những ưu điểm này bị giảm sút nghiêm trọng do phần cứng bổ sung đi kèm với các yêu cầu quản lý và an toàn. Kết quả thực tế là pin axit chì có những ưu điểm khác biệt, đặc biệt khi xem xét các ứng dụng không bị giới hạn bởi trọng lượng hoặc việc chấp nhận phí. Chi phí ban đầu thấp hơn chi phí nhà máy sản xuất ắc quy axit chì; Giá thu mua thấp và chi phí khấu hao thấp của axit chì kết hợp với tác động môi trường thấp và tính an toàn vốn có của nó, mang lại những lợi thế sau:
- Giá mua thấp hơn. Giá khoảng 1/4 của Li-ion tương đương. Chi phí vận hành thấp hơn để cung cấp tổng chi phí sở hữu thấp hơn trong phần lớn các ứng dụng.
- Khả năng tái chế. Gần như 100% nguyên liệu ắc quy axit chì đều được tái chế. Giá trị phế liệu có thể mang lại doanh thu bổ sung lên đến 20% chi phí nguyên liệu pin. Pin Lithium không có cơ sở hạ tầng hoặc quy trình thương mại để tái chế
- Sự an toàn. Tính chất hóa học của axit chì vốn đã an toàn hơn so với hóa học của pin lithium ion
- Sự bền vững. Có nhiều nguồn cung cấp axit chì được thiết lập tốt, đặc biệt là từ các cơ sở tái chế. Lithium và các vật liệu catốt khác có thể được cung cấp từ các khu vực nhạy cảm về chính trị. Cả năng lực khai thác và sản xuất vật liệu toàn cầu hiện tại sẽ không hỗ trợ sự gia tăng nhanh chóng trong sản xuất pin Lithium ion.
- Khí thải carbon. Sản xuất pin axít chì có tác dụng thúc đẩy lượng khí thải carbon bằng một phần ba so với pin lithium ion.
Một bức tranh khác với bức tranh do các công ty sản xuất pin lithium ion vẽ. Mặc dù không thể lập luận rằng axit chì có nhược điểm về mật độ năng lượng, nhưng thực tế là pin axit chì vẫn là một loại pin an toàn, có tính cạnh tranh cao và là sự lựa chọn tốt nhất của công nghệ pin trong nhiều ứng dụng.
Pin lithium ion là gì
Vật liệu cực âm và cực dương: Mặc dù các tế bào niken-kim loại hyđrua (Ni-MH) ban đầu được ưa chuộng vào những năm 1990, nhưng sản phẩm pin sạc lithium ion thương mại đầu tiên trên thế giới đã được Sony Corporation phát hành vào năm 1991. Ngoài hàm lượng năng lượng cao, cả về khối lượng và thể tích, loại pin này cũng cung cấp các đặc tính nhiệt độ thấp, đặc tính tải và đặc tính chu kỳ tuyệt vời. Do đó, nó nhanh chóng chiếm lĩnh thị trường và trở thành nguồn cung cấp năng lượng không thể thiếu cho các thiết bị âm thanh và hình ảnh, máy tính cá nhân, điện thoại di động và các thiết bị di động khác.
Công nghệ pin tiên tiến ngày nay bắt đầu với việc khám phá ra độ dẫn ion cao của pha rắn NaAl 11 O 17 , được gọi là natri β-alumina, bởi Kummer và các đồng nghiệp tại phòng thí nghiệm Ford Motor Co. [1. Olof Ramsrtomström, về giải Nobel Hóa học, Cơ sở khoa học về giải Nobel Hóa học 2019; 2. YFY Yao và JT Kummer, J. Inorg. Nucl. Chèm. 29, 2453 (1967)].
Điều này dẫn đến nhận thức rằng vận chuyển ion trong chất rắn thực sự có thể rất nhanh và nó có thể dẫn đến nhiều loại công nghệ mới. Ngay sau đó, các nhà nghiên cứu tại Ford đã chỉ ra rằng người ta có thể sử dụng chất điện phân rắn có độ dẫn điện cao để sản xuất một loại pin hoàn toàn mới, sử dụng natri nóng chảy ở điện cực âm và dung dịch natri nóng chảy trong lưu huỳnh làm điện cực dương, với chất dẫn natri chất rắn điện li ở giữa [N. Weber và JT Kummer, Proc. Nguồn điện hàng năm Conf. 21, 37 (năm 1967)].
Như dự kiến, người ta đã sớm xem xét khả năng của các hệ thống lithium tương tự, vì người ta nhận ra rằng một tế bào lithium tương đương khác sẽ tạo ra điện áp cao hơn một tế bào natri. Ngoài ra, lithium có trọng lượng thấp hơn natri, một lợi thế khác.
Không thể sử dụng liti nguyên tố vì nhiệt độ nóng chảy thấp. Thay vào đó, các hợp kim lithium rắn, chủ yếu là hệ Li / Si và Li / Al, đã được nghiên cứu [ RA Huggins, J. Power Sources 81–82, 13 (1999)].
Vào thời điểm đó, một số vật liệu đã được nghiên cứu như là chất phản ứng điện cực dương, trong đó phần lớn chú ý đến việc sử dụng FeS hoặc FeS 2 . Khi phản ứng với lithium, những vật liệu này trải qua các phản ứng hoàn nguyên , với sự biến mất của các pha ban đầu và hình thành các pha mới [DR Vissers, Z. Tomczuk và RK Steunenberg, J. Electrochem. Soc. 121, 665 (1974)].
Pin lithium ion được phát minh khi nào?
Giáo sư Whittingham đã khám phá sự xen phủ điện hóa trong các vật liệu như vậy và năm 1973 đã đề xuất các vật liệu đó như điện cực trong pin. Công việc này đã tạo ra một loại pin có thể sạc lại hoạt động vào năm 1976 . Tế bào thành công bao gồm kim loại liti làm cực dương và titan sunfua (TiS 2 ) làm cực âm, với liti hexafluorophosphat ( LiPF 6 ) làm chất điện phân trong propylen cacbonat (PC) làm dung môi. Những nghiên cứu đầy hứa hẹn này đã truyền cảm hứng cho Whittingham khám phá sự xen phủ điện hóa trong các vật liệu như điện cực trong pin. Một loại pin có thể sạc lại hoạt động sau đó đã được chứng minh vào năm 1976
[(a) Whittingham, MS Electrointercalation in Transition-Metal Disulphides. J. Chèm. Soc., Chem. Commun. 1974, 328–329.] (Với Công ty Nghiên cứu và Kỹ thuật Exxon).
(b) Whittingham, MS Batterie à Base de Chalcogénures. Bằng sáng chế số của Bỉ. 819672, năm 1975.
(c) Whittingham, MS Điện lưu trữ và Hóa học xen kẽ. Khoa học 1976, 192 (4244), 1126–1127.
Nhưng thành công chỉ tồn tại trong thời gian ngắn. Trong quá trình đạp xe lặp đi lặp lại, liti kim loại hình thành các đuôi gai ở bề mặt kim loại khi đi xe đạp, dẫn đến đoản mạch.
Vấn đề này đã tạo động lực cho một tìm kiếm mới về các giải pháp thay thế và cấu hình “tế bào chuyển ion” (còn gọi là “ghế bập bênh”), trong đó cả hai điện cực đều có thể chứa các ion đã được đề xuất.
Nếu vật liệu điện cực dương ban đầu chứa lithium và một số hoặc tất cả lithium bị loại bỏ trong lần sạc đầu tiên, tế bào sẽ phát triển tiềm năng. Do đó, có thể có các vật liệu điện cực dương phản ứng với liti ở điện thế trên khoảng 3V, nếu chúng đã chứa liti, và liti này có thể được chiết xuất bằng điện hóa.
Ai là người phát minh ra pin lithium ion?
Cách tiếp cận này, liên quan đến việc sử dụng các vật liệu đã có lithium, lần đầu tiên được chứng minh bởi Giáo sư Goodenough. Các ví dụ đầu tiên về các vật liệu ban đầu chứa liti và loại bỏ liti khỏi chúng bằng phương pháp điện hóa là công trình nghiên cứu về Li1-xCoO2 vào năm 1980.
[K. Mizushima, PC Jones, PJ Wiseman và JB Goodenough, Mater. Res. Bò đực. 15, 783 (1980)] và Li1 − xNiO2
[JB Goodenough, K. Mizushima và T. Takada, Jpn. J. Appl. Thể chất. 19 (bổ sung 19-3), 305 (1980)]
Song song với việc phát triển cực dương, các vật liệu làm cực âm tốt hơn cũng được tìm kiếm để thu được một tế bào emf cao hơn kết hợp với các cực dương có tiềm năng cao hơn so với liti kim loại. Một bước đột phá đến vào năm 1979/1980 khi John B. Goodenough và các đồng nghiệp của ông tại Oxford
Đại học, Vương quốc Anh, đã phát hiện ra rằng LixCoO2, một chalcogenide kim loại xen kẽ khác thuộc loại MX2, có thể dùng làm vật liệu catốt.
[Đủ rồi, JB; Mizushima, K. Chất dẫn ion nhanh. Bằng sáng chế Hoa Kỳ số. 4,357,215, năm 1982].
[Mizushima, K .; Jones, PC; Wiseman, PJ; Goodenough, JB LixCoO2 (0 <x <-1): Mới
Vật liệu catốt cho pin có mật độ năng lượng cao. Mater. Res. Bò đực. 1980, 15 (6), 783–789].
Cấu trúc của vật liệu tương tự như Lix TiS2 với khoảng trống van der Waals giữa coban dioxide (CoO2 ) các lớp trong đó các ion liti có thể được liên kết mà không cần mở rộng mạng tinh thể nhiều. Goodenough lý luận rằng khi X trong MX2 là một phần tử có độ âm điện nhỏ, quá trình hấp thụ cation tạo thành sẽ liên quan đến sự thay đổi năng lượng tự do âm lớn và điện áp tế bào cao (ΔG = -nFE). Với một oxy X, tình huống được coi là đặc biệt hứa hẹn, cũng vì các ion liti đã được đề xuất là đủ di động trong các mảng oxy được đóng gói gần nhau.
Lý do được chứng minh là đúng và vật liệu CoO2 cho thấy một thế năng rất cao ~ 4 đến 5 V so với Li + / Li. Các nghiên cứu điện hóa được thực hiện trong trường hợp này với một chất điện phân bao gồm liti tetrafluoroborat (LiBF4) trong propylen cacbonat.
Khám phá này cho phép sử dụng vật liệu anốt có điện thế cao hơn kim loại liti, thúc đẩy quá trình tìm kiếm vật liệu cacbon thích hợp. Xem xét sự khó khăn của việc giải quyết vấn đề xen phủ điện hóa của than chì, các phương án khác đã được nghiên cứu để thay thế.
Pin lithium ion được phát minh ở đâu?
Một bước đột phá đến vào năm 1985 khi một nhóm người Nhật Bản do Akira Yoshino (thuộc Tập đoàn Asahi Kasei) lãnh đạo đã phát hiện ra sợi carbon phát triển theo pha hơi (VGCF) và sau đó là than cốc dầu mỏ được xử lý nhiệt. Vật liệu thứ hai được biết là có chứa hỗn hợp các vùng tinh thể (graphitic) và không kết tinh, và các nhà nghiên cứu có thể xác định các chất lượng đặc biệt ổn định, nhưng hiệu suất cao, với các mức độ kết tinh cụ thể.
[Akira Yoshino, Sự ra đời của pin Li-Ion, Các tiểu luận của Angewandte, Angew., Chem. Int. Ed., 2012 , 51, 5798-5800]
Với những vật liệu cực dương hiệu quả này, Yoshino đã phát triển một loại pin lithium-ion hoạt động hiệu quả dựa trên cấu hình tế bào chuyển ion. Do đó, vật liệu cacbon được xác định đã được sử dụng làm cực dương và vật liệu LixCoO2 của Goodenough (thường chứa một lượng nhỏ thiếc) được sử dụng làm cực âm. Các lớp phân tách bao gồm polyetylen hoặc polypropylen đã được sử dụng và chất điện phân bao gồm liti perclorat (LiClO4) trong propylen cacbonat (PC).
Yoshino cũng đã chứng minh độ an toàn của loại pin này vào năm 1986 bằng cách thả một quả nặng lên pin. Không có vụ cháy hoặc nổ nào xảy ra trong khi pin sử dụng cực dương kim loại lithium phản ứng dữ dội.

Hình 8. Yoshino kiểm tra độ an toàn đầu tiên với pin Li-ion của mình vào năm 1986.
A) Thời điểm cục sắt va chạm với pin
B) Nguyên mẫu pin Li-ion sau va chạm
C) Pin anốt bằng kim loại Li sau va chạm
[Nhà cung cấp hình ảnh: Akira Yoshino, Sự ra đời của pin Li-Ion, Các bài luận của Angewandte, Angew., Chem. Int. Ed., 2012, 51, 5798-5800]
Những khám phá và phát triển này cuối cùng đã dẫn đến việc phát hành pin lithium thương mại
vào năm 1991. Với sự phát triển hơn nữa, pin Li-ion đã được Sony thương mại hóa vào năm 1991 và bởi liên doanh của Asahi Kasei và Toshiba vào năm 1992.
[Nishi, Y., Sự phát triển của Pin Lithium Ion thứ cấp. Chèm. Rec. 2001, 1, 406–413]
Pin được làm từ vật liệu cực dương làm từ than cốc dầu mỏ, LixCoO2 làm cực âm và chất điện phân không chứa nước bao gồm lithium hexafluorophosphate (LiPF6) trong propylene carbonate (PC). Điện áp sạc cao (lên đến 4,1 V), với năng lượng cụ thể được ghi lại là ~ 80 Wh / kg và mật độ năng lượng là ~ 200 Wh / lít.
So với các loại pin khác có mặt trên thị trường vào thời điểm đó, pin lithium nhanh chóng trở nên rất cạnh tranh và về cơ bản là mở đường cho cuộc cách mạng di động sắp tới.
Đồng thời, người ta thấy rằng than chì thực sự có thể được sử dụng kết hợp với thành phần chất điện ly thích hợp. [Fong R, Sacken U von, Dahn JR, Nghiên cứu về sự xen kẽ của Lithium thành cácbon bằng cách sử dụng các tế bào điện hóa không chứa nước. J. Điện hóa. Soc. 1990, 137 (7), 2009–2013]
Bằng cách sử dụng dung môi có chứa ethylene cacbonat, cho đến nay thường bị bỏ qua do nhiệt độ nóng chảy cao hơn, một pha điện phân rắn (SEI) được hình thành trên bề mặt của điện cực graphit trong chu kỳ sạc / xả, do đó bảo vệ vật liệu carbon khỏi bị tróc vảy và phân hủy thêm . [Peled, E. Hành vi điện hóa của kim loại đất kiềm và kiềm trong hệ thống pin không chứa nước, Mô hình xen kẽ chất điện ly rắn. J. Điện hóa. Soc. Năm 1979, 126 (12), 2047–2051.
Khám phá này nhanh chóng được cộng đồng pin áp dụng và pin lithium-ion thế hệ tiếp theo dựa trên than chì làm vật liệu cực dương đã được phát triển. Với vật liệu cực dương này, pin có điện áp sạc 4,2 V đã được sản xuất ngay sau đó, dẫn đến mật độ năng lượng ~ 400 Wh / lít.
Sự phát triển của pin lithium-ion không chỉ dừng lại ở những khám phá quan trọng này, mà nhiều cải tiến và lựa chọn thay thế đã được báo cáo. Ví dụ, vật liệu cathode mới liên tục được xác định để sử dụng trong các ứng dụng pin cụ thể và hai vật liệu như vậy có nguồn gốc từ nhóm của Goodenough: vật liệu spinel Li1-xMn2O4 và vật liệu olivin LixFePO4 (LFP).
[Padhi, AK; Nanjundaswami, KS; Goodenough, JB Phospho-Olivin làm Vật liệu điện cực dương cho pin Lithium có thể sạc lại. J. Điện hóa. Soc. 1997, 144, 1188–1194.
Thackeray, MM; David, WIF; Bruce, PG; Goodenough, JB Lithium chèn vào Mangan Spinels. Mater. Res. Bò đực. Năm 1983, 18, 461–472].
Vật liệu thứ hai bị hạn chế bởi tiềm năng so với Li + / Li thấp hơn một chút so với LixCoO2, nhưng có độ ổn định cao và có thể được sử dụng ở tốc độ sạc cao. Một số vật liệu điện cực và hệ thống điện phân khác cũng đã được phát hiện, dẫn đến các vật liệu lưu trữ năng lượng ngày càng được cải tiến vì lợi ích của xã hội.
Loại pin nào được sử dụng trong xe điện?
Ngày nay, hầu hết các xe điện đều sử dụng pin Li-ion. Trước đó, pin Ni-MH và axit-chì đã được sử dụng, nhưng việc sử dụng chúng từ từ giảm do sự ra đời của pin Li-ion, có năng lượng riêng cao hơn và giá trị mật độ năng lượng cao hơn. Năng lượng riêng của pin axit chì là khoảng 40-50 Wh / kg trong khi pin Li-ion có khoảng 150 Wh / kg. Giá trị mật độ năng lượng cho pin axit-chì là 80-100 Wh / lít trong khi pin Li-ion đạt hơn 250 Wh / lít.
Các tế bào hình trụ với cực âm niken-coban-nhôm (NCA) và cực dương hỗn hợp silicon / graphite, chẳng hạn như những tế bào được sử dụng trong các gói pin Tesla mới nhất (2019-2020), đã đạt khoảng 270 Wh / kg và 650 Wh / lít. Một công nghệ mới được gọi là Licerion của Sion Power tuyên bố năng lượng cụ thể 500 Wh / kg và mật độ năng lượng 1000 Wh / L và> 450 chu kỳ trong tế bào phát triển 0,4 Ah.
Đối với pin nhỏ, chúng tôi nói về Wh. Đối với hệ thống công suất cao hơn, đơn vị kWh được sử dụng. Giá trị Wh chia cho 103 sẽ cho kWh.
Như vậy 850 Wh = 850/1000 = 0,850 kWh.
Các tế bào được sử dụng trong pin EV ngày nay có thể đạt năng lượng cụ thể danh nghĩa là 140 -170 Wh / kg. Năng lượng cụ thể của bộ pin thu được thường thấp hơn từ 30 đến 40%, hoặc 80 -120 Wh / kg. Sự giảm thiểu này là do một số dây dẫn kết nối nối tiếp và song song, BMS và hệ thống quản lý nhiệt (làm mát hoặc sưởi ấm). Vào năm 2019, tỷ lệ gói các thành phần không phải tế bào đã giảm xuống khoảng 28%.
Cho đến nay, các tế bào đầu tiên được đưa vào các mô-đun và sau đó được đưa vào các gói. Cả hai Công ty Công nghệ Amperex Đương đại Limited, Trung Quốc ( CATL) và Tesla đã quyết định rằng họ muốn loại bỏ các mô-đun và đặt các ô vào các gói trực tiếp. CATL đã làm như vậy và gọi nó là công nghệ cell-to-pack . Trong khi thông tin về điều này là khan hiếm, công ty tuyên bố rằng điều này có thể làm tăng năng lượng cụ thể lên 10-15% và cải thiện việc sử dụng khối lượng lên 15-20%. Tổng cộng, nó có thể làm giảm 40% các bộ phận cần thiết cho bộ pin. [https: //cleantechnica.com/2020/02/18/how-catl-lithium-iron-phosphate-bataries-could-be-leading-to-100-kwh-tesla-model-3/]
Chỉ định pin Lithium
Ủy ban Kỹ thuật Điện Quốc tế (IEC) và Viện Tiêu chuẩn Ấn Độ đã thiết lập một ký hiệu chung để mô tả hóa học và kích thước của các tế bào Lithium-ion.
[ Tế bào và pin lithium thứ cấp cho các ứng dụng di động, Ủy ban Kỹ thuật Điện Quốc tế, IEC 61960-1 và IEC 61960-2 và IS 16047: 2012 ].
Các chữ cái chỉ ra yếu tố hóa học và hình thức trong khi các con số chỉ định kích thước vật lý của tế bào. Chữ cái đầu tiên mô tả hóa học chung, chữ cái thứ hai chỉ ra chất hóa học catốt cụ thể và chữ cái thứ ba chỉ hình dạng.
Chữ cái đầu tiên: I – Hóa học liti-ion
Chữ cái thứ hai: C- coban, F- sắt, Fp – sắt photphat, N- niken, M-mangan, Mp- mangan photphat, T- titan, V –vanadi và x – những chất khác.
Chữ cái thứ ba: R- hình trụ, P-lăng trụ
Hai số đầu tiên theo sau chỉ đường kính bằng mm và ba số cuối cùng để chỉ chiều cao bằng phần mười mm. Do đó, một tế bào được ký hiệu ICR19 / 66 là một tế bào ion Lithium có cực âm coban có đường kính là> 18 mm và ≤ 19 mm và chiều cao tổng thể tối đa là> 65 mm và ≤ 66 mm.
Đối với các ô hình lăng trụ, các chữ cái đầu tiên có nghĩa giống nhau nhưng hai số đầu tiên chỉ chiều rộng tính bằng mm, hai số tiếp theo là chiều cao tính bằng mm và hai số cuối là chiều dài tính bằng mm. Do đó, ký hiệu tế bào IMP9 / 35/150 mô tả một tế bào ion Lithium hình lăng trụ với một tế bào catốt mangan có độ dày tối đa là > 8 mm và ≤ 9 mm và chiều rộng tối đa là > 34 mm và ≤ 35 mm và chiều cao tổng thể tối đa là > 149 mm và ≤ 150 mm.
Pin Lithium-ion hoạt động như thế nào?
pin lithium ion được tạo ra như thế nào
Kim loại liti có số nguyên tử 3, mật độ 0,534 g / cc, có thế khử tiêu chuẩn rất thấp (cặp Li + / Li -3,05 V so với SHE) và dung tích riêng lý thuyết là 3860 Ah / kg (2061 mAh / cc) là trọng lượng nhẹ nhất, điện áp cao nhất và mật độ năng lượng lớn nhất trong tất cả các kim loại. (So sánh với chì có số nguyên tử 82, mật độ 11,29 g / cc, dung tích riêng lý thuyết là 257,8 Ah / kg và thế khử tiêu chuẩn là -0,35V so với SHE).
Pin Lithium ion - Vật liệu hoạt động
Các vật liệu hoạt động của điện cực dương là bất kỳ một trong số các oxit hỗn hợp như LiCoO2 hoặc LiMnO2 hoặc LiFePO4. Điện cực âm chủ yếu là than chì và các hợp chất cacbon vô định hình. Chất điện phân hữu cơ (chứa muối dẫn liti phân ly như LIPF6) được sử dụng. Sử dụng thiết bị phân tách bằng polypropylene (PP) hoặc polyethene (PE) hoặc hỗn hợp. Các ion lithium di chuyển qua lại giữa các điện cực của pin lithium-ion trong quá trình sạc và xả và được xen kẽ vào các vật liệu hoạt động như mô tả bên dưới:

Hình 9. Quang cảnh bùng nổ của một tế bào Lithium ion
Nhà cung cấp hình ảnh: Zhang Z., Ramadass P. (2012) Hệ thống và Công nghệ Pin Lithium-Ion. Trong: Meyers RA (eds) Encyclopaedia of Sustainable Science and Technology. Springer, New York, NY, trang 6124. http s: //doi.org/10.1007/978-1-4419-0851-3_663
Cách sạc pin lithium ion
Trong quá trình phóng điện trong tế bào Lithium ion (LIB), các ion lithium từ cực dương được khử xen kẽ (hoặc chiết xuất) vào chất điện phân và các ion lithium này từ chất điện phân được xen kẽ vào vật liệu catốt . Sự chuyển động này của các ion từ anot sang catot kèm theo sự giải phóng các electron chạy trong mạch ngoài. Quá trình ngược lại xảy ra trong quá trình sạc khi các ion liti di chuyển từ cực âm và xen kẽ trong cực dương thông qua chất điện phân . LIB thương mại thường sử dụng các oxit kim loại chuyển tiếp như LiCoO 2 , LiMn 2 O 4 và LiFePO 4 làm vật liệu cực âm, được phủ trên một bộ thu dòng bằng nhôm.
Mười đến hai mươi phần trăm carbon dẫn điện và 5 %–10% chất kết dính cao phân tử như polyvinylidene difluoride (PVDF) và polytetrafluoroethylene (PTFE) cũng được thêm vào cùng với vật liệu hoạt tính để tăng cường độ dẫn điện tử và đạt được độ bám dính tốt hơn của vật liệu điện cực, tương ứng. Vật liệu cực dương được phủ trên một bộ thu dòng bằng đồng với cacbon dẫn điện và PVDF nếu được yêu cầu.
Hai điện cực được ngăn cách bằng một bộ phân cách xốp (màng polyetylen hoặc polypropylen dày 10–20 µm) ngâm trong dung dịch điện phân (LiPF6 trong dung môi hữu cơ). Cả dung dịch tách và dung dịch điện phân nên có độ dẫn ion tốt hơn. Tế bào này thường được chế tạo trong một vỏ kim loại theo kiểu Jellyroll với một bộ phân tách nhúng chất điện phân ở giữa hai điện cực. Sơ đồ của LIB được hiển thị trong các hình, trong đó các quá trình sạc và phóng điện điển hình được hiển thị.
Pin sạc lại Lithium-ion (Li-ion) sử dụng việc chèn / chiết có thể đảo ngược các ion lithium (Li + ) (loại khách) vào hoặc từ ma trận chủ (vật liệu hoạt động của điện cực dương và âm) được gọi là hợp chất chèn lithium khi phóng điện và sạc các quá trình xảy ra. Pin lithium ion đã được gọi là pin ghế bập bênh vì các ion lithium “đá” qua lại giữa các điện cực dương và âm khi tế bào được sạc và xả.
Vật liệu hoạt động tích cực thường là oxit kim loại có cấu trúc phân lớp, chẳng hạn như oxit liti coban (LiCoO 2 ), hoặc vật liệu có cấu trúc dạng đường hầm, chẳng hạn như oxit mangan liti (LiMn 2 O 4 ) , chủ yếu trên bộ thu dòng nhôm . Vật liệu hoạt động tiêu cực thường là cacbon graphit , cũng là một vật liệu phân lớp, chủ yếu là trên một bộ thu dòng điện bằng đồng. Trong quá trình phóng điện tích, các ion liti được đưa vào hoặc chiết xuất từ không gian kẽ giữa các lớp nguyên tử của vật liệu hoạt động.
Các chất điện phân không chứa nước hoặc chất điện phân hữu cơ được sử dụng trong các tế bào liti.
Bộ phân cách cho pin lithium-ion là màng vi xốp polyolefin polyetylen (PE) và polypropylen (PP).
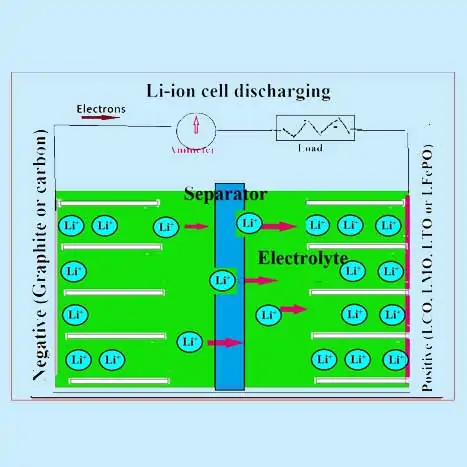

Phản ứng tế bào điện hóa trong pin lithium ion
Trong một tế bào ion Lithi điển hình, các phản ứng chung sau đây xảy ra.
Phản ứng điện cực dương:
LiMO 2 ⇔ Li 1-x MO 2 + x Li + + xe –
Phản ứng điện cực âm:
C + y Li + + ye – ⇔ Li y C
Tổng số phản ứng tế bào:
LiMO 2 + x / y C ⇔ x / y Li y C + Li 1-x MO 2
M = các kim loại như Co, Mn, Ni, Ti, v.v.
Thông thường x là khoảng 0,5 và y là khoảng 0,16, do đó x / y là khoảng 3. [Jeff Dahn và Grant M. Ehrlich. “Pin Lithium ion”, Sổ tay về Pin của Linden, ấn bản lần thứ 4, Thomas B. Reddy (Ed.), McGraw
Chất điện giải và chất điện phân rắn (SEI)
Như đã đề cập trước đó, chất điện phân không chứa nước hoặc chất điện phân hữu cơ được sử dụng trong pin lithium. Tế bào Li hoạt động ở điện áp tương đối cao hơn, lên đến 4,2 V trên mỗi tế bào. Mặc dù các muối lithium cồng kềnh như lithium hexafluorophosphate (LiPF6), lithium hexafluoro arsenate (LiAsF6), lithium tetrafluoroborate (LiBF4), lithium perchlorate (LiClO4), lithium trifluoromethanesulphonate (LiCF3SO3), lithium difluoro (oxalat), v.v. , là các chất điện ly thực tế (muối điện ly duy trì), chúng yêu cầu dung môi thích hợp ổn định ở điện áp cao hơn như vậy. Hầu hết các dung môi như vậy có hằng số điện môi cao, tạo điều kiện cho sự phân ly ion dễ dàng hơn và sự tồn tại của các ion Li có nồng độ cao. Những dung môi như vậy cũng đóng vai trò là vỏ bọc solvat hóa cho sự tồn tại ổn định của các ion Li, do đó làm giảm ảnh hưởng của các anion đối chất.
Nhược điểm của việc có hằng số điện môi cao là chúng có giá trị độ nhớt cao hơn dẫn đến tính linh động của các ion bị suy giảm . Để khắc phục độ dẫn ion thấp hơn, dung môi có độ nhớt thấp thường được trộn với dung môi có độ nhớt cao. Tuy nhiên, vì các dung môi có độ nhớt thấp có khả năng phân ly ion thấp hơn , nên bắt buộc phải đạt được một tỷ lệ trộn tối ưu để hỗn hợp có cả độ dẫn ion tốt và tính di động tốt. Là dung môi không chứa nước, hỗn hợp của etylen cacbonat (EC) với các cacbonat alkyl mạch thẳng ít nhớt hơn như dimetyl cacbonat (DMC), dietyl cacbonat (DEC) và etyl metyl cacbonat (EMC) được sử dụng trong LIB có bán trên thị trường.
Dung môi aprotic là ete, este và alkyl cacbonat: Chúng là dietyl ete (DEE), tetrahydrofuran (THF), dioxolan, etylen cacbonat (EC), propylen cacbonat (PC), đimetyl cacbonat (DMC), dietyl cacbonat (DEC), etyl metyl cacbonat (EMC), metyl fomat, γ-butyrolacton (BL), metyl axetat, axetonitril (AN), đimetyl sulfoxit (DMSO), đimetylformamit (DMF), metyl clorua, nitrometan, v.v.)
Chất điện phân lỏng là dung dịch của muối liti trong một hoặc nhiều dung môi hữu cơ, điển hình là cacbonat
Propylen cacbonat (PC) không thể được sử dụng làm chất điện phân nếu graphit được sử dụng làm cực dương, vì chất trước đây phân hủy trên bề mặt graphit; Máy tính được sử dụng một mình, không có EC hoặc bổ sung nhỏ LiBOB) Li bisoxalato borat), có thể gây ra sự suy thoái trong các điện cực graphit vì nó đồng xen kẽ với lithium, dẫn đến hiện tượng tróc da.
Chất điện ly là bất biến (cùng số lượng các ion đi vào chất điện phân trong quá trình tích điện và
phóng điện). Muối điện li thường được hòa tan trong dung môi hữu cơ cacbonat. Mỗi nhà sản xuất có sự kết hợp khác nhau của các dung môi với ethylene cacbonat (EC) là mẫu số chung cho hầu hết
Hình thành lớp giữa các pha điện giải rắn (SEI) là một chức năng quan trọng khác được thực hiện bởi các chất điện giải. Khi nhúng một kim loại kiềm vào chất điện phân của pin, hoặc khi đặt điện thế âm lên cacbon hoặc điện cực trơ được nhúng trong chất điện phân, SEI bắt đầu hình thành.
Lớp SEI được hình thành ngay lập tức khi kim loại tiếp xúc với dung dịch, bao gồm các sản phẩm khử không hòa tan và hòa tan một phần của các thành phần chất điện ly. SEI là yếu tố quan trọng quyết định độ an toàn, khả năng sử dụng điện, hình thái của cặn lithium, thời hạn sử dụng và chu kỳ của pin. Độ bám dính tốt với cực dương cũng rất quan trọng.
Như đã nhấn mạnh ở trên, pin kiềm hoặc kiềm thổ sơ cấp hoặc thứ cấp trong thực tế chỉ có thể được chế tạo khi có thể ngừng hòa tan hoặc ăn mòn cực dương. Do đó, chất điện phân phải được thiết kế để chứa ít nhất một tiền chất SEI phản ứng nhanh với liti (hoặc với cực dương kim loại kiềm) để tạo thành chất điện ly xen kẽ rắn không hòa tan. Các sản phẩm của quá trình khử anion muối thường là các hợp chất vô cơ như LiF, LiCl và Li 2 O, chúng kết tủa trên bề mặt điện cực. Việc giảm dung môi được theo sau bởi sự hình thành của cả các thành phần SEI không hòa tan như Li 2 CO 3 và các polyme và bán cacbonat hòa tan một phần.
Trong trường hợp của điện cực cacbon, điện áp tại đó SEI được hình thành phụ thuộc vào loại cacbon, đặc tính xúc tác của bề mặt của nó (hàm lượng tro, loại mặt phẳng tinh thể, tỷ lệ mặt phẳng bazơ-cạnh), nhiệt độ, nồng độ và các loại dung môi, muối và tạp chất, và mật độ dòng điện. Trong lần sạc đầu tiên của pin lithium-ion, sẽ có sự hao hụt dung lượng được gọi là “tổn thất dung lượng không thể phục hồi” (Q IR ) chủ yếu cần thiết cho sự hình thành SEI.
Ngoài sự hình thành SEI, Q IR có thể do mất công suất kết hợp với sự hình thành các sản phẩm khử hòa tan (Q SP ).
SEI không bị ô nhiễm là yếu tố cần thiết cho thời gian sử dụng lâu dài của pin. Nó thậm chí còn trở nên quan trọng hơn trong quá trình đạp xe ở tốc độ cao và ở độ sâu xả lớn hơn.
SEI trong các dung dịch lithium hexafluorophosphate (LiPF6) và lithium hexafluoroarsenate (LiAsF6) có điện trở suất cao hơn so với các dung dịch của các muối khác. Điều này là do sự thay đổi điện trở suất góp phần vào điện trở được kiểm soát bởi loài dẫn đến trở kháng giao diện cao của cực dương lithium trong chất điện phân LiPF6 và LiAsF6. Ngoài ra, Li2CO3 được cho là một trong những chất thụ động tốt nhất để tăng cường hiệu quả chu trình của lithium [J Electrochem Soc., 164 (7) A1703-A1719 (2017)].
Bộ phân tách cho pin lithium-ion
Bộ phân tách cho pin lithium-ion là các màng vi xốp polyolefin và thường là polyetylen (PE) và polypropylen (PP) được kéo theo hai trục, PE được kéo theo hai trục hoặc PP / PE / PP được kéo theo nhiều trục.
Nguyên liệu cho các vật liệu hoạt động trong pin lithium ion
Pin Lithium ion sử dụng các vật liệu catốt khác nhau. Cực dương luôn luôn được làm từ cacbon, ngoại trừ một số loại như cực dương oxit titan-niobi, hợp kim Li-Si, v.v. Bảng và hình dưới đây cung cấp một số ý tưởng về các chất hóa học khác nhau được sử dụng trong các loại pin này.

Hình 12. Tóm tắt một số lựa chọn hóa học điện cực hiện tại và tương lai cho pin Lithium ion. Dung lượng đề xuất của Li (Si) bằng 50% dung lượng lý thuyết của vật liệu, tương tự như trường hợp được tìm thấy đối với một số vật liệu điện cực dương
[Nguồn: Yu Miao, Patrick Hynan, Annette von Jouanne và Alexandre Yokochi, Energies 2019, 12, 1074; doi: 10.3390 / en12061074]
Bảng 1.
Đặc điểm của các tế bào ion Lithium với các vật liệu catốt khác nhau
| Vật liệu cathode | Li-Ni-Co-Al (NCA) | Li-Ni-Mn-Co (NMC) | Li-MnO2 (LMO) | Li-Iron Phosphate (LFP) | Li Titanate (LTO) | Li Coban Oxit (LCO) |
|---|---|---|---|---|---|---|
| Điện áp danh định của ô (V) | 3.6 | 3.65 (2.7-4.2) | 3.8 | 3.25 (2-3.6) | 3.2 | 3.6 |
| Năng lượng riêng lý thuyết (Wh / kg) | 279 | 256 | 148 | 128 (373) | 293 (175) | 274 (370) (x = 0,5) |
| Công suất cụ thể cho cực âm (Ah / Kg) Tiềm năng so với Li / Li + (V) | 180-200 (3.8) | 200 | 148 (4.1) | 150-170 (3.45) | 175 | 274 (3,9) (x = 0,5) |
| Năng lượng riêng cho cực âm (Wh / Kg) | 680-760 | 610-680 | 410-492 548 | 518-587 544 | -- | 546 |
| Sự an toàn | an toàn | Vừa phải | An toàn | Cao | Rất tốt | Vừa phải |
Vật liệu catốt trong pin lithium ion
Vật liệu làm catốt phải thỏa mãn một số yêu cầu mà việc lựa chọn vật liệu làm điện cực dương phụ thuộc vào.
- Để cung cấp công suất cao, các vật liệu này phải kết hợp một lượng lớn lithium khi được chế tạo.
- Hơn nữa, các vật liệu phải xen kẽ một cách thuận nghịch với ít thay đổi cấu trúc để cho phép vòng đời dài, hiệu suất ampe giờ cao và hiệu suất năng lượng cao.
- Để đạt được điện thế tế bào cao và mật độ năng lượng cao, phản ứng trao đổi liti phải xảy ra ở điện thế cao so với liti.
- Để tạo điều kiện thuận lợi cho quá trình sạc và phóng điện ở tốc độ cao, độ dẫn điện tử và tính linh động của ion lithium trong vật liệu phải cao.
- Vật liệu làm điện cực dương không được hòa tan trong chất điện phân và phải có sẵn với giá cả phải chăng. Để giảm thiểu chi phí, việc chuẩn bị từ các nguyên liệu rẻ tiền trong một quy trình chi phí thấp được ưu tiên
LiFePO 4 là một ngoại lệ đối với quy tắc này. Trong LiFePO 4 , sự vận chuyển ion lithium đầy đủ đạt được bằng cách sử dụng các hạt điện cực có kích thước hạt nanomet. [Jeff Dahn và Grant M. Ehrlich. “Pin lithium ion”, Sổ tay Pin của Linden, ấn bản lần thứ 4, Thomas B. Reddy (Ed.), McGraw Hill, trang 26.6, 2011]
Các vật liệu hoạt động tích cực (PAM) trong pin Lithium ion khác nhau tùy thuộc vào nhà sản xuất. Vật liệu catốt có thể được phân thành ba loại lớn [ Arumugam Manthiram, Nature Communications (2020) 11: 1550]. Họ đang:
Ôxít phân lớp - vật liệu catốt trong pin lithium ion
Một số ôxit thuộc loại tổng quát LiMO 2 (trong đó M = vanadi, crom, coban và niken) kết tinh theo cấu trúc phân lớp trong đó ion Li + và M 3+ chiếm giữ [các làn của cấu trúc muối mỏ thay thế để tạo ra một chuỗi lớp của O-Li-OMO.
Trong catốt ôxít phân lớp LiCoO 2 , sự khác biệt lớn về điện tích và kích thước giữa các ion Li + và Co 3+ hóa trị ba dẫn đến thứ tự cation tốt, điều này rất quan trọng để hỗ trợ sự khuếch tán và dẫn điện lithium-ion hai chiều nhanh trong mặt phẳng lithium.
Vật liệu catốt yêu cầu mức độ tinh khiết cực cao và phải gần như hoàn toàn không có các tạp chất kim loại không mong muốn – đặc biệt là sắt, vanadi và lưu huỳnh.

Hình 13. Sơ đồ đơn giản của một cấu trúc phân lớp trong đó có sự thay thế của
các lớp cation giữa các lớp ion oxit đóng gói chặt chẽ.
[Nhà cung cấp hình ảnh: Robert A. Huggins, Pin nâng cao, Các khía cạnh của khoa học vật liệu, Springer, New York, 2009, tr.168]
Độ ổn định cấu trúc tốt cùng với độ dẫn điện và ion lithium cao mang lại đặc tính phóng điện nhanh với khả năng đảo ngược tốt. Với những tính năng này, LiCoO2 vẫn là một trong những cực âm tốt nhất cho đến nay với điện áp hoạt động cao ~ 4 V.
hai thách thức lớn liên quan đến cực âm sunfua được theo đuổi trong những năm 1970. Nó không chỉ cho phép tăng đáng kể điện áp hoạt động từ< 2,5 V đến ~ 4 V mà còn là việc lắp ráp tế bào mà không cần sử dụng cực dương liti kim loại.
Oxit Spinel - vật liệu catốt trong pin lithium ion
Lớp thứ hai của catốt là Spinel LiMn 2 O 4 . (Công thức chung là AB 2 O 4 ). Mặc dù cấu trúc này thường được vẽ bằng hệ tọa độ lập phương, nhưng nó cũng có các lớp ion oxit song song trên mặt phẳng (111), và có cả vị trí phối trí bát diện và vị trí phối trí tứ diện giữa các mặt phẳng ion oxit. Số trang trí bát diện bằng số ion oxit, nhưng có gấp đôi số trang trí tứ diện. Tính ổn định cấu trúc ba chiều và độ dẫn điện và ion lithium cao cung cấp các đặc tính phóng điện thậm chí nhanh hơn cho Li 1 – x Mn 2 O 4 với khả năng đảo ngược tốt so với LiCoO 2 .
Một lợi thế quan trọng khi đi từ LiCoO 2 sang LiMn 2 O 4 là chi phí giảm đáng kể vì mangan có giá thành thấp hơn hai bậc so với Co. Tuy nhiên, một vấn đề quan trọng đối với LiMn 2 O 4 là sự hòa tan mangan từ mạng tinh thể vào chất điện phân với sự hiện diện của một lượng nhỏ (mức ppm) của ion H + (tính axit) trong chất điện phân do sự mất cân đối nổi tiếng của Mn 3 + thành Mn 4+ và Mn 2+ trong axit.

Hình 14. Sơ đồ cấu trúc spinel trong đó các cation được phân bố giữa các mặt phẳng đóng gói (111) của các ion oxit giữa các vị trí tứ diện và bát diện [ Nhà cung cấp dịch vụ: Robert A. Huggins, Pin nâng cao, Các khía cạnh khoa học vật liệu, Springer, New York, 2009, tr.17].
Vật liệu cực âm Lithium-Nickel-Mangan Oxide (LNMO) điện áp cao xuất hiện đầy hứa hẹn trong các loại pin thế hệ tiếp theo. Nhưng trở ngại là thiếu chất điện phân có thể xử lý các áp lực của pin dựa trên LNMO. Các tế bào pin dựa trên cực âm LNMO mang lại kết quả ngang bằng với các loại pin dựa trên lithium hiệu suất cao khác, nhưng với chi phí thấp hơn đáng kể.
Tuy nhiên, các nhà sản xuất chất điện phân đang thu được những kết quả rất hứa hẹn từ quá trình nghiên cứu & phát triển đang diễn ra, tại một thời điểm nào đó, sẽ tạo ra chất điện phân hoạt động tốt trong một tế bào pin LNMO. https: //blog.topsoe.com/the-cathode-material-for-next-generation-lithium-ion-bataries-is-ready
Gần đây, việc tăng hàm lượng Ni và giảm hoặc loại bỏ hàm lượng coban trong catốt NMC đang trở nên nổi bật hơn nhiều [ Li, W., Erickson., E. & Manthiram, A. , Nat. Năng lượng 5, 26 – 24 (2020)].
Poly-anion oxit - vật liệu catốt trong pin lithium ion
Loại oxit thứ ba là oxit polyanion. Các oxit polyanion như Fe 2 (MoO 4 ) 3 và Fe 2 (WO 4 ) 3 được phát hiện là trải qua quá trình chèn / chiết thuận nghịch của hai ion liti trên mỗi đơn vị công thức để tạo ra Li 2 Fe 2 (MoO 4 ) 3 hoặc Li 2 Fe 2 ( WO 4 ) 3 cả bằng phương pháp hóa học và điện hóa
[Manthiram, A., Goodenough, JB Lithium chèn khung Fe 2 (MO 4 ) 3 : so sánh M = W với M = Mo. J. Chem trạng thái rắn. 71, 349– 360 (1987)].
Dựa trên các tác phẩm của Manthiram và Goodenough,
[Manthiram, A. & Goodenough, JB chèn Lithium vào khung Fe 2 (MO 4 ) 3 : so sánh M = W với M = Mo. J. Chem trạng thái rắn. 71, 349–360 (1987). Chèn Manthiram, A. & Goodenough, JB Lithium vào khung Fe 2 (SO 4 ) 3 . J. Nguồn điện 26, 403–406 (1989).]
Việc khám phá các phốt phát chứa lithium làm cực âm đã dẫn đến việc xác định olivin LiFePO 4 làm cực âm [Padhi, AK, Nanjundaswamy, KS & Goodenough, JB Phospho-Olivin làm vật liệu điện cực dương cho pin lithium có thể sạc lại. J. Điện hóa. Soc. 144, 1188–1194 (1997] vào năm 1997.
Tuy nhiên, lớp ôxít polyanion có tính dẫn điện tử kém. [ Arumugam Manthiram, Nature Communications (2020) 11: 1550].
Việc khám phá các phốt phát chứa lithium làm cực âm đã dẫn đến việc xác định olivin LiFePO 4 làm cực âm [Padhi, AK, Nanjundaswamy, KS & Goodenough, JB Phospho-Olivin làm vật liệu điện cực dương cho pin lithium có thể sạc lại. J. Điện hóa. Soc. 144, 1188–1194 (1997] vào năm 1997.
Tuy nhiên, lớp oxit polyanion có tính dẫn điện tử kém. [ Arumugam Manthiram, Nature Communications (2020) 11: 1550].
Sản xuất vật liệu Cathode - Pin Lithium ion
Trước đó, các hợp chất catốt oxit kim loại liti được tạo ra từ liti cacbonat và một muối của kim loại đã chọn bằng một loạt các phản ứng thay thế hóa học được thực hiện trong dung dịch. Sản phẩm mong muốn được kết tủa và sấy khô.
LiCoO 2 lần đầu tiên được điều chế bằng phương pháp tổng hợp thông thường được chỉ ra trong hình . Tricoban tetraoxit (Co 3 0 4 ) và liti cacbonat (Li 2 CO 3 ) được trộn đều, sau đó được nung trong luồng không khí ở nhiệt độ khoảng 950ºC. Tuy nhiên, bằng phương pháp này, rất khó để chuẩn bị các hạt thô của LiCoO 2 và chỉ có thể thu được các hạt mịn có đường kính từ 1-3 pm.
Theo quan điểm an toàn, các vật liệu điện cực hoạt động tốt không được mong muốn. Trong trường hợp lạm dụng như đoản mạch bên ngoài hoặc nghiền nát, các hạt mịn có diện tích bề mặt riêng lớn dễ dàng phản ứng cùng một lúc và tất cả năng lượng tế bào được giải phóng đột ngột trong một thời gian rất ngắn kèm theo sự tăng nhiệt độ. Trong trường hợp xấu nhất, tế bào có thể bốc cháy [Yoshio Nishi, trong Pin Lithium ion, M. Wakihara và 0. Yamamoto (Eds.). trang 192-193].
Pin lithium ion được sản xuất như thế nào? sơ đồ
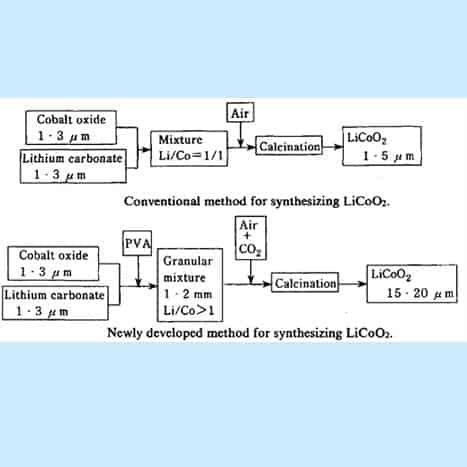
Hình 15. Lưu đồ chế tạo Li-CoO 2
[Nhà cung cấp hình ảnh: Yoshio Nishi, trong Pin Lithium ion, M. Wakihara và 0. Yamamoto (Eds.). trang 192-193].
Một quy trình được cải tiến để tổng hợp lithium coban có kích thước hạt lớn hơn: Điểm đầu tiên là một lượng nhỏ nhựa PVA được thêm vào hỗn hợp nguyên liệu (Co 3 0 4 và Li 2 CO 3 )) để tạo thành viên dạng hạt bằng máy tạo hạt . Bằng cách thiêu kết các viên trong luồng không khí có chứa lượng khí C0 2 thích hợp, các hạt liti coban có đường kính trung bình 20pm được tổng hợp. Điểm thứ hai là chúng tôi sử dụng một lượng hơi quá nhiều lithium cacbonat (Li 2 CO 3 ) trong nguyên liệu, do đó tỷ lệ nguyên tử Li / Co trong nguyên liệu lớn hơn một. Quy trình này cũng thuận lợi để thu được các hạt thô, và ngoài ra, LiCoO 2 thu được chứa một lượng nhỏ Li 2 CO 3 dư.
Điểm đầu tiên là một lượng nhỏ nhựa PVA được thêm vào hỗn hợp nguyên liệu thô (Co304 và Li 2 CO 3 ) để tạo thành viên nén dạng hạt bằng máy tạo hạt. Bằng cách thiêu kết, Lithium coban oxit có thể được điều chế dễ dàng bằng cách nung ở nhiệt độ cao hỗn hợp đo phân cực của liti cacbonat Li 2 CO 3 và oxit coban, Co 3 O 4 hoặc coban kim loại ở 600–800 ° C, sau đó ủ sản phẩm ở 900 ° C trong nhiều giờ, tất cả đều ở trong môi trường oxy.
Nó cũng có thể thu được bằng cách nung oxit ngậm nước với hydroxit liti lên đến 750–900 ° C.
Phương pháp thứ ba sử dụng liti axetat, axetat coban và axit xitric với lượng mol bằng nhau trong dung dịch nước. Gia nhiệt ở 80 ° C biến hỗn hợp thành dạng gel trong suốt nhớt. Gel khô sau đó được nghiền và làm nóng dần đến 550 ° C. (https: //en.wikipedia.org/wiki/Lithium_cobalt_oxide).
Một số ví dụ điển hình như: Phương pháp sol-gel
Trong quy trình sol-gel, dung dịch nước của chất phản ứng và dung dịch chất tạo chelat được trộn lẫn. Dung môi bay hơi chậm tạo ra sol và đun nóng vừa phải sol thu được sẽ tạo ra gel. Sau đó được nung ở nhiệt độ thích hợp để có được sản phẩm mong muốn.
Ví dụ 1.
Tổng hợp LiCoO 2 từ các chất tạo phức khác nhau: Các muối được sử dụng là coban nitrat hexa hiđrat (Co (NO 3 ) 2 .6H 2 O, và liti nitrat, LiNO 3 khan. Gel được sản xuất bằng cách sử dụng bốn chất tạo phức khác nhau: axit xitric, khan (C 3 H 4 OH (COOH) 3 , glycine, (H 2 NCH 2 COOH); tinh bột (tinh bột ngô thương mại và gelatine).
Người ta điều chế được 5 dung dịch chứa LiNO 3 và Co (NO 3 ) 2 .6H 2 O trong 20 ml nước, có tỉ lệ Li: Co = 1.1: 1. Một chất tạo phức cụ thể được thêm vào mỗi dung dịch: ( i ) axit xitric (4,611 g) pha loãng trong 5 ml nước; ( ii ) glyxin (1,501 g); ( iii ) tinh bột (1.250 g); ( iv ) gelatine (3.500 g) và ( v ) mẫu thử trắng.
Bốn dung dịch đầu tiên được đun nóng ở nhiệt độ 70 đến 80 ° C trong bể chứa glycerine cho đến khi tạo thành gel. Khoảng thời gian của quá trình này là khác nhau đối với từng chất tạo gel: ( i ) axit xitric (5 giờ), ( ii ) glycine (3 giờ), ( iii ) tinh bột (1 giờ), ( iv ) gelatine (3 giờ) . Việc sản xuất bột kết tinh cho tất cả các mẫu được thực hiện trong hai giai đoạn trong lò nung múp: đầu tiên là nung vật liệu ở 300 ° C trong 20-30 phút và sau đó nung ở 700 ° C trong 24 giờ. [Bruno GA Freitas và những người khác, J. Braz. Chèm. Soc. 28, 11, tháng 11 năm 2017].
Ví dụ 2.
Được điều chế bằng phương pháp Sol-Gel
LiNO3 lần đầu tiên được hòa tan trong dung dịch axit xitric. LiNO3, Ni (NO3) 2.6H2O Co (Ac) 2.4H2O và Mg (NO3) 2.6H2O được sử dụng làm nguyên liệu ban đầu của lithium, niken, coban và magie trong LiNi 0,7 – 𝑥 M 𝑥 Co 0,3 O2 (0 ⩽ 𝑥 ⩽ 0,1), tương ứng. Số mol axit xitric bằng tổng số mol Co, Ni, Mg. Sau đó, Co (Ac) 2 4H2O, Ni (NO3) 2 6H2O và Mg (NO3) 2 6H2O được thêm vào hỗn hợp. Toàn bộ hỗn hợp được đun cách thủy ở nhiệt độ 80 ° C. Trong quá trình đun nóng tạo thành dung dịch trong, màu hồng, không có kết tủa. Cuối cùng, dung dịch trong suốt được làm khô từ từ và chuyển thành gel. Xerogel được làm khô, mài, và sau đó được xử lý nhiệt trong lò ở 120 ° C trong 12 giờ.
Tiền chất gel được nung ở 500 ° C trong không khí trong 6 giờ, và làm nguội đến nhiệt độ phòng trong lò nung ống. Các sản phẩm đã qua xử lý nhiệt được nghiền trong cối mã não để thu được bột. Và sau đó bột được nung ở 800 ° C trong 12 giờ. Để chế tạo cực âm, các sản phẩm đã điều chế trước tiên được trộn với axetylen đen và polyvinylidene florua (80: 8:12 về khối lượng) trong 𝑁-metyl pyrrolidon (NMP). Sau đó, bùn thu được được phủ lên lá Al và sấy khô ở 80 o C trong 18 giờ để ép cuộn tiếp. . [ Hailang Zhang, Những tiến bộ trong Khoa học và Kỹ thuật Vật liệu, Tập 2014, Bài báo ID 746341, ]

Hình 16. Lưu đồ cho quá trình sol-gel để điều chế lithium manganate
( Nhà cung cấp hình ảnh: YS Lee, YK Sun và KS, Nahm, Solid State Ionics 109 (1998) 285 do M. Pasquali, S. Passerini và G Pistoia đưa ra, trong Pin Lithium, Khoa học và Công nghệ, ed. của GA Nazri và G. Pistoia, Springer, New York, (2009), tr. 318)
Sản xuất vật liệu Anode trong pin Lithium ion
Con đường khuyến khích dẫn đến LIB với mật độ năng lượng và công suất được cải thiện là việc lựa chọn vật liệu anốt phù hợp có thể cung cấp công suất cao và dễ dàng khuếch tán ion Li-ion vào anốt, cùng với tuổi thọ chu kỳ tốt và không bị lo ngại về an toàn.
Dựa trên các vật liệu tiền thân, cực dương cacbon có thể được phân loại thành một số loại như dưới đây.
Nguyên liệu tiền chất và các thông số xử lý xác định bản chất của cacbon được tạo ra. Vật liệu có thể được graphit hóa bằng cách xử lý ở nhiệt độ cao (2000 đến 3000 ° C) được gọi là cacbon mềm .
Khi graphit hóa, rối loạn bậc hai được loại bỏ dần dần khi nhiệt độ tăng, và sức căng trong vật liệu được giảm bớt [T. Zheng, JN Reimers và JR Dahn, Thể chất. Rev. B 51 , 734 (1995)] Cacbon cứng , chẳng hạn như những loại được chế biến từ nhựa phenolic, không thể dễ dàng bị graphit hóa, ngay cả khi được xử lý ở 3000 ° C. Nguyên liệu dạng cốc được chuẩn bị ở khoảng 1000 ° C, thường từ tiền chất dầu hỏa thơm [Jeff Dahn và Grant M. Ehrlich. “Pin Lithium ion”, Sổ tay Pin của Linden, ấn bản lần thứ 4, Thomas B. Reddy (Ed.), McGraw Hill, trang 26, 2011]

Hình 17. Phân loại tiền chất vật liệu anode carbon
[Tín dụng: Jeff Dahn và Grant M. Ehrlich. “Pin Lithium ion”, Sổ tay Pin của Linden, ấn bản lần thứ 4, Thomas B. Reddy (Ed.), McGraw Hill, trang 26, 2011]
Goriparti chia vật liệu anốt của LIB thành ba loại tùy thuộc vào cơ chế phản ứng của chúng với lithium [ Subrahmanyam Goriparti, Ermanno Miele, Francesco De Angelis, Enzo Di Fabrizio, Remo Proietti Zaccaria, Claudio Capiglia, J Power Sources 257 (2014) 421-443]
Nhóm intercalation / de-intercalation
Loại cực dương này bao gồm các vật liệu oxit titan và cacbon. Khả năng lưu trữ xảy ra thông qua một con đường xen kẽ gắn liền với diện tích bề mặt, hình thái, độ kết tinh và định hướng của nó. Cacbon mềm thường được chấp nhận và sử dụng trong ngành sản xuất pin. Người ta thấy rằng carbon mềm là một công nghệ khá trưởng thành, trong khi carbon cứng có thể là một giải pháp thay thế thú vị, đặc biệt cho các ứng dụng đòi hỏi công suất lớn như trong lĩnh vực xe điện. Các cực dương Titan Oxit đã được sử dụng bởi một số ngành công nghiệp pin.


Graphene cũng được xem xét rộng rãi. Đặc biệt, người ta thấy rằng các tính chất điện của chúng làm cho vật liệu này đặc biệt thích hợp cho các cực dương kim loại / graphene lai (ví dụ graphene với SnO2 và Fe2O3). Các ống nano carbon (CNTs) có ý nghĩa quan trọng đối với kết quả học tập rất thú vị của chúng, mặc dù chi phí sản xuất có thể cản trở việc ứng dụng chúng làm vật liệu hoạt động cực dương trong ngành sản xuất pin trong tương lai.


Tuy nhiên, đối với pin EV lớn, graphit giá rẻ thường được ưu tiên hơn do cân nhắc về chi phí.
Trong loại thứ hai, các vật liệu hợp kim như Si, Ge, SiO, SnO2 đã được mô tả. Những vật liệu này có thể cung cấp công suất lớn hơn và mật độ năng lượng cao so với nhóm trước, bằng cách phản ứng với lithium trong cơ chế điện hóa hợp kim / khử hợp kim. Tuy nhiên, quá trình này có nghĩa là mở rộng khối lượng lớn dẫn đến mất công suất đáng kể khi đạp xe. Việc giảm từ kích thước khối lượng lớn xuống kích thước nano, cùng với việc hiện thực hóa các cấu trúc phức tạp bằng sự kết hợp với ma trận dẫn điện, đã được đề xuất để khắc phục các vấn đề nêu trên và cải thiện hiệu suất tổng thể của anode.
Silicon và SnO2 và composite của chúng với carbon là những vật liệu hứa hẹn nhất cho các ứng dụng trong pin lithium trong tương lai, tuy nhiên, một cách rẻ tiền để sản xuất hàng loạt chúng là vật liệu anốt vẫn cần thiết. Mặt khác, Ge, mặc dù thú vị vì các đặc tính điện hóa của nó và kết quả thí nghiệm xuất sắc trong phòng thí nghiệm nhưng lại có nhược điểm là nguyên tố đứng thứ năm mươi về độ phong phú trong vỏ Trái đất. Do đó, nó có vẻ không phải là một lựa chọn tốt cho việc ứng dụng đại trà công nghệ pin lithium.
Trong nhóm thứ ba, các vật liệu phản ứng với liti theo kiểu phản ứng chuyển đổi đã được mô tả. Đặc biệt, các oxit kim loại / photphua / nitrit / sunfua đã được xem xét. Tuy nhiên, những vật liệu này vẫn còn rất xa so với thị trường pin lithium thương mại rộng lớn, do khả năng duy trì dung lượng kém và độ trễ tiềm ẩn lớn. Do đó, một loạt các dạng cấu trúc nano của các vật liệu này cũng đã được nghiên cứu để giải quyết các vấn đề đã được xác định ở trên.
Công nghệ nano chắc chắn là một cách tiếp cận đáng gờm để tạo ra thế hệ vật liệu cực dương tiếp theo cho pin lithium. Tuy nhiên, để sử dụng các vật liệu được mô tả làm cực dương hiệu quả trong LIB thương mại, đặc biệt là cho các ứng dụng EV, cần phải nghiên cứu thêm. Trên thực tế, cần phải đạt được cả năng lượng cao hơn và mật độ công suất cao hơn cùng với việc phát triển các quy trình chế tạo rẻ tiền để tổng hợp quy mô lớn vật liệu nano. Hơn nữa, việc nghiên cứu các cơ chế quy định sự tương tác giữa liti và các dạng nano của các vật liệu được mô tả cùng với các đặc tính vận chuyển điện tử tại giao diện điện cực / chất điện phân có tầm quan trọng thiết yếu đối với việc thiết kế thế hệ tiếp theo của vật liệu hoạt động anốt được chế tạo bằng công nghệ nano .
Các điện cực âm hiện đang được sử dụng trong pin lithium liên quan đến dung dịch rắn của lithium ở một trong các dạng carbon. Các tế bào liti hoạt động ở nhiệt độ trên điểm nóng chảy của liti nhất thiết phải sử dụng hợp kim thay vì liti nguyên tố. Đây thường là các pha kim loại nhị phân hoặc bậc ba. Ngày càng có nhiều mối quan tâm hiện nay về khả năng sử dụng hợp kim kim loại thay vì cacbon ở nhiệt độ môi trường xung quanh, với mục tiêu giảm thể tích điện cực, cũng như đạt được công suất tăng lên đáng kể. [Robert A. Huggins, Pin nâng cao, Các khía cạnh của Khoa học Vật liệu, Springer, New York, 2009, tr.123].
Graphit là chất lưỡng tính, và cation hoặc anion có thể được chèn vào nó giữa các lớp graphene. Khi các cation được chèn vào, cấu trúc graphit chủ sẽ mang điện tích âm. Ví dụ về cation là Li + , K + , Rb + và Cs + . Khi các anion được đưa vào, cấu trúc graphit chủ sẽ mang điện tích dương và các ví dụ về anion là Br – , SO2 – , SbF6 –
Việc chèn các kim loại kiềm vào cacbon lần đầu tiên được chứng minh vào năm 1926 [K. Fredenhagen và G. Cadenbach, Z. Anorg. Allg. Chèm. 158, 249 (1926)] và sự tổng hợp hóa học của lithium-cacbon đã được chứng minh vào năm 1955 [ D. Guerard, A. Herold, Carbon 13, 337 (1975 )]. tia X Các thí nghiệm quang phổ quang phát xạ cho thấy rằng liti được chèn vào sẽ nhường điện tử của nó cho cacbon, và do đó cấu trúc có thể được xem như các ion Li + chứa giữa các lớp cacbon của cấu trúc graphit
[GK Wertheim, PMTh.M. Van Attekum và S. Basu, Solid State Commun. 33, 1127 (1980)]. Đánh giá chung về công trình ban đầu về việc đưa các loài vào than chì có thể được tìm thấy trong
[LB Ebert, Các hợp chất xen kẽ của than chì, trong Tạp chí Hàng năm về Khoa học Vật liệu,
Tập 6, ed. của RA Huggins, Đánh giá hàng năm, Palo Alto, CA (1976), tr. 181].
Yếu tố quan trọng trong độ tinh khiết của vật liệu làm anốt là cần phải loại bỏ bất kỳ loại ôxy nào trên bề mặt vì chúng sẽ phản ứng với chất điện phân. Để ngăn chặn phản ứng này, các nhà sản xuất nướng than chì ở 1100ºC) trong môi trường khử hoặc làm trơ. Điều này làm tăng chi phí cho các mục đích sử dụng khác, so với than chì. Carbon (90%) được trộn với một số thành phần khác để tạo ra chất bôi trơn cực dương hoặc bùn. Đối với cực âm, polyvinylidene fluoride (PVDF) được sử dụng làm chất kết dính (-5%), và một lượng nhỏ carbon đen được thêm vào để đảm bảo độ dẫn điện. Ngoài ra, n-metyl pyrrolidon (NMP) được sử dụng để hòa tan các vật liệu để tạo thành một hỗn hợp đồng nhất. Áp suất đảm bảo kích thước hạt đồng đều (Sandi 1999).
Lithium titanate (LTO) đang được rất nhiều người quan tâm. Tế bào LTO hoạt động ở nhiệt độ thấp hơn so với các chất hóa học khác và cung cấp mật độ năng lượng cao. Tuy nhiên, các tế bào như vậy bị điện áp danh định thấp hơn, trong khoảng 2,2–2,3 V trên mỗi tế bào. [Norio Takami, Hiroki Inagaki, Yoshinao Tatebayashi, Hidesato Saruwatari, Keizoh Honda, Shun Egusa, J Power Sources 244 (2013) 469-475]
Vật liệu điện cực, thường là graphite, giãn nở 10% trong quá trình sạc. Than chì lấy lại thể tích ban đầu của nó khi các ion liti giảm dần. Các ion liti sẽ không chỉ xen kẽ vào graphit nếu nhôm được sử dụng mà còn được chèn vào dây dẫn, do đó tạo thành hợp kim nhôm – liti. Quá trình ngược lại sẽ xảy ra trong quá trình xả. Nhôm sẽ bị phân hủy sau một vài chu kỳ và sẽ trở nên vô dụng như một bộ sưu tập hiện tại.
Tuy nhiên, nếu điện cực âm được làm từ liti titanat thay vì graphit, tình hình sẽ thay đổi đáng kể. Thế điện cực của Li 4 Ti 5 O 12 cao hơn khoảng 1,4 V so với graphite (điện thế tế bào thấp hơn khoảng 1,4 V, 2,2 V so với 3,6 V). Điều này sẽ ngăn không cho các ion liti xen vào nhôm. Do đó, nhôm được ưa chuộng hơn đồng vì các lý do liên quan đến chi phí và trọng lượng. Li 4 Ti 5 O 12 được sử dụng chủ yếu trong các ứng dụng tĩnh vì điện áp tế bào thấp hơn của nó. [ Călin Wurm và cộng sự, trong Pin Lithium-Ion, Reiner Korthauer (ed), Dịch bởi Michael Wuest và.al., Springer, 2018. Trang 57 ].
Quy trình sản xuất liti titanat: Hỗn hợp titan điôxít và hợp chất liti (bất kỳ một trong số này: liti cacbonat, liti hydroxit, liti nitrat và liti oxit) được thiêu kết trước ở nhiệt độ từ 670 oC đến 800 oC . Thu được hợp chất gồm TiO 2 và Li 2 TiO 3 hoặc hợp chất gồm TiO 2 , Li 2 TiO 3 và Li 4 Ti 5 O 12 . Sau đó, hợp chất được thiêu kết ở nhiệt độ trong khoảng 800 đến 950 ° C. [Tetsuya Yamawaki et.al., US Patent 6.645.673 B2, 2003 Được giao cho Toho Titanium Co., Ltd., Chigasaki]
Pin sạc SCiB ™ của Toshiba (https://www.scib.jp/en/)
SCiB ™ sử dụng oxit titan lithium (LTO) trong cực dương của nó để đạt được sự an toàn, tuổi thọ cao, hiệu suất ở nhiệt độ thấp, sạc nhanh, công suất đầu vào / đầu ra cao và công suất hiệu quả lớn. SCiB ™ đã tìm thấy các ứng dụng rộng rãi trong các ứng dụng xe cộ, công nghiệp và cơ sở hạ tầng, bao gồm ô tô, xe buýt, toa xe lửa, thang máy và nhà máy điện.
Sản xuất bộ tách pin Lithium ion
Có hai loại quy trình: ướt và khô. Các nhà sản xuất Nhật Bản sử dụng một quy trình ướt, trong đó polyme được hòa tan trong dầu. Dầu sau đó được làm bay hơi để lại một lớp màng xốp. Họ sử dụng các polyme có trọng lượng phân tử siêu cao để sản xuất Celgard, ba lớp màng polyme thổi được dát mỏng, kéo xuống và ủ dưới điểm nóng chảy để kiểm soát cấu trúc polyme. Sau đó, tấm được kéo căng nhanh chóng để có được độ xốp.
Có hai loại quy trình: ướt và khô. Các nhà sản xuất Nhật Bản sử dụng một quy trình ướt, trong đó polyme được hòa tan trong dầu. Dầu sau đó được làm bay hơi để lại một lớp màng xốp. Họ sử dụng các polyme có trọng lượng phân tử siêu cao để sản xuất Celgard, ba lớp màng polyme thổi được dát mỏng, kéo xuống và ủ dưới điểm nóng chảy để kiểm soát cấu trúc polyme. Sau đó, tấm được kéo căng nhanh chóng để có được độ xốp.
[Pekala, RW, et al., 2000, “Phân cách: Cơ hội bị bỏ qua để nâng cao hiệu suất pin?” Hội thảo và triển lãm quốc tế lần thứ 17 về Pin chính và phụ, Ft. Lauderdale, Fla., Ngày 6-9 tháng 3]
Quá trình này rất nhạy cảm với các điều kiện vận hành và thậm chí thay đổi theo lô nguyên liệu, vì vậy cần kiểm soát cẩn thận [Linda Gaines và Roy Cuenca, Chi phí pin Lithium ion cho xe cộ, ANL Báo cáo ANL / ESD-42, tháng 5 năm 2000, trang 20] .
Tuy nhiên, độ dày bổ sung cần thiết trong dải phân cách cho các ô EV / HEV sẽ bù đắp cho độ bền bị giảm. [Y. Nishi, trong: M. Wakihara, O. Yamamoto (Eds.), Pin Lithium Ion, Wiley / VCH / Kodansha, Tokyo, 1998, tr. 195.
P. Arora, Z. Zhang, Chem. Rev. 104 (2004) 4419].
Ngoài các đặc tính thông thường như độ bền cơ học tốt, tính thấm chất điện ly, các chất phân tách xốp siêu nhỏ này hiển thị đặc tính bảo vệ trong quá trình lạm dụng tế bào. Ví dụ, nếu nhiệt độ tế bào tăng bất thường do phóng điện quá mức, chẳng hạn, nhiệt sinh ra sẽ làm mềm PE và đóng các vi hạt trong màng. Đây được gọi là dấu phân cách “tắt máy”. Khi quá trình tắt máy xảy ra, quá trình vận chuyển ion giữa các điện cực sẽ bị dừng lại một cách hiệu quả và dòng điện ngừng chạy. Nếu bộ phân tách có thể giữ được tính toàn vẹn cơ học trên nhiệt độ tắt của nó, nó có thể cung cấp mức độ an toàn cho thiết bị; nếu không, các điện cực có thể tiếp xúc trực tiếp, phản ứng hóa học, dẫn đến hiện tượng thoát nhiệt.
Tuy nhiên, có thể do quán tính nhiệt, nhiệt độ có thể tiếp tục tăng ngay cả sau khi tắt máy. Trong điều kiện như vậy, bộ phân tách sẽ nóng chảy và làm ngắn các điện cực, dẫn đến các phản ứng dữ dội và sinh nhiệt. Hiện tượng này được gọi là “sự tan chảy” hoặc “sự cố” của dải phân cách. Do đó, để đảm bảo an toàn cho tế bào, sự chênh lệch giữa nhiệt độ “tắt máy” và “nhiệt độ nóng chảy” phải càng lớn càng tốt.
Các dải phân cách được làm hoàn toàn bằng polyetylen mật độ cao nóng chảy ở 135 ° C và mất tính toàn vẹn cơ học trên nhiệt độ này. Tuy nhiên, các dải phân cách được làm bằng cách ghép các lớp polypropylene và polyethylene duy trì tính toàn vẹn cơ học ít nhất lên đến 165 ° C, điểm nóng chảy của polypropylene. Điều thú vị là mặc dù polyetylen có trọng lượng phân tử siêu cao nóng chảy ở 135 ° C, các thiết bị phân tách được làm từ vật liệu này vẫn giữ được tính toàn vẹn cơ học của chúng lên đến ít nhất 180 ° C vì độ nhớt của vật liệu để nó duy trì tính toàn vẹn về mặt vật lý.
Các thiết bị phân tách tắt là đáng tin cậy và các nhà sản xuất pin lithium-ion đang ngày càng lựa chọn việc kết hợp chúng trong các sản phẩm của họ. Các thiết bị phân tách tắt phổ biến nhất có polypropylene trọng lượng phân tử cao được pha trộn với polyethylene trọng lượng phân tử siêu cao. Ở đây, đặc tính tắt máy độc đáo của polyethylene được kết hợp một cách thuận lợi với tính toàn vẹn cơ học cao của polypropylene ở nhiệt độ cao. Bởi vì việc tắt máy là không thể đảo ngược, một khi được kích hoạt, các dải phân cách này sẽ khiến các tế bào bị hư hỏng vĩnh viễn. [PG Balakrishnan, R. Ramesh, T. Prem Kumar , J. Nguồn điện. 155 (2006) 401–414]
Các vật liệu khác trong pin Lithium ion
Có các vật liệu khác giống như bộ thu dòng điện như nhôm, niken và lá đồng , chất kết dính như chất đồng trùng hợp tyrene-butadiene (SBR) và p olyvinylidene fluoride (PVDF), chất điện phân và dung môi, chất phụ gia dẫn điện cực âm, chất phân tách.
Ưu điểm & Hạn chế của Pin Lithium-ion - Sản xuất tế bào ion liti
Tỷ lệ khối lượng anốt trên catốt
Điều rất quan trọng là không có kim loại lithium nào được hình thành trong quá trình hoạt động của tế bào. Sự lắng đọng của kim loại tạo thành các đuôi gai làm ngắn tế bào bên trong. Việc kiểm soát điện áp trong quá trình sạc và cân bằng tế bào giúp giảm thiểu vấn đề này ở một mức độ rất lớn. Phương pháp chính để kiểm soát sự lắng đọng liti là tỷ lệ giữa công suất cực dương và dung lượng cực âm của các tấm riêng lẻ trong tế bào. Điện cực anot có công suất sử dụng cao hơn catot khoảng 10% . Điều này ngăn chặn sự lắng đọng kim loại liti trên cực dương trong quá trình sạc, vì cực âm quyết định dung lượng của tế bào. Nếu kim loại liti đóng cặn trên bề mặt điện cực, nó sẽ phản ứng với chất điện phân và có thể bắt đầu sự thoát nhiệt.

Hình 21. Tỷ lệ dung lượng cực dương và cực âm trong tế bào ion Lithi
( Nhà cung cấp hình ảnh: Ralph J. Brodd và Kazuo Tagawa, trong Những tiến bộ trong pin Lithium-Ion, Walter A. van Schalkwijk và Bruno Scrosati (Eds), Kluwer Academic Publishers, New York, trang 272, 2002.)
Quy trình lắp ráp tế bào ion liti
Quá trình lắp ráp tế bào cho pin Lithium ion đòi hỏi độ chính xác và độ chính xác khi phủ lớp điện cực âm và dương bằng vật liệu hoạt tính. Quá trình sơn phủ là một yếu tố quan trọng để đảm bảo sản phẩm có công suất cao, độ tin cậy cao. Nếu lớp phủ có chất lượng kém sẽ chỉ tạo ra pin hiệu suất thấp. Các bước ban đầu trong việc chuẩn bị khối lượng hoạt động quyết định kết quả.
Cohen và Gutoff [E. Cohen và E. Gutoff, Công nghệ sơn và sấy hiện đại, Wiley-VCH,
New York, 1992] mô tả phương pháp luận để đạt được kỹ thuật phủ tốt nhất cho một ứng dụng cụ thể, dựa trên tính chất lưu biến của bùn phủ, độ chính xác và tốc độ phủ cần thiết.

Hình 22. Quá trình phủ cực dương và cực âm
( Nhà cung cấp hình ảnh: Ralph J. Brodd và Kazuo Tagawain trong Những tiến bộ trong pin Lithium-Ion, Walter A. van Schalkwijk và Bruno Scrosati (Eds), Kluwer Academic Publishers, New York, trang 273, 2002.)
Biểu đồ quy trình sản xuất pin Lithium ion

Hình 23. BIỂU ĐỒ LƯU LƯỢNG SẢN XUẤT TẾ BÀO ION LITHIUM
[Ralph J. Brodd và Kazuo Tagawa trong Những tiến bộ trong pin Lithium-Ion, Walter A. van Schalkwijk và Bruno Scrosati (Eds.), Kluwer Academic Publishers, New York, trang 271, 2002.]

Tín dụng: Electropaedia https: //www.mpoweruk.com/battery_manrantyuring.htm
Hình 24. Sơ đồ quy trình sản xuất điện cực từ nguyên liệu thô
Cụm tế bào ion lithium




Các nhà sản xuất pin Lithium ion nhằm vào các điểm sau khi lắp ráp các tế bào:
- Các thiết kế cho tế bào Lithium ion phải tạo ra mật độ dòng điện đồng nhất trong toàn bộ khu vực điện cực.
- Để đảm bảo tiếp xúc tốt giữa các vật liệu hoạt động (AM) và bộ thu hiện tại
- Các điện cực có diện tích bề mặt lớn được sử dụng để cung cấp cho các tế bào hiệu suất tốc độ cao. Điều này làm giảm sự phân cực, tức là tổn thất điện áp do động học của các phản ứng điện cực và làm giảm điện áp rơi trên bộ phân tách.
Cấu trúc lỗ và sự kết hợp của các cacbon dẫn điện giúp vật liệu hoạt động tiếp xúc tốt giữa các hạt.
Tiếp xúc tốt là điều cần thiết giữa các vật liệu hoạt động, cacbon dẫn điện và bộ thu dòng điện , để sử dụng đầy đủ các vật liệu hoạt động và mang lại hiệu quả tốt trong quá trình thực hiện tốc độ cao.
Hỗn hợp catốt coban được chuẩn bị từ LiCoO2 (một loại bột màu đen) + chất kết dính PVdF (một loại nhựa nhiệt dẻo fluoropolymer bán tinh thể màu trắng) + N-metyl pyrrolidon (NMP, một chất lỏng hữu cơ không màu) làm dung môi. LICoO2 không dẫn điện, một chất pha loãng dẫn điện, luôn có màu đen carbon, được thêm vào để tăng cường độ dẫn điện của LiCoO2.
Tỷ lệ và lượng nguyên liệu được xác định bởi thiết kế ngăn và kích thước của máy trộn. Quy trình trộn chuyên sâu được sử dụng để trộn khô vật liệu hoạt tính không dẫn điện và carbon trước khi thêm dung môi phủ và chất kết dính.
Hỗn hợp này được trộn khô để tạo ra một lớp phủ đồng nhất của các phần tử của vật liệu hoạt động với một màng mỏng của cacbon dẫn điện để cải thiện tiếp xúc điện giữa AM và lưới thu dòng (lá nhôm, dày 20 mm), do đó đảm bảo sử dụng đầy đủ tất cả AM. Polyme NMP được hòa tan trong dung môi phủ trong một thùng chứa riêng biệt. Hỗn hợp hỗn hợp khô và dung dịch dung môi sau đó được kết hợp để tạo thành một loại bùn.
Các chất bổ sung dung môi được sử dụng để điều chỉnh độ nhớt của bùn (hoặc sơn) cho hoạt động sơn phủ . Polyvinylenedifluoride (PVdF) là chất kết dính được lựa chọn và dung môi là N-methylpyrollidinone (NMP). Bùn từ hoạt động trộn được đặt trong các thùng kín, đóng vai trò là phương tiện chứa và trung chuyển cho các hoạt động phủ. Một lượng chính xác bùn phủ được bơm từ thùng chứa bằng máy bơm bánh răng, hoặc máy bơm chính xác tương tự, để tránh bất kỳ luồng không khí nào trong chất lỏng đi vào đầu lớp phủ.
Hỗn hợp cực dương được chuẩn bị theo cách tương tự với cacbon cứng, chất kết dính PVdF và NMP. Hỗn hợp này được phủ trên một lá đồng được sử dụng làm lưới (độ dày 10 mm).
Lớp phủ được thực hiện trên cả hai mặt với độ dày khoảng 100 mm cho cả cực dương và cực âm. Bằng cách giảm độ dày lớp phủ, tổng diện tích bề mặt sẽ tăng lên đối với một thể tích nhất định của ô. Các chất điện phân hữu cơ được sử dụng có độ dẫn điện thấp hơn so với chất điện phân lỏng và do đó diện tích bề mặt cao hơn này sẽ tạo điều kiện cho một tế bào phóng điện cao.
Độ dày điện cực phụ thuộc vào công suất tối đa yêu cầu. Một tính năng độc đáo của công nghệ sản xuất pin Lithium ion là nó cho phép nhiều thiết kế tỷ lệ công suất / năng lượng với cùng một công nghệ sản xuất điện cực [Broussely, Nazri trang 651]. Nhưng bộ sưu tập hiện tại phù hợp và tab, hình dạng và thiết kế tế bào là quan trọng.
Lắp ráp tế bào: Lá bọc được tráng đi qua tủ sấy để làm bay hơi dung môi và để lại một lượng chính xác khối lượng hoạt động trên lá. Nhiều dung môi phủ được phân loại là nguy hiểm và không được thải vào khí quyển. Như một biện pháp tiết kiệm chi phí, dung môi thường được thu hồi để tái sử dụng trong quá trình này. Để tránh bất kỳ sự ô nhiễm nào của môi trường, dung môi có thể được đốt.
Hầu hết các tế bào ion Lithi đều có hình trụ. Cuộn thạch được làm phẳng để lấy các phần tử cho các tế bào hình lăng trụ .
Các tế bào hình lăng trụ thuận lợi cho việc lấp đầy thể tích tốt hơn, nhưng có khả năng phình ra khi chu kỳ hoặc lão hóa. Các lon tế bào hình trụ cung cấp độ bền cơ học tốt hơn, ổn định kích thước tốt và áp suất đồng nhất trong các phần tử.
Hoạt động phủ tạo ra lớp phủ gián đoạn để phù hợp với chiều dài của cuộn dây. Máy quấn dây được thiết kế để vận hành tự động để sử dụng với các cuộn cực âm và cực dương khô và bộ phân tách (độ dày từ 25mm trở xuống, PP hoặc PE hoặc hỗn hợp).
Các hoạt động bắt đầu bằng cách hàn các mấu vào phần không được phủ của lá. Sau đó, máy quấn dây sẽ cắt dải theo chiều dài thích hợp và cuộn dây kết hợp cực dương-phân tách-cực âm thành một cuộn dây chặt chẽ hoặc suốt chỉ theo kiểu cuộn dây. Khi đường kính lõi quấn tăng lên, máy quấn dây sẽ tự động bù đắp để duy trì lực căng không đổi khi cuộn dây tăng đường kính để có dung sai gần với đường kính. Gió elip đối với các tế bào lăng trụ là một quá trình phức tạp hơn và chậm hơn.
Sau khi cuộn dây, cuộn dây được kiểm tra quần short bên trong trước khi lắp vào lon. Các lon thép phải sạch và được mạ niken để tạo bề mặt ổn định và giảm thiểu sự ăn mòn của lon trước khi lắp ráp ô. Chì cực dương được hàn vào đáy lon và dây dẫn cực âm được hàn vào lỗ thông hơi an toàn. Chất điện phân được thêm vào tế bào đã lắp ráp một nửa. Quá trình lắp ráp hoàn thành với việc gấp mép nắp trên.
Việc loại bỏ sớm các lỗi tế bào tiềm ẩn là một biện pháp kinh tế và ngăn ngừa các tế bào xấu hoạt động nhiều hơn. Suốt chỉ được lắp vào hộp để có thể cung cấp áp suất không đổi để giữ các thành phần của phần tử gần nhau, do đó loại bỏ bất kỳ cơ hội nào cho khoảng trống giữa chúng. Một số nhà sản xuất có thể chèn một trục gá để ổn định tâm của cuộn dây.
Trừ khi tất cả các thao tác được thực hiện trong phòng khô hoặc hộp khô , nước hấp thụ trong các vật liệu hoạt động phải được loại bỏ bằng nhiệt và chân không trước quá trình nạp chất điện phân.
Việc điền đầy chân không chính xác chất điện phân được thực hiện để đảm bảo chất điện phân thấm qua và lấp đầy hoàn toàn các lỗ rỗng có sẵn trong cấu trúc phân tách và điện cực. Máy bơm chính xác đo thể tích tính toán của chất điện phân cần thiết để tế bào hoạt động tốt. Luôn luôn tất cả các nhà sản xuất sử dụng LiPF 6 (một hợp chất tinh thể màu trắng vô cơ) làm chất điện phân và các muối cacbonat mạch vòng (EC, etylen cacbonat) hoặc mạch thẳng (DMC, dimetyl cacbonat, DEC, dietyl cacbonat, hoặc EMC, etyl-metyl cacbonat, v.v.) dung môi cho muối điện phân này.
Chất điện phân dựa trên hỗn hợp dung môi của ethylene carbonate (EC) với dimethyl carbonate (DMC) và / hoặc diethyl carbonate (DEC) thường được sử dụng cho pin lithium ion kết hợp với catốt “4 V” (coban, niken và manganate) vì khả năng oxy hóa cao của dung môi.
Sau khi làm đầy tế bào bằng chất điện phân, tế bào được niêm phong bằng cách nén có kiểm soát của một miếng đệm polyme hoặc grommet đặt giữa hộp tế bào và tấm trên cùng. Áp lực lên miếng đệm vòng đệm polyme được kiểm soát để giữ cho nó nằm trong giới hạn đàn hồi của polyme. Nếu vượt quá giới hạn đàn hồi, polyme nguội sẽ chảy và làm hỏng niêm phong.
Mỗi nhà sản xuất sử dụng một cấu trúc cơ học hơi khác nhau để làm kín các ô nhưng kết quả cuối cùng về cơ bản là giống hệt nhau. Thông thường, một vai hoặc gờ được hình thành gần đầu ô. Điều này đóng vai trò là cơ sở cho con dấu và giữ cho cuộn băng ở vị trí và ngăn chặn việc lồng vào hoặc thay đổi vị trí của suốt chỉ dưới tác động của rung và sốc.
Bất kỳ sự thay đổi nào về vị trí đều gây ra sự thay đổi trong phân bố dòng điện và dẫn đến vòng đời kém hoặc lớp mạ lithium trong các tế bào hiệu suất cao. Con dấu tấm trên cùng của ngăn chứa một lỗ thông hơi, một phần tử hệ số nhiệt độ dương (PTC) và một thiết bị an toàn ngắt dòng điện (CID). Cả CID và PTC đều là các thiết bị an toàn được thiết kế để kích hoạt và ngăn chặn nhiệt độ và áp suất nguy hiểm phát triển bên trong tế bào. Mỗi lô thiết bị được kiểm tra hoạt động thích hợp trước khi đưa vào bộ phận lắp ráp trên cùng.
Sau khi niêm phong được áp dụng, các tế bào có thể được rửa sạch, áo khoác và dán nhãn. Chúng được cấp một số sê-ri để theo dõi ngày sản xuất và để xác định tất cả các thành phần của tế bào (vật liệu điện cực, chất điện phân, chất phân tách và những thứ tương tự). Thông tin về dung lượng và điện áp được lưu trữ cùng với số ô và được sử dụng sau đó để so khớp với các ô để lắp ráp gói.
Các tế bào có thể được hàn bằng tia laze với con dấu bằng thủy tinh với kim loại để cung cấp con dấu kín lâu dài. Với các tế bào lớn hơn, cần phải cẩn thận hơn để đảm bảo hoạt động an toàn, ngay cả trong điều kiện lạm dụng.
Trong khi các quy trình, ở trên, được mô tả cho các ô kín nhỏ được sử dụng trong thiết bị điện tử di động, quy trình cho các pin công nghiệp lớn hơn để lưu trữ năng lượng, không gian và các ứng dụng EV tuân theo cùng một phác thảo chung.
Pin Lithium ion - Sự hình thành và lão hóa
Khi được lắp ráp, các ion Li không được pha tạp vào cacbon cực dương và do đó tế bào không hiển thị điện áp. Trong quá trình sạc ban đầu, một phần các ion Li từ PAM LiCoO 2 không được pha tạp để trở thành Li 1-x CoO 2 và các ion Lithium này được pha tạp vào cực dương cacbon (C y ) để trở thành Li x C y . Khi điện áp sạc đạt 4,1 đến 4,2 V, giá trị của x là khoảng 0,5. (ví dụ: 50%) cho thấy rằng 50% Li từ LiCoO 2 đã được sử dụng.
Một khía cạnh khác cần lưu ý là một phần của các ion Lithium đã pha tạp chất sẽ không quay trở lại và vẫn ở trong cực dương. trong đó, các ion Lithium x-dx ở lại mà không đóng góp vào công suất. Đây là khoảng 10 đến 20% lithium không thể đảo ngược, có nghĩa là hiệu suất của lần sạc ban đầu là 80 đến 90%. Từ chu kỳ thứ hai, lượng không thể thay đổi không tăng và ô hiển thị 100% dung lượng do nhà sản xuất thiết kế.
Sau khi rửa và chạy nhanh, nhưng trước khi bắt đầu quá trình hình thành, điện áp và trở kháng của tất cả các ô đều được ghi lại để loại bỏ bất kỳ ô bị lỗi nào. Sau đó, các tế bào được sạc lần đầu tiên
(sạc ban đầu hoặc sạc hình thành). Các điều kiện của lần sạc đầu tiên rất quan trọng vì ít nhất hai lý do:
1) lớp interphase điện phân rắn (SEI) hình thành trên cực dương để bảo vệ nó khỏi phản ứng tự phát với chất điện phân trong quá trình hoạt động bình thường của tế bào và 2) nó thiết lập sự tiếp xúc điện tốt giữa các vật liệu hoạt động và chất điện phân. Lần sạc đầu tiên tuân theo quy trình được khuyến nghị của nhà sản xuất để sạc pin nhưng thường bắt đầu ở dòng điện thấp hơn và sau đó tăng lên dòng sạc bình thường ở khoảng một phần ba quãng đường của chu kỳ sạc. Các tế bào có thể tiếp tục quay vòng trong giới hạn điện áp để sạc và phóng điện trong một hoặc hai chu kỳ nữa sau khi hình thành.
Sau khi hình thành hoặc chu kỳ, điện áp và dung lượng của tế bào được đo và lưu trữ để sử dụng sau này trong quá trình lựa chọn tế bào . Thời gian lão hóa thay đổi giữa hai tuần và một tháng, tùy thuộc vào nhà sản xuất. Điện áp của các tế bào được đo lại sau khi lưu trữ. Sự khác biệt về điện áp khi bắt đầu và kết thúc khoảng thời gian lưu trữ được sử dụng để sắp xếp các ô có quần ngắn “mềm” hoặc “vi mô”. Các tế bào có quần ngắn bên trong sẽ có điện áp thấp hơn sau khi lưu trữ và tự tách ra khỏi phân phối điện áp và công suất bình thường. Có thể cần phải di tản các tế bào lớn hơn sau khi hình thành để loại bỏ khí hình thành.
Để có mô tả chi tiết về quy trình lắp ráp, bạn đọc tham khảo
- Kaoru Nakajima và Yoshio Nishi Chương 5 trong: Hệ thống lưu trữ năng lượng cho thiết bị điện tử, Ed Tetsuya Osaka và Madhav Datta, Gordon and Reach Science Publishers, Amsterdam, 2000.
- Quy trình sản xuất tế bào Lithium-Ion, Ralph J. Brodd và Kazuo Tagawa, Chương 9 trong: Những tiến bộ trong pin Lithium-Ion, Walter A. van Schalkwijk và Bruno Scrosati (Eds), Kluwer Academic Publishers, New York, trang 273, 2002 .
- Pin Lithium, Khoa học và Công nghệ, ed. của GA Nazri và G. Pistoia, Springer, New York, 2009.
- Pin Lithium-Ion, Reiner Korthauer (ed) (2018), được dịch bởi Michael Wuest và.al., Springer, 2018.
- Kazuo Tagawa và Ralph J. Brodd, Quy trình sản xuất chế tạo pin Lithium-Ion trong Pin Lithium-Ion, Yoshio M., Brodd RJ, Kozawa A. (eds) Springer, New York, NY. https: //doi.org/10.1007/978-0-387-34445-4_8]
- Zhang Z., Ramadass P. (2012) Hệ thống và Công nghệ Pin Lithium-Ion. Trong: Meyers RA (ed) Encyclopaedia of Sustainable Science and Technology. Springer, New York. https: //doi.org/10.1007/978-1-4419-0851-3_663
- Sổ tay Hóa học thiết kế gói pin Lithium-Ion, Thành phần, Loại và Thuật ngữ, John Warner, Elsevier, 2018




