Cómo funciona la batería de iones de litio
La percepción del público es que las baterías de plomo-ácido son una tecnología antigua. La batería de iones de litio tiene una percepción diferente, es moderna, más limpia, tiene una densidad de energía 3 o 4 veces mayor y un ciclo de vida más largo. Con todo esto, ¿qué posibles ventajas podría aportar la tecnología de plomo-ácido de 150 años de antigüedad? Bueno, en realidad, no todo es lo que parece, mire detrás de los titulares los datos utilizados en las afirmaciones de marketing, y luego aplique un poco de sentido común, investigación básica y algo de ciencia rudimentaria. Descubrirá que la historia real es bastante diferente.
El primer error se refiere a las densidades de energía volumétrica y específica. Los valores de 4 a 5 veces se refieren únicamente a la densidad de energía específica y a un número limitado de químicas de baterías de iones de litio, algunas de las cuales aún no se utilizan comercialmente. Fig. 2 compara varios cátodos para pilas de iones de litio, que van desde unos 100 Wh/kg para la química Li-FePO4 más segura hasta más de 200 Wh/kg para la variante de níquel-cobalto-óxido de aluminio. A continuación se presenta el diagrama de la batería de plomo-ácido:


Estos valores sólo se aplican al nivel de una sola célula, no al paquete o al estado en servicio. Fig. 3 muestra las densidades energéticas de diferentes químicas de baterías a nivel de célula y de sistema. Las densidades energéticas de las celdas de las baterías de iones de litio se reducen prácticamente a la mitad cuando están completamente instaladas con todos los equipos de conexión, refrigeración, seguridad y gestión de la batería.
La ventaja a nivel de célula de 3 a 5 veces la densidad de energía específica se reduce a 2 o 3 veces. Dependiendo de la química del cátodo de litio, podríamos estar casi a la par con la densidad energética de las baterías de iones de litio y las de plomo-ácido para un sistema de baterías completamente instalado en algunas aplicaciones.
El otro factor, el del ciclo de vida, también es fuente de confusión. ¿Cuántos ciclos puede realizar una batería de iones de litio antes de que su capacidad caiga por debajo del 80% de su capacidad nominal? ¿Dos, tres mil? La tabla 1 ofrece un resumen de los diferentes materiales para cátodos de iones de litio en cuanto a su rendimiento y vida útil.
Ventajas de la química de las baterías de plomo-ácido
Las baterías son dispositivos extraños. Nadie los quiere, pero todos los necesitan. Sólo se compran cuando se necesitan. ¿Cuántas personas planean un viaje al centro comercial local para comprar pilas? Son una compra de rencor y sólo se compran cuando es absolutamente necesario. Un buen vendedor puede venderte dos pares de zapatos, dos coches y quizás dos casas si tienes el dinero, pero no puede venderte dos baterías de automóvil SLI. Cuando compras una batería, ya sea una batería solar para un panel solar, una bicicleta eléctrica o un sistema de respaldo de baterías de SAI e inversor o una batería de tracción para carretillas elevadoras, ¿no te gustaría saber más sobre ella?
¿Cómo funcionan las baterías de plomo-ácido, cuáles son las diferencias entre tipos y modelos, y qué hay de los diferentes tipos de química? Pueden ser caros. En una aplicación comercial o doméstica, ¿cuál es la rentabilidad, la vida útil y el coste de sustitución de una batería de plomo? ¿El tamaño que necesita, el espacio disponible, la eficiencia energética de la batería de plomo y el tiempo de recarga? Además, están los costes ocultos de la seguridad, la eliminación y la huella de carbono. En este artículo se comparan las baterías de plomo-ácido con las de iones de litio y se abordan muchos de los conceptos erróneos asociados a estos dos productos químicos.
Qué batería de iones de litio es mejor
| Material del cátodo | Nombre corto | Tensión nominal | Energía específica Wh/kg (célula) | Ciclo de vida | Comentarios |
|---|---|---|---|---|---|
|
Óxido de cobalto y litio (LiCoO2) |
LCO | 3.6 | 150-200 | 500-1000 | Dispositivos portátiles: desbordamiento térmico por sobrecarga |
| Óxido de litio y manganeso (LiMn2O4) | OVM | 3.7 | 100-150 | 300-700 | Herramientas eléctricas y dispositivos médicos: más seguros que el LCO |
| Óxido de litio, níquel, manganeso y cobalto (LiNiMnCO2) | NMC | 3.6/3.7 | 150-220 | 1000-2000 | Bicicletas eléctricas, vehículos eléctricos, industria - alta duración del ciclo |
| Fosfato de litio y hierro (LiFePO4) | LFP | 3.2 | 90-120 | 1000-2000 | EV, SLI, Leisure - la más segura de todas las baterías de iones de litio |
| Óxido de litio, níquel, cobalto y aluminio (LiNiCoAlO2) | NCA | 3.6 | 200-260 | 500 | Industrial, tren motriz EV (Tesla) TR a 150C, CL 500 |
| Titanato de litio (Li4Ti5O12) | LTO | 2.4 | 50-80 | SAI, energía solar, tren motriz para vehículos eléctricos (Honda, Mitsubishi). CL 3000-7000 - muy seguro |
Como se puede ver, todos se sitúan en la franja de los 800 a los 2000 ciclos. En comparación, una batería de plomo-ácido bien diseñada puede alcanzar fácilmente más de 1600 ciclos al 80% de DOD. Entonces, ¿cómo se explica todo esto cuando se considera el coste de propiedad? Esto nos lleva al siguiente punto, que es el precio de las baterías de plomo. ¿Cuánto cuesta una batería de iones de litio en comparación con una batería de plomo? ¿Costo de la planta de fabricación de baterías de iones de litio? Naturalmente, la batería de iones de litio es más cara, pero cuánto más. De nuevo, esto depende del nivel que se considere. Los comunicados de prensa nos dirán que los precios de los iones de litio están bajando y que ahora están en el rango de 2-3 veces el del plomo-ácido.
¿De verdad? Los precios medios en una búsqueda reciente en Internet en el Reino Unido para obtener los precios de las baterías de ocio disponibles en el mercado de 12V y 100 Ah, tanto para las baterías de iones de litio como para las de plomo:
batería de iones de litio $960 o $800/kwh
Batería de plomo 215 dólares o 180 dólares/kwh
Obviamente, la vida de la batería de iones de litio tiene que ser 4 veces superior a la de la batería de plomo equivalente para obtener el mismo valor. Como hemos visto, este no es el caso.


En todos los casos, la construcción de la batería de plomo-ácido fue la más rentable, incluso cuando se instaló una batería de plomo-ácido más grande para obtener una mejor aceptación de la carga y una mayor vida útil del ciclo. En este ejemplo, la aplicación era una torre de telecomunicaciones en la India. El mismo principio es válido en la mayoría de las aplicaciones y geografías, más aún en los climas más fríos. La otra idea errónea es que el Li-ion es una tecnología más limpia y menos contaminante que el plomo-ácido. Las emisiones de la cuna a la puerta para diferentes químicas de baterías se dan en las Figs. 5 y 6.
Esta figura muestra el límite de operaciones para la fabricación de baterías. Desde la extracción y el transporte de las materias primas, pasando por todas las etapas de procesamiento, hasta el punto en que las baterías están listas para ser enviadas.
La tabla 2 es una situación real en la que se comparan los aspectos económicos del uso de una batería de iones de litio y de una batería de plomo-ácido que funcionan durante diferentes periodos de vida.
| Partida de gastos | Costes diarios de funcionamiento USD | Costes diarios de funcionamiento USD |
|---|---|---|
| 3 años | Batería de plomo-ácido | Batería de iones de litio |
| Amortización | 8.30 | 16.90 |
| Diesel (entregado) | 15.50 | 15.50 |
| Mantenimiento | 2.46 | 2.46 |
| Electricidad | 1.47 | 1.47 |
| Carga de la batería | 0.65 | 0.50 |
| Total día/mes | 28.38/851 | 36.83/1105 |
| 6 años | ||
| Amortización | 5.86 | 8.46 |
| Diesel | 15.50 | 15.50 |
| Mantenimiento | 2.46 | 2.46 |
| Electricidad | 1.47 | 1.47 |
| Carga de la batería | 0.54 | 0.50 |
| Total día/mes | 25.83/775 | 28.39/852 |
Estos datos, procedentes de los Laboratorios Nacionales Argonne, muestran que el proceso total de fabricación, incluyendo la extracción y el transporte de las materias primas para las baterías de iones de litio, es más de 4 veces superior al valor del ácido de plomo. En cuanto a la extracción de materiales, el suministro de materiales básicos para los cátodos, como el cobalto y el manganeso, y el litio no son del todo seguros. Los procesos de extracción y recuperación existen, pero el número de minas y centros de fabricación puede limitar la oferta si la demanda aumenta considerablemente. El mapa geopolítico también predice la incertidumbre de algunas fuentes de estos materiales.
¿Son reciclables las baterías de iones de litio?
La reciclabilidad y la seguridad de estos productos químicos son factores importantes. Se sabe que casi todos los componentes de las baterías de plomo-ácido se reciclan al 100%, mientras que no existen procesos comerciales para reciclar las baterías de iones de litio. Esta situación es comprensible si se tiene en cuenta que los componentes más caros de Li, Co, Mn, etc. son sólo una pequeña fracción del total de la batería de iones de litio. Por ejemplo, el litio representa alrededor del 4% del peso total de la célula. A esto hay que añadir el hecho obvio de que el litio es altamente reactivo (la base de su alta densidad energética), lo que comprensiblemente hace que sea caro extraerlo de los residuos.
El factor adicional de la complejidad con muchos materiales diferentes en su construcción dificulta el reciclaje, tanto técnica como económicamente. ¿El resultado? Sencillamente, no hay ningún incentivo comercial para reciclar estas baterías. Por esta razón, las instalaciones de reciclaje están todavía en fase piloto y, en su mayoría, financiadas por el gobierno.
En la actualidad, la gran mayoría de las baterías de iones de litio desechadas se encuentran almacenadas a la espera de un avance tecnológico o de una legislación que obligue a su reciclaje. Si se aplicara esto último, habría un coste, en última instancia, para el consumidor. Esto aumentaría aún más el precio de la célula de iones de litio en comparación con los tipos de baterías de plomo-ácido.
¿Puede explotar la batería de iones de litio?
Por último, tenemos la seguridad. Que sepamos, ninguna aplicación de baterías de plomo-ácido ha sido objeto de una retirada de seguridad, como sabemos que es el caso de las baterías de iones de litio de los dispositivos electrónicos portátiles e incluso de los vehículos eléctricos. Fig. 7 muestra lo que le ocurrió a un nuevo Volvo híbrido en el Reino Unido hace apenas un par de semanas, en el momento de escribir este artículo. En este caso, sus baterías de iones de litio se incendiaron mientras se cargaban.
Incendios de baterías de iones de litio
Figura 7 Incendio provocado por una batería de iones de litio en un vehículo eléctrico híbrido de Volvo: Abril de 2018-residencia del Reino Unido


Este vídeo muestra un incendio muy reciente causado por una batería de litio. Posiblemente debido a un desequilibrio en las células y un BMS inadecuado.
Incluso cuando se almacenan o transportan, las baterías de iones de litio han sido la causa de incendios gravemente peligrosos. Aunque estas ocasiones son raras, hay que reconocerlas, y hay que instalar un equipo de seguridad adecuado y un software de gestión de la batería. Los bomberos de Nueva York, por ejemplo, todavía están decidiendo cómo abordar los incendios de baterías de iones de litio. Esto sugiere que es necesario revisar las medidas de seguridad existentes para las baterías de iones de litio en todo el mundo.
A continuación, la opinión del Departamento de Bomberos de Nueva York:
Cita del artículo de noticias: Conducción de servicios públicos de AWS 15 de noviembre de 2016 «El fuego no es el mayor problema», dijo Rogers. Los bomberos están formados para hacer frente a los incendios, pero tienen que saber a qué se enfrentan. Las baterías de iones de litio pueden liberar ácidos tóxicos y vapores inflamables. Algunos de esos vapores son consumidos por el fuego, pero si no lo son, podrían inflamarse o ser un problema para los bomberos. El mayor problema es lo que ocurre en el «postoperatorio», es decir, después de extinguir el fuego. Incluso si una batería se apaga puede volver a encenderse hasta 72 horas, dijo Rogers. -Lt. Departamento de Bomberos Paul Rogers de la división de operaciones de materiales peligrosos de Nueva York»
¿Batería de iones de litio o batería de plomo?
La batería de iones de litio tiene sin duda mejores características de rendimiento que la de plomo-ácido. Sin embargo, estas ventajas se ven muy reducidas por el hardware adicional asociado a los requisitos de seguridad y gestión. El resultado neto es que las baterías de plomo-ácido tienen claras ventajas, especialmente cuando se consideran aplicaciones que no están restringidas por el peso o la aceptación de carga. El menor coste inicial de la planta de fabricación de baterías de plomo-ácido; El bajo precio de compra y el bajo coste de amortización del plomo-ácido, combinados con su bajo impacto medioambiental y su seguridad inherente, proporcionan las siguientes ventajas
- Precio de compra más bajo. El precio es aproximadamente la cuarta parte de un equivalente de Li-ion. Los menores costes de funcionamiento para dar un menor coste total de propiedad en la mayoría de las aplicaciones.
- Reciclabilidad. Casi el 100% de los materiales de las baterías de plomo se reciclan. El valor de la chatarra puede proporcionar unos ingresos adicionales de hasta el 20% del coste del material de la batería. Las baterías de litio no tienen infraestructura ni proceso comercial para su reciclaje
- La seguridad. La química del plomo-ácido es intrínsecamente más segura que la de la batería de iones de litio
- La sostenibilidad. Hay muchas fuentes de suministro de plomo-ácido bien establecidas, sobre todo en las instalaciones de reciclaje. El litio y otros materiales catódicos pueden proceder de zonas políticamente sensibles. Tanto la actual capacidad mundial de extracción de materiales como la de fabricación no permitirían un rápido aumento de la producción de baterías de iones de litio.
- Huella de carbono. La fabricación de baterías de plomo-ácido tiene una huella de carbono de la cuna a la puerta de un tercio de la de las baterías de iones de litio.
Una imagen diferente a la que pintan las empresas de baterías de iones de litio. Aunque no se puede argumentar que el plomo-ácido tiene una desventaja en cuanto a densidad energética, el hecho es que la batería de plomo-ácido sigue siendo muy segura, competitiva y la mejor opción de tecnología de baterías en muchas aplicaciones.
Qué es la batería de iones de litio
Materiales del cátodo y del ánodo: Aunque las pilas de hidruro metálico de níquel (Ni-MH) fueron las preferidas inicialmente en la década de 1990, el primer producto comercial de pilas de iones de litio fue lanzado en 1991 por Sony Corporation. Además del alto contenido energético, tanto en masa como en volumen, esta batería también ofrecía excelentes características de baja temperatura, características de carga y características de ciclo. Como resultado, rápidamente capturó el mercado y se convirtió en una fuente de energía indispensable para equipos de audio y vídeo, ordenadores personales, teléfonos portátiles y otros equipos portátiles
La tecnología actual de baterías avanzadas comenzó con el descubrimiento de la alta conductividad iónica de la fase sólida NaAl11O17, llamada β-alúmina de sodio, por Kummer y sus colaboradores en el laboratorio de Ford Motor Co. [1. Olof Ramsrtomström, sobre el premio Nobel de Química, Antecedentes científicos del Premio Nobel de Química 2019; 2. Y.F.Y. Yao y J.T. Kummer, J. Inorg. Nucl. Chem. 29, 2453 (1967)].
Esto llevó a comprender que el transporte iónico en los sólidos puede ser realmente muy rápido, y que podría conducir a una variedad de nuevas tecnologías. Poco después, los investigadores de Ford demostraron que se puede utilizar un electrolito sólido altamente conductor para producir un tipo de batería completamente nuevo, utilizando sodio fundido en el electrodo negativo y una solución fundida de sodio en azufre como electrodo positivo, con el electrolito sólido conductor de sodio entre ambos [N. Weber y J.T. Kummer, Proc. Annual Power Sources Conf. 21, 37 (1967) ].
Como era de esperar, pronto se estudió la posibilidad de utilizar sistemas de litio análogos, ya que se reconoció que una célula de litio equivalente debería producir voltajes más altos que una célula de sodio. Además, el litio tiene un peso menor que el sodio, otra ventaja.
El litio elemental no podía utilizarse, debido a su bajo punto de fusión. En su lugar, se investigaron las aleaciones sólidas de litio, principalmente los sistemas Li/Si y Li/Al [R.A. Huggins, J. Power Sources 81-82, 13 (1999)].
En esa época se investigaron varios materiales como reactivos de electrodos positivos, y se prestó mayor atención al uso de FeS o FeS2. Al reaccionar con el litio, estos materiales sufren reacciones de reconstitución, con la desaparición de las fases iniciales y la formación de otras nuevas [D.R. Vissers, Z. Tomczuk y R.K. Steunenberg, J. Electrochem. Soc. 121, 665 (1974)].
¿Cuándo se inventó la batería de iones de litio?
El profesor Whittingham exploró la intercalación electroquímica en dichos materiales y en 1973 propuso dichos materiales como electrodos en baterías. Este trabajo dio lugar a una batería recargable que funcionaba en 1976. La célula conseguida estaba compuesta por litio metálico como ánodo y sulfuro de titanio (TiS2) como cátodo, con hexafluorofosfato de litio(LiPF6) como electrolito en carbonato de propileno (PC) como disolvente. Estos prometedores estudios inspiraron a Whittingham a explorar la intercalación electroquímica en dichos materiales como electrodos en baterías. Posteriormente, en 1976, se demostró una batería recargable que funcionaba.
(a) Whittingham, M. S. Electrointercalación en disulfuros de metales de transición. J. Chem. Soc., Chem. Commun. 1974, 328-329.] (con Exxon Research and Engineering Company).
(b)Whittingham, M. S. Batterie à Base de Chalcogénures. Patente belga nº 819672, 1975.
(c)Whittingham, M. S. Almacenamiento de energía eléctrica y química de intercalación. Science 1976, 192 (4244), 1126-1127.
Pero el éxito duró poco. Al repetir los ciclos, el litio metálico formó dendritas en la superficie del metal al ciclar, lo que dio lugar a cortocircuitos.
Este problema impulsó la búsqueda de soluciones alternativas y se propuso una configuración de «célula de transferencia de iones» (también llamada «silla mecedora»), en la que ambos electrodos pueden albergar iones.
Si un material de electrodo positivo contiene inicialmente litio y una parte o todo el litio se elimina durante la primera carga, la célula desarrolla potencial. Por lo tanto, es posible tener materiales de electrodos positivos que reaccionen con el litio a potenciales superiores a unos 3V, si ya contienen litio, y este litio puede ser extraído electroquímicamente.
¿Quién inventó la batería de iones de litio?
Este enfoque, que implica el uso de materiales en los que el litio ya está presente, fue demostrado por primera vez por el profesor Goodenough. Los primeros ejemplos de materiales que contenían inicialmente litio, y que eliminaban electroquímicamente el litio de ellos, fueron los trabajos sobre Li1-xCoO2 en 1980.
[K. Mizushima, P.C. Jones, P.J. Wiseman y J.B. Goodenough, Mater. Res. Bull. 15, 783 (1980)] y Li1-xNiO2
[J.B. Goodenough, K. Mizushima y T. Takada, Jpn. J. Appl. Phys. 19 (Suppl. 19-3), 305 (1980)].
Paralelamente al desarrollo del ánodo, también se buscaron mejores materiales para el cátodo con el fin de adquirir una mayor emf de la célula en combinación con ánodos de mayor potencial que el litio metálico. En 1979/1980 se produjo un gran avance cuando John B. Goodenough y sus colaboradores de Oxford
University, Reino Unido, descubrió que el LixCoO2, otro calcogenuro metálico intercalado del tipo MX2, podía servir como material catódico.
[Goodenough, J. B.; Mizushima, K. Fast Ion Conductors. Patente estadounidense nº 4.357.215, 1982].
[Mizushima, K.; Jones, P. C.; Wiseman, P. J.; Goodenough, J. B. LixCoO2 (0<x<-1): Un nuevo
Material de cátodo para baterías de alta densidad energética. Mater. Res. Toros. 1980, 15 (6), 783-789].
La estructura del material era análoga a la del LixTiS2 con huecos de van der Waals entre el dióxido de cobalto (CoO2) capas en las que los iones de litio podrían unirse sin mucha expansión de la red. Goodenough razonó que cuando X en MX2 es un elemento electronegativo pequeño, un proceso de captación de cationes resultante estaría asociado a un gran cambio de energía libre negativa y a un alto voltaje de la célula (ΔG = -nFE). Con una X de oxígeno, la situación se consideró especialmente prometedora, dado también que se propuso que los iones de litio fueran lo suficientemente móviles en conjuntos de oxígeno muy empaquetados.
El razonamiento resultó ser correcto, y el material CoO2 mostró un potencial muy alto de ~4 a 5 V en relación con el Li+/Li. Los estudios electroquímicos se realizaron en este caso con un electrolito compuesto por tetrafluoroborato de litio (LiBF4) en carbonato de propileno.
Este descubrimiento permitió el uso de materiales anódicos con potenciales más altos que el metal de litio, lo que impulsó la búsqueda de materiales carbonosos adecuados. Teniendo en cuenta la dificultad de resolver el problema de la intercalación electroquímica del grafito, se investigaron otras opciones.
¿Dónde se inventó la batería de iones de litio?
En 1985 se produjo un gran avance cuando un grupo japonés dirigido por Akira Yoshino (de Asahi Kasei Corporation) descubrió las fibras de carbono cultivadas en fase de vapor (VGCF) y posteriormente el coque de petróleo tratado térmicamente. Se sabía que este último material contenía una mezcla de dominios cristalinos (grafíticos) y no cristalinos, y los investigadores pudieron identificar calidades particularmente estables, pero de alto rendimiento, con grados específicos de cristalinidad.
[Akira Yoshino, The Birth of Li-Ion Battery, Angewandte Essays, Angew. Int. Ed., 2012, 51, 5798-5800]
Con estos eficaces materiales para el ánodo, Yoshino desarrolló una batería de iones de litio eficaz y operativa basada en la configuración de celdas de transferencia de iones. Así, el material carbonoso identificado se utilizó como ánodo y el material LixCoO2 de Goodenough (que suele contener pequeñas cantidades de estaño) se utilizó como cátodo. Se utilizaron capas separadoras compuestas de polietileno o polipropileno y el electrolito estaba compuesto por perclorato de litio (LiClO4) en carbonato de propileno (PC).
Yoshino también demostró la seguridad de esta batería en 1986 dejando caer un peso sobre ella. No se produjeron incendios ni explosiones, mientras que las pilas con ánodo de metal de litio reaccionaron violentamente.

Figura 8. Las primeras pruebas de seguridad de Yoshino con su batería de iones de litio en 1986.
A) El momento en que un bulto de hierro choca con la batería
B) Prototipo de batería de iones de litio tras la colisión
C) Batería metálica de ánodos de litio después de la colisión
[Crédito: Akira Yoshino, The Birth of Li-Ion Battery, Angewandte Essays, Angew. Int. Ed., 2012, 51, 5798-5800 ]
Estos descubrimientos y desarrollos condujeron finalmente al lanzamiento de una batería de litio comercial
en 1991. Con un mayor desarrollo, la batería de iones de litio fue comercializada por Sony en 1991 y por una empresa conjunta de Asahi Kasei y Toshiba en 1992.
[Nishi, Y., The Development of Lithium Ion Secondary Batteries. Chem. Rec. 2001, 1, 406-413].
La batería se basaba en un material anódico a base de coque de petróleo, LixCoO2 como cátodo, y un electrolito sin agua compuesto por hexafluorofosfato de litio (LiPF6) en carbonato de propileno (PC). El voltaje de carga fue alto (hasta 4,1 V), con una energía específica registrada de ~80 Wh/kg y una densidad energética de ~200 Wh/litro.
En comparación con otras baterías que había en el mercado en ese momento, la batería de litio se hizo rápidamente muy competitiva y esencialmente allanó el camino para la próxima revolución móvil.
Más o menos al mismo tiempo, se descubrió que el grafito podía utilizarse en combinación con una composición de electrolito adecuada. [Fong R, Sacken U von, Dahn J. R., Studies of Lithium Intercalation into Carbons Using Nonaqueous Electrochemical Cells. J. Electrochem. Soc. 1990, 137 (7), 2009-2013].
Mediante el uso de disolventes que contienen carbonato de etileno, hasta ahora generalmente descartado debido a su mayor punto de fusión, se formó una interfase de electrolito sólido (SEI) en la superficie del electrodo de grafito durante el ciclo de carga/descarga, protegiendo así el material de carbono de la exfoliación y la posterior descomposición. [Peled, E. The Electrochemical Behaviour of Alkali and Alkaline Earth Metals in Nonaqueous Battery Systems, The Solid Electrolyte Interphase Model. J. Electrochem. Soc. 1979, 126 (12), 2047-2051.
Este descubrimiento fue rápidamente adoptado por la comunidad de baterías, y se desarrolló una batería de iones de litio de nueva generación basada en el grafito como material anódico. Con este material anódico, se produjeron poco después baterías con voltajes de carga de 4,2 V, lo que dio lugar a una densidad energética de ~400 Wh/litro.
El desarrollo de la batería de iones de litio no se detuvo con estos importantes descubrimientos, sino que desde entonces se han registrado muchas mejoras y alternativas. Por ejemplo, se han identificado continuamente nuevos materiales catódicos para su uso en aplicaciones específicas de baterías, y dos de estos materiales proceden del grupo de Goodenough: el material de espinela Li1-xMn2O4 y el material de olivino LixFePO4 (LFP).
[Padhi, A. K.; Nanjundaswami, K. S.; Goodenough, J. B. Phospho-Olivines as Positive-Electrode Materials for Rechargeable Lithium Batteries. J. Electrochem. Soc. 1997, 144, 1188-1194.
Thackeray, M. M.; David, W. I. F.; Bruce, P. G.; Goodenough, J. B. Lithium Insertion into Manganese Spinels. Mater. Res. Bull. 1983, 18, 461-472].
Este último material está limitado por un potencial frente al Li+/Li algo menor que el LixCoO2, pero tiene una gran estabilidad y puede utilizarse a altas velocidades de carga. También se han descubierto otros materiales de electrodos y sistemas de electrolitos, lo que ha dado lugar a materiales de almacenamiento de energía cada vez mejores en beneficio de la sociedad.
¿Qué tipo de batería se utiliza en los vehículos eléctricos?
Hoy en día, la mayoría de los vehículos eléctricos utilizan baterías de iones de litio. Anteriormente, se utilizaban baterías de Ni-MH y de plomo, pero su uso fue disminuyendo poco a poco debido a la llegada de las baterías de iones de litio, que poseen mayores valores de energía específica y densidad energética. La energía específica de las baterías de plomo-ácido es de unos 40-50 Wh/kg, mientras que la batería de iones de litio tiene unos 150 Wh/kg. El valor de la densidad energética de las baterías de plomo-ácido es de 80-100 Wh/litro, mientras que las de iones de litio tienen más de 250 Wh/litro.
Las celdas cilíndricas con cátodos de níquel-cobalto-aluminio (NCA) y ánodos compuestos de silicio/grafito, como los utilizados en los últimos paquetes de baterías de Tesla (2019-2020), han alcanzado aproximadamente 270 Wh/kg y 650 Wh/litro. Una nueva tecnología llamada Licerion de Sion Power afirma tener una energía específica de 500 Wh/kg y una densidad de energía de 1000 Wh/L y >450 ciclos en células de desarrollo de 0,4 Ah.
En el caso de las baterías pequeñas, se habla en términos de Wh. Para los sistemas de mayor capacidad, se utiliza la unidad kWh. El valor del Wh dividido entre 103 dará el kWh.
Así, 850 Wh = 850/1000 = 0,850 kWh.
Las celdas utilizadas en las baterías de los vehículos eléctricos actuales pueden alcanzar una energía específica nominal de 140 -170 Wh/kg. La energía específica del paquete de baterías resultante suele ser entre un 30% y un 40% menor, es decir, entre 80 y 120 Wh/kg. La reducción se debe a varios cables de conexión en serie y en paralelo, al BMS y al sistema de gestión térmica (refrigeración o calefacción). En 2019, el porcentaje del paquete de componentes no celulares ha bajado a cerca del 28 %.
Hasta ahora, las células se ponían primero en módulos y luego en paquetes. Ambos Contemporary Amperex Technology Co. Limited, China (CATL) y Tesla han decidido que quieren deshacerse de los módulos y colocar las células en paquetes directamente. CATL ya lo ha hecho y lo llama tecnología cell-to-pack . Aunque la información al respecto es escasa, la empresa afirma que esto puede aumentar la energía específica en un 10-15% y mejorar la utilización del volumen en un 15-20%. En total, se dice que puede reducir las piezas necesarias para los paquetes de baterías en un 40%. [https ://cleantechnica.com/2020/02/18/how-catl-lithium-iron-phosphate-batteries-could-be-leading-to-100-kwh-tesla-model-3/]
Designación de la batería de litio
La Comisión Electrotécnica Internacional (CEI) y la Institución India de Normalización han establecido una denominación común para describir la química y el tamaño de las pilas de iones de litio.
[Pilas y baterías de litio secundarias para aplicaciones portátiles, Comisión Electrotécnica Internacional, IEC 61960-1 e IEC 61960-2 e IS 16047: 2012].
Las letras designan la química y el factor de forma, mientras que los números especifican las dimensiones físicas de la célula. La primera letra describe la química general, la segunda letra designa la química específica del cátodo y la tercera letra designa la forma.
Primera letra: I – Química de iones de litio
Segunda letra: C- cobalto, F- hierro, Fp – fosfato de hierro, N- níquel, M-manganeso, Mp- fosfato de manganeso, T- titanio, V -vanadio y x – otros.
Tercera letra: R- cilíndrica, P-prismática
Los dos primeros números que siguen designan el diámetro en mm y los tres últimos la altura en décimas de mm. Así, una célula designada ICR19/66 es una célula de iones de litio con un cátodo de cobalto que tiene un diámetro que es > 18 mm y ≤ 19 mm y una altura total máxima que es > 65 mm y ≤ 66 mm.
Para las celdas prismáticas, las letras iniciales tienen el mismo significado, pero los dos primeros números designan la anchura en mm, los dos siguientes la altura en mm y los dos últimos la longitud en mm. Así, la denominación de célula IMP9/35/150 describe una célula prismática de iones de litio con una célula de cátodo de manganeso cuyo espesor máximo es > 8 mm y ≤ 9 mm y una anchura máxima que es > 34 mm y ≤ 35 mm y una altura total máxima que es > 149 mm y ≤ 150 mm.
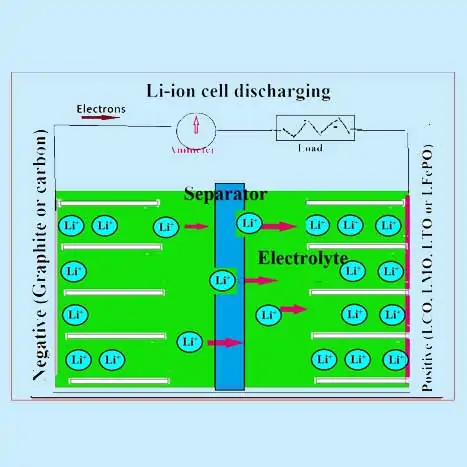
¿Cómo funciona una batería de iones de litio?
cómo se fabrica la batería de iones de litio
El litio metálico con número atómico 3, densidad de 0,534 g/cc, con un potencial de reducción estándar muy bajo (par Li+/Li -3,05 V frente a SHE) y una capacidad específica teórica de 3.860 Ah/kg (2.061 mAh/cc) es el más ligero, el de mayor tensión y el de mayor densidad energética de todos los metales. (Compárese con el plomo de número atómico 82, densidad 11,29 g/cc, capacidad específica teórica de 257,8 Ah/kg y potencial de reducción estándar de -0,35V frente a SHE).
Batería de iones de litio - Materiales activos
Los materiales activos del electrodo positivo son cualquiera de los óxidos mixtos como LiCoO2 o LiMnO2 o LiFePO4. El electrodo negativo es principalmente grafito y compuestos de carbono amorfo. Se utiliza un electrolito orgánico (que contiene una sal conductora de litio disociada, como LIPF6). Se utiliza un separador de polipropileno (PP) o de polietileno (PE) o mixto. Los iones de litio migran de un lado a otro de los electrodos de las baterías de iones de litio durante la carga y la descarga y se intercalan en los materiales activos, como se describe a continuación:

Figura 9. Despiece de una célula de iones de litio
Crédito: Zhang Z., Ramadass P. (2012) Lithium-Ion Battery Systems and Technology. En: Meyers R.A. (eds) Encyclopaedia of Sustainability Science and Technology. Springer, Nueva York, NY, pp 6124. http s://doi.org/10.1007/978-1-4419-0851-3_663
Cómo se carga la batería de iones de litio
Durante un proceso de descarga en una célula de iones de litio (LIB), los iones de litio del ánodo se desintercalan (o se extraen) en el electrolito y estos iones de litio del electrolito se intercalan en el material del cátodo. Este movimiento de los iones del ánodo al cátodo va acompañado de la liberación de electrones que fluye en el circuito externo. El proceso inverso se produce durante el proceso de carga, donde los iones de litio se desplazan desde el cátodo y se intercalan en el ánodo a través del electrolito. Las LIB comerciales suelen utilizar óxidos de metales de transición, como LiCoO2, LiMn2O4 y LiFePO4, como material del cátodo, que se recubre sobre un colector de corriente de aluminio.
Junto con el material activo, se añade entre un 10 y un 20 por ciento de carbono conductor y entre un 5 y un 10 de aglutinantes poliméricos, como el difluoruro de polivinilideno (PVDF) y el politetrafluoroetileno (PTFE), para mejorar la conductividad electrónica y conseguir una mejor adhesión del material del electrodo, respectivamente. El material del ánodo se recubre sobre un colector de corriente de cobre con carbón conductor y PVDF si es necesario.
Los dos electrodos están separados por un separador poroso (película de polietileno o polipropileno de 10-20 µm de grosor) empapado en una solución electrolítica (LiPF6 en un disolvente orgánico). Tanto el separador como la solución electrolítica deben tener una mejor conductividad iónica. La célula suele estar fabricada en una carcasa metálica en forma de jellyroll con un separador sumergido en electrolito entre los dos electrodos. En las figuras se muestra un esquema de una LIB, donde se muestran los procesos típicos de carga y descarga.
Las baterías recargables de iones de litio (Li-ion) emplean una inserción/extracción reversible de iones de litio (Li+) (especies invitadas) en o desde una matriz anfitriona (materiales activos de electrodos positivos y negativos) denominada compuestos de inserción de litio cuando se producen los procesos de descarga y carga. Las baterías de iones de litio se conocen como baterías de mecedora porque los iones de litio «se balancean» entre los electrodos positivo y negativo cuando la célula se carga y se descarga.
El material activo positivo suele ser un óxido metálico con una estructura en capas, como el óxido de cobalto y litio (LiCoO2), o un material con una estructura en túnel, como el óxido de manganeso y litio (LiMn2O4), sobre todo en un colector de corriente de aluminio. El material activo negativo suele ser un carbono grafítico, también un material en capas, sobre todo en un colector de corriente de cobre. En el proceso de carga-descarga, los iones de litio se insertan o extraen del espacio intersticial entre las capas atómicas de los materiales activos.
En las pilas de litio se utilizan electrolitos no acuosos u orgánicos.
Los separadores para las baterías de iones de litio son películas microporosas de poliolefina, polietileno (PE) y polipropileno (PP).

Reacciones electroquímicas de las pilas de iones de litio
En una célula típica de iones de litio se producen las siguientes reacciones genéricas.
Reacción del electrodo positivo:
LiMO2 ⇔ Li1-xMO2 + x Li+ + x e-
Reacción del electrodo negativo:
C + y Li+ + ye- ⇔ LiyC
Reacción celular total:
LiMO2 + x/y C ⇔ x/y LiyC + Li1-xMO2
M = metales como Co, Mn, Ni, Ti, etc.
Normalmente x es aproximadamente 0,5 e y es aproximadamente 0,16, por lo tanto x/y es aproximadamente 3. [Jeff Dahn y Grant M. Ehrlich. «Lithium ion batteries», Linden’s Handbook of Batteries,4ª edición, Thomas B. Reddy (Ed.), McGraw
Electrolito e interfase sólido-electrolito (SEI)
Como se ha mencionado anteriormente, en las pilas de litio se utilizan electrolitos no acuosos o electrolitos orgánicos. Las pilas de litio funcionan a voltajes comparativamente más altos, de hasta 4,2 V por célula. Aunque las sales de litio voluminosas, como el hexafluorofosfato de litio (LiPF6), el hexafluoro arseniato de litio (LiAsF6), el tetrafluoroborato de litio (LiBF4), el perclorato de litio (LiClO4), el trifluorometanosulfonato de litio (LiCF3SO3), el difluoro(oxalato)borato de litio (LIODFB), etc. son los electrolitos propiamente dichos (sales electrolíticas sustentadoras), requieren disolventes adecuados y estables a una tensión tan elevada. La mayoría de estos disolventes tienen constantes dieléctricas elevadas, lo que facilita la disociación iónica y la existencia de iones de litio altamente concentrados. Dichos disolventes también sirven como vainas de solvatación para la existencia estable de los iones de Li, disminuyendo así la influencia de los aniones contrarios.
La desventaja de tener constantes dieléctricas elevadas es que tienen valores de viscosidad más altos, lo que provoca que la movilidad de los iones se vea afectada. Para superar la menor conductividad iónica, los disolventes de baja viscosidad suelen mezclarse con disolventes de alta viscosidad. Sin embargo, como los disolventes poco viscosos tienen una disociación iónica menor, es imprescindible encontrar una proporción de mezcla óptima para que la mezcla tenga una buena conductividad iónica y una buena movilidad. Como disolventes no acuosos, las mezclas de carbonato de etileno (EC) con carbonatos de alquilo lineales menos viscosos, como el carbonato de dimetilo (DMC), el carbonato de dietilo (DEC) y el carbonato de etilo (EMC), se utilizan en las LIB disponibles en el mercado.
Los disolventes apróticos son éteres, ésteres y carbonatos de alquilo: Son el éter dietílico (DEE), el tetrahidrofurano (THF), el dioxolano, el carbonato de etileno (EC), el carbonato de propileno (PC), el carbonato de dimetilo (DMC), el carbonato de dietilo (DEC) carbonato de etilo (EMC), formiato de metilo, γ-butirolactona (BL), acetato de metilo, acetonitrilo (AN), dimetilsulfóxido (DMSO), dimetilformamida (DMF), cloruro de metilo, nitrometano, etc.)
Los electrolitos líquidos son soluciones de una sal de litio en uno o más disolventes orgánicos, normalmente carbonatos
El carbonato de propileno (PC) no puede utilizarse como electrolito si se va a utilizar grafito como ánodo, ya que el primero se descompone en la superficie del grafito; el PC utilizado solo, sin CE o pequeñas adiciones de LiBOB) borato de bisoxalato de Li), puede provocar la degradación de los electrodos de grafito, ya que se cointercala con el litio, lo que provoca su exfoliación.
El electrolito es invariable (entra el mismo número de iones que sale del electrolito durante la carga y
de descarga). La sal electrolítica se suele disolver en disolventes orgánicos de carbonato. Cada fabricante tiene una combinación diferente de disolventes, siendo el carbonato de etileno (CE) un denominador común para la mayoría
La formación de la capa interfase sólido-electrolito (SEI) es otra función importante que realizan los electrolitos. Cuando un metal alcalino se sumerge en el electrolito de una batería, o cuando se aplica un potencial negativo a un carbón o a un electrodo inerte sumergido en el electrolito, se empieza a formar un SEI.
La capa SEI que se forma instantáneamente al entrar en contacto el metal con la solución, está formada por productos de reducción insolubles y parcialmente solubles de los componentes del electrolito. El SEI es el factor clave que determina la seguridad, la capacidad de potencia, la morfología de los depósitos de litio, la vida útil y el ciclo de vida de la batería. También es importante una buena adherencia al ánodo.
Como se ha destacado anteriormente, sólo se pueden construir pilas primarias o secundarias alcalinas o alcalinotérreas prácticas si se puede detener la disolución o corrosión del ánodo. Por lo tanto, el electrolito debe estar diseñado para contener al menos un precursor de SEI que reaccione rápidamente con el litio (o con el ánodo de metal alcalino) para formar una interfase sólido-electrolito insoluble. Los productos de la reducción de los aniones salinos son típicamente compuestos inorgánicos como LiF, LiCl y Li2O, que precipitan en la superficie del electrodo. A la reducción del disolvente le sigue la formación de componentes SEI insolubles, como el Li2CO3, y de semicarbonatos y polímeros parcialmente solubles.
En el caso del electrodo de carbono, la tensión a la que se forma el SEI depende del tipo de carbono, de las propiedades catalíticas de su superficie (contenido de cenizas, tipo de plano cristalográfico, relación entre plano basal y plano de borde), de la temperatura, de la concentración y de los tipos de disolventes, sales e impurezas, y de la densidad de corriente. En la primera carga de una batería de iones de litio, se produce una pérdida de capacidad denominada «pérdida de capacidad irreversible» (QIR), necesaria principalmente para la formación del SEI.
Además de la formación del SEI, el QIR puede ser causado por la pérdida de capacidad asociada a la formación de productos de reducción solubles (QSP).
Un SEI libre de contaminación es esencial para la larga vida útil de la batería. Se vuelve aún más importante durante los ciclos a altas velocidades y a una mayor profundidad de descarga.
El SEI en soluciones de hexafluorofosfato de litio (LiPF6) y de hexafluoroarsenato de litio (LiAsF6) tiene una resistividad mayor en comparación con las soluciones de otras sales. Esto se debe a los cambios de resistividad que contribuyen a la resistencia controlada por las especies que conducen a la alta impedancia interfacial del ánodo de litio en los electrolitos LiPF6 y LiAsF6. Además, se afirma que el Li2CO3 es uno de los mejores agentes pasivantes para la mejora de la eficiencia del ciclo del litio [J Electrochem Soc.,164 (7) A1703-A1719 (2017)].
Separadores para baterías de iones de litio
Los separadores para las baterías de iones de litio son películas microporosas de poliolefina y generalmente son de polietileno (PE) y polipropileno (PP) estirados uniaxialmente, de PE estirado biaxialmente o de PP/PE/PP estirado multiaxialmente.
Materias primas para los materiales activos de la batería de iones de litio
Las baterías de iones de litio utilizan diferentes materiales catódicos. El ánodo es invariablemente de carbono, excepto algunos como los ánodos de óxido de titanio-niobio, la aleación Li-Si, etc. La tabla y la figura siguientes dan algunas ideas sobre las diferentes químicas empleadas en estas baterías.

Figura 12. Resumen de algunas opciones químicas de electrodos actuales y futuras para las baterías de iones de litio. La capacidad propuesta del Li(Si) es el 50% de la capacidad teórica del material, similar al caso encontrado para algunos de los materiales de electrodos positivos
[Crédito: Yu Miao, Patrick Hynan, Annette von Jouanne y Alexandre Yokochi, Energies 2019, 12, 1074; doi:10.3390/en12061074].
Tabla 1.
Características de las células de iones de litio con diferentes materiales de cátodo
| Material del cátodo | Li-Ni-Co-Al (NCA) | Li-Ni-Mn-Co (NMC) | Li-MnO2 (LMO) | Fosfato de litio y hierro (LFP) | Titanato de litio (LTO) | Óxido de Li-Cobalto (LCO) |
|---|---|---|---|---|---|---|
| Tensión nominal de una célula (V) | 3.6 | 3.65 (2.7-4.2) | 3.8 | 3.25 (2-3.6) | 3.2 | 3.6 |
| Energía específica teórica (Wh/kg) | 279 | 256 | 148 | 128 (373) | 293 (175) | 274 (370) (x=0.5) |
| Capacidad específica de los cátodos (Ah/Kg) Potencial frente a Li/Li+ (V) | 180-200 (3.8) | 200 | 148 (4.1) | 150-170 (3.45) | 175 | 274 (3.9) (x=0.5) |
| Energía específica de los cátodos (Wh/Kg) | 680-760 | 610-680 | 410-492 548 | 518-587 544 | -- | 546 |
| Seguridad | seguro | Moderado | Seguro | Alto | Muy bueno | Moderado |
Materiales del cátodo en la batería de iones de litio
Los materiales del cátodo deben satisfacer varios requisitos de los que depende la selección del material del electrodo positivo.
- Para proporcionar una alta capacidad, estos materiales deben incorporar una gran cantidad de litio tal y como están hechos.
- Además, los materiales deben intercalarse de forma reversible con pocos cambios estructurales para permitir una larga vida útil, una alta eficiencia en amperios hora y una alta eficiencia energética.
- Para lograr un alto voltaje de la célula y una alta densidad de energía, la reacción de intercambio de litio debe ocurrir a un alto potencial en relación con el litio.
- Para facilitar los procesos de carga y descarga de alta velocidad, la conductividad electrónica y la movilidad de los iones de litio en el material deben ser altas.
- El material del electrodo positivo no debe disolverse en el electrolito y debe estar disponible a un coste asequible. Para minimizar el coste, se prefiere la preparación a partir de materiales baratos en un proceso de bajo coste
El LiFePO4 es una excepción a esta regla. En el LiFePO4, el transporte adecuado de iones de litio se consigue mediante el uso de partículas de electrodo con un tamaño de partícula nanométrico. [Jeff Dahn y Grant M. Ehrlich. «Lithium ion batteries», Linden’s Handbook of Batteries,4th edition, Thomas B. Reddy (Ed.), McGraw Hill, pp. 26.6, 2011].
Los materiales activos positivos (PAM) de las pilas de iones de litio varían en función del fabricante. Los materiales catódicos pueden clasificarse en tres grandes categorías [Arumugam Manthiram, Nature Communications (2020) 11:1550]. Son:
Óxidos estratificados: materiales catódicos para baterías de iones de litio
Varios óxidos del tipo general LiMO2 (donde M =vanadio, cromo, cobalto y níquel) cristalizan en una estructura de capas en la que los iones Li+ y M3+ ocupan los [carriles de la estructura de la sal de roca alternativamente para dar una secuencia de capas de O-Li-O-M-O.
En el cátodo de óxido estratificado LiCoO2, las grandes diferencias de carga y tamaño entre los iones Li+ y Co3+ trivalentes conducen a un buen ordenamiento de los cationes, lo que es crítico para soportar la rápida difusión bidimensional de los iones de litio y la conductividad en el plano del litio.
Los materiales catódicos requieren niveles de pureza extremadamente altos y deben estar casi totalmente libres de impurezas metálicas no deseadas, especialmente hierro, vanadio y azufre.

Figura 13. Esquema simplificado de una estructura estratificada en la que se produce una ocupación alterna del
capas de cationes entre las capas de iones de óxido de paquete cerrado.
[Crédito: Robert A. Huggins, Advanced Batteries, Materials Science Aspects, Springer, Nueva York, 2009, p.168].
La buena estabilidad estructural junto con la alta conductividad eléctrica y de iones de litio ofrece características de carga-descarga rápida con buena reversibilidad. Con estas características, el LiCoO2 se mantiene como uno de los mejores cátodos hasta la fecha con un alto voltaje de funcionamiento de ~4 V. El cátodo de LiCoO2 resolvió
dos grandes retos asociados a los cátodos de sulfuro que se perseguían en los años 70. Esto permitió no sólo un aumento sustancial de la tensión de funcionamiento de <2,5 V a ~4 V, sino también el montaje de una célula sin necesidad de emplear un ánodo de litio metálico.
Óxidos de espinela: materiales catódicos para baterías de iones de litio
La segunda clase de cátodo es la espinela LiMn2O4. (La fórmula general es AB2O4). Aunque esta estructura se representa generalmente en coordenadas cúbicas, también tiene capas paralelas de iones de óxido en los planos (111), y hay sitios coordinados octaédricamente y sitios coordinados tetraédricamente entre los planos de iones de óxido. El número de sitios octaédricos es igual al número de iones de óxido, pero hay el doble de sitios tetraédricos. La estabilidad estructural tridimensional y la alta conductividad eléctrica y de iones de litio ofrecen características de carga-descarga aún más rápidas para el Li1-xMn2O4 con buena reversibilidad en comparación con el LiCoO2.
Una ventaja importante al pasar de LiCoO2 a LiMn2O4 es la importante reducción de costes, ya que el manganeso tiene un coste dos órdenes de magnitud inferior al del Co. Sin embargo, un problema crítico con el LiMn2O4 es la disolución del manganeso de la red en el electrolito en presencia de cantidades mínimas (niveles de ppm) de iones H+ (acidez) en el electrolito debido a las conocidas desproporciones de Mn3+ a Mn4+ y Mn2+ en el ácido.

Figura 14 . Esquema de la estructura de la espinela en la que los cationes se distribuyen entre los planos (111) de los iones de óxido entre sitios tetraédricos y octaédricos [Crédito: Robert A. Huggins, Advanced Batteries, Materials Science Aspects, Springer, Nueva York, 2009, p.17].
El material de cátodo de litio-níquel-óxido de manganeso (LNMO) de alto voltaje parece prometedor en las baterías de próxima generación. Pero el escollo es la falta de un electrolito que pueda soportar las tensiones de una batería basada en LNMO. Las celdas de las baterías basadas en cátodos LNMO ofrecen resultados equivalentes a los de otras baterías de litio de alto rendimiento, pero a un coste considerablemente inferior.
Sin embargo, los fabricantes de electrolitos están obteniendo resultados muy prometedores de la investigación y el desarrollo en curso que, en algún momento, darán lugar a electrolitos que funcionarán bien en una célula de batería LNMO. https ://blog.topsoe.com/el-material-del-cátodo-para-la-nueva-generación-de-baterías-de-ion-litio-está-listo
Más recientemente, el aumento del contenido de Ni y la disminución o eliminación del contenido de cobalto en los cátodos de NMC está cobrando mucha importancia [Li, W., Erickson., E. & Manthiram, A. High-nickel layered oxide cathodes for lithium-based automotive batteries, Nat. Energy 5, 26-24(2020)].
Óxidos de poli-anión: materiales de cátodo en la batería de iones de litio
La tercera clase de óxidos son los óxidos de polianiones. Se descubrió que los óxidos polianiónicos como el Fe2(MoO4)3 y el Fe2(WO4)3 sufren una inserción/extracción reversible de dos iones de litio por unidad de fórmula para dar Li2Fe2(MoO4)3 o Li2Fe2(WO4)3 tanto por métodos químicos como electroquímicos
[Manthiram, A., Goodenough, J. B. Inserción de litio en estructuras de Fe2(MO4)3 : comparación de M = W con M = Mo. J. Solid State Chem. 71, 349–360 (1987)].
Basado en los trabajos de Manthiram y Goodenough,
[Manthiram, A. & Goodenough, J. B. Inserción de litio en estructuras de Fe2(MO4)3: comparación de M = W con M = Mo. J. Solid State Chem. 71, 349-360 (1987). Manthiram, A. & Goodenough, J. B. Lithium insertion into Fe2(SO4)3 framework. J. Power Sources 26, 403-406 (1989)].
La exploración de los fosfatos que contienen litio como cátodos llevó a la identificación de la olivina LiFePO4 como cátodo [Padhi, A. K., Nanjundaswamy, K. S. & Goodenough, J. B. Phospho-Olivines as positive electrode materials for rechargeable lithium batteries. J. Electrochem. Soc. 144, 1188-1194 (1997) en 1997.
Sin embargo, la clase de óxido de polianiones adolece de una escasa conductividad electrónica. [Arumugam Manthiram, Nature Communications (2020) 11:1550].
La exploración de los fosfatos que contienen litio como cátodos llevó a la identificación de la olivina LiFePO4 como cátodo [Padhi, A. K., Nanjundaswamy, K. S. & Goodenough, J. B. Phospho-Olivines as positive electrode materials for rechargeable lithium batteries. J. Electrochem. Soc. 144, 1188-1194 (1997) en 1997.
Sin embargo, la clase de óxido de polianiones adolece de una escasa conductividad electrónica. [Arumugam Manthiram, Nature Communications (2020) 11:1550].
Fabricación de materiales catódicos - Batería de iones de litio
Anteriormente, los compuestos de cátodos de óxido de metal de litio se fabricaban a partir de carbonato de litio y una sal del metal elegido mediante una serie de reacciones de sustitución química realizadas en solución. El producto deseado se precipita y se seca por aspersión.
El LiCoO2 se preparó primero por el método de síntesis convencional indicado en la figura. Se mezclaron bien el tetraóxido de tricobalto (Co304) y el carbonato de litio (Li2CO3), y a continuación se calcinaron en el flujo de aire a una temperatura de unos 950ºC. Sin embargo, con este método era muy difícil preparar partículas gruesas de LiCoO2 y sólo se podían obtener partículas finas con diámetros de 1-3 pm.
Los materiales finos de los electrodos activos no son deseables desde el punto de vista de la seguridad. En el caso de abusos como un cortocircuito externo o un aplastamiento, las partículas finas con gran superficie específica reaccionan fácilmente de una sola vez y toda la energía de la célula se libera bruscamente en muy poco tiempo con el consiguiente aumento de temperatura. En el peor de los casos, la célula puede incendiarse [Yoshio Nishi, en Lithium ion Batteries, M. Wakihara y 0. Yamamoto (Eds.). página 192-193].
¿Cómo se fabrica la batería de iones de litio? diagrama de flujo
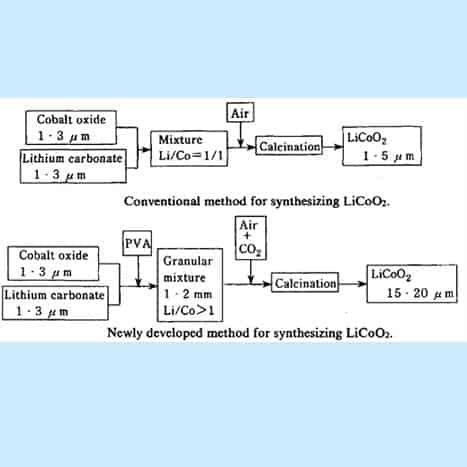
Figura 15. Diagrama de flujo para fabricar Li-CoO2
[Crédito: Yoshio Nishi, en Lithium ion Batteries, M. Wakihara y 0. Yamamoto (Eds.). página 192-193].
Un proceso mejorado para sintetizar cobaltita de litio de mayor tamaño de partícula: El primer punto es que se añade una pequeña cantidad de resina PVA en las mezclas de materias primas (Co304 y Li2CO3)) para formar gránulos con un granulador. Al sinterizar los gránulos en un flujo de aire que contiene una cantidad adecuada de gas C02, se sintetizan partículas de cobaltita de litio con un diámetro medio de 20pm. El segundo punto es que utilizamos una cantidad ligeramente excesiva de carbonato de litio (Li2CO3) en las materias primas, por lo que la relación atómica Li/Co en las materias primas es mayor que uno. Este procedimiento también es favorable para obtener partículas gruesas y, además, el LiCoO2 resultante contiene una pequeña cantidad de Li2CO3 residual.
El primer punto es que se añade una pequeña cantidad de resina PVA en las mezclas de materias primas (Co304 y Li2CO3) para formar gránulos con un granulador. Por sinterización, el óxido de cobalto de litio puede prepararse fácilmente mediante la cocción a alta temperatura de una mezcla estequiométrica de carbonato de litio Li2CO3 y óxido de cobalto, Co3O4 o cobalto metálico, a 600-800°C, y luego el recocido del producto a 900°C durante muchas horas, todo ello bajo una atmósfera de oxígeno.
También puede obtenerse por calcinación del óxido hidratado con hidróxido de litio hasta 750-900°C.
Un tercer método utiliza acetato de litio, acetato de cobalto y ácido cítrico en cantidades molares iguales, en solución acuosa. El calentamiento a 80°C convierte la mezcla en un gel viscoso y transparente. A continuación, el gel seco se tritura y se calienta gradualmente hasta alcanzar los 550°C. (https: //en.wikipedia.org/wiki/Lithium_cobalt_oxide).
Algunos ejemplos típicos son: Método sol-gel
En un proceso sol-gel, se mezclan las soluciones acuosas de los reactivos y una solución de agente quelante. La evaporación lenta del disolvente genera un sol y un calentamiento moderado del sol así obtenido produce un gel. Este último se calcina a la temperatura adecuada para obtener el producto deseado.
Ejemplo 1.
Síntesis de LiCoO2 a partir de diferentes agentes complejantes: Las sales utilizadas fueron nitrato de cobalto hexa hidratado (Co(NO3)2.6H2O, y nitrato de litio, LiNO3 anhidro. El gel se produjo utilizando cuatro agentes complejantes diferentes: ácido cítrico, anhidro (C3H4OH(COOH)3, glicina, (H2NCH2COOH); almidón (almidón de maíz comercial y gelatina).
Se preparan cinco soluciones que contienen LiNO3 y Co(NO3)2.6H2O en 20 ml de agua, con una proporción de Li:Co = 1,1:1. A cada solución se le añade un agente complejante específico: (i) ácido cítrico (4,611 g) diluido en 5 ml de agua;(ii) glicina (1,501 g);(iii) almidón (1,250 g);(iv) gelatina (3,500 g) y(v) prueba en blanco.
Las cuatro primeras soluciones se calentaron a una temperatura de 70 a 80°C en un baño de glicerina hasta la formación del gel. El tiempo de este proceso es diferente para cada agente gelificante: (i) ácido cítrico (5 horas),(ii) glicina (3 horas),(iii) almidón (1 hora),(iv) gelatina (3 horas). La producción de polvos cristalinos para todas las muestras se realizó en dos etapas en un horno de mufla: primero con la cocción de los materiales a 300°C durante 20-30 minutos y posteriormente el calentamiento a 700°C durante 24 h. [Bruno G. A. Freitas y otros, J. Braz. Chem. Soc. 28, 11, nov. 2017].
Ejemplo 2.
Preparado por el método Sol-Gel
El LiNO3 se disuelve primero en una solución de ácido cítrico. Se utilizaron LiNO3, Ni(NO3)2.6H2O Co(Ac)2.4H2O y Mg(NO3)2.6H2O como materiales de partida de litio, níquel, cobalto y magnesio en LiNi0.7-𝑥M𝑥Co0.3O2(0 ⩽ 𝑥 ⩽ 0.1), respectivamente. La cantidad de ácido cítrico es igual a la cantidad molar total de Co, Ni y Mg. A continuación, se añadieron a la mezcla Co(Ac)2 4H2O, Ni(NO3)2 6H2O y Mg(NO3)2 6H2O. Toda la mezcla se calentó en baño de agua a 80∘C. Durante el proceso de calentamiento, se formó una solución clara, de color rosa, sin ninguna precipitación. Por último, la solución clara se secó lentamente y se convirtió en gel. El xerogel se secó, se molió y se trató térmicamente en un horno a 120°C durante 12 horas.
El precursor del gel se calcinó a 500°C en aire durante 6 horas, y se enfrió a temperatura ambiente en un horno de tubo. Los productos tratados térmicamente se molieron en un mortero de ágata para obtener polvos. A continuación, el polvo se calcinó a 800°C durante 12 horas. Para la fabricación de los cátodos, los productos preparados se mezclaron primero con negro de acetileno y fluoruro de polivinilideno (80: 8:12 en peso) en 𝑁-metilpirrolidona (NMP). A continuación, la pasta obtenida se recubrió sobre una lámina de Al y se secó a 80oC durante 18 h para su posterior prensado con rodillo. . [Hailang Zhang, Advances in Materials Science and Engineering Vol 2014, Article ID 746341,]

Figura 16. Diagrama de flujo del proceso sol-gel para preparar manganato de litio
(Crédito: Y.S. Lee, Y.K. Sun y K.S, Nahm, Solid State Ionics 109 (1998) 285 según M. Pasquali, S. Passerini y G Pistoiaen Baterías de litio, ciencia y tecnología, ed. por G. A. Nazri y G. Pistoia, Springer, Nueva York, (2009), p. 318)
Fabricación de materiales para ánodos en baterías de iones de litio
El camino alentador que conduce a las LIBs con una densidad de energía y potencia mejorada es la selección de materiales anódicos adecuados que puedan proporcionar una alta capacidad y facilidad de difusión de los iones de litio en el ánodo, junto con una buena vida de ciclo y libre de problemas de seguridad.
En función de los materiales precursores, los ánodos de carbono pueden clasificarse en varios tipos, como se indica a continuación.
El material precursor y los parámetros de procesamiento determinan la naturaleza del carbono producido. Los materiales que pueden ser grafitizados por tratamiento a alta temperatura (2000 a 3000°C) se denominan carbones blandos .
Tras la grafitización, el desorden turboestático se elimina progresivamente con el aumento de la temperatura, y la tensión en el material se alivia [T. Zheng, J. N. Reimers y J. R. Dahn, Física. Rev. B 51, 734 (1995)] Carbones duros , como los preparados a partir de resina fenólica, no pueden grafitizarse fácilmente, ni siquiera cuando se tratan a 3000°C. Los materiales de tipo coque se preparan a unos 1000°C, normalmente a partir de un precursor de petróleo aromático [Jeff Dahn y Grant M. Ehrlich. «Baterías de iones de litio», Linden’s Handbook of Batteries,4ª edición, Thomas B. Reddy (Ed.), McGraw Hill, pp. 26., 2011]

Figura 17. Clasificación de los materiales de ánodos de carbono
[Crédito: Jeff Dahn y Grant M. Ehrlich. «Baterías de iones de litio», Linden’s Handbook of Batteries,4ª edición, Thomas B. Reddy (Ed.), McGraw Hill, pp. 26., 2011]
Goriparti divide los materiales del ánodo de la LIB en tres categorías dependiendo de su mecanismo de reacción con el litio [Subrahmanyam Goriparti, Ermanno Miele, Francesco De Angelis, Enzo Di Fabrizio, Remo Proietti Zaccaria, Claudio Capiglia, J Power Sources 257 (2014) 421-443].
El grupo de intercalación/desintercalación
Esta categoría de ánodos incluye materiales carbonosos y óxidos de titanio. La capacidad de almacenamiento que se produce a través de una vía de intercalación está estrechamente relacionada con el área superficial, la morfología, la cristalinidad y su orientación. Los carbones blandos son comúnmente bien aceptados y utilizados en la industria de las baterías. Se ha visto que el carbono blando es una tecnología bastante madura, mientras que el carbono duro puede presentar una solución alternativa interesante, especialmente para aplicaciones que requieren gran capacidad, como en el sector de los vehículos eléctricos. Los ánodos de óxido de titanio ya son utilizados por algunas industrias de baterías.


El grafeno también fue objeto de una amplia revisión. En particular, se vio que sus propiedades eléctricas hacen que este material sea especialmente adecuado para ánodos híbridos de grafeno/metal (por ejemplo, grafeno con SnO2 y Fe2O3). Los nanotubos de carbono (CNT) fueron significativos por sus muy interesantes resultados académicos, aunque el coste de producción podría dificultar su aplicación como material activo anódico en la industria de las baterías para el futuro.


Sin embargo, para las grandes baterías de los vehículos eléctricos, normalmente se prefieren los grafitos de bajo coste por razones de coste.
En una segunda categoría, se describieron materiales de aleación como Si, Ge, SiO, SnO2. Estos materiales pueden proporcionar mayores capacidades y una alta densidad energética en comparación con el grupo anterior, al reaccionar con el litio en un mecanismo electroquímico de aleación/desaleación. Sin embargo, este proceso implica una gran expansión de volumen que da lugar a una importante pérdida de capacidad en los ciclos. La reducción de las dimensiones del bulto a la nanoescala, junto con la realización de estructuras complejas mediante la combinación con matrices conductoras, se ha propuesto para superar los problemas mencionados y mejorar el rendimiento general del ánodo.
El silicio y el SnO2, así como sus compuestos con carbono, son los materiales más prometedores para su aplicación en las futuras baterías de litio; sin embargo, sigue siendo necesaria una forma económica de producirlos en masa como materiales anódicos. Por otro lado, el Ge, aunque interesante por sus propiedades electroquímicas y sus excelentes resultados experimentales en laboratorio, sufre el inconveniente de ser el quincuagésimo elemento en términos de abundancia en la corteza terrestre. Por lo tanto, no parece ser una buena opción para la aplicación masiva de la tecnología de baterías de litio.
En el tercer grupo, se describieron materiales que reaccionan con el litio en forma de reacción de conversión. En particular, se consideraron los óxidos/fósforos/nitruros/sulfuros metálicos. Sin embargo, estos materiales aún están lejos del gran mercado de las baterías de litio comerciales, debido a la escasa retención de la capacidad y a la gran histéresis potencial. Por lo tanto, también se han investigado diversas formas nanoestructuradas de estos materiales para resolver los problemas mencionados.
La nanotecnología es definitivamente un enfoque formidable para la ingeniería de la próxima generación de materiales de ánodos para baterías de litio. Sin embargo, para utilizar los materiales descritos como ánodos eficaces en las LIBs comerciales, especialmente para las aplicaciones en vehículos eléctricos, es necesario realizar más trabajos de investigación. De hecho, es necesario conseguir tanto una mayor energía como una mayor densidad de potencia junto con el desarrollo de procesos de fabricación baratos para la síntesis a gran escala de materiales de tamaño nanométrico. Además, la investigación de los mecanismos que rigen la interacción entre el litio y las formas nanoestructuradas de los materiales descritos, junto con las propiedades de transporte de electrones en la interfaz electrodo/electrolito, es de crucial importancia para el diseño de la próxima generación de materiales activos anódicos diseñados mediante nanotecnología.
Los electrodos negativos que se emplean actualmente en las pilas de litio implican una solución sólida de litio en una de las formas de carbono. Las pilas de litio que funcionan a temperaturas superiores al punto de fusión del litio deben utilizar necesariamente aleaciones en lugar de litio elemental. Se trata generalmente de fases metálicas binarias o ternarias. También está aumentando el interés actual por la posibilidad de utilizar aleaciones metálicas en lugar de carbones a temperatura ambiente, con el objetivo de reducir el volumen del electrodo, así como de conseguir un aumento significativo de la capacidad. [Robert A. Huggins, Advanced Batteries, Materials Science Aspects, Springer, Nueva York, 2009, p.123].
El grafito es anfótero y en él se pueden introducir cationes o aniones entre las capas de grafeno. Cuando se insertan cationes, la estructura del grafito anfitrión adquiere una carga negativa. Los ejemplos de cationes son Li+, K+, Rb+ y Cs+. Cuando se insertan aniones, la estructura del grafito anfitrión adquiere una carga positiva, y los ejemplos de aniones son Br – ,SO2- , SbF6-
La inserción de metales alcalinos en el carbono se demostró por primera vez en 1926 [ K. Fredenhagen y G. Cadenbach, Z. Anorg. Allg. Chem. 158, 249 (1926)] y la síntesis química de los litio-carburos se demostró en 1955 [D. Guerard, A. Herold, Carbon 13, 337 (1975)]. Rayos X Los experimentos de espectroscopia de fotoemisión mostraron que el litio insertado cede su electrón al carbono, y por lo tanto la estructura puede ser vista como iones Li+ contenidos entre las capas de carbono de la estructura del grafito
[G.K. Wertheim, P.M.Th.M. Van Attekum y S. Basu, Solid State Commun. 33, 1127 (1980)]. Una revisión general de los primeros trabajos sobre la inserción de especies en el grafito puede encontrarse en
[L.B. Ebert, Intercalation Compounds of Graphite, en Annual Review of Materials Science,
Vol. 6, ed. por R.A. Huggins, Annual Reviews, Palo Alto, CA (1976), p. 181].
El factor importante en la pureza del material del ánodo es la necesidad de eliminar cualquier especie que contenga oxígeno en la superficie, ya que ésta reaccionaría con el electrolito. Para evitar esta reacción, los fabricantes cuecen el grafito a 1100ºC) en atmósferas reductoras o inertes. Esto aumenta el coste para otros usos, en comparación con el grafito. El carbono (90%) se mezcla con otros ingredientes para hacer la pasta anódica o lodo. Al igual que en el cátodo, se utiliza fluoruro de polivinilideno (PVDF) como aglutinante (-5%) y se añade una pequeña cantidad de negro de humo para garantizar la conductividad. Además, se utiliza n-metilpirrolidona (NMP) para solubilizar los materiales y formar una mezcla uniforme. La presión asegura un tamaño de grano uniforme (Sandi 1999).
El titanato de litio (LTO) está ganando mucho interés. Las pilas LTO funcionan a una temperatura más baja que otros productos químicos y ofrecen una alta densidad de potencia. Sin embargo, estas células tienen una tensión nominal más baja, del orden de 2,2-2,3 V por célula. [Norio Takami, Hiroki Inagaki, Yoshinao Tatebayashi, Hidesato Saruwatari, Keizoh Honda, Shun Egusa, J Power Sources 244 (2013) 469-475].
El material del electrodo, normalmente grafito, se expande un 10% durante el proceso de carga. El grafito recupera su volumen original cuando los iones de litio se desintercalan. Los iones de litio no sólo se intercalarían en el grafito si se utiliza aluminio, sino que también se introducirían en el conductor, formando así una aleación de aluminio-litio. El proceso inverso ocurriría durante la descarga. El aluminio se degradaría después de algunos ciclos y sería inútil como colector de corriente.
Sin embargo, si el electrodo negativo está hecho de titanato de litio en lugar de grafito, la situación cambia radicalmente. El potencial del electrodo de Li4Ti5O12 es aproximadamente 1,4 V más alto que el del grafito (el voltaje de la célula es aproximadamente 1,4 V más bajo, 2,2 V frente a 3,6 V). Esto evitaría que los iones de litio se intercalaran en el aluminio. Por tanto, se prefiere el aluminio al cobre por razones de coste y peso. El Li4Ti5O12 se emplea principalmente en aplicaciones estacionarias debido a su menor voltaje de celda. [Călin Wurm et al., en Lithium-Ion Batteries, Reiner Korthauer (ed), Traducido por Michael Wuest et.al., Springer, 2018. pp. 57].
Proceso para producir titanato de litio: Una mezcla de dióxido de titanio y un compuesto de litio (cualquiera de estos: carbonato de litio, hidróxido de litio, nitrato de litio y óxido de litio) se presinteriza a una temperatura de entre 670°C y 800°C. Se obtiene un compuesto formado por TiO2, y Li2TiO3 o un compuesto formado por TiO2, Li2TiO3, y Li4Ti5O12. A continuación, el compuesto se sinteriza a una temperatura comprendida entre 800 y 950°C. [Tetsuya Yamawaki et.al., U S Patent 6,645,673 B2, 2003 Assigned to Toho Titanium Co., Ltd., Chigasaki].
Batería recargable SCiB™ de Toshiba (https://www.scib.jp/en/)
SCiB™ utiliza óxido de titanio de litio (LTO) en su ánodo para lograr seguridad, larga vida, rendimiento a baja temperatura, carga rápida, alta potencia de entrada/salida y gran capacidad efectiva. SCiB™ ha encontrado amplias aplicaciones en vehículos, industrias e infraestructuras, incluyendo automóviles, autobuses, vagones de tren, ascensores y centrales eléctricas.
Producción de separadores de baterías de iones de litio
Existen dos tipos de proceso: húmedo y seco. Los fabricantes japoneses utilizan un proceso húmedo en el que el polímero se disuelve en aceite. A continuación, el aceite se evapora para dejar una película porosa. Utilizan polímeros de peso molecular ultra alto para producir Celgard, se laminan tres capas de película de polímero soplado, se estiran y se recuecen por debajo del punto de fusión para controlar la estructura del polímero. A continuación, la lámina se estira rápidamente para obtener la porosidad.
Existen dos tipos de proceso: húmedo y seco. Los fabricantes japoneses utilizan un proceso húmedo en el que el polímero se disuelve en aceite. A continuación, el aceite se evapora para dejar una película porosa. Utilizan polímeros de peso molecular ultra alto para producir Celgard, se laminan tres capas de película de polímero soplado, se estiran y se recuecen por debajo del punto de fusión para controlar la estructura del polímero. A continuación, la lámina se estira rápidamente para obtener la porosidad.
[Pekala, R.W., et al., 2000, «Separators: An Overlooked Opportunity to Enhance Battery Performance?», 17th International Seminar and Exhibit on Primary and Secondary Batteries, Ft. Lauderdale, Fla., March 6-9].
Este proceso es muy sensible a las condiciones de funcionamiento e incluso varía con los lotes de material, por lo que es necesario un control cuidadoso [Linda Gaines y Roy Cuenca, Cost of Lithium ion batteries for Vehicles, ANL Report ANL/ESD-42, mayo de 2000, pp. 20 ].
Sin embargo, el grosor adicional requerido en los separadores para las células EV/HEV compensa la menor resistencia. [Y. Nishi, en: M. Wakihara, O. Yamamoto (Eds.), Lithium Ion Batteries, Wiley/VCH/Kodansha, Tokio, 1998, p. 195.
P. Arora, Z. Zhang, Chem. Rev. 104 (2004) 4419].
Además de las características convencionales, como la buena resistencia mecánica y la permeabilidad al electrolito, estos separadores microporosos presentan una propiedad protectora durante el abuso de las células. Por ejemplo, si la temperatura de la célula aumenta anormalmente debido a una sobrecarga excesiva, por ejemplo, el calor generado ablanda el PE y cierra los microporos de la película. Esto se denomina separador «shutdown». Una vez que se produce la desconexión, el transporte iónico entre los electrodos se detiene efectivamente y la corriente deja de fluir. Si el separador puede conservar la integridad mecánica por encima de su temperatura de desconexión, puede proporcionar un margen de seguridad al dispositivo; de lo contrario, los electrodos pueden entrar en contacto directo, reaccionar químicamente y provocar un desbordamiento térmico.
Sin embargo, es posible que, debido a la inercia térmica, la temperatura siga aumentando incluso después de la parada. En tales condiciones, el separador se fundiría y provocaría un cortocircuito en los electrodos, lo que daría lugar a reacciones violentas y a la generación de calor. Este fenómeno se denomina «fusión» o «ruptura» del separador. Por lo tanto, para garantizar la seguridad de la célula, la diferencia entre las temperaturas de «apagado» y «fusión» debe ser lo más grande posible.
Los separadores fabricados íntegramente con polietileno de alta densidad se funden a 135°C y pierden su integridad mecánica por encima de esta temperatura. Sin embargo, los separadores fabricados mediante la laminación de capas de polipropileno y polietileno mantienen la integridad mecánica al menos hasta los 165°C, el punto de fusión del polipropileno. Es interesante señalar que, aunque el polietileno de peso molecular ultra alto se funde a 135°C, los separadores fabricados con este material conservan su integridad mecánica hasta al menos 180°C, ya que la viscosidad del material es tal que mantiene la integridad física.
Los separadores de cierre son fiables y los fabricantes de baterías de iones de litio optan cada vez más por incorporarlos a sus productos. Los separadores de cierre más comunes tienen polipropileno de alto peso molecular mezclado con polietileno de peso molecular súper alto. Aquí, la propiedad única de apagado del polietileno se combina favorablemente con la alta integridad mecánica del polipropileno a temperaturas elevadas. Como el apagado es irreversible, una vez accionados, estos separadores dejan las células dañadas permanentemente. [ P.G. Balakrishnan, R. Ramesh, T. Prem Kumar, J. Power Sources. 155 (2006) 401-414]
Otros materiales en la batería de iones de litio
Hay otros materiales como los colectores de corriente, como las láminas de aluminio, níquel y cobre, los aglutinantes, como elcopolímero de estireno-butadieno (SBR ) yel fluoruro de polivinilideno (PVDF), los electrolitos y disolventes, los aditivos conductores del cátodo y el separador.
Ventajas y limitaciones de la batería de iones de litio - Fabricación de células de iones de litio
Relación de peso entre el ánodo y el cátodo
Es muy importante que no se forme metal de litio durante el funcionamiento de la célula. La deposición del metal forma dendritas que cortocircuitan internamente la célula. El control de la tensión durante la carga y el equilibrio de las células ayudan a reducir en gran medida este problema. El principal método para controlar la deposición de litio es la relación entre la capacidad del ánodo y la del cátodo de las placas individuales de la célula. El electrodo anódico tiene un 10% más de capacidad útil que el cátodo. Esto evita la deposición de metal de litio en el ánodo durante la carga, ya que el cátodo determina la capacidad de la célula. Si el metal de litio se deposita en la superficie del electrodo, reacciona con el electrolito y podría iniciar el desbordamiento térmico.

Figura 21. Relación de capacidad del ánodo y del cátodo en la célula de iones de litio
(Crédito: Ralph J. Brodd y Kazuo Tagawa, en Advances in Lithium-Ion Batteries, Walter A. van Schalkwijk y Bruno Scrosati (Eds), Kluwer Academic Publishers, Nueva York, pp. 272, 2002).
Procesos de montaje de células de iones de litio
Los procesos de ensamblaje de celdas para una batería de iones de litio requieren precisión y exactitud a la hora de recubrir el stock de electrodos positivos y negativos con el material activo. El proceso de revestimiento es un elemento crítico para garantizar un producto de alta capacidad y fiabilidad. Si los revestimientos son de mala calidad, sólo se producirán baterías de bajo rendimiento. Los pasos iniciales en la preparación de la masa activa determinan el resultado.
Cohen y Gutoff [E. Cohen y E. Gutoff, Modern Coating and Drying Technology, Wiley-VCH,
Nueva York, 1992] describen una metodología para llegar a la mejor técnica de recubrimiento para una aplicación concreta, basada en la reología de la lechada de recubrimiento, la precisión requerida y la velocidad de recubrimiento.

Figura 22. Proceso de recubrimiento de ánodos y cátodos
(Crédito: Ralph J. Brodd y Kazuo Tagawain en Advances in Lithium-Ion Batteries, Walter A. van Schalkwijk y Bruno Scrosati (Eds), Kluwer Academic Publishers, New York, pp. 273, 2002).
Diagrama de flujo para la fabricación de una batería de iones de litio

Figura 23. DIAGRAMA DE FLUJO PARA LA FABRICACIÓN DE PILAS DE IONES DE LITIO
[Ralph J. Brodd y Kazuo Tagawa en Advances in Lithium-Ion Batteries, Walter A. van Schalkwijk y Bruno Scrosati (Eds.), Kluwer Academic Publishers, Nueva York, pp. 271, 2002].

Crédito: Electropaedia https: //www.mpoweruk.com/battery_manufacturing.htm
Figura 24. Diagrama de flujo para la fabricación de electrodos a partir de materias primas
Conjunto de células de iones de litio




Los fabricantes de baterías de iones de litio tienen en cuenta los siguientes puntos al ensamblar las celdas:
- El diseño de la célula de iones de litio debe dar lugar a una densidad de corriente uniforme en toda la zona de los electrodos.
- Para garantizar un buen contacto entre los materiales activos (AM) y el colector de corriente
- Se emplean electrodos de gran superficie para dotar a las células de un alto rendimiento. Esto reduce la polarización, es decir, las pérdidas de tensión debidas a la cinética de las reacciones del electrodo y disminuye la caída de tensión a través del separador.
La estructura de los poros y la combinación de carbones conductores proporcionan un buen contacto entre partículas del material activo.
Un buen contacto es esencial entre los materiales activos, el carbón conductor y el colector de corriente, para la plena utilización de los materiales activos y para una buena eficiencia durante el rendimiento de alta tasa.
La mezcla de cátodos de cobalto se prepara a partir de LiCoO2 (un polvo negro) + aglutinante PVdF (un termoplástico fluoropolímero blanco semicristalino) + N-metilpirrolidona (NMP, un líquido orgánico incoloro) como disolvente. Como el LiCoO2 no es conductor, se añade un diluyente conductor, siempre un negro de humo, para mejorar la conductividad del LiCoO2.
La proporción y las cantidades de los materiales vienen determinadas por el diseño de la célula y el tamaño de la mezcladora. Se utiliza un procedimiento de mezcla intensiva para mezclar en seco el material activo no conductor y el carbón antes de añadir el disolvente de recubrimiento y el aglutinante.
La mezcla se mezcla en seco para obtener un recubrimiento uniforme de las partículas del material activo con una fina película del carbón conductor, de forma que se mejore el contacto eléctrico entre el AM y la rejilla del colector de corriente (papel de aluminio de 20 mm de grosor), garantizando así el pleno aprovechamiento de todo el AM. El polímero NMP se disuelve en el disolvente de recubrimiento en un recipiente separado. La mezcla seca y la solución de disolvente se combinan para formar una pasta.
Las adiciones de disolvente se utilizan para ajustar la viscosidad de la pasta (o pintura) para la operación derecubrimiento . Elfluoruro de polivinilo (PVdF) es el aglutinante elegido y el El disolvente es la N-metilpirolidinona (NMP). La pasta procedente de la operación de mezclado se coloca en contenedores sellados, que sirven de depósito y medio de transferencia para las operaciones de revestimiento. Se bombean cantidades precisas de lodo de recubrimiento desde el contenedor de almacenamiento con una bomba de engranajes, o una bomba de precisión similar, para evitar cualquier arrastre de aire en el fluido que va al cabezal de recubrimiento.
La mezcla del ánodo se prepara de forma similar con carbón duro, aglutinante PVdF y NMP. Esta mezcla se recubre sobre una lámina de cobre utilizada como rejilla (10 mm de grosor).
El revestimiento se realiza por ambas caras con un grosor de unos 100 mm tanto para los ánodos como para los cátodos. Al disminuir el grosor del recubrimiento se consigue un aumento de la superficie total para un volumen definido de la célula. Los electrolitos orgánicos utilizados poseen una menor conductividad en comparación con los acuosos, por lo que esta mayor superficie facilitará una célula de descarga de alta potencia.
El grosor del electrodo depende de la potencia máxima requerida. Una característica única de la tecnología de fabricación de baterías de iones de litio es que permite una amplia gama de diseños de relación potencia/energía con la misma tecnología de fabricación de electrodos [Broussely, Nazri pp 651]. Sin embargo, la recogida de corriente y la tabulación adecuadas, la forma y el diseño de las celdas son importantes.
Montaje de la célula: La lámina recubierta pasa por un horno para evaporar el disolvente y dejar una cantidad precisa de masa activa en la lámina. Muchos disolventes de revestimiento están clasificados como peligrosos y no pueden liberarse a la atmósfera. Como medida de ahorro, el disolvente suele recuperarse para su reutilización en el proceso. Para evitar la contaminación del medio ambiente, el disolvente puede ser incinerado.
La mayoría de las células de iones de litio tienen forma cilíndrica. El rollo de gelatina se aplana para obtener elementos para las células prismáticas.
Las celdas prismáticas son favorables para un mejor llenado del volumen, pero son susceptibles de abombarse al ciclar o envejecer. Los botes de células cilíndricas ofrecen una mayor resistencia mecánica, una buena estabilidad dimensional y una presión uniforme en los elementos.
La operación de recubrimiento produce un recubrimiento interrumpido que se ajusta a la longitud de la bobina. Las bobinadoras están diseñadas para funcionar de forma automática para su uso con rollos jumbo secos de cátodos y ánodos y separadores (de 25 mm o menos de grosor, ya sean de PP o PE o mixtos).
Las operaciones comienzan con la soldadura de las lengüetas en la sección no recubierta de las láminas. A continuación, la máquina de bobinado corta la tira a la longitud adecuada y enrolla la combinación ánodo-separador-cátodo en una bobina apretada o bobina en forma de rollo. A medida que el núcleo bobinado aumenta de diámetro, la máquina de bobinado compensa automáticamente para mantener una tensión constante a medida que la bobina aumenta de diámetro para una tolerancia estrecha en el diámetro. El viento elíptico para las células prismáticas es un proceso más complejo y lento.
Tras el bobinado, se comprueba que la bobina no tenga cortocircuitos internos antes de introducirla en la lata. Las latas de acero deben estar limpias y niqueladas para proporcionar una superficie estable y minimizar la corrosión de la lata antes del montaje de la célula. El cable del ánodo se suelda al fondo de la lata y el del cátodo al respiradero de seguridad. Se añade el electrolito a la célula semimontada. El montaje se completa con el engaste de la tapa superior.
El rechazo temprano de los posibles fallos de las células es una medida económica y evita que se trabaje más en las células malas. La bobina se introduce en la lata para que ésta ejerza una presión constante que mantenga unidos los componentes del elemento, eliminando así cualquier posibilidad de que haya huecos entre ellos. Algunos fabricantes pueden insertar un mandril para estabilizar el centro de la bobina.
A menos que todas las operaciones se realicen en un sala seca o caja seca el agua absorbida en los materiales activos debe eliminarse mediante calor y vacío antes del proceso de llenado del electrolito.
El llenado al vacío de precisión del electrolito se realiza para asegurar que el electrolito permea y llena completamente la porosidad disponible en las estructuras del separador y del electrodo. Las bombas de precisión miden el volumen calculado de electrolito necesario para el buen funcionamiento de la célula. Invariablemente, todos los fabricantes emplean LiPF6 (un compuesto cristalino blanco inorgánico) como electrolito y carbonatos cíclicos (EC, carbonato de etileno) o lineales (DMC, carbonato de dimetilo, DEC, carbonato de dietilo, o EMC, carbonato de etilo, etc.) son los disolventes de esta sal electrolítica.
Los electrolitos basados en mezclas de disolventes de carbonato de etileno (EC) con carbonato de dimetilo (DMC) y/o carbonato de dietilo (DEC) se utilizan habitualmente para las baterías de iones de litio en combinación con cátodos de «4 V» (cobalato, níquel y manganato) debido al alto potencial de oxidación de los disolventes.
Después de llenar la célula con el electrolito, la célula se sella mediante la compresión controlada de una junta o ojal de polímero colocado entre la lata de la célula y la placa superior. La presión sobre la junta de polímero se controla para mantenerla dentro del límite elástico del polímero. Si se superan los límites elásticos, el polímero fluye en frío y compromete la estanqueidad.
Cada fabricante utiliza una construcción mecánica algo diferente para sellar las células, pero los resultados finales son esencialmente idénticos. Por lo general, se forma un hombro o saliente cerca de la parte superior de la celda. Esto sirve como base para el sello y para mantener el rollo de gelatina en su lugar y evitar el telescópico o el cambio de posición de la bobina enrollada bajo la influencia de las vibraciones y los golpes.
Cualquier cambio de posición provoca un cambio en la distribución de la corriente y da lugar a una mala duración de los ciclos o a la formación de placas de litio en las células de alto rendimiento. La junta de la placa superior de la célula contiene un respiradero, un elemento de coeficiente de temperatura positivo (PTC) y unos dispositivos de seguridad de interrupción de corriente (CID). Tanto el CID como el PTC son dispositivos de seguridad diseñados para activarse y evitar que se desarrollen temperaturas y presiones peligrosas en el interior de la célula. Cada lote de dispositivos se comprueba para ver si funciona correctamente antes de incorporarlo al conjunto superior.
Una vez aplicado el precinto, las cubetas pueden ser lavadas, encamisadas y etiquetadas. Se les asigna un número de serie para rastrear el día de fabricación e identificar todos los componentes de la célula (materiales de los electrodos, electrolito, separador y similares). La información sobre la capacidad y el voltaje se almacena con el número de la célula y se utiliza más tarde para hacer coincidir las células para el montaje del paquete.
Las celdas se pueden soldar con láser con juntas de vidrio a metal para proporcionar cierres herméticos de larga duración. Con las celdas más grandes, hay que tener más cuidado para garantizar un funcionamiento seguro, incluso en condiciones de abuso.
Mientras que los procesos anteriores se describen para las pequeñas celdas selladas utilizadas en la electrónica portátil, el proceso para las baterías industriales más grandes para el almacenamiento de energía, el espacio y las aplicaciones de los vehículos eléctricos siguen el mismo esquema general.
Batería de iones de litio - Formación y envejecimiento
Tal y como está montada, los iones de Li no están dopados en el carbono del ánodo, por lo que la célula no muestra tensión. Durante la carga inicial, una parte de los iones de Li de la PAM LiCoO2 se desdobla para convertirse en Li1-xCoO2 y estos iones de Litio se dopan en el ánodo de carbono (Cy) para convertirse en LixCy. Cuando la tensión de carga alcanza entre 4,1 y 4,2 V, el valor de x es de aproximadamente 0,5. (es decir, el 50 %), lo que indica que se ha utilizado el 50 % del Li de LiCoO2.
Otro aspecto a destacar es que una parte de los iones de litio dopados no retorna y permanece en el ánodo. donde, x-dx Los iones de litio permanecen sin contribuir a la capacidad. Se trata de un 10 a 20 % de litio irreversible, lo que significa que la eficacia de la carga inicial es del 80 al 90 %. A partir del segundo ciclo, la cantidad irreversible no aumenta y la célula muestra la capacidad del 100 % diseñada por el fabricante.
Tras el lavado y el encamisado, pero antes del inicio del proceso de formación, se registran la tensión y la impedancia de todas las células para descartar las células defectuosas. Las células se cargan por primera vez
(carga inicial o de formación). Las condiciones del primer cargo son importantes por al menos dos razones:
1) la capa de interfase de electrolito sólido (SEI) se forma en el ánodo para protegerlo de la reacción espontánea con el electrolito durante el funcionamiento normal de la célula, y 2) establece el buen contacto eléctrico entre los materiales activos y el electrolito. La primera carga sigue el procedimiento recomendado por el fabricante para la carga de las células, pero a menudo comienza con una corriente más baja y luego aumenta a la corriente de carga normal en aproximadamente un tercio del período de carga. Las células pueden seguir ciclando dentro de los límites de tensión de carga y descarga durante uno o dos ciclos más después de la formación.
Tras la formación o el ciclado, se miden el voltaje y la capacidad de la célula y se almacenan para su uso posterior en el proceso de selección de la célula. El periodo de envejecimiento varía entre dos semanas y un mes, según el fabricante. La tensión de las células se vuelve a medir después del almacenamiento. Las diferencias de tensión al principio y al final del periodo de almacenamiento se utilizan para clasificar las células con «cortocircuitos» o «microcortes». Las células con cortocircuitos internos tendrán una tensión más baja después del almacenamiento y se separarán de la distribución normal de la tensión y la capacidad. Puede ser necesario evacuar las celdas más grandes después de la formación para eliminar los gases de formación.
Para una descripción detallada del proceso de ensamblaje, se remite al lector a
- Kaoru Nakajima y Yoshio Nishi Capítulo 5 en: Energy Storage Systems for Electronics, Ed Tetsuya Osaka y Madhav Datta, Gordon and Reach Science Publishers, Amsterdam, 2000.
- Lithium-Ion Cell Production Processes, Ralph J. Brodd y Kazuo Tagawa, Capítulo 9 en: Advances in Lithium-Ion Batteries, Walter A. van Schalkwijk and Bruno Scrosati (Eds), Kluwer Academic Publishers, New York, pp. 273, 2002.
- Baterías de litio, ciencia y tecnología, ed. por G. A. Nazri y G. Pistoia, Springer, Nueva York, 2009.
- Baterías de iones de litio, Reiner Korthauer (ed) (2018), Traducido por Michael Wuest et.al., Springer, 2018.
- Kazuo Tagawa y Ralph J. Brodd, Production Processes for Fabrication of Lithium-Ion Batteries in Lithium-Ion Batteries, Yoshio M., Brodd R.J., Kozawa A. (eds) Springer, New York, NY. https: //doi.org/10.1007/978-0-387-34445-4_8]
- Zhang Z., Ramadass P. (2012) Lithium-Ion Battery Systems and Technology. En: Meyers R.A. (ed) Encyclopaedia of Sustainability Science and Technology. Springer, Nueva York. https: //doi.org/10.1007/978-1-4419-0851-3_663
- Manual de diseño de baterías de iones de litio: química, componentes, tipos y terminología, John Warner, Elsevier, 2018




