Como funciona a bateria de iões de lítio
A percepção no domínio público é que as baterias de chumbo-ácido são tecnologia antiga. A bateria de iões de lítio tem uma percepção diferente, é moderna, mais limpa, tem 3 ou 4 vezes a densidade de energia e uma duração de ciclo mais longa. Com tudo isto, que possíveis vantagens poderia trazer à mesa a tecnologia do chumbo ácido com 150 anos de idade? Bem, na verdade, nem tudo é como parece, olhe para trás das manchetes os dados utilizados nas alegações de marketing, depois aplique um pouco de senso comum, pesquisa básica e alguma ciência rudimentar. Você vai descobrir que a verdadeira história é bem diferente.
O primeiro equívoco diz respeito às densidades volumétricas e específicas de energia. Os valores das manchetes de 4 a 5 vezes referem-se apenas à densidade específica de energia e a um número limitado de baterias de iões de lítio, algumas das quais ainda não estão em uso comercial. Fig. 2 compara vários cátodos para células de bateria de íons de lítio, que variam de cerca de 100Wh/kg para a mais segura química Li-FePO4 até mais de 200Wh/kg para a variante de óxido de níquel-cobalto-alumínio. O diagrama da bateria de chumbo-ácido é apresentado abaixo:


Estes valores só se aplicam ao nível de célula única, não à embalagem ou à condição em serviço. Fig. 3 mostra as densidades de energia de diferentes químicos de bateria a nível de célula e sistema. A densidade de energia das células das baterias de íons de lítio é praticamente reduzida pela metade quando totalmente instaladas com todas as conexões, resfriamento, segurança e equipamento de gerenciamento de baterias.
A vantagem do nível celular de 3 a 5 vezes a densidade de energia específica é reduzida para 2 a 3 vezes. Dependendo da química do cátodo de lítio, podemos quase estar olhando para a paridade entre as baterias de íons de lítio e a densidade de energia das baterias de ácido de chumbo para um sistema de baterias totalmente instalado em algumas aplicações.
O outro factor, o da vida do ciclo, é também uma fonte de confusão. Quantos ciclos uma bateria de íons de lítio pode realizar antes que a capacidade caia abaixo de 80% da sua classificação de placa de identificação? Dois, três mil? A Tabela 1 apresenta um resumo dos diferentes materiais catódicos de íon-lítio para o desempenho e a vida útil do ciclo.
Vantagens da química de baterias de chumbo-ácido
As baterias são dispositivos estranhos. Ninguém os quer, mas todos precisam deles. Eles só são comprados quando necessário. Quantas pessoas planeiam ir ao centro comercial local à loja de montras para comprar pilhas? São uma compra rancorosa e só comprada quando absolutamente necessária. Um bom vendedor pode vender-lhe dois pares de sapatos, dois carros e talvez duas casas se você tiver o dinheiro, mas ele não pode vender-lhe duas baterias de automóvel SLI. Quando você compra uma bateria, seja uma bateria solar para um painel solar, uma bicicleta elétrica ou uma UPS e um sistema de backup de bateria do inversor ou uma bateria de tração para empilhadeiras, você não gostaria de saber mais sobre isso?
Como funcionam as baterias de chumbo ácido, quais são as diferenças entre tipos e modelos, e que tal os diferentes produtos químicos? Eles podem ser caros. Numa aplicação comercial ou doméstica, qual é o retorno do investimento, qual é a duração e o custo de substituição de uma bateria de chumbo-ácido? O tamanho que precisa, o espaço disponível, a eficiência energética da bateria de chumbo ácido e o tempo de recarga? E depois, há os custos ocultos da segurança, da eliminação e da pegada de carbono. Este artigo compara baterias de chumbo ácido com baterias de iões de lítio e aborda muitos dos equívocos associados a estes dois produtos químicos.
Qual é a melhor bateria de iões de lítio
| material catódico | Nome curto | Tensão nominal | Energia específica Wh/kg (célula) | Duração do ciclo | Comentários |
|---|---|---|---|---|---|
|
Óxido de Cobalto de Lítio (LiCoO2) |
LCO | 3.6 | 150-200 | 500-1000 | Dispositivos portáteis - thermal runaway por sobrecarga |
| Óxido de Manganês Lítio (LiMn2O4) | LMO | 3.7 | 100-150 | 300-700 | Ferramentas eléctricas, dispositivos médicos - mais seguros do que o LCO |
| Óxido de Cobalto de Lítio Níquel Manganês (LiNiMnCO2) | NMC | 3.6/3.7 | 150-220 | 1000-2000 | E-bikes, EV, industriais - ciclo de vida alto |
| Fosfato de Lítio e Ferro (LiFePO4) | LFP | 3.2 | 90-120 | 1000-2000 | EV, SLI, Lazer - o mais seguro de todos os produtos químicos para baterias de iões de lítio |
| Óxido de alumínio lítio/níquel-cobalto (LiNiCoAlO2) | NCA | 3.6 | 200-260 | 500 | Industrial, EV powertrain (Tesla) TR a 150C, CL 500 |
| Titanato de lítio (Li4Ti5O12) | LTO | 2.4 | 50-80 | UPS, Solar, EV powertrain (Honda, Mitsubishi). CL 3000-7000 - muito seguro |
Como pode ser visto, todos se enquadram na faixa dos ciclos de 800 a 2000. Em comparação, uma bateria de chumbo ácido bem concebida pode facilmente alcançar mais de 1600 ciclos a 80% de DOD. Então como tudo isto se soma quando se considera o custo de propriedade? Isto leva-nos ao próximo ponto que é o preço da bateria de chumbo-ácido. Quanto custa uma bateria de iões de lítio em comparação com uma bateria de chumbo-ácido? Custo da fábrica de produção de baterias de iões de lítio? Naturalmente, a bateria de iões de lítio é mais cara, mas quanto mais. Mais uma vez, isto depende do nível a ser considerado. Os comunicados de imprensa nos dirão que os preços do íon de lítio estão caindo e agora estão na faixa de 2 a 3 vezes a do ácido de chumbo.
A sério? Os preços médios em uma pesquisa recente na internet no Reino Unido para obter preços em baterias de lazer comercialmente disponíveis de 12V e 100 Ah tanto para baterias de íons de lítio quanto para baterias de chumbo-ácido:
bateria de íons de lítio $960 ou $800/kwh
Bateria de chumbo ácido $215 ou $180/kwh
Obviamente, a vida da bateria de iões de lítio tem de ser 4 vezes superior à da bateria de chumbo-ácido equivalente para obter o mesmo valor. Como já vimos, não é este o caso.


Em todos os casos, a construção da bateria de chumbo-ácido foi a mais económica, mesmo quando foi instalada uma bateria de chumbo-ácido maior para proporcionar uma melhor aceitação da carga e uma maior duração do ciclo. Neste exemplo, a aplicação foi uma torre de telecomunicações na Índia. O mesmo princípio se aplica à maioria das aplicações e geografias, mais ainda em climas mais frios. A outra concepção errada é que o Li-ion é uma tecnologia mais limpa e menos poluente do que o chumbo-ácido. As emissões do berço ao portão para diferentes químicos de bateria são dadas em Figs. 5 e 6.
Esta figura mostra o limite de operações para o fabrico de baterias. Desde a extracção e transporte de matérias-primas até ao ponto em que as baterias estão prontas para serem expedidas, passando por todas as etapas de processamento.
A tabela 2 é uma situação da vida real comparando a economia do uso de bateria de íons de lítio e bateria de ácido de chumbo trabalhando em diferentes períodos de vida.
| Item de custo | Custos diários de funcionamento USD | Custos diários de funcionamento USD |
|---|---|---|
| 3 Anos | Bateria de chumbo-ácido | bateria de íons de lítio |
| Amortização | 8.30 | 16.90 |
| Diesel (entregue) | 15.50 | 15.50 |
| Manutenção | 2.46 | 2.46 |
| Electricidade | 1.47 | 1.47 |
| Carregamento da bateria | 0.65 | 0.50 |
| Total dia/mês | 28.38/851 | 36.83/1105 |
| 6 anos | ||
| Amortização | 5.86 | 8.46 |
| Diesel | 15.50 | 15.50 |
| Manutenção | 2.46 | 2.46 |
| Electricidade | 1.47 | 1.47 |
| Carregamento da bateria | 0.54 | 0.50 |
| Total dia/mês | 25.83/775 | 28.39/852 |
Estes dados dos Laboratórios Nacionais Argonne, mostram que o processo total de fabricação, incluindo a extração e o transporte de matérias-primas para baterias de íons de lítio são mais de 4 vezes o valor de ácido de chumbo. Quanto à extracção de materiais, o fornecimento de materiais catódicos básicos como o cobalto e o manganês e o lítio não é completamente certo. Os processos de extracção e recuperação existem, mas o número de minas e locais de fabrico pode limitar a oferta se a procura aumentar significativamente. O mapa geo-político também prevê incerteza para algumas fontes destes materiais.
As baterias de iões de lítio são recicláveis
A reciclabilidade e segurança destes produtos químicos são factores importantes. Sabe-se que quase todos os componentes das baterias de chumbo-ácido são 100% reciclados, enquanto não existem processos comerciais de reciclagem de baterias de iões de lítio. Esta situação é compreensível quando se considera que os componentes mais caros de Li, Co, Mn etc. são apenas uma pequena fracção do total da bateria de iões de lítio. Por exemplo, o lítio é cerca de 4% do peso total da célula. Acrescente-se a isto o facto óbvio de o lítio ser altamente reactivo (a base da sua elevada densidade energética), o que, compreensivelmente, encarece a sua extracção dos resíduos.
O factor adicional de complexidade com muitos materiais diferentes na sua construção torna a reciclagem difícil, tanto técnica como economicamente. O resultado? Não há simplesmente nenhum incentivo comercial para reciclar estas baterias. Por esta razão, as instalações de reciclagem ainda se encontram na fase piloto e são financiadas, na sua maioria, pelo governo.
Atualmente, a grande maioria das baterias de íons de lítio sucateadas são estocadas à espera de um avanço tecnológico ou de legislação para forçar sua reciclagem. Se este último fosse implementado, então haveria um custo, em última análise para o consumo. Isso aumentaria ainda mais o preço da célula de íon-lítio em comparação com os tipos de baterias de chumbo-ácido.
Pode a bateria de iões de lítio explodir
Finalmente, temos segurança. Nenhuma aplicação de bateria de chumbo-ácido do nosso conhecimento jamais teve um recall de segurança, como sabemos ser o caso da bateria de íon-lítio em dispositivos eletrônicos portáteis e até mesmo em veículos elétricos. Fig. 7 mostra o que aconteceu a um novo Volvo híbrido no Reino Unido há apenas algumas semanas, no momento em que este artigo foi escrito. Neste caso, as suas baterias de iões de lítio pegaram fogo quando estavam carregadas.
Incêndios de bateria de iões de lítio
Figura 7 Incêndio causado por uma bateria de iões de lítio num veículo eléctrico híbrido Volvo: Abril 2018-UK residência


Este vídeo mostra um incêndio muito recente causado por uma bateria de lítio. Possivelmente devido ao desequilíbrio nas células e à BMS inadequada.
Mesmo quando as baterias de iões de lítio armazenadas ou transportadas têm sido a causa de incêndios gravemente perigosos. Embora estas ocasiões sejam raras, têm de ser reconhecidas, e têm de ser instalados equipamentos de segurança e software de gestão de baterias adequados. Os bombeiros de Nova Iorque, por exemplo, ainda estão no processo de decidir como combater os incêndios com baterias de iões de lítio. Isto sugere fortemente que as medidas de segurança existentes para as baterias de iões de lítio em todo o mundo precisam de ser revistas.
A seguir está a vista dos Bombeiros de Nova Iorque:
Citação de artigo de notícia: AWS Utility Drive 15 de Novembro, 2016 “O fogo não é o maior problema”, disse Rogers. Os bombeiros são treinados para lidar com os incêndios, mas eles precisam saber com o que estão lidando. As baterias de iões de lítio podem libertar ácidos tóxicos e vapores inflamáveis. Alguns desses vapores são consumidos pelo fogo, mas se não forem, podem incendiar-se ou ser um problema para os bombeiros. O maior problema é o que acontece “pós-operação”, ou seja, depois que o incêndio é extinto. Mesmo que uma bateria seja desligada, pode reacender-se por até 72 horas, disse Rogers. -Lt. Paul Rogers Fire Department of New York’s hazardous materials operations division”
Bateria de iões de lítio ou bateria de chumbo ácido?
A bateria de iões de lítio tem certamente melhores características de desempenho do que o ácido de chumbo. No entanto, estas vantagens são severamente reduzidas pelo hardware adicional associado aos requisitos de segurança e gestão. O resultado líquido é que as baterias de chumbo-ácido têm vantagens distintas, particularmente quando se consideram aplicações que não são limitadas pelo peso ou aceitação de carga. O custo inicial mais baixo da fábrica de baterias de chumbo-ácido; o baixo preço de compra e o baixo custo de amortização do ácido chumbo combinado com o seu baixo impacto ambiental e segurança inerente, proporcionam as seguintes vantagens:
- Preço de compra mais baixo. O preço é cerca de um quarto do equivalente a um ião de lítio. Os custos operacionais mais baixos para dar um custo total de propriedade mais baixo na maioria das aplicações.
- Reciclabilidade. Quase 100% de todos os materiais das baterias de chumbo ácido são reciclados. O valor da sucata pode proporcionar uma receita adicional de até 20% do custo do material da bateria. As baterias de lítio não têm infra-estrutura ou processo comercial para reciclagem
- Segurança. A química do ácido de chumbo é intrinsecamente mais segura do que a da bateria de iões de lítio.
- Sustentabilidade. Existem muitas fontes bem estabelecidas de abastecimento de chumbo ácido, particularmente de instalações de reciclagem. O lítio e outros materiais catódicos podem ser fornecidos a partir de áreas politicamente sensíveis. Tanto a atual extração global de materiais como a capacidade de fabricação não suportariam um rápido aumento na produção de bateria de íons de lítio.
- Pegada de carbono. A fabricação de baterias de chumbo-ácido tem uma pegada de carbono de um terço da pegada das baterias de íons de lítio.
Um quadro diferente daquele pintado pelas empresas de baterias de iões de lítio. Embora não se possa argumentar que o ácido de chumbo tem uma desvantagem na densidade de energia, o fato é que a bateria de chumbo-ácido ainda é uma bateria altamente segura, competitiva e a melhor escolha de tecnologia de bateria em muitas aplicações.
O que é a bateria de iões de lítio
Materiais catódicos e anódicos: Embora as células de níquel-hidreto metálico (Ni-MH) tenham sido favorecidas inicialmente nos anos 90, o primeiro produto comercial de baterias recarregáveis de íon de lítio do mundo foi lançado em 1991 pela Sony Corporation. Além do alto conteúdo energético, tanto em massa como em volume, esta bateria também ofereceu excelentes características de baixa temperatura, características de carga e características de ciclo. Como resultado, captou rapidamente o mercado e tornou-se uma fonte indispensável de energia para equipamentos de áudio e vídeo, computadores pessoais, telefones portáteis e outros equipamentos portáteis.
A avançada tecnologia de baterias de hoje começou com a descoberta da alta condutividade iónica do NaAl11O17 de fase sólida, chamado sódio β-alumina, por Kummer e colegas de trabalho no laboratório da Ford Motor Co. [1. Olof Ramsrtomström, sobre o Prémio Nobel da Química, Antecedentes científicos sobre o Prémio Nobel da Química de 2019; 2. Y.F.Y. Yao e J.T. Kummer, J. Inorg. Nucl. Química. 29, 2453 (1967)].
Isto levou à constatação de que o transporte iônico em sólidos pode na verdade ser muito rápido, e que pode levar a uma variedade de novas tecnologias. Pouco tempo depois, pesquisadores da Ford mostraram que se pode usar um eletrólito sólido altamente condutor para produzir um tipo inteiramente novo de bateria, usando sódio fundido no eletrodo negativo e uma solução fundida de sódio em enxofre como eletrodo positivo, com o eletrólito sólido condutor de sódio entre [N. Weber e J.T. Kummer, Proc. Annual Power Sources Conf. 21, 37 (1967) ].
Como seria de esperar, logo foi considerada a possibilidade de sistemas de lítio análogos, pois foi reconhecido que uma célula de lítio equivalente deveria produzir tensões mais elevadas do que uma célula de sódio. Além disso, o lítio tem um peso inferior ao do sódio, outra vantagem.
O lítio elementar não podia ser usado, devido ao seu baixo ponto de fusão. Em vez disso, foram investigadas ligas de lítio sólidas, principalmente os sistemas Li/Si e Li/Al [R.A. Huggins, J. Power Sources 81-82, 13 (1999)].
Diversos materiais foram investigados como reagentes de eletrodos positivos naquela época, com maior atenção dada ao uso de FeS ou FeS2. Após reação com lítio, esses materiais sofrem reações de reconstituição, com o desaparecimento das fases iniciais e a formação de novas fases [D. R. Vissers, Z. Tomczuk e R. K. Steunenberg, J. Electrochem. Soc. 121, 665 (1974)].
Quando foi inventada a bateria de iões de lítio?
Whittingham explorou a intercalação eletroquímica em tais materiais e em 1973 propôs tais materiais como eletrodos em baterias. Este trabalho resultou em uma bateria funcional e recarregável em 1976. A célula de sucesso foi composta de lítio metálico como anodo e sulfureto de titânio (TiS2) como cátodo, com hexafluorofosfato de lítio(LiPF6) como electrólito em carbonato de propileno (PC) como solvente. Estes estudos promissores inspiraram a Whittingham a explorar a intercalação eletroquímica em materiais como eletrodos em baterias. Uma bateria funcional e recarregável foi posteriormente demonstrada em 1976.
[(a)Whittingham, M. S. Electrointercalation in Transition-Metal Disulphides. J. Chem. Soc., Chem. Commun. 1974, 328–329.] (com Exxon Research and Engineering Company).
(b)Whittingham, M. S. Batterie à Base de Chalcogénures. Patente belga no. 819672, 1975.
(c)Whittingham, M. S. Armazenamento de Energia Elétrica e Química de Intercalação. Science 1976, 192 (4244), 1126-1127.
Mas o sucesso foi de curta duração. Em ciclos repetidos, o lítio metálico formou dendritos na superfície metálica em ciclos, resultando em curto-circuitos.
Este problema deu ímpeto a uma nova busca por soluções alternativas e uma configuração de “células de transferência de íons” (também chamada de “cadeira de balanço”), onde ambos os eletrodos podem acomodar íons foi proposto.
Se um material de eletrodo positivo contém inicialmente lítio e algum ou todo o lítio é removido durante o primeiro carregamento, a célula desenvolve potencial. Portanto, é possível ter materiais de eletrodos positivos que reagem com lítio em potenciais acima de 3V, se eles já contiverem lítio, e esse lítio pode ser extraído eletro-quimicamente.
Quem inventou a bateria de iões de lítio?
Esta abordagem, envolvendo o uso de materiais em que o lítio já está presente, foi demonstrada pela primeira vez pelo Prof. Os primeiros exemplos de materiais contendo inicialmente lítio, e eliminando electroquimicamente o lítio deles, foram os trabalhos sobre Li1-xCoO2, em 1980.
[K. Mizushima, P.C. Jones, P.J. Wiseman e J.B. Goodenough, Mater. Res. Bull. 15, 783 (1980)] e Li1-xNiO2
[J.B. Goodenough, K. Mizushima e T. Takada, Jpn. J. Appl. Phys. 19 (Suppl. 19-3), 305 (1980)]
Em paralelo com o desenvolvimento dos ânodos, também foram procurados melhores materiais catódicos para adquirir um emf de células mais elevado em combinação com ânodos de maior potencial do que o lítio metálico. Um avanço veio em 1979/1980 quando John B. Goodenough e os seus colegas de trabalho em Oxford
University, UK, descobriu que o LixCoO2, outro calcogeneto metálico intercalado do tipo MX2, poderia servir como um material catódico.
[Goodenough, J. B.; Mizushima, K. Fast Ion Conductors. Patente americana no. 4.357.215, 1982].
[Mizushima, K.; Jones, P. C.; Wiseman, P. J.; Goodenough, J. B. LixCoO2 (0<x<-1): Um Novo
Material Catódico para Baterias de Alta Densidade Energética. Mat. Res. Bull. 1980, 15 (6), 783–789].
A estrutura do material era análoga à de LixTiS2 com van der Waals entre o dióxido de cobalto (CoO2) camadas nas quais os íons de lítio poderiam ser ligados sem muita expansão da malha. Bem pensado que quando X em MX2 é um pequeno elemento eletronegativo, um processo de absorção de cátions resultante estaria associado a uma grande mudança negativa de energia livre e uma alta tensão celular (ΔG = -nFE). Com um X de oxigénio, a situação foi considerada especialmente promissora, também dado que foram propostos iões de lítio para serem suficientemente móveis em matrizes de oxigénio fechadas.
O raciocínio provou ser correto e o material CoO2 mostrou um potencial muito alto de ~4 a 5 V em relação ao Li+/Li. Os estudos eletroquímicos foram realizados neste caso com um eletrólito composto de tetrafluoroborato de lítio (LiBF4) em carbonato de propileno.
Esta descoberta permitiu a utilização de materiais anódicos com potenciais mais elevados do que o lítio metálico, promovendo a procura de materiais carbonáceos adequados. Considerando a dificuldade de resolver o problema da intercalação eletroquímica da grafite, outras opções foram investigadas em seu lugar.
Onde foi inventada a bateria de iões de lítio?
Um avanço veio em 1985 quando um grupo japonês liderado por Akira Yoshino (da Asahi Kasei Corporation) descobriu as fibras de carbono produzidas a vapor (VGCF) e mais tarde o coque de petróleo tratado termicamente. Este último material era conhecido por conter uma mistura de domínios cristalinos (gráficos) e não cristalinos, e os pesquisadores puderam identificar qualidades particularmente estáveis, mas de alto desempenho, com graus específicos de cristalinidade.
[Akira Yoshino, The Birth of Li-Ion Battery, Angewandte Essays, Angew., Chem. Int. Ed., 2012, 51, 5798-5800]
Com estes materiais anódicos eficazes, Yoshino desenvolveu uma bateria de iões de lítio eficiente e funcional com base na configuração da célula de transferência iónica. O material carbonoso identificado foi assim utilizado como anodo e o material LixCoO2 da Goodenough (tipicamente contendo pequenas quantidades de estanho) foi utilizado como catodo. Foram utilizadas camadas separadoras compostas de polietileno ou polipropileno e o eletrólito foi composto de perclorato de lítio (LiClO4) em carbonato de propileno (PC).
Yoshino também provou a segurança desta bateria em 1986 ao deixar cair um peso sobre a bateria. Não ocorreram incêndios ou explosões, enquanto as baterias usando ânodo de lítio metálico reagiram de forma violenta.

Figura 8. Os primeiros testes de segurança do Yoshino com a sua bateria de iões de lítio em 1986.
A) O momento em que um caroço de ferro colide com a bateria
B) Protótipo de bateria de íon-lítio após colisão
C) Bateria do ânodo metálico Li após a colisão
[Crédito: Akira Yoshino, The Birth of Li-Ion Battery, Angewandte Essays, Angew., Chem. Int. Ed., 2012, 51, 5798-5800 ]
Estas descobertas e desenvolvimentos acabaram por levar ao lançamento de uma bateria comercial de lítio
em 1991. Com o desenvolvimento posterior, a bateria de iões de lítio foi comercializada pela Sony em 1991 e por uma empresa conjunta da Asahi Kasei e da Toshiba em 1992.
[Nishi, Y., The Development of Lithium Ion Secondary Batteries. Chem. Rec. 2001, 1, 406-413]
A bateria foi baseada em um material anódico à base de coque de petróleo, LixCoO2 como cátodo, e um eletrólito livre de água composto de hexafluorofosfato de lítio (LiPF6) em carbonato de propileno (PC). A tensão de carga era alta (até 4,1 V), com uma energia específica registrada de ~80 Wh/kg e densidade de energia de ~200 Wh/litro.
Comparada com outras baterias que estavam no mercado na altura, a bateria de lítio rapidamente se tornou muito competitiva e essencialmente abriu o caminho para a revolução móvel que se aproximava.
Ao mesmo tempo, verificou-se que a grafite podia ser realmente utilizada em combinação com uma composição electrolítica adequada. [Fong R, Sacken U von, Dahn J. R., Studies of Lithium Intercalation into Carbons Using Nonaqueous Electrochemical Cells. J. Electrochem. Soc. 1990, 137 (7), 2009-2013].
Utilizando solventes contendo carbonato de etileno, até então geralmente desconsiderados devido ao seu maior ponto de fusão, formou-se uma interfase sólida do eletrólito (SEI) na superfície do eletrodo de grafite durante o ciclo de carga/descarga, protegendo assim o material de carbono da esfoliação e posterior decomposição. [Peled, E. The Electrochemical Behaviour of Alkali and Alkaline Earth Metals in Nonaqueous Battery Systems, The Solid Electrolyte Interphase Model. J. Electrochem. Soc. 1979, 126 (12), 2047–2051.
Esta descoberta foi rapidamente adotada pela comunidade de baterias, e uma bateria de íon-lítio de próxima geração baseada em grafite, à medida que o material do ânodo era desenvolvido. Com este material anódico, as baterias com tensões de carga de 4,2 V foram produzidas pouco depois, resultando na densidade de energia de ~400 Wh/litro.
O desenvolvimento da bateria de lítio-íon não parou com estas importantes descobertas, mas muitas melhorias e alternativas foram relatadas desde então. Por exemplo, novos materiais catódicos têm sido continuamente identificados para uso em aplicações de baterias específicas, e dois desses materiais tiveram origem no grupo da Goodenough: o material espinélico Li1-xMn2O4 e o material olivino LixFePO4 (LFP).
[Padhi, A. K.; Nanjundaswami, K. S.; Goodenough, J. B. Phospho-Olivines as Positive-Electrode Materials for Rechargeable Lithium Batteries. J. Electrochem. Soc. 1997, 144, 1188-1194.
Thackeray, M. M.; David, W. I. F.; Bruce, P. G.; Goodenough, J. B. Inserção de Lítio em Espinélulas de Manganês. Mater. Res. Bull. 1983, 18, 461–472].
Este último material é limitado por um potencial um pouco menor em relação ao Li+/Li do que o LixCoO2, mas tem alta estabilidade e pode ser usado com taxas de carga elevadas. Vários outros materiais de eletrodos e sistemas de eletrólitos também foram descobertos, levando a materiais de armazenamento de energia sempre melhorados para o benefício da sociedade.
Que tipo de bateria é utilizada em veículos eléctricos?
Hoje em dia, a maioria dos EV usa baterias de iões de lítio. Anteriormente, foram usadas baterias de Ni-MH e chumbo-ácido, mas o seu uso diminuiu lentamente devido ao advento das baterias de iões de lítio, que possuem maiores valores de energia específica e maior densidade de energia. A energia específica das baterias de chumbo ácido é de cerca de 40-50 Wh/kg enquanto a bateria de iões de lítio tem cerca de 150 Wh/kg. O valor da densidade de energia para baterias de chumbo-ácido é de 80-100 Wh/litro enquanto a bateria de iões de lítio tem mais de 250 Wh/litro.
As células cilíndricas com catodos de níquel-cobalto-alumínio (NCA) e ânodos compostos de silício/grafite, como os utilizados nos últimos pacotes de baterias Tesla (2019-2020), atingiram aproximadamente 270 Wh/kg e 650 Wh/litro. Uma nova tecnologia chamada Licerion by Sion Power reivindica 500 Wh/kg de energia específica e 1000 Wh/L de densidade energética e >450 ciclos em células de desenvolvimento de 0,4 Ah.
Para pilhas pequenas, falamos em termos de Wh. Para sistemas de maior capacidade, é utilizada a unidade de kWh. O valor de Wh dividido por 103 dará o kWh.
Assim 850 Wh = 850/1000 = 0,850 kWh.
As células utilizadas na bateria EV actual podem atingir uma energia nominal específica de 140 -170 Wh/kg. A energia específica da bateria resultante é tipicamente 30 a 40 por cento mais baixa, ou 80 -120 Wh/kg. A redução deve-se a várias séries e fios de ligação paralelos, BMS e sistema de gestão térmica (refrigeração ou aquecimento). Em 2019, a percentagem de componentes não celulares desceu para cerca de 28 %.
Até agora, as células eram primeiro colocadas em módulos e depois colocadas em pacotes. Ambos Contemporary Amperex Technology Co. Limited, China (CATL) e Tesla decidiram que querem se livrar dos módulos e colocar as células em pacotes diretamente. CATL já o fez e chama-lhe tecnologia de célula a embalagem . Embora a informação sobre isto seja escassa, a empresa afirma que isto pode aumentar a energia específica em 10-15% e melhorar a utilização do volume em 15-20%. No total, pode alegadamente reduzir em 40% as peças necessárias para os pacotes de baterias. [https ://cleantechnica.com/2020/02/18/how-catl-lithium-iron-phosphate-batteries-could-be-leading-to-100-kwh-tesla-model-3/]
Designação da Bateria de Lithium
A Comissão Electrotécnica Internacional (IEC) e a Indian Standards Institution estabeleceram uma designação comum para descrever a química e o tamanho das células de iões de lítio.
[Pilhas e baterias de lítio secundário para aplicações portáteis, Comissão Electrotécnica Internacional, IEC 61960-1 e IEC 61960-2 e IS 16047: 2012].
As letras designam a química e o fator de forma, enquanto os números especificam as dimensões físicas da célula. A primeira letra descreve a química geral, a segunda letra designa a química catódica específica e a terceira letra designa a forma.
Primeira carta: I – Química de iões de lítio
Segunda carta: C – cobalto, F – ferro, Fp – fosfato de ferro, N – níquel, M – manganês, Mp – fosfato de manganês, T – titânio, V -vanádio e x – outros.
Terceira carta: R- cilíndrico, P-prismático
Os dois primeiros números que se seguem designam o diâmetro em mm e os três últimos designam a altura em décimos de mm. Assim, uma célula designada ICR19/66 é uma célula de íon lítio com um cátodo de cobalto que tem um diâmetro que é > 18 mm e ≤ 19 mm e uma altura total máxima que é > 65 mm e ≤ 66 mm.
Para as células prismáticas as letras iniciais têm o mesmo significado mas os dois primeiros números designam a largura em mm, os dois números seguintes são a altura em mm e os dois últimos números são o comprimento em mm. Assim, uma designação celular IMP9/35/150 descreve uma célula de iões de lítio prismáticos com uma célula catódica de manganês cuja espessura máxima é > 8 mm e ≤ 9 mm e uma largura máxima que é > 34 mm e ≤ 35 mm e uma altura total máxima que é > 149 mm e ≤ 150 mm.
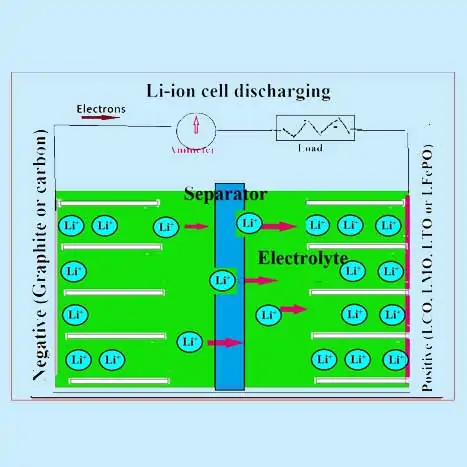
Como funciona uma bateria de iões de lítio?
como é feita a bateria de iões de lítio
Metal lítio com número atômico 3, densidade de 0,534 g/cc, com potencial de redução padrão muito baixo (casal Li+/Li -3,05 V vs. SSMA) e capacidade específica teórica de 3860 Ah/kg (2061 mAh/cc) é o peso mais leve, maior tensão e maior densidade de energia de todos os metais. (Compare com chumbo de número atômico 82, densidade 11,29 g/cc, capacidade específica teórica de 257,8 Ah/kg e potencial de redução padrão de -0,35V vs. SSMA).
Bateria de íons de lítio - Materiais ativos
Os materiais ativos do eletrodo positivo são qualquer um dos óxidos mistos como LiCoO2 ou LiMnO2 ou LiFePO4. O eletrodo negativo é principalmente grafite e compostos de carbono amorfo. É utilizado um electrólito orgânico (contendo um sal condutor de lítio dissociado, como o LIPF6). É utilizado um polipropileno (PP) ou polietileno (PE) ou um separador misto. Os íons de lítio migram entre os eletrodos das baterias de íons de lítio durante o carregamento e a descarga e são intercalados nos materiais ativos, conforme descrito abaixo:

Figura 9. Uma vista explodida de uma célula de iões de lítio
Crédito: Zhang Z., Ramadass P. (2012) Lithium-Ion Battery Systems and Technology. Para dentro: Meyers R.A. (eds) Encyclopaedia of Sustainability Science and Technology. Springer, Nova Iorque, NY, pp. 6124. http s://doi.org/10.1007/978-1-4419-0851-3_663
Como a bateria de iões de lítio carrega
Durante um processo de descarga em uma célula de íons de lítio (LIB), os íons de lítio do ânodo são desintercalados (ou extraídos) para o eletrólito e esses íons de lítio do eletrólito são intercalados no material catódico. Este movimento dos íons de ânodo para cátodo é acompanhado pela liberação de elétrons que flui no circuito externo. O processo inverso ocorre durante o processo de carga onde os íons de lítio se movem do cátodo e se intercalam no ânodo através do eletrólito. Os LIBs comerciais normalmente usam óxidos metálicos de transição como LiCoO2, LiMn2O4 e LiFePO4 como material catódico, que é revestido sobre um coletor de corrente de alumínio.
Dez a vinte por cento do carbono condutivo e 5 a 10 dos ligantes poliméricos como difluoreto de polivinilideno (PVDF) e politetrafluoroetileno (PTFE) também são adicionados juntamente com material ativo para melhorar a condutividade eletrônica e conseguir melhor aderência do material do eletrodo, respectivamente. O material do ânodo é revestido sobre um coletor de corrente de cobre com carbono condutor e PVDF, se necessário.
Os dois eletrodos são separados por um separador poroso (película de polietileno ou polipropileno de espessura 10-20 µm) embebido em uma solução eletrolítica (LiPF6 em um solvente orgânico). Tanto o separador como a solução electrolítica devem ter uma melhor condutividade iónica. A célula é normalmente fabricada num invólucro metálico em forma de gelatina com um separador por imersão de electrólitos entre os dois eléctrodos. Um esquema de uma LIB é mostrado nas figuras, onde são mostrados os processos típicos de carga e descarga.
As baterias recarregáveis de iões de lítio (Li-ion) empregam uma inserção/extração reversível de iões de lítio (Li+) (espécies hospedeiras) para ou a partir de uma matriz hospedeira (materiais activos de eléctrodos positivos e negativos) chamada compostos de inserção de lítio quando os processos de descarga e carga ocorrem. As baterias de iões de lítio têm sido referidas como baterias de cadeira de balanço porque os iões de lítio “balançam” entre os eléctrodos positivo e negativo à medida que a célula é carregada e descarregada.
O material activo positivo é tipicamente um óxido metálico com uma estrutura em camadas, como o óxido de lítio cobalto (LiCoO2), ou um material com uma estrutura em túnel, como o óxido de lítio manganês (LiMn2O4), na sua maioria num colector de corrente de alumínio. O material ativo negativo é tipicamente um carbono grafico, também um material estratificado, a maioria em um coletor de corrente de cobre. No processo de carga-descarga, os íons de lítio são inseridos ou extraídos do espaço intersticial entre as camadas atômicas dos materiais ativos.
Eletrolíticos não aquosos ou eletrólitos orgânicos são usados em células de lítio.
Os separadores para baterias de iões de lítio são filmes poliolefínicos microporosos de polietileno (PE) e polipropileno (PP).

Reações eletroquímicas das células em bateria de íons de lítio
Em uma célula típica de íons de lítio, ocorrem as seguintes reações genéricas.
Reacção positiva do eléctrodo:
LiMO2 ⇔ Li1-xMO2 + x Li+ + x e-
Reacção de eléctrodo negativa:
C + y Li+ + ye- ⇔ LiyC
Reacção celular total:
LiMO2 + x/y C ⇔ x/y LiyC + Li1-xMO2
M = metais como Co, Mn, Ni, Ti, etc.
Normalmente x é cerca de 0,5 e y é cerca de 0,16, portanto x/y é cerca de 3. [Jeff Dahn e Grant M. Ehrlich. “Lithium ion batteries”, Linden’s Handbook of Batteries,4ª edição, Thomas B. Reddy (Ed.), McGraw
Electrólito e Electrólito Sólido Interfásico (SEI)
Como mencionado anteriormente, electrólitos não aquosos ou electrólitos orgânicos são utilizados em células de lítio. As células Li operam com tensões comparativamente mais elevadas, até 4,2 V por célula. Embora sais volumosos de lítio como o hexafluorofosfato de lítio (LiPF6), arseniato de lítio hexafluoro (LiAsF6), tetrafluoroborato de lítio (LiBF4), perclorato de lítio (LiClO4), trifluorometanossulfonato de lítio (LiCF3SO3), difluoro(oxalato)borato de lítio (LIODFB), etc. Os electrólitos reais (que sustentam os sais electrolíticos), são os que necessitam de solventes adequados estáveis a uma tensão tão elevada. A maioria desses solventes tem altas constantes dielétricas, facilitando a dissociação iônica e a existência de íons de lítio altamente concentrados. Tais solventes também servem como bainhas de solvência para a existência estável dos íons Li, diminuindo assim a influência dos ânions contrários.
A desvantagem de ter constantes dielétricas altas é que elas têm valores de viscosidade mais altos que resultam em mobilidade prejudicada dos íons. Para superar a baixa condutividade iónica, os solventes de baixa viscosidade são normalmente misturados com solventes de alta viscosidade. Mas, como os solventes de baixa viscosidade têm uma menor dissociação iônica, torna-se imperativo atingir uma ótima proporção de mistura para que a mistura tenha boa condutividade iônica e boa mobilidade. Como solventes não aquosos, misturas de carbonato de etileno (EC) com carbonatos de alquilo lineares menos viscosos como o carbonato dimetílico (DMC), o carbonato dietílico (DEC) e o carbonato etil metílico (EMC) são utilizados em LIBs disponíveis comercialmente.
Os solventes aprox. são éteres, ésteres e carbonatos alquílicos: São éter dietílico (DEE), tetrahidrofurano (THF), dioxolano, carbonato de etileno (EC), carbonato de propileno (PC), carbonato de dimetilo (DMC), carbonato de dietilo (DEC), metil carbonato de etilo (CEM), metilformamida, γ-butyrolactone (BL), acetato de metilo, acetonitrilo (AN), sulfóxido de dimetilo (DMSO), dimetilformamida (DMF), cloreto de metilo, nitrometano, etc.)
Electrólitos líquidos são soluções de um sal de lítio em um ou mais solventes orgânicos, tipicamente carbonatos.
O carbonato de propileno (PC) não pode ser usado como eletrólito se a grafite for usada como anodo, pois o primeiro se decompõe na superfície da grafite; PC usado sozinho, sem CE ou pequenas adições de LiBOB) Li bisoxalato de borato), pode causar degradação nos eletrodos de grafite, pois co-intercala com o lítio, resultando em esfoliação.
O eletrólito é invariante (o mesmo número de íons que entram e saem do eletrólito durante a carga e
descarga). O sal eletrolítico é normalmente dissolvido em solventes carbonatados orgânicos. Cada fabricante tem uma combinação diferente de solventes com carbonato de etileno (EC), sendo um denominador comum para a maioria dos
A formação da camada interfásica de electrólitos sólidos (SEI) é outra função importante desempenhada pelos electrólitos. Quando um metal alcalino é imerso em um eletrólito de bateria, ou quando um potencial negativo é aplicado a um carbono ou a um eletrodo inerte imerso no eletrólito, um SEI começa a se formar.
A camada SEI formada instantaneamente ao contato do metal com a solução, consiste em produtos de redução insolúveis e parcialmente solúveis de componentes eletrolíticos. SEI é o fator chave que determina a segurança, capacidade de energia, morfologia dos depósitos de lítio, vida útil e duração do ciclo da bateria. A boa aderência ao ânodo também é importante.
Como enfatizado acima, as práticas pilhas alcalinas primárias ou secundárias ou alcalinas só podem ser construídas se a dissolução ou corrosão do ânodo puder ser interrompida. Portanto, o eletrólito deve ser projetado para conter pelo menos um precursor SEI que reage rapidamente com o lítio (ou com o ânodo álcali-metal) para formar uma interfase insolúvel sólido-eletrólito. Os produtos da redução de aniões salinos são tipicamente compostos inorgânicos como LiF, LiCl e Li2O, que precipitam na superfície do eléctrodo. A redução do solvente é seguida da formação de componentes insolúveis do SEI como o Li2CO3 e de semi-carbonatos e polímeros parcialmente solúveis.
No caso do eléctrodo de carbono, a tensão de formação do SEI depende do tipo de carbono, das propriedades catalíticas da sua superfície (teor de cinzas, tipo de plano cristalográfico, relação entre o plano basal e o plano da borda), da temperatura, concentração e tipos de solventes, sais e impurezas, e da densidade da corrente. Na primeira carga de uma bateria de iões de lítio, há uma perda de capacidade chamada “perda irreversível de capacidade” (QIR), principalmente necessária para a formação do SEI.
Além da formação do SEI, o QIR pode ser causado pela perda de capacidade associada à formação de produtos de redução solúvel (QSP).
O SEI sem contaminação é essencial para a longa duração do ciclo da bateria. Torna-se ainda mais importante durante a ciclagem a taxas elevadas e a uma maior profundidade de descarga.
O SEI em soluções de hexafluorofosfato de lítio (LiPF6) e hexafluoroarsenato de lítio (LiAsF6) tem uma maior resistividade em comparação com soluções de outros sais. Isto é devido a mudanças de resistividade que contribuem para a resistência controlada pelas espécies que levam à alta impedância interfacial do ânodo de lítio nos eletrólitos LiPF6 e LiAsF6. Além disso, Li2CO3 é declarado como um dos melhores agentes passivantes para o aumento da eficiência da ciclagem do lítio [J Electrochem Soc.,164 (7) A1703-A1719 (2017)].
Separadores para baterias de lítio-íon
Os separadores para baterias de iões de lítio são filmes microporosos de poliolefinas e são geralmente polietileno (PE) e polipropileno (PP), PE biaxialmente estirado ou PP/PE/PP multiaxialmente estirado.
Matérias-primas para os materiais activos em bateria de iões de lítio
As baterias de iões de lítio utilizam diferentes materiais catódicos. O ânodo é invariavelmente à base de carbono, excepto alguns como ânodos de óxido de titânio-nióbio, liga de Li-Si, etc. A seguinte tabela e figura dão algumas idéias sobre os diferentes produtos químicos empregados nestas baterias.

Figura 12. Um resumo de algumas opções atuais e futuras da química de eletrodos para baterias de íons de lítio. A capacidade proposta do Li(Si) é de 50% da capacidade teórica do material, semelhante ao caso encontrado para parte do material do eletrodo positivo
Crédito: Yu Miao, Patrick Hynan, Annette von Jouanne, e Alexandre Yokochi, Energies 2019, 12, 1074; doi:10.3390/en12061074]
Tabela 1.
Características das células de íons de lítio com diferentes materiais catódicos
| Material Catódico | Li-Ni-Co-Al (NCA) | Li-Ni-Mn-Co (NMC) | Li-MnO2 (LMO) | Fosfato de Li-Iron (LFP) | Li Titanate (LTO) | Óxido de Cobalto Li (LCO) |
|---|---|---|---|---|---|---|
| Tensão Nominal de uma célula (V) | 3.6 | 3.65 (2.7-4.2) | 3.8 | 3.25 (2-3.6) | 3.2 | 3.6 |
| Energia Teórica Específica (Wh/kg) | 279 | 256 | 148 | 128 (373) | 293 (175) | 274 (370) (x=0.5) |
| Capacidade específica para cátodos (Ah/Kg) Potencial vs Li/Li+ (V) | 180-200 (3.8) | 200 | 148 (4.1) | 150-170 (3.45) | 175 | 274 (3.9) (x=0.5) |
| Energia específica para cátodos (Wh/Kg) | 680-760 | 610-680 | 410-492 548 | 518-587 544 | -- | 546 |
| Segurança | cofre | Moderado | Cofre | Alto | Muito Bom | Moderado |
Materiais catódicos em bateria de íons de lítio
Os materiais catódicos devem satisfazer vários requisitos dos quais depende a seleção do material do eletrodo positivo.
- Para proporcionar alta capacidade, estes materiais devem incorporar uma grande quantidade de lítio, tal como é feito.
- Além disso, os materiais devem reversivelmente intercalar-se com pouca mudança estrutural para permitir uma longa vida útil do ciclo, alta eficiência em ampere-hora e alta eficiência energética.
- Para atingir alta tensão celular e alta densidade de energia, a reação de troca de lítio deve ocorrer com um alto potencial em relação ao lítio.
- Para facilitar os processos de carga e descarga de alta taxa, a condutividade eletrônica e a mobilidade de íons de lítio no material deve ser alta.
- O material do eletrodo positivo não deve se dissolver no eletrólito e deve estar disponível a um custo acessível. Para minimizar o custo, é preferível a preparação a partir de materiais baratos num processo de baixo custo
O LiFePO4 é uma excepção a esta regra. No LiFePO4, o transporte adequado de íons de lítio é conseguido através do uso de partículas de eletrodos com tamanho de partícula nanométrica. [Jeff Dahn e Grant M. Ehrlich. “Lithium ion batteries”, Linden’s Handbook of Batteries,4ª edição, Thomas B. Reddy (Ed.), McGraw Hill, pp. 26.6, 2011].
Os materiais ativos positivos (PAM) em células de íons de lítio variam de acordo com o fabricante. Os materiais catódicos podem ser classificados em três grandes categorias [Arumugam Manthiram, Nature Communications (2020) 11:1550] . Elas são:
Óxidos em camadas - materiais catódicos em bateria de íons de lítio
Vários óxidos do tipo geral LiMO2 (onde M =vanádio, cromo, cobalto e níquel) cristalizam em uma estrutura em camadas na qual os íons Li+ e M3+ ocupam a alternância [pistas da estrutura de sal de rocha para dar uma seqüência de camadas de O-Li-O-M-O.
No cátodo de óxido de lítio LiCoO2 em camadas, as grandes diferenças de carga e tamanho entre os íons Li+ e os íons Co3+ trivalentes levam a um bom ordenamento catiônico, que é crítico para suportar uma rápida difusão bidimensional de íons de lítio e condutividade no plano do lítio.
Os materiais catódicos requerem níveis de pureza extremamente elevados e devem estar quase totalmente isentos de impurezas metálicas indesejáveis – nomeadamente ferro, vanádio e enxofre.

Figura 13. Esquema simplificado de uma estrutura em camadas na qual existe uma ocupação alternada do
camadas de catiões entre as camadas de íons de óxido de cálcio fechadas.
[Crédito: Robert A. Huggins, Advanced Batteries, Materials Science Aspects, Springer, New York, 2009, p.168]
A boa estabilidade estrutural juntamente com a elevada condutividade eléctrica e de iões de lítio oferece características de carga-descarga rápida com boa reversibilidade. Com estas características, LiCoO2 permanece como um dos melhores catodos até à data com uma alta tensão de funcionamento de ~4 V. O cátodo LiCoO2 resolvido
dois grandes desafios associados aos cátodos de sulfureto perseguidos nos anos 70. Ele permitiu não só um aumento substancial da tensão operacional de <2,5 V para ~4 V, mas também a montagem de uma célula sem a necessidade de empregar um ânodo de lítio metálico.
Óxidos de spinel - materiais catódicos em bateria de íons de lítio
A segunda classe de cátodo é o espinélio LiMn2O4. (A fórmula geral é AB2O4). Embora esta estrutura seja geralmente retratada em coordenadas cúbicas, ela também possui camadas paralelas de íons óxidos em (111) planos, e existem tanto locais coordenados octahedralmente quanto locais coordenados tetraetricamente entre os planos de íons óxidos. O número de locais octaédricos é igual ao número de iões de óxido, mas há o dobro de locais tetraédricos. A estabilidade estrutural tridimensional e a alta condutividade elétrica e de íons de lítio oferecem características de carga-descarga ainda mais rápidas para Li1-xMn2O4 com boa reversibilidade em comparação com o LiCoO2.
Uma vantagem importante ao passar de LiCoO2 para LiMn2O4 é a redução significativa no custo, já que o manganês é duas ordens de magnitude inferior ao custo do Co. Entretanto, uma questão crítica com o LiMn2O4 é a dissolução do manganês da malha para o eletrólito na presença de quantidades vestigiais (níveis de ppm) de íons H+ (acidez) no eletrólito devido às bem conhecidas desproporções de Mn3+ a Mn4+ e Mn2+ em ácido.

Figura 14 . Esquema da estrutura espinélica na qual os cátions são distribuídos entre os planos fechados (111) de íons de óxido entre os locais tetraédricos e octaédricos [Crédito: Robert A. Huggins, Advanced Batteries, Materials Science Aspects, Springer, New York, 2009, p.17].
O material catódico de alta voltagem óxido de lítio-níquel-manganês (LNMO) parece promissor nas baterias da próxima geração. Mas o obstáculo é a falta de um eletrólito que possa lidar com as tensões de uma bateria baseada em LNMO. As células de bateria baseadas em cátodo LNMO fornecem resultados ao mesmo nível de outras baterias de alto desempenho baseadas em lítio, mas a um custo consideravelmente mais baixo.
No entanto, os fabricantes de electrólitos estão a obter resultados muito promissores da investigação e desenvolvimento em curso que, a dada altura, resultarão em electrólitos que funcionarão bem numa célula de bateria LNMO. https ://blog.topsoe.com/the-cathode-material-for-next-generation-lithium-ion-batteries-is-ready
Mais recentemente, o aumento do conteúdo de Ni e a redução ou eliminação do conteúdo de cobalto nos catodos NMC está se tornando muito mais proeminente [Li, W., Erickson., E. & Manthiram, A. Catodos de óxido de lítio para baterias automotivas à base de lítio, Nat. Energy 5, 26-24(2020)].
Óxidos de polianião - materiais catódicos em bateria de iões de lítio
A terceira classe de óxidos é a dos óxidos de polianião. Óxidos de polianião como Fe2(MoO4)3 e Fe2(WO4)3 foram submetidos a inserção/extração reversível de dois íons de lítio por unidade de fórmula para dar Li2Fe2(MoO4)3 ou Li2Fe2(WO4)3 ambos por métodos químicos e eletroquímicos
[Manthiram, A., Goodenough, J. B. Inserção de lítio em estruturas Fe2(MO4)3 : comparação de M = W com M = Mo. J. Química de Estado Sólido. 71, 349–360 (1987)].
Baseado nas obras de Manthiram e Goodenough,
[Manthiram, A. & Goodenough, J. B. Inserção de lítio em estruturas Fe2(MO4)3: comparação de M = W com M = Mo. J. Química de Estado Sólido. 71, 349–360 (1987). Manthiram, A. & Goodenough, J. B. Inserção de lítio na estrutura Fe2(SO4)3. J. Power Sources 26, 403-406 (1989)].
A exploração de fosfatos contendo lítio como cátodos levou à identificação de LiFePO4 olivina como cátodo [Padhi, A. K., Nanjundaswamy, K. S. & Goodenough, J. B. Phospho-Olivines como materiais de eletrodo positivo para baterias de lítio recarregáveis. J. Electrochem. Soc. 144, 1188-1194 (1997] em 1997.
Mas, a classe de óxido de polianião sofre de baixa condutividade electrónica.[Arumugam Manthiram, Nature Communications (2020) 11:1550].
A exploração de fosfatos contendo lítio como cátodos levou à identificação de LiFePO4 olivina como cátodo [Padhi, A. K., Nanjundaswamy, K. S. & Goodenough, J. B. Phospho-Olivines como materiais de eletrodo positivo para baterias de lítio recarregáveis. J. Electrochem. Soc. 144, 1188-1194 (1997] em 1997.
Mas, a classe de óxido de polianião sofre de baixa condutividade electrónica.[Arumugam Manthiram, Nature Communications (2020) 11:1550].
Fabricação de materiais catódicos - Bateria de iões de lítio
Anteriormente, os compostos catódicos de óxido de lítio metálico eram feitos de carbonato de lítio e um sal do metal escolhido por meio de uma série de reações químicas de substituição realizadas em solução. O produto desejado é precipitado e seco por spray.
LiCoO2 foi inicialmente preparado pelo método de síntese convencional indicado na figura. O tetraóxido de tricobalto (Co304) e o carbonato de lítio (Li2CO3) foram bem misturados, seguidos pela calcinação no fluxo de ar a uma temperatura de cerca de 950ºC. Por este método, porém, era muito difícil preparar partículas grossas de LiCoO2 e só se conseguiam obter partículas finas com diâmetros de 1-3 pm.
Materiais de eletrodos ativos finos não são desejáveis do ponto de vista da segurança. No caso de abusos como curto-circuito externo ou esmagamento, partículas finas com grande área de superfície específica reagem facilmente de uma só vez e toda a energia da célula é libertada abruptamente num curto espaço de tempo com o consequente aumento da temperatura. Na pior das hipóteses, a célula pode pegar fogo [Yoshio Nishi, em Lithium ion Batteries, M. Wakihara e 0. Yamamoto (Eds.). página 192-193].
Como é fabricada a bateria de iões de lítio? fluxograma
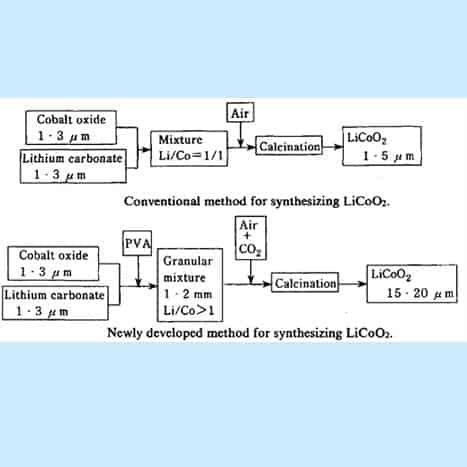
Figura 15. Fluxograma para fazer o Li-CoO2
[Crédito: Yoshio Nishi, em Lithium ion Batteries, M. Wakihara e 0. Yamamoto (Eds.). página 192-193].
Um processo melhorado para sintetizar cobaltita de lítio de maior tamanho de partícula: O primeiro ponto é que uma pequena quantidade de resina PVA é adicionada nas misturas de matérias-primas (Co304 e Li2CO3) para formar granulados granulados com um granulador. Ao sinterizar as pastilhas em um fluxo de ar contendo quantidade adequada de gás C02, são sintetizadas partículas de lítio cobaltita com diâmetro médio de 20pm. O segundo ponto é que usamos uma quantidade ligeiramente excessiva de carbonato de lítio (Li2CO3) nas matérias-primas, de modo que a razão Li/Co atômica nas matérias-primas é maior do que uma. Este procedimento também é favorável para a obtenção de partículas grosseiras e, além disso, o LiCoO2 resultante contém uma pequena quantidade de Li2CO3 residual.
O primeiro ponto é que uma pequena quantidade de resina de PVA é adicionada nas misturas de matérias-primas (Co304 e Li2CO3) para formar granulados granulados com um granulador. A sinterização do óxido de cobalto de lítio pode ser facilmente preparada através da queima a alta temperatura de uma mistura estequiométrica de carbonato de lítio Li2CO3 e óxido de cobalto, Co3O4 ou cobalto metálico a 600-800°C, recozendo depois o produto a 900°C durante muitas horas, tudo sob uma atmosfera de oxigénio.
Também pode ser obtido por calcinação de óxido hidratado com hidróxido de lítio até 750-900°C.
Um terceiro método utiliza acetato de lítio, acetato de cobalto e ácido cítrico em quantidades molares iguais, em solução aquosa. O aquecimento a 80°C transforma a mistura num gel transparente viscoso. O gel seco é então moído e aquecido gradualmente até 550°C. (https: //en.wikipedia.org/wiki/Lithium_cobalt_oxide).
Alguns exemplos típicos são: Método Sol-gel
Em um processo sol-gel, as soluções aquosas dos reagentes e uma solução de agente quelante são misturadas. A evaporação lenta do solvente gera um sol e um aquecimento moderado do sol assim obtido produz um gel. Este último é calcinado a uma temperatura adequada para obter o produto desejado.
Exemplo 1.
Síntese de LiCoO2 a partir de diferentes agentes complexantes: Os sais utilizados foram o nitrato de cobalto hexa hidratado (Co(NO3)2,6H2O, e o nitrato de lítio, LiNO3 anidro. O gel foi produzido utilizando quatro agentes complexantes diferentes: ácido cítrico, anidro (C3H4OH(COOH)3, glicina, (H2NCH2COOH); amido (amido de milho comercial e gelatina).
São preparadas cinco soluções contendo LiNO3 e Co(NO3)2.6H2O em 20 ml de água, com uma proporção de Li:Co = 1.1:1. Um agente complexante específico é adicionado a cada solução:i) ácido cítrico (4,611 g) diluído em 5 ml de água;ii) glicina (1,501 g);iii) amido (1,250 g);iv) gelatina (3,500 g) ev) ensaio em branco.
As primeiras quatro soluções foram aquecidas a uma temperatura de 70 a 80°C em banho de glicerina até a formação do gel. A quantidade de tempo deste processo é diferente para cada agente gelificante:(i) ácido cítrico (5 horas),(ii) glicina (3 horas),(iii) amido (1 hora),(iv) gelatina (3 horas). A produção de pós cristalinos para todas as amostras foi realizada em duas etapas em um forno de mufla: primeiro com a queima dos materiais a 300°C por 20-30 minutos e depois com o aquecimento a 700°C por 24 h. [Bruno G. A. Freitas e outros, J. Braz. Chem. Soc. 28, 11, Nov. 2017].
Exemplo 2.
Preparado por um método Sol-Gel
O LiNO3 é dissolvido pela primeira vez em solução de ácido cítrico. LiNO3, Ni(NO3)2.6H2O Co(Ac)2.4H2O e Mg(NO3)2.6H2O foram utilizados como matérias primas de lítio, níquel, cobalto e magnésio em LiNi0.7-𝑥M𝑥Co0.3O2(0 ⩽ 𝑥 ⩽ 0.1), respectivamente. A quantidade de ácido cítrico é igual à quantidade molar total de Co, Ni, e Mg. Em seguida, Co(Ac)2 4H2O, Ni(NO3)2 6H2O e Mg(NO3)2 6H2O foram adicionados à mistura. Toda a mistura foi aquecida por banho-maria em 80∘C. Durante o processo de aquecimento, forma-se uma solução transparente e cor-de-rosa sem qualquer precipitação. Finalmente, a solução transparente foi lentamente seca e transformada em gel. O xerogel foi seco, moído e depois tratado termicamente num forno a 120°C durante 12h.
O precursor do gel foi calcinado a 500°C em ar por 6 horas, e resfriado à temperatura ambiente em um forno tubular. Os produtos tratados termicamente foram moídos numa argamassa de ágata para obter os pós. E depois o pó foi calcinado a 800°C durante 12 horas. Para a fabricação dos cátodos, os produtos preparados foram primeiramente misturados com acetileno preto e fluoreto de polivinilideno (80: 8:12 em peso) em 𝑁-methyl pyrrolidone (NMP). O chorume obtido foi então revestido em folha de alumínio e seco a 80oC durante 18 h para nova prensagem do rolo. . [Hailang Zhang, Advances in Materials Science and Engineering Vol 2014, Artigo ID 746341,]

Figura 16. Fluxograma do processo sol-gel para preparar o manganato de lítio
(Crédito: Y.S. Lee, Y.K. Sun e K.S., Nahm, Solid State Ionics 109 (1998) 285 como dado por, M. Pasquali, S. Passerini e G. Pistoiaem Lithium Batteries, Science and Technology, ed. por G. A. Nazri e G. Pistoia, Springer, Nova York, (2009), p. 318)
Fabricação de materiais anódicos em bateria de íons de lítio
O caminho encorajador que leva aos LIBs com melhor energia e densidade de potência é a seleção de materiais anódicos adequados que podem proporcionar alta capacidade e facilidade de difusão de Li-ion para o ânodo, juntamente com uma boa vida útil do ciclo e livre de preocupações de segurança.
Com base nos materiais precursores, os ânodos de carbono podem ser classificados em vários tipos, como indicado abaixo.
O material precursor e os parâmetros de processamento determinam a natureza do carbono produzido. Os materiais que podem ser grafitados por tratamento a alta temperatura (2000 a 3000°C) são denominados carbonos macios .
Ao grafitar, o distúrbio turboestático é removido progressivamente com o aumento da temperatura e a tensão no material é aliviada [T]. Zheng, J. N. Reimers, e J. R. Dahn, Física. Rev. B 51, 734 (1995)] Carvões duros como as preparadas a partir de resina fenólica, não podem ser facilmente grafitadas, mesmo quando tratadas a 3000°C. Os materiais do tipo coque são preparados a cerca de 1000°C, normalmente a partir de um precursor aromático de petróleo [Jeff Dahn e Grant M. Ehrlich. “Lithium ion batteries”, Linden’s Handbook of Batteries,4ª edição, Thomas B. Reddy (Ed.), McGraw Hill, pp. 26., 2011]

Figura 17. Classificação de materiais precursores de ânodos de carbono
[Crédito: Jeff Dahn e Grant M. Ehrlich. “Lithium ion batteries”, Linden’s Handbook of Batteries,4ª edição, Thomas B. Reddy (Ed.), McGraw Hill, pp. 26., 2011]
Goriparti divide os materiais anódicos da LIB em três categorias dependendo do seu mecanismo de reacção com o lítio [Subrahmanyam Goriparti, Ermanno Miele, Francesco De Angelis, Enzo Di Fabrizio, Remo Proietti Zaccaria, Claudio Capiglia, J Power Sources 257 (2014) 421-443]
O grupo de intercalação/de-intercalação
Esta categoria de ânodo inclui materiais carbonáceos e óxidos de titânio. A capacidade de armazenamento que ocorre através de um caminho de intercalação está intimamente associada à área de superfície, morfologia, cristalinidade e sua orientação. Os carbonos macios são geralmente bem aceitos e utilizados na indústria de baterias. Foi visto que o carbono macio é uma tecnologia bastante madura, enquanto o carbono duro pode apresentar uma solução alternativa interessante, especialmente para aplicações que requerem alta capacidade, como no setor de veículos elétricos. Os ânodos de óxido de titânio já são utilizados por algumas indústrias de baterias.


O Graphene também foi amplamente revisto. Em particular, verificou-se que as suas propriedades eléctricas tornam este material especialmente adequado para os ânodos híbridos grafeno/metal (por exemplo, grafeno com SnO2 e Fe2O3). Os nano-tubos de carbono (CNTs) foram significativos pelos seus resultados académicos muito interessantes, embora o custo de produção possa dificultar a sua aplicação como material anódico activo na indústria de baterias para o futuro.


No entanto, para grandes baterias EV, os grafites de baixo custo são normalmente preferidos devido a considerações de custo.
Em uma segunda categoria, foram descritos materiais de liga como Si, Ge, SiO, SnO2. Estes materiais podem fornecer maiores capacidades e alta densidade de energia em relação ao grupo anterior, reagindo com lítio em um mecanismo eletroquímico de liga/deliga. No entanto, este processo implica uma grande expansão de volume que resulta numa perda substancial de capacidade ao pedalar. A redução das dimensões a granel para a nanoescala, juntamente com a realização de estruturas complexas pela combinação com matrizes condutoras, foi proposta para superar as questões acima especificadas e para melhorar o desempenho geral do ânodo.
Silício e SnO2 e seu composto com carbono são os materiais mais promissores para aplicações em futuras baterias de lítio, no entanto, ainda é necessária uma forma barata para sua produção em massa como materiais anódicos. Por outro lado, Ge, embora interessante por suas propriedades eletroquímicas e excelentes resultados experimentais em laboratório, sofre do inconveniente de ser o elemento do quinquagésimo escalão em termos de abundância na crosta terrestre. Portanto, parece não ser uma boa opção para a aplicação em massa da tecnologia de bateria de lítio.
No terceiro grupo, foram descritos os materiais que reagem com lítio de maneira de reação de conversão. Em particular, foram considerados os óxidos/fosforetos/nitretos/sulfuretos metálicos. No entanto, estes materiais ainda estão longe do grande mercado comercial de baterias de lítio, devido à fraca retenção de capacidade e à grande histerese potencial. Portanto, uma variedade de formas nano-estruturadas destes materiais também foram investigadas para resolver os problemas acima identificados.
Uma nanotecnologia é definitivamente uma abordagem formidável para a engenharia da próxima geração de materiais anódicos para baterias de lítio. Para utilizar os materiais descritos como ânodos eficazes em LIBs comerciais, especialmente para aplicações EV, é contudo necessário mais trabalho de pesquisa. Na verdade, é necessário conseguir tanto uma maior energia como uma maior densidade de potência, juntamente com o desenvolvimento de processos de fabricação baratos para a síntese em larga escala de materiais nanosized. Além disso, a investigação dos mecanismos que regem a interacção entre o lítio e as formas nanosizadas dos materiais descritos, juntamente com as propriedades de transporte de electrões na interface eléctrodo/electrolito, é de importância crucial para a concepção da próxima geração de materiais anódicos activos concebidos pela nanotecnologia.
Os eletrodos negativos atualmente empregados nas células de lítio envolvem uma solução sólida de lítio em uma das formas de carbono. As células de lítio que operam a temperaturas acima do ponto de fusão do lítio devem necessariamente usar ligas de lítio em vez de lítio elementar. Estas são geralmente fases binárias ou ternárias metálicas. Há também um interesse crescente na possibilidade do uso de ligas metálicas em vez de carbonos à temperatura ambiente, com o objectivo de reduzir o volume do eléctrodo, bem como de conseguir um aumento significativo da capacidade. [Robert A. Huggins, Advanced Batteries, Materials Science Aspects, Springer, Nova York, 2009, p.123].
A grafite é anfotérica, e tanto cátions como ânions podem ser inseridos nela entre as camadas de grafeno. Quando os cátions são inseridos, a estrutura de grafite do hospedeiro assume uma carga negativa. Exemplos de cátions são Li+, K+, Rb+, e Cs+. Quando os ânions são inseridos, a estrutura de grafite do hospedeiro assume uma carga positiva, e os exemplos de ânions são Br − , SO2- , SbF6-
A inserção de metais alcalinos no carbono foi demonstrada pela primeira vez em 1926 [ K. Fredenhagen e G. Cadenbach, Z. Anorg. Allg. Chem. 158, 249 (1926)] e a síntese química de lítio-carboneto foi demonstrada em 1955 [D. Guerard, A. Herold, Carbon 13, 337 (1975)]. Raio-x experimentos com espectroscopia de fotoemissão mostraram que o lítio inserido entrega o seu elétron ao carbono, e assim a estrutura pode ser vista como íons Li+ contidos entre as camadas de carbono da estrutura de grafite
[G.K. Wertheim, P.M.Th.M. Van Attekum e S. Basu, Solid State Commun. 33, 1127 (1980)]. Uma revisão geral do trabalho inicial sobre a inserção de espécies em grafite pode ser encontrada em
[L.B. Ebert, Intercalation Compounds of Graphite, em Annual Review of Materials Science,
Vol. 6, Ed. por R.A. Huggins, Annual Reviews, Palo Alto, CA (1976), p. 181].
O fator importante na pureza do material do ânodo é a necessidade de eliminar qualquer espécie contendo oxigênio na superfície, pois estas reagiriam com o eletrólito. Para evitar esta reacção, os fabricantes cozem o grafite a 1100ºC) em atmosferas redutoras ou inertes. Isto aumenta o custo para outros usos, em comparação com o grafite. O carbono (90%) é misturado com vários outros ingredientes para fazer a pasta de ânodo ou chorume. Tal como no cátodo, o fluoreto de polivinilideno (PVDF) é usado como ligante (-5%), e uma pequena quantidade de negro de fumo é adicionada para garantir a condutividade. Além disso, a n-metilpirrolidona (NMP) é utilizada para solubilizar os materiais para formar uma mistura uniforme. A pressão assegura uma granulometria uniforme (Sandi 1999).
O titanato de lítio (LTO) está ganhando muito interesse. As células LTO operam a uma temperatura mais baixa do que outras químicas e oferecem uma alta densidade de potência. No entanto, tais células sofrem de uma tensão nominal mais baixa, na faixa de cerca de 2,2-2,3 V por célula. Norio Takami, Hiroki Inagaki, Yoshinao Tatebayashi, Hidesato Saruwatari, Keizoh Honda, Shun Egusa, J Power Sources 244 (2013) 469-475]
O material do eletrodo, tipicamente grafite, expande em 10 % durante o processo de carga. O grafite recupera seu volume original quando os íons de lítio se desintercalam. Os iões de lítio não só seriam intercalados no grafite se fosse utilizado alumínio, mas também inseridos no condutor, formando assim uma liga de alumínio-lítio. O processo inverso ocorreria durante o descarregamento. O alumínio seria degradado após alguns ciclos e seria inútil como um coletor de corrente.
Entretanto, se o eletrodo negativo é feito de titanato de lítio em vez de grafite, a situação muda drasticamente. O potencial de eletrodos do Li4Ti5O12 é cerca de 1,4 V maior que o da grafite (a tensão da célula é cerca de 1,4 V menor, 2,2 V contra 3,6 V). Isto evitaria que os íons de lítio fossem intercalados no alumínio. Portanto, o alumínio é preferível ao cobre por razões relacionadas com o custo e o peso. Li4Ti5O12 é utilizado principalmente em aplicações estacionárias devido à sua menor tensão de célula.Călin Wurm et al., em Lithium-Ion Batteries, Reiner Korthauer (ed), Translated by Michael Wuest et.al., Springer, 2018. pp. 57].
Processo para a produção de titanato de lítio: Uma mistura de dióxido de titânio e um composto de lítio (qualquer um destes: carbonato de lítio, hidróxido de lítio, nitrato de lítio e óxido de lítio) é pré-sinterizada a uma temperatura entre 670°C e 800°C. É obtido um composto constituído por TiO2, e Li2TiO3 ou um composto constituído por TiO2, Li2TiO3, e Li4Ti5O12. O composto é então sinterizado a uma temperatura na faixa de 800 a 950°C. [Tetsuya Yamawaki et.al., U S Patent 6,645,673 B2, 2003 Assigned to Toho Titanium Co., Ltd., Chigasaki]
Toshiba’s SCiB™ Bateria recarregável (https://www.scib.jp/en/)
SCiB™ utiliza óxido de lítio e titânio (LTO) em seu ânodo para alcançar segurança, longa vida útil, desempenho a baixa temperatura, carregamento rápido, alta potência de entrada/saída e grande capacidade efetiva. SCiB™ encontrou amplas aplicações em veículos, aplicações industriais e de infra-estrutura, incluindo automóveis, ônibus, vagões ferroviários, elevadores e usinas de energia.
Produção de separador de iões de lítio
Dois tipos de processo estão disponíveis: úmido e seco. Os fabricantes japoneses utilizam um processo úmido no qual o polímero é dissolvido em óleo. O óleo é então evaporado para deixar um filme poroso. Eles utilizam polímeros de ultra-alto peso molecular para produzir Celgard, três camadas de filme de polímero soprado são laminadas, puxadas para baixo e recozidas abaixo do ponto de fusão para controlar a estrutura do polímero. A folha é então rapidamente esticada para obter porosidade.
Dois tipos de processo estão disponíveis: úmido e seco. Os fabricantes japoneses utilizam um processo úmido no qual o polímero é dissolvido em óleo. O óleo é então evaporado para deixar um filme poroso. Eles utilizam polímeros de ultra-alto peso molecular para produzir Celgard, três camadas de filme de polímero soprado são laminadas, puxadas para baixo e recozidas abaixo do ponto de fusão para controlar a estrutura do polímero. A folha é então rapidamente esticada para obter porosidade.
[Pekala, R.W., et al., 2000, “Separadores”: An Overlooked Opportunity to Enhance Battery Performance?”, 17th International Seminar and Exhibit on Primary and Secondary Batteries, Ft. Lauderdale, Fla., March 6-9].
Este processo é muito sensível às condições de operação e até varia com os lotes de material, portanto é necessário um controle cuidadoso [Linda Gaines e Roy Cuenca, Cost of Lithium ion batteries for Vehicles, ANL Report ANL/ESD-42, maio de 2000, pp. 20 ].
No entanto, a espessura adicional necessária em separadores para células EV/HEV compensa a resistência reduzida. [Y. Nishi, entra: M. Wakihara, O. Yamamoto (Eds.), Lithium Ion Batteries, Wiley/VCH/Kodansha, Tóquio, 1998, p. 195.
P. Arora, Z. Zhang, Chem. Rev. 104 (2004) 4419].
Além das características convencionais, como boa resistência mecânica, permeabilidade eletrolítica, estes separadores microporosos apresentam uma propriedade protetora durante o abuso celular. Por exemplo, se a temperatura da célula subir anormalmente devido a uma sobrecarga excessiva, por exemplo, o calor gerado amolece o PE e fecha os microporos do filme. Isto é chamado de separador “desligar”. Uma vez que o desligamento ocorre, o transporte iônico entre os eletrodos é efetivamente interrompido e a corrente deixa de fluir. Se o separador puder manter a integridade mecânica acima de sua temperatura de desligamento, ele pode proporcionar uma margem de segurança ao dispositivo; caso contrário, os eletrodos podem entrar em contato direto, reagir quimicamente, levando à fuga térmica.
No entanto, é possível que, devido à inércia térmica, a temperatura possa continuar a subir mesmo após o desligamento. Nessas condições, o separador derreteria e encurtaria os eléctrodos, levando a reacções violentas e à geração de calor. Este fenômeno é chamado “derretimento” ou “quebra” do separador. Portanto, a fim de garantir a segurança da célula, a diferença entre as temperaturas de “desligamento” e “derretimento” deve ser a maior possível.
Os separadores feitos inteiramente de polietileno de alta densidade derretem a 135°C e perdem a integridade mecânica acima desta temperatura. Contudo, os separadores feitos por camadas de laminação de polipropileno e polietileno mantêm a integridade mecânica pelo menos até 165°C, o ponto de fusão do polipropileno. É interessante notar que embora o polietileno de ultra-alto peso molecular derreta a 135°C, os separadores feitos deste material retêm sua integridade mecânica até pelo menos 180°C, pois a viscosidade do material é tal que mantém sua integridade física.
Os separadores são fiáveis e os fabricantes de baterias de iões de lítio estão a optar cada vez mais pela sua incorporação nos seus produtos. Os separadores de desligamento mais comuns têm polipropileno de alto peso molecular misturado com polietileno de super-alto peso molecular. Aqui, a propriedade única de desligamento do polietileno é combinada favoravelmente com a alta integridade mecânica do polipropileno a temperaturas elevadas. Como o desligamento é irreversível, uma vez accionado, estes separadores deixam as células permanentemente danificadas. [P.G. Balakrishnan, R. Ramesh, T. Prem Kumar, J. Power Sources. 155 (2006) 401–414]
Outros materiais em bateria de iões de lítio
Existem outros materiais como coletores de corrente como alumínio, folhas de níquel e cobre, ligantes comocopolímero de estireno-butadieno (SBR), efluoreto de polivinilideno (PVDF), eletrólitos e solventes, aditivos condutores de cátodo, separador.
Vantagens & Limitações da Bateria de iões de lítio - Fabrico de células de iões de lítio
Relação entre o peso do ânodo e do cátodo
É muito importante que não se forme metal de lítio durante a operação celular. A deposição dos dendritos das formas metálicas que internamente encurtam a célula. O controle de voltagem durante o carregamento e o equilíbrio celular ajudam a reduzir este problema em grande parte. O principal método para controlar a deposição de lítio é a relação entre o ânodo e a capacidade catódica das placas individuais na célula. O eléctrodo anódico tem uma capacidade de utilização cerca de 10% maior do que o cátodo. Isto evita a deposição de lítio metálico no ânodo durante a carga, uma vez que o cátodo determina a capacidade da célula. Se houver depósitos de lítio metálico na superfície do eletrodo, ele reage com o eletrólito e pode iniciar uma fuga térmica.

Figura 21. Taxa de capacidade anódica e catódica na célula de íons de lítio
(Crédito: Ralph J. Brodd e Kazuo Tagawa, em Advances in Lithium-Ion Batteries, Walter A. van Schalkwijk e Bruno Scrosati (Eds), Kluwer Academic Publishers, New York, pp. 272, 2002).
Processos de montagem de células de íons de lítio
Os processos de montagem de células para uma bateria de íons de lítio requerem precisão e precisão ao revestir o estoque de eletrodos positivos e negativos revestidos com o material ativo. O processo de revestimento é um elemento crítico para garantir um produto de alta capacidade e alta confiabilidade. Se os revestimentos forem de má qualidade, apenas serão produzidas baterias de baixo desempenho. Os passos iniciais na preparação da massa activa determinam o resultado.
Cohen e Gutoff [E. Cohen e E. Gutoff, Modern Coating and Drying Technology, Wiley-VCH,
New York, 1992] descreve uma metodologia para chegar à melhor técnica de revestimento para uma determinada aplicação, baseada na reologia do slurry de revestimento, que requer precisão e velocidade de revestimento.

Figura 22. Processo de revestimento anódico e catódico
(Crédito: Ralph J. Brodd e Kazuo Tagawain in Advances in Lithium-Ion Batteries, Walter A. van Schalkwijk e Bruno Scrosati (Eds), Kluwer Academic Publishers, New York, pp. 273, 2002).
Fluxograma para fabricação de bateria de íons de lítio

Figura 23. FLUXOGRAMA PARA FABRICAÇÃO DE CÉLULAS DE ÍONS DE LÍTIO
[Ralph J. Brodd e Kazuo Tagawa em Avanços em Baterias de Lithium-Ion, Walter A. van Schalkwijk e Bruno Scrosati (Eds.), Kluwer Academic Publishers, New York, pp. 271, 2002].

Crédito: Electropaedia https: //www.mpoweruk.com/battery_manufacturing.htm
Figura 24. Fluxograma para o fabrico de eléctrodos a partir de matérias-primas
Conjunto de células de íons de lítio




Os fabricantes de baterias de íons de lítio visam os seguintes pontos durante a montagem das células:
- Os desenhos para a célula de íons de lítio devem resultar em uma densidade de corrente uniforme em toda a área do eletrodo.
- Para assegurar um bom contacto entre os materiais activos (AM) e o colector actual
- Os eletrodos de grande superfície são empregados para dar às células um desempenho de alta taxa. Isto reduz a polarização, ou seja, as perdas de tensão devido à cinética das reações do eletrodo e diminui a queda de tensão através do separador.
A estrutura dos poros e a combinação de carbonos condutores proporcionam um bom contacto inter-partículas do material activo.
Umbom contato é essencial entre os materiais ativos, o carbono condutivo e o coletor de corrente, para o pleno aproveitamento dos materiais ativos e para uma boa eficiência durante a alta taxa de desempenho.
A mistura de cobalto catódico é preparada a partir de LiCoO2 (um pó preto) + ligante PVdF (um fluoropolímero termoplástico semi-cristalino branco) + N-metilpirrolidona (NMP, um líquido orgânico incolor) como solvente. Sendo LICoO2 não condutor, um diluente condutor, invariavelmente um negro de fumo, é adicionado para melhorar a condutividade do LiCoO2.
A relação e as quantidades dos materiais são determinadas pelo design da célula e pelo tamanho do misturador. Um procedimento intensivo de mistura é utilizado para misturar a seco o material activo não condutor e o carbono antes de adicionar o solvente de revestimento e o aglutinante.
A mistura é misturada a seco para dar um revestimento uniforme das partículas do material activo com uma película fina do carbono condutor de modo a que o contacto eléctrico entre o AM e a grelha colectora de corrente (folha de alumínio, 20 mm de espessura) seja melhorado, garantindo assim o pleno aproveitamento de todo o AM. O polímero NMP é dissolvido no solvente do revestimento em um recipiente separado. A mistura a seco e a solução de solvente são então combinados para formar um chorume.
As adições de solventes são utilizadas para ajustar a viscosidade da lama (ou tinta) para a operação derevestimento . Opolivinilenodifluoreto de vinilo (PVdF) é o ligante de eleição e o O solvente é N-metilpyrollidinona (NMP). O chorume da operação de mistura é colocado em recipientes selados, que servem como reservatório e meio de transferência para as operações de revestimento. Quantidades precisas de polpa de revestimento são bombeadas do recipiente de armazenamento com uma bomba de engrenagem, ou bomba de precisão similar, para evitar qualquer arrastamento de ar no fluido que vai para o cabeçote de revestimento.
A mistura de ânodos é preparada de forma semelhante com carbono duro, ligante PVdF e NMP. Esta mistura é revestida sobre uma folha de cobre utilizada como grelha (10 mm de espessura).
O revestimento é feito em ambos os lados até cerca de 100 mm de espessura, tanto para ânodos como para cátodos. Diminuindo a espessura do revestimento consegue-se um aumento na área total da superfície para um volume definido da célula. Os eletrólitos orgânicos utilizados possuem menor condutividade em comparação com os aquosos e, portanto, esta maior superfície facilitará uma célula de descarga de alta potência.
A espessura do eléctrodo depende da potência máxima necessária. Uma característica única da tecnologia de fabricação de baterias de íons de lítio é que ela permite uma ampla gama de projetos de relação potência/energia com a mesma tecnologia de fabricação de eletrodos [Broussely, Nazri pp 651]. Mas a recolha de corrente e as separações adequadas, a forma e o design das células são importantes.
Montagem de células: A folha revestida passa por um forno para evaporar o solvente e deixar uma quantidade precisa de massa ativa sobre a folha. Muitos solventes de revestimento são classificados como perigosos e não podem ser liberados para a atmosfera. Como medida de economia de custos, o solvente é geralmente recuperado para reutilização no processo. Para evitar qualquer contaminação do ambiente, o solvente pode ser incinerado.
A maioria das células de íons de lítio são de forma cilíndrica. O rolo de geleia é achatado para obter elementos para as células prismáticas.
As células prismáticas são favoráveis para um melhor enchimento do volume, mas são susceptíveis de inchar ao ciclismo ou ao envelhecimento. As latas de células cilíndricas oferecem melhor resistência mecânica, boa estabilidade dimensional e pressão uniforme nos elementos.
A operação de revestimento produz revestimento interrompido para corresponder ao comprimento da bobina. As bobinadeiras são projetadas para operar automaticamente para uso com rolos jumbo secos de cátodos e ânodos e separador (25mm ou menos de espessura, seja PP ou PE ou misto).
As operações começam por soldar as abas na secção não revestida das folhas. A máquina enroladora corta então a tira no comprimento adequado e enrola a combinação anode-separador-cátodo em uma bobina apertada ou bobina em forma de geleia. À medida que o núcleo enrolado aumenta de diâmetro, a máquina de enrolar compensa automaticamente para manter uma tensão constante à medida que a bobina aumenta de diâmetro para uma tolerância próxima ao diâmetro. O vento elíptico para as células prismáticas é um processo mais complexo e mais lento.
Após o enrolamento, a bobina é verificada quanto à existência de calções internos antes de ser inserida na lata. As latas de aço devem ser limpas e niqueladas para proporcionar uma superfície estável e minimizar a corrosão da lata antes da montagem da célula. O chumbo anódico é soldado ao fundo da lata e o chumbo catódico é soldado ao respiro de segurança. O electrólito é adicionado à célula semi-montada. A montagem é terminada com o engaste da tampa superior.
A rejeição precoce de possíveis falhas celulares é uma medida econômica e evita mais trabalho com células ruins. A bobina é inserida na lata para que a lata proporcione uma pressão constante para manter os componentes do elemento juntos, eliminando assim qualquer possibilidade de vazios entre eles. Alguns fabricantes podem inserir um mandril para estabilizar o centro da bobina.
A menos que todas as operações sejam realizadas em um quarto seco ou caixa seca A água absorvida nos materiais activos deve ser removida por calor e vácuo antes do processo de enchimento do electrólito.
O preenchimento preciso a vácuo do eletrólito é feito para garantir que o eletrólito penetre e preencha completamente a porosidade disponível no separador e nas estruturas do eletrodo. Bombas de precisão medem o volume calculado de electrólito necessário para um bom funcionamento celular. Invariavelmente todos os fabricantes empregam o LiPF6 (um composto inorgânico cristalino branco) como o eletrólito e os carbonatos cíclicos (EC, carbonato de etileno) ou carbonatos lineares (DMC, dimetil carbonato, DEC, carbonato de dietila, ou EMC, etil-mettil carbonato, etc.) são os solventes para este sal eletrolítico.
Electrólitos à base de misturas de solventes de carbonato de etileno (EC) com carbonato de dimetilo (DMC) e/ou carbonato de dietilo (DEC) são normalmente utilizados para baterias de iões de lítio em combinação com catodos de “4 V” (cobalato, níquel e manganato) devido ao elevado potencial de oxidação dos solventes.
Após encher a célula com electrólito, a célula é selada por compressão controlada de uma junta de polímero ou anel isolante colocado entre a lata da célula e a placa superior. A pressão sobre a junta de vedação em polímero é controlada para mantê-la dentro do limite elástico do polímero. Se os limites elásticos forem ultrapassados, o polímero flui a frio e compromete o selo.
Cada fabricante utiliza uma construção mecânica um pouco diferente para selar as células, mas os resultados finais são essencialmente idênticos. Normalmente, forma-se um ombro ou um parapeito perto do topo da cela. Isto serve como base para a vedação e para manter o rolo de gelatina no lugar e evitar a telescopagem ou mudança de posição da bobina enrolada sob a influência de vibração e choque.
Qualquer mudança de posição causa uma mudança na distribuição atual e resulta em uma má vida útil do ciclo ou revestimento de lítio em células de alto desempenho. A vedação da placa superior da célula contém um respiro, um elemento de coeficiente de temperatura positiva (PTC) e um dispositivo de segurança com interrupção de corrente (CID). Tanto o CID como o PTC são dispositivos de segurança concebidos para activar e prevenir o desenvolvimento de temperaturas e pressões perigosas no interior da célula. Cada lote de dispositivos é verificado antes da incorporação no conjunto superior para verificar o funcionamento adequado.
Após a aplicação do selo, as células podem ser lavadas, revestidas e etiquetadas. Eles recebem um número de série para rastrear o dia de fabricação e identificar todos os componentes da célula (materiais do eletrodo, eletrólito, separador e similares). As informações sobre capacidade e tensão são armazenadas com o número de células e usadas posteriormente para combinar células para a montagem da embalagem.
As células podem ser soldadas a laser com selos de vidro a metal para fornecer selos herméticos de longa duração. Com as células maiores, é necessário ter mais cuidado para garantir um funcionamento seguro, mesmo em condições de abuso.
Enquanto os processos acima são descritos para pequenas células seladas usadas em eletrônica portátil, o processo para baterias industriais maiores para armazenamento de energia, espaço e aplicações EV seguem o mesmo esquema geral.
Bateria de iões de lítio - Formação e envelhecimento
Conforme montados, os íons Li não são dopados no ânodo de carbono e, portanto, a célula não apresenta voltagem. Durante a carga inicial, uma parte dos íons Li do PAM LiCoO2 não é dopada para se tornar Li1-xCoO2 e esses íons de lítio são dopados no ânodo de carbono (Cy) para se tornarem LixCy. Quando a tensão de carga atinge 4,1 a 4,2 V, o valor de x é cerca de 0,5. (ou seja, 50%) indicando que 50% da Li do LiCoO2 foi utilizada.
Outro aspecto a ser notado é que uma parte dos íons de lítio dopados não retorna e permanece no ânodo. onde, os iões de lítio x-dx ficam sem contribuir para a capacidade. Isto é cerca de 10 a 20 % de lítio irreversível, o que significa que a eficiência da carga inicial é de 80 a 90 %. A partir do segundo ciclo, a quantidade irreversível não aumenta e a célula mostra a capacidade de 100 % projetada pelo fabricante.
Após a lavagem e o revestimento, mas antes do início do processo de formação, a voltagem e impedância de todas as células são registradas para classificar quaisquer células defeituosas. As células são então carregadas pela primeira vez
(carga inicial ou carga de formação). As condições da primeira taxa são importantes por pelo menos duas razões:
1) a camada sólida interfásica do eletrólito (SEI) se forma no ânodo para protegê-lo de reagir espontaneamente com o eletrólito durante o funcionamento normal da célula, e 2) estabelece o bom contato elétrico entre os materiais ativos e o eletrólito. A primeira carga segue o procedimento recomendado pelo fabricante para carregar as células, mas muitas vezes começa com uma corrente mais baixa e depois aumenta para a corrente de carga normal a cerca de um terço do caminho para o período de carga. As células podem continuar a circular dentro dos limites de tensão de carga e descarga durante um ou dois ciclos após a formação.
Após a formação ou ciclagem, a tensão e a capacidade da célula são medidas e armazenadas para uso posterior no processo de seleção da célula. O período de envelhecimento varia entre duas semanas e um mês, dependendo do fabricante. A tensão das células é medida novamente após o armazenamento. As diferenças de tensão no início e no final do período de armazenamento são utilizadas para classificar as células com shorts “macios” ou “micro”. As células com curtos-circuitos internos terão uma tensão mais baixa após o armazenamento e se separarão da tensão normal e da distribuição de capacidade. Pode ser necessário evacuar as células maiores após a formação para remover os gases de formação.
Para uma descrição detalhada do processo de montagem, os leitores são encaminhados para
- Kaoru Nakajima e Yoshio Nishi Capítulo 5 in: Energy Storage Systems for Electronics, Ed Tetsuya Osaka e Madhav Datta, Gordon and Reach Science Publishers, Amsterdam, 2000.
- Lithium-Ion Cell Production Processes, Ralph J. Brodd e Kazuo Tagawa, Capítulo 9 in: Advances in Lithium-Ion Batteries, Walter A. van Schalkwijk e Bruno Scrosati (Eds), Kluwer Academic Publishers, Nova York, pp. 273, 2002.
- Baterias de lítio, Ciência e Tecnologia, Ed. por G. A. Nazri e G. Pistoia, Springer, Nova Iorque, 2009.
- Lithium-Ion Batteries, Reiner Korthauer (ed) (2018), Traduzido por Michael Wuest et.al., Springer, 2018.
- Kazuo Tagawa e Ralph J. Brodd, Processos de Produção para Fabricação de Baterias de Íons de Lítio em Baterias de Íons de Lítio, Yoshio M., Brodd R.J., Kozawa A. (eds) Springer, Nova Iorque, NY. https: //doi.org/10.1007/978-0-387-34445-4_8]
- Zhang Z., Ramadass P. (2012) Lithium-Ion Battery Systems and Technology. Para dentro: Meyers R.A. (ed) Encyclopaedia of Sustainability Science and Technology. Springer, Nova lorque. https: //doi.org/10.1007/978-1-4419-0851-3_663
- The Handbook of Lithium-Ion Battery Pack Design Chemistry, Components, Types and Terminology, John Warner, Elsevier, 2018




