كيف تعمل بطارية ليثيوم أيون
التصور السائد في المجال العام هو أن بطاريات الرصاص الحمضية هي تقنية قديمة. بطارية ليثيوم أيون لها تصور مختلف ، فهي حديثة وأنظف ولديها 3 أو 4 أضعاف كثافة الطاقة وعمر دورة أطول. مع كل هذا ، ما هي المزايا المحتملة التي يمكن أن تقدمها تقنية حمض الرصاص التي يبلغ عمرها 150 عامًا؟ حسنًا ، في الواقع ، ليس كل شيء كما يبدو ، انظر إلى ما وراء العناوين الرئيسية في البيانات المستخدمة في ادعاءات التسويق ، ثم طبق القليل من الفطرة السليمة والبحث الأساسي وبعض العلوم الأولية. ستجد أن القصة الحقيقية مختلفة نوعًا ما.
يتعلق المفهوم الخاطئ الأول بكثافات الطاقة الحجمية والنوعية. تتعلق القيم الرئيسية من 4 إلى 5 مرات فقط بكثافة الطاقة المحددة وعدد محدود من كيماويات بطاريات أيونات الليثيوم ، وبعضها لا يزال غير مستخدم تجاريًا. تين. يقارن الشكل 2 العديد من الكاثودات لخلايا بطارية أيونات الليثيوم ، وتتراوح هذه من حوالي 100 واط في الساعة / كجم بالنسبة لكيمياء Li-FePO4 الأكثر أمانًا إلى أكثر من 200Wh / kg لمتغير أكسيد النيكل والكوبالت والألمنيوم. ويرد أدناه مخطط بطارية الرصاص الحمضية:


تنطبق هذه القيم فقط على مستوى الخلية المفردة ، وليس على حالة الحزمة أو الخدمة. تين. يوضح الشكل 3 كثافات الطاقة لمختلف كيميائيات البطاريات على مستوى الخلية والنظام. تنخفض كثافة طاقة خلايا بطارية أيون الليثيوم إلى النصف تقريبًا عند تركيبها بالكامل مع جميع التوصيلات ، ومعدات التبريد ، والسلامة ، وإدارة البطارية.
يتم تقليل ميزة مستوى الخلية من 3 إلى 5 أضعاف كثافة الطاقة المحددة إلى 2 إلى 3 مرات. اعتمادًا على كيمياء كاثود الليثيوم ، يمكننا تقريبًا النظر في التكافؤ بين بطاريات أيون الليثيوم وكثافة طاقة بطاريات الرصاص الحمضية لنظام بطارية مثبت بالكامل في بعض التطبيقات.
العامل الآخر ، عامل دورة الحياة ، هو أيضًا مصدر ارتباك. كم عدد الدورات التي يمكن أن تؤديها بطارية ليثيوم أيون قبل أن تنخفض السعة إلى أقل من 80٪ من تصنيف اللوحة؟ اثنان ، ثلاثة آلاف؟ يعطي الجدول 1 ملخصًا لمواد Li-ion الكاثود المختلفة للأداء ودورة الحياة.
مزايا كيمياء بطاريات الرصاص الحمضية
البطاريات هي أجهزة غريبة. لا أحد يريدهم ، لكن الجميع يحتاجهم. يتم شراؤها فقط عند الحاجة. كم عدد الأشخاص الذين يخططون لرحلة إلى المركز التجاري المحلي إلى متجر النوافذ للبطاريات؟ إنها عملية شراء ضغينة ولا يتم شراؤها إلا عند الضرورة القصوى. يمكن للبائع الجيد أن يبيع لك زوجًا من الأحذية وسيارتين وربما منزلين إذا كان لديك المال ، لكنه لا يستطيع بيع بطاريتين من بطاريات السيارات SLI. عندما تشتري بطارية سواء كانت بطارية شمسية للوحة شمسية أو دراجة كهربائية أو UPS ونظام النسخ الاحتياطي للبطارية العاكس أو بطارية الجر للرافعات الشوكية ألا ترغب في معرفة المزيد عنها؟
كيف تعمل بطاريات الرصاص الحمضية ، وما هي الاختلافات بين الأنواع والنماذج ، وماذا عن الكيمياء المختلفة؟ يمكن أن تكون باهظة الثمن. في التطبيق التجاري أو المحلي ، ما هو العائد ، وما هو العمر الافتراضي وتكلفة استبدال بطارية الرصاص الحمضية؟ الحجم الذي تحتاجه ، والمساحة المتاحة ، وكفاءة الطاقة لبطارية الرصاص الحمضية ووقت إعادة الشحن؟ ثم هناك التكاليف الخفية للسلامة والتخلص والبصمة الكربونية. تقارن هذه المقالة بطاريات الرصاص الحمضية ببطارية أيون الليثيوم وتعالج العديد من المفاهيم الخاطئة المرتبطة بكل من هذين المركبين الكيميائيين.
أي بطارية ليثيوم أيون هي الأفضل
| مادة الكاثود | اسم قصير | الجهد الاسمي | طاقة محددة Wh / kg (خلية) | دورة الحياة | تعليقات |
|---|---|---|---|---|---|
|
أكسيد الكوبالت الليثيوم (LiCoO2) |
LCO | 3.6 | 150-200 | 500-1000 | الأجهزة المحمولة - هروب حراري عند الشحن الزائد |
| أكسيد المنغنيز الليثيوم (LiMn2O4) | LMO | 3.7 | 100-150 | 300-700 | الأدوات الكهربائية والأجهزة الطبية - أكثر أمانًا من LCO |
| أكسيد الكوبالت والمنغنيز والنيكل الليثيوم (LiNiMnCO2) | NMC | 3.6/3.7 | 150-220 | 1000-2000 | دراجات كهربائية ، كهربائية ، صناعية - دورة حياة عالية |
| فوسفات الحديد الليثيوم (LiFePO4) | LFP | 3.2 | 90-120 | 1000-2000 | EV ، SLI ، وقت الفراغ - الأكثر أمانًا من بين جميع كيماويات بطاريات أيونات الليثيوم |
| أكسيد الألومنيوم والنيكل والكوبالت (LiNiCoAlO2) | NCA | 3.6 | 200-260 | 500 | مجموعة نقل الحركة الصناعية والمركبات الكهربائية (تسلا) TR عند 150 درجة مئوية ، CL 500 |
| تيتانات الليثيوم (Li4Ti5O12) | LTO | 2.4 | 50-80 | UPS ، الطاقة الشمسية ، مجموعة نقل الحركة (هوندا ، ميتسوبيشي). CL 3000-7000 - آمن جدًا |
كما يتضح ، تقع جميعها ضمن نطاق دورة 800 إلى 2000. بالمقارنة ، يمكن لبطارية حمض الرصاص المصممة جيدًا أن تحقق بسهولة أكثر من 1600 دورة إلى 80٪ DOD. فكيف يتراكم كل هذا عند النظر في تكلفة الملكية؟ هذا يقودنا إلى النقطة التالية وهي سعر بطارية الرصاص الحمضية. ما هي تكلفة بطارية ليثيوم أيون مقارنة ببطارية حمض الرصاص؟ تكلفة مصنع تصنيع بطارية ليثيوم أيون؟ بطبيعة الحال ، تعتبر بطارية الليثيوم أيون أغلى ثمناً ، ولكن ما هو أكثر من ذلك بكثير. مرة أخرى ، هذا يعتمد على المستوى الذي يتم النظر فيه. ستخبرنا البيانات الصحفية أن أسعار Li-ion آخذة في الانخفاض وهي الآن في حدود 2-3 مرات من حمض الرصاص.
هل حقا؟ متوسط الأسعار في بحث حديث على الإنترنت في المملكة المتحدة للحصول على أسعار بطاريات الترفيه المتاحة تجاريًا بقدرة 12 فولت و 100 أمبير في الساعة لكل من بطاريات الليثيوم أيون وبطاريات الرصاص الحمضية:
بطارية ليثيوم أيون 960 دولار أو 800 دولار للكيلو وات
بطارية الرصاص الحمضية 215 دولارًا أو 180 دولارًا للكيلووات ساعة
من الواضح أن عمر بطارية الليثيوم أيون يجب أن يكون 4 أضعاف عمر بطارية الرصاص الحمضية المكافئة للحصول على نفس القيمة. كما رأينا ، هذا ليس هو الحال.


في جميع الحالات ، كان بناء بطارية الرصاص الحمضية هو الأكثر فعالية من حيث التكلفة حتى عندما تم تركيب بطارية حمض الرصاص الكبيرة لتوفير قبول شحن أفضل وعمر دورة أطول. في هذا المثال ، كان التطبيق عبارة عن برج اتصالات في الهند. ينطبق نفس المبدأ في معظم التطبيقات والمناطق الجغرافية ، وبشكل أكبر في المناخات الباردة. الاعتقاد الخاطئ الآخر هو أن Li-ion هي تقنية أنظف وأقل تلويثًا من حمض الرصاص. تم تقديم انبعاثات المهد إلى البوابة للعديد من كيميائية البطاريات في التين. 5 و 6.
يوضح هذا الشكل حدود عمليات تصنيع البطاريات. من استخراج المواد الخام ونقلها من خلال جميع خطوات المعالجة إلى النقطة التي تكون فيها البطاريات جاهزة للشحن.
الجدول 2 هو حالة واقعية تقارن اقتصاديات استخدام بطارية ليثيوم أيون وبطارية حمض الرصاص التي تعمل على مدى فترات حياة مختلفة.
| البند التكلفة | تكاليف الجري اليومية بالدولار الأمريكي | تكاليف الجري اليومية بالدولار الأمريكي |
|---|---|---|
| 3 سنوات | بطارية الرصاص الحمضية | بطارية ليثيوم أيون |
| الإطفاء | 8.30 | 16.90 |
| ديزل (تسليم) | 15.50 | 15.50 |
| اعمال صيانة | 2.46 | 2.46 |
| كهرباء | 1.47 | 1.47 |
| البطارية تشحن | 0.65 | 0.50 |
| إجمالي اليوم / الشهر | 28.38/851 | 36.83/1105 |
| 6 سنوات | ||
| الإطفاء | 5.86 | 8.46 |
| ديزل | 15.50 | 15.50 |
| اعمال صيانة | 2.46 | 2.46 |
| كهرباء | 1.47 | 1.47 |
| البطارية تشحن | 0.54 | 0.50 |
| إجمالي اليوم / الشهر | 25.83/775 | 28.39/852 |
توضح هذه البيانات من مختبرات أرجون الوطنية أن إجمالي عملية التصنيع بما في ذلك استخراج ونقل المواد الخام لبطاريات الليثيوم أيون تزيد عن 4 أضعاف قيمة حمض الرصاص. فيما يتعلق باستخراج المواد ، فإن توريد مواد الكاثود الأساسية مثل الكوبالت والمنغنيز والليثيوم غير مؤكد تمامًا. توجد عمليات الاستخراج والاستعادة ولكن عدد المناجم ومواقع التصنيع قد يحد من العرض إذا زاد الطلب بشكل كبير. تتنبأ الخريطة الجيوسياسية أيضًا بعدم اليقين لبعض مصادر هذه المواد.
هل بطارية ليثيوم أيون قابلة لإعادة التدوير
تعد قابلية إعادة التدوير والسلامة لهذه المواد الكيميائية من العوامل المهمة. من المعروف أن جميع مكونات بطاريات الرصاص الحمضية تقريبًا معاد تدويرها بنسبة 100٪ بينما لا توجد عمليات تجارية لإعادة تدوير بطارية أيون الليثيوم. هذا الموقف مفهوم عندما تفكر في أن المكونات الأكثر تكلفة من Li و Co و Mn وما إلى ذلك ليست سوى جزء صغير من إجمالي بطارية ليثيوم أيون. على سبيل المثال ، يمثل الليثيوم حوالي 4٪ من إجمالي وزن الخلية. أضف إلى ذلك الحقيقة الواضحة وهي أن الليثيوم شديد التفاعل (أساس كثافة طاقته العالية) ، مما يجعل استخراجه من النفايات مكلفًا بشكل مفهوم.
عامل التعقيد الإضافي مع العديد من المواد المختلفة في بنائه يجعل إعادة التدوير صعبة ، من الناحيتين التقنية والاقتصادية. النتائج؟ ببساطة لا يوجد حافز تجاري لإعادة تدوير هذه البطاريات. لهذا السبب ، لا تزال مرافق إعادة التدوير في المرحلة التجريبية ومعظمها ممول من الحكومة.
في الوقت الحاضر ، يتم تخزين الغالبية العظمى من بطاريات أيونات الليثيوم المخردة في انتظار حدوث اختراق تقني أو تشريع لفرض إعادة تدويرها. إذا تم تنفيذ هذا الأخير ، فستكون هناك تكلفة ، في النهاية على الاستهلاك. سيؤدي ذلك إلى زيادة سعر خلية Li-ion مقارنة بأنواع بطاريات الرصاص الحمضية.
يمكن أن تنفجر بطارية ليثيوم أيون
أخيرًا ، لدينا الأمان. لم يتم استدعاء أي تطبيقات لبطاريات الرصاص الحمضية على حد علمنا من أي وقت مضى للسلامة كما نعلم هو الحال مع بطارية Li-ion في الأجهزة الإلكترونية المحمولة وحتى المركبات الكهربائية. تين. يوضح رقم 7 ما حدث لسيارة فولفو هجينة جديدة في المملكة المتحدة قبل أسبوعين فقط ، وقت كتابة هذا المقال. في هذه الحالة ، اشتعلت النيران في بطاريات الليثيوم أيون عند الشحن.
حرائق بطارية ليثيوم أيون
الشكل 7 حريق ناجم عن بطارية Li-ion في سيارة فولفو الكهربائية الهجينة: أبريل 2018 – مقر الإقامة في المملكة المتحدة


يُظهر هذا الفيديو حريقًا حديثًا جدًا بسبب بطارية ليثيوم. ربما بسبب عدم التوازن في الخلايا و BMS غير المناسب.
حتى عند تخزين أو نقل بطاريات أيونات الليثيوم كانت سببًا في نشوب حرائق خطيرة. في حين أن هذه المناسبات نادرة ، يجب الاعتراف بها ، ويجب تثبيت معدات السلامة المناسبة وبرامج إدارة البطارية. لا تزال إدارة الإطفاء في نيويورك ، على سبيل المثال ، في طور اتخاذ قرار بشأن كيفية معالجة حرائق بطاريات أيونات الليثيوم. هذا من شأنه أن يشير بقوة إلى أن تدابير السلامة الحالية لبطاريات الليثيوم أيون في جميع أنحاء العالم تحتاج إلى المراجعة.
فيما يلي المنظر من إدارة المطافئ في نيويورك:
اقتباس من مقال إخباري: محرك الأداة المساعدة AWS 15 نوفمبر 2016 قال روجرز “ليست النار هي المشكلة الأكبر”. رجال الإطفاء مدربون على التعامل مع الحرائق ، لكنهم بحاجة إلى معرفة ما يتعاملون معه. يمكن أن تطلق بطاريات Li-ion الأحماض السامة والأبخرة القابلة للاشتعال. بعض هذه الأبخرة تلتهمها النيران ، ولكن إذا لم تكن كذلك ، فقد تشتعل أو تسبب مشكلة لرجال الإطفاء. أكبر مشكلة هي ما يحدث “بعد العملية” ، أي بعد إطفاء الحريق. قال روجرز إنه حتى إذا تم إيقاف تشغيل البطارية ، فقد تشتعل مرة أخرى لمدة تصل إلى 72 ساعة. -Lt. Paul Rogers Fire Department بقسم عمليات المواد الخطرة بنيويورك “
بطارية ليثيوم أيون أو بطارية حمض الرصاص؟
من المؤكد أن بطارية ليثيوم أيون لها خصائص أداء أفضل من حمض الرصاص. ومع ذلك ، يتم تقليل هذه المزايا بشكل كبير من خلال الأجهزة الإضافية المرتبطة بمتطلبات السلامة والإدارة. والنتيجة النهائية هي أن بطاريات الرصاص الحمضية لها مزايا مميزة ، لا سيما عند النظر في التطبيقات غير المقيدة بالوزن أو قبول الشحن. التكلفة الأولية المنخفضة لتكلفة مصنع تصنيع بطاريات الرصاص الحمضية ؛ يوفر سعر الشراء المنخفض وتكلفة الاستهلاك المنخفضة لحمض الرصاص جنبًا إلى جنب مع تأثيره البيئي المنخفض وسلامته المتأصلة المزايا التالية:
- سعر شراء أقل. السعر هو حوالي ربع مكافئ Li-ion. انخفاض تكاليف التشغيل لإعطاء تكلفة إجمالية أقل للملكية في غالبية التطبيقات.
- إعادة التدوير. يتم إعادة تدوير ما يقرب من 100٪ من جميع مواد بطاريات الرصاص الحمضية. يمكن أن توفر قيمة الخردة عائدات إضافية تصل إلى 20٪ من تكلفة مواد البطارية. لا تحتوي بطاريات الليثيوم على بنية أساسية أو عملية تجارية لإعادة التدوير
- أمان. تعد كيمياء حمض الرصاص أكثر أمانًا بطبيعتها من تلك الموجودة في بطارية أيون الليثيوم
- الاستدامة. هناك العديد من المصادر الراسخة للإمداد بحمض الرصاص ، لا سيما من مرافق إعادة التدوير. يمكن توفير الليثيوم ومواد الكاثود الأخرى من المناطق الحساسة سياسياً. لن تدعم القدرة العالمية الحالية لاستخراج المواد وتصنيعها زيادة سريعة في إنتاج بطارية ليثيوم أيون.
- أثار الكربون. يحتوي تصنيع بطاريات الرصاص الحمضية على بصمة كربونية من المهد إلى البوابة تبلغ ثلث تلك الموجودة في بطاريات أيونات الليثيوم.
صورة مختلفة عن تلك التي رسمتها شركات بطاريات أيونات الليثيوم. في حين أنه لا يمكن القول أن حمض الرصاص له عيب في كثافة الطاقة ، فإن الحقيقة هي أن بطارية الرصاص الحمضية لا تزال آمنة للغاية وتنافسية وخيار أفضل لتكنولوجيا البطاريات في العديد من التطبيقات.
ما هي بطارية ليثيوم أيون
مواد الكاثود والأنود: على الرغم من تفضيل خلايا هيدريد معدن النيكل (Ni-MH) في البداية في التسعينيات ، فقد تم إصدار أول منتج تجاري لبطارية ليثيوم أيون قابلة لإعادة الشحن في العالم في عام 1991 بواسطة شركة Sony Corporation. بالإضافة إلى محتوى الطاقة العالي ، من حيث الكتلة والحجم على حد سواء ، توفر هذه البطارية أيضًا خصائص درجات حرارة منخفضة ممتازة وخصائص تحميل وخصائص دورة. ونتيجة لذلك ، استحوذت على السوق بسرعة وأصبحت مصدرًا لا غنى عنه للطاقة لأجهزة الصوت والفيديو ، وأجهزة الكمبيوتر الشخصية ، والهواتف المحمولة ، وغيرها من المعدات المحمولة
بدأت تقنية البطاريات المتقدمة اليوم باكتشاف الموصلية الأيونية العالية للمرحلة الصلبة NaAl 11 O 17 ، والتي تسمى الصوديوم β-alumina ، بواسطة كومر وزملاؤها في مختبر شركة Ford Motor Co. [1. أولوف رامسرتمستروم على جائزة نوبل في الكيمياء. خلفية علمية عن جائزة نوبل في الكيمياء 2019 ؛ 2. YFY Yao و JT Kummer و J. Inorg. نوكل. علم. 29, 2453 (1967)].
أدى ذلك إلى إدراك أن النقل الأيوني في المواد الصلبة يمكن أن يكون سريعًا جدًا في الواقع ، وأنه قد يؤدي إلى مجموعة متنوعة من التقنيات الجديدة. بعد ذلك بوقت قصير ، أظهر الباحثون في Ford أنه يمكن للمرء استخدام إلكتروليت صلب عالي التوصيل لإنتاج نوع جديد تمامًا من البطاريات ، باستخدام الصوديوم المنصهر في القطب السالب ومحلول مصهور من الصوديوم في الكبريت كقطب موجب ، مع موصل الصوديوم. إلكتروليت صلب بين [N. ويبر وجي تي كومير ، بروك. مصادر الطاقة السنوية Conf. 21 ، 37 (1967)].
كما هو متوقع ، سرعان ما تم النظر في إمكانية وجود أنظمة ليثيوم مماثلة ، حيث تم التعرف على أن خلية الليثيوم المكافئة بخلاف ذلك يجب أن تنتج جهدًا أعلى من خلية الصوديوم. بالإضافة إلى ذلك ، فإن الليثيوم له وزن أقل من الصوديوم ، وهي ميزة أخرى.
لا يمكن استخدام عنصر الليثيوم ، بسبب انخفاض نقطة انصهاره. بدلاً من ذلك ، تم فحص سبائك الليثيوم الصلبة ، وبشكل أساسي أنظمة Li / Si و Li / Al ، [ RA Huggins، J. Power Sources 81-82، 13 (1999)].
تم فحص عدد من المواد كمواد تفاعل قطب موجب في ذلك الوقت ، مع إيلاء أكبر قدر من الاهتمام لاستخدام FeS أو FeS 2 . عند التفاعل مع الليثيوم ، تخضع هذه المواد لتفاعلات إعادة التشكيل ، مع اختفاء المراحل الأولية وتشكيل أطوار جديدة [دكتور فيسرز ، ز. شركة 121, 665 (1974)].
متى تم اختراع بطارية الليثيوم أيون؟
استكشف البروفيسور ويتنجهام الإقحام الكهروكيميائي في مثل هذه المواد وفي عام 1973 اقترح مواد مثل الأقطاب الكهربائية في البطاريات. نتج عن هذا العمل بطارية عاملة وقابلة لإعادة الشحن في عام 1976 . تتكون الخلية الناجحة من معدن الليثيوم باعتباره الأنود وكبريتيد التيتانيوم (TiS 2 ) ككاثود ، مع سداسي فلورو فوسفات الليثيوم ( LiPF 6 ) كمحلول إلكتروليت في كربونات البروبيلين (PC) كمذيب. ألهمت هذه الدراسات الواعدة Whittingham لاستكشاف التبادل الكهروكيميائي في مواد مثل الأقطاب الكهربائية في البطاريات. تم عرض بطارية عاملة وقابلة لإعادة الشحن لاحقًا في عام 1976
[(أ) Whittingham، MS Electrointercalation in Transition-Metal Disulphides. J. كيم. المجتمع ، علم. كومون. 1974 ، 328-329.] (مع شركة إكسون للأبحاث والهندسة).
(ب) Whittingham، MS Batterie à Base de Chalcogénures. براءة الاختراع البلجيكية رقم. 819672، 1975.
(ج) Whittingham ، MS تخزين الطاقة الكهربائية وكيمياء الإقحام. علم 1976 ، 192 (4244) ، 1126-1127.
لكن النجاح لم يدم طويلا. في التدوير المتكرر ، شكل الليثيوم المعدني التشعبات على سطح المعدن أثناء ركوب الدراجات ، مما أدى إلى دوائر قصيرة.
أعطت هذه المشكلة قوة دافعة لبحث جديد عن حلول بديلة وتم اقتراح تكوين خلايا “خلية نقل الأيونات” (وتسمى أيضًا “الكرسي الهزاز”) ، حيث يمكن لكلا القطبين استيعاب الأيونات.
إذا كانت مادة القطب الموجب تحتوي في البداية على الليثيوم وتمت إزالة بعض أو كل الليثيوم أثناء الشحن الأول ، فإن الخلية تطور جهدًا. لذلك ، من الممكن الحصول على مواد قطب موجبة تتفاعل مع الليثيوم بجهد أعلى من حوالي 3 فولت ، إذا كانت تحتوي بالفعل على الليثيوم ، ويمكن استخلاص هذا الليثيوم كيميائيًا.
من اخترع بطارية ليثيوم أيون؟
هذا النهج ، الذي يتضمن استخدام المواد التي يوجد فيها الليثيوم بالفعل ، تم توضيحه لأول مرة بواسطة البروفيسور جودناف. كانت الأمثلة الأولى للمواد التي تحتوي في البداية على الليثيوم ، والتي تحذف الليثيوم منها كهربيًا ، هي العمل على Li1 xCoO2 في عام 1980.
[ك. ميزوشيما ، بي سي جونز ، بي جي وايزمان وجي بي جودينو ، ماتر. الدقة. ثور. 15 ، 783 (1980)] و Li1 xNiO2
[JB Goodenough، K. Mizushima and T. Takada، Jpn. J. أبل. فيز. 19 (ملحق 19-3) ، 305 (1980)]
بالتوازي مع تطوير الأنود ، تم أيضًا البحث عن مواد أفضل للكاثود من أجل الحصول على قوة emf أعلى للخلية بالاقتران مع أنودات ذات إمكانات أعلى من الليثيوم المعدني. حدث تقدم كبير في 1979/1980 عندما حصل جون ب. جودينو وزملاؤه في أكسفورد
اكتشفت الجامعة ، المملكة المتحدة ، أن LixCoO2 ، وهو معدن كالكوجينيد مقسم آخر من النوع MX2 ، يمكن أن يكون بمثابة مادة كاثودية.
[Goodenough ، JB ؛ ميزوشيما ، ك.موصلات أيون سريعة. براءة الاختراع الأمريكية لا. 4357215 ، 1982].
[ميزوشيما ، ك. جونز ، بيسي ؛ وايزمان ، PJ ؛ Goodenough ، JB LixCoO2 (0 <x <-1): جديد
مادة الكاثود للبطاريات ذات كثافة الطاقة العالية. ماطر. الدقة. ثور. 1980 ، 15 (6) ، 783-789].
كان هيكل المادة مشابهًا لـ Lix TiS2 مع فجوات فان دير فالس بين ثاني أكسيد الكوبالت (CoO2 ) الطبقات التي يمكن أن ترتبط فيها أيونات الليثيوم دون الكثير من التمدد الشبكي. سبب Goodenough أنه عندما X في MX2 هو عنصر كهرسلبي صغير ، فإن عملية امتصاص الكاتيون الناتجة سترتبط بتغير كبير في الطاقة الحرة السلبية وبجهد خلية مرتفع (ΔG = -nFE). مع X من الأكسجين ، كان الوضع واعدًا بشكل خاص ، نظرًا لأنه تم اقتراح أيونات الليثيوم لتكون متحركة بدرجة كافية في صفائف الأكسجين المعبأة.
ثبت أن المنطق صحيح ، وأظهرت مادة CoO2 إمكانات عالية جدًا تتراوح من 4 إلى 5 فولت بالنسبة إلى Li + / Li. أجريت الدراسات الكهروكيميائية في هذه الحالة باستخدام إلكتروليت يتكون من الليثيوم رباعي فلورو بورات (LiBF4) في كربونات البروبيلين.
مكّن هذا الاكتشاف من استخدام مواد الأنود ذات الإمكانات الأعلى من معدن الليثيوم ، مما زاد من البحث عن المواد الكربونية المناسبة. بالنظر إلى صعوبة حل مشكلة الإقحام الكهروكيميائي للجرافيت ، تم بحث خيارات أخرى بدلاً من ذلك.
أين تم اختراع بطارية الليثيوم أيون؟
حدث تقدم كبير في عام 1985 عندما اكتشفت مجموعة يابانية بقيادة أكيرا يوشينو (من شركة أساهي كاسي) ألياف الكربون المزروعة بمرحلة البخار (VGCF) ثم فحم الكوك المعامل حرارياً في وقت لاحق. كان من المعروف أن المادة الأخيرة تحتوي على مزيج من المجالات البلورية (الجرافيتية) وغير البلورية ، ويمكن للباحثين تحديد الصفات المستقرة بشكل خاص ، ولكن عالية الأداء ، مع درجات معينة من التبلور.
[أكيرا يوشينو ، ولادة بطارية Li-Ion ، مقالات Angewandte ، Angew. ، Chem. كثافة العمليات Ed.، 2012 ، 51، 5798-5800]
باستخدام مواد الأنود الفعالة هذه ، طور Yoshino بطارية ليثيوم أيون فعالة وعاملة بناءً على تكوين خلية نقل الأيونات. وهكذا تم استخدام المادة الكربونية التي تم تحديدها كأنود وتم استخدام مادة LixCoO2 الخاصة بـ Goodenough (التي تحتوي عادةً على كميات صغيرة من القصدير) ككاثود. تم استخدام طبقات فاصلة مكونة من البولي إيثيلين أو البولي بروبلين ويتكون الإلكتروليت من فوق كلورات الليثيوم (LiClO4) في كربونات البروبيلين (PC).
أثبت يوشينو أيضًا سلامة هذه البطارية في عام 1986 بإلقاء وزن على البطارية. لم تحدث حرائق أو انفجارات بينما تفاعلت البطاريات التي تستخدم أنود معدن الليثيوم بعنف.

الشكل 8. أول اختبارات السلامة التي أجراها يوشينو باستخدام بطارية Li-ion الخاصة به في عام 1986.
أ) لحظة اصطدام كتلة حديدية بالبطارية
ب) نموذج أولي لبطارية ليثيوم أيون بعد الاصطدام
ج) بطارية ليثيوم أنود معدنية بعد الاصطدام
[الائتمان: أكيرا يوشينو ، ولادة بطارية Li-Ion Battery ، مقالات Angewandte ، Angew. ، Chem. كثافة العمليات Ed.، 2012، 51، 5798-5800]
أدت هذه الاكتشافات والتطورات في النهاية إلى إطلاق بطارية ليثيوم تجارية
في عام 1991. مع مزيد من التطوير ، تم تسويق بطارية Li-ion من قبل شركة Sony في عام 1991 ومن خلال مشروع مشترك بين Asahi Kasei و Toshiba في عام 1992.
[نيشي ، واي ، تطوير بطاريات ليثيوم أيون الثانوية. علم. تسجيل 2001 ، 1 ، 406-413]
اعتمدت البطارية على مادة الأنود القائمة على كوك البترول ، LixCoO2 ككاثود ، وإلكتروليت خالٍ من الماء مكون من سداسي فلورو فوسفات الليثيوم (LiPF6) في كربونات البروبيلين (PC). كان جهد الشحن مرتفعًا (حتى 4.1 فولت) ، مع طاقة محددة مسجلة تبلغ حوالي 80 واط / كجم وكثافة طاقة تبلغ 200 واط / لتر.
بالمقارنة مع البطاريات الأخرى التي كانت موجودة في السوق في ذلك الوقت ، سرعان ما أصبحت بطارية الليثيوم تنافسية للغاية ومهدت الطريق بشكل أساسي لثورة الهاتف المحمول القادمة.
في نفس الوقت تقريبًا ، وجد أنه يمكن استخدام الجرافيت بالفعل مع تركيبة إلكتروليت مناسبة. [Fong R، Sacken U von، Dahn JR، دراسات عن إقحام الليثيوم في الكربون باستخدام خلايا كهروكيميائية غير مائية. J. Electrochem. شركة 1990 ، 137 (7) ، 2009-2013]
باستخدام المذيبات التي تحتوي على كربونات الإيثيلين ، والتي تم تجاهلها بشكل عام حتى الآن بسبب نقطة انصهارها العالية ، تم تشكيل الطور البيني للكهرباء الصلبة (SEI) على سطح قطب الجرافيت أثناء دورة الشحن / التفريغ ، وبالتالي حماية مادة الكربون من التقشير والمزيد من التحلل . [بيليد ، إي. السلوك الكهروكيميائي للمعادن الأرضية القلوية والقلوية في أنظمة البطاريات غير المائية ، نموذج الطور المنحل بالكهرباء الصلبة. J. Electrochem. شركة 1979 ، 126 (12) ، 2047-2051.
تم تبني هذا الاكتشاف بسرعة من قبل مجتمع البطاريات ، وتم تطوير بطارية ليثيوم أيون من الجيل التالي تعتمد على الجرافيت كمادة الأنود. باستخدام مادة الأنود هذه ، تم إنتاج بطاريات بجهد شحن 4.2 فولت بعد فترة وجيزة ، مما أدى إلى كثافة طاقة تبلغ 400 واط / لتر.
لم يتوقف تطوير بطارية الليثيوم أيون مع هذه الاكتشافات المهمة ، ولكن تم الإبلاغ عن العديد من التحسينات والبدائل منذ ذلك الحين. على سبيل المثال ، تم تحديد مواد الكاثود الجديدة باستمرار لاستخدامها في تطبيقات بطاريات محددة ، وقد نشأت اثنتان من هذه المواد من مجموعة Goodenough: مادة الإسبينيل Li1-xMn2O4 والمادة الأوليفين LixFePO4 (LFP).
[بادي ، أ. نانجونداسوامي ، كانساس ؛ Goodenough ، JB Phospho-Olivines كمواد موجبة للإلكترود لبطاريات الليثيوم القابلة لإعادة الشحن. J. Electrochem. شركة 1997 ، 144 ، 1188-1194.
ثاكيراي ، مم ؛ ديفيد ، WIF ؛ بروس ، PG ؛ Goodenough ، إدخال الليثيوم JB في إسبنيل المنغنيز. ماطر. الدقة. ثور. 1983 ، 18 ، 461-472].
المادة الأخيرة محدودة بإمكانية أقل إلى حد ما مقابل Li + / Li من LixCoO2 ، ولكنها تتمتع بثبات عالٍ ويمكن استخدامها بمعدلات شحن عالية. كما تم اكتشاف العديد من مواد الإلكترود وأنظمة الإلكتروليت الأخرى ، مما يؤدي إلى تحسين مواد تخزين الطاقة باستمرار لصالح المجتمع.
ما نوع البطارية المستخدمة في السيارات الكهربائية؟
في الوقت الحاضر ، تستخدم معظم المركبات الكهربائية بطاريات Li-ion. في وقت سابق ، تم استخدام بطاريات Ni-MH وبطاريات الرصاص الحمضية ، لكن استخدامها انخفض ببطء بسبب ظهور بطاريات Li-ion ، التي تمتلك طاقة محددة أعلى وقيم كثافة طاقة أعلى. تبلغ الطاقة المحددة لبطاريات الرصاص الحمضية حوالي 40-50 واط / كجم بينما تبلغ طاقة بطارية Li-ion حوالي 150 واط / كجم. تبلغ قيمة كثافة الطاقة لبطاريات الرصاص الحمضية 80-100 واط / لتر بينما حصلت بطارية Li-ion على أكثر من 250 واط / لتر.
وصلت الخلايا الأسطوانية مع كاثودات النيكل والكوبالت والألمنيوم (NCA) والأنودات المركبة من السيليكون / الجرافيت ، مثل تلك المستخدمة في أحدث حزم بطاريات تسلا (2019-2020) ، إلى ما يقرب من 270 واط / كجم و 650 واط / لتر. هناك تقنية جديدة تسمى Licerion by Sion Power تطالب بـ 500 واط / كجم من الطاقة المحددة و 1000 واط / لتر من كثافة الطاقة و> 450 دورة في خلايا نمو 0.4 آه.
بالنسبة للبطاريات الصغيرة ، نتحدث من حيث Wh. بالنسبة للأنظمة ذات السعة العالية ، يتم استخدام وحدة كيلووات ساعة. قيمة Wh مقسومة على 103 سوف تعطي kWh.
إذن 850 Wh = 850/1000 = 0.850 kWh.
يمكن أن تصل الخلايا المستخدمة في بطارية EV اليوم إلى طاقة محددة اسمية من 140-170 واط / كجم. عادةً ما تكون الطاقة المحددة لحزمة البطارية الناتجة أقل بنسبة 30 إلى 40 في المائة ، أو 80-120 واط / كجم. يرجع الانخفاض إلى عدة سلاسل ووصلة توصيل متوازية ، BMS ونظام الإدارة الحرارية (التبريد أو التدفئة). في عام 2019 ، انخفضت النسبة المئوية لحزمة المكونات غير الخلوية إلى حوالي 28٪.
حتى الآن ، تم وضع الخلايا أولاً في وحدات ثم يتم وضعها في حزم. على حد سواء شركة تكنولوجيا امبيركس المعاصرة المحدودة ، الصين قررت شركتا ( CATL) و Tesla أنهما يريدان التخلص من الوحدات ووضع الخلايا في حزم مباشرة. قامت CATL بذلك بالفعل وتطلق عليها تقنية خلية إلى حزمة . في حين أن المعلومات حول هذا نادرة ، تدعي الشركة أن هذا يمكن أن يزيد من طاقة معينة بنسبة 10-15٪ وتحسين استخدام الحجم بنسبة 15-20٪. في المجموع ، يمكن أن تقلل من الأجزاء اللازمة لحزم البطاريات بنسبة 40٪. [https: //cleantechnica.com/2020/02/18/how-catl-lithium-iron-phosphate-battery-could-be-leading-to-100-kwh-tesla-model-3/]
تعيين بطارية الليثيوم
أنشأت اللجنة الكهروتقنية الدولية (IEC) ومؤسسة المعايير الهندية تسمية مشتركة لوصف الكيمياء وحجم خلايا الليثيوم أيون.
[ خلايا وبطاريات الليثيوم الثانوية للتطبيقات المحمولة ، اللجنة الكهروتقنية الدولية ، IEC 61960-1 و IEC 61960-2 و IS 16047: 2012 ].
تحدد الحروف الكيمياء وعامل الشكل بينما تحدد الأرقام الأبعاد المادية للخلية. يصف الحرف الأول الكيمياء العامة ، بينما يشير الحرف الثاني إلى كيمياء الكاثود المحددة ، بينما يشير الحرف الثالث إلى الشكل.
الحرف الأول: I- كيمياء أيونات الليثيوم
الحرف الثاني: C- كوبالت ، F- حديد ، Fp – فوسفات الحديد ، N- نيكل ، M- منجنيز ، Mp- فوسفات المنغنيز ، تيتانيوم ، V- فاناديوم و x- أخرى.
الحرف الثالث: R- أسطواني ، ف منشور
الرقمان الأولان اللذان يتبعان يحددان القطر بالملليمتر والأخر ثلاثة يحددان الارتفاع بعشر ملم. وبالتالي فإن الخلية المعينة ICR19 / 66 هي خلية أيون الليثيوم مع كاثود كوبالت بقطر يبلغ> 18 مم و 19 مم والحد الأقصى للارتفاع الكلي هو> 65 ملم و 66 ملم.
بالنسبة للخلايا المنشورية ، فإن الأحرف الأولية لها نفس المعنى ولكن أول رقمين يعينان العرض بالملم ، والرقمان التاليان هما الارتفاع بالملم والرقمان الأخيران هما الطول بالملم. وهكذا ، يصف التعيين الخلوي IMP9 / 35/150 خلية أيون الليثيوم المنشورية مع خلية كاثود منجنيز يبلغ سمكها الأقصى > 8 مم و 9 مم وبحد أقصى للعرض > 34 مم و 35 مم وأقصى ارتفاع إجمالي هو > 149 مم و 150 مم.
كيف تعمل بطارية ليثيوم أيون؟
كيف تصنع بطارية ليثيوم أيون
معدن ليثيوم برقم ذري 3 ، كثافة 0.534 جم / سم مكعب ، مع إمكانية تقليل قياسية منخفضة جدًا (زوج Li + / Li -3.05 فولت مقابل SHE) والقدرة النظرية المحددة 3860 آه / كجم (2061 مللي أمبير / سم مكعب) هو أخف وزن وأعلى جهد وأكبر كثافة طاقة من بين جميع المعادن. (قارن بالرصاص ذي الرقم الذري 82 ، الكثافة 11.29 جم / سم مكعب ، السعة النظرية المحددة 257.8 آه / كجم وإمكانية الاختزال القياسية بـ -0.35 فولت مقابل SHE).
بطارية ليثيوم أيون - مواد فعالة
المواد الفعالة للإلكترود الموجب هي أي من الأكاسيد المختلطة مثل LiCoO2 أو LiMnO2 أو LiFePO4. القطب السالب هو أساسا من الجرافيت ومركبات الكربون غير المتبلورة. يتم استخدام إلكتروليت عضوي (يحتوي على ملح موصل من الليثيوم مثل LIPF6). يتم استخدام مادة البولي بروبيلين (PP) أو البولي إيثيلين (PE) أو الفاصل المختلط. تهاجر أيونات الليثيوم ذهابًا وإيابًا بين أقطاب بطاريات الليثيوم أيون أثناء الشحن والتفريغ ويتم دمجها في المواد الفعالة كما هو موضح أدناه:

الشكل 9. منظر مفجر لخلية ليثيوم أيون
الائتمان: Zhang Z. ، Ramadass P. (2012) أنظمة وتقنيات بطارية ليثيوم أيون. في: Meyers RA (محرران) موسوعة علوم وتكنولوجيا الاستدامة. سبرينغر ، نيويورك ، نيويورك ، ص 6124. http: //doi.org/10.1007/978-1-4419-0851-3_663
كيف يتم شحن بطارية ليثيوم أيون
أثناء عملية التفريغ في خلية أيون الليثيوم (LIB) ، يتم فصل أيونات الليثيوم من القطب الموجب (أو استخلاصها) في المنحل بالكهرباء ويتم إقحام أيونات الليثيوم من الإلكتروليت في مادة الكاثود . تترافق حركة الأيونات من القطب الموجب إلى القطب السالب مع إطلاق الإلكترونات التي تتدفق في الدائرة الخارجية. تحدث العملية العكسية أثناء عملية الشحن حيث تتحرك أيونات الليثيوم من الكاثود وتنقسم في القطب الموجب عبر الإلكتروليت . عادةً ما تستخدم LIBs التجارية أكاسيد معدنية انتقالية مثل LiCoO 2 و LiMn 2 O 4 و LiFePO 4 كمادة الكاثود ، والتي يتم تغليفها فوق مجمع تيار الألومنيوم.
تمت إضافة عشرة إلى عشرين في المائة من الكربون الموصل %–10% من المواد اللاصقة البوليمرية مثل بولي فينيلدين ديفلورايد (PVDF) وبولي تترافلورو إيثيلين (PTFE) مع مادة فعالة لتعزيز التوصيل الإلكتروني وتحقيق التصاق أفضل لمادة القطب الكهربائي ، على التوالي. يتم طلاء مادة الأنود فوق مجمع التيار النحاسي بكربون موصل و PVDF إذا لزم الأمر.
يتم فصل القطبين بواسطة فاصل مسامي (غشاء بولي إيثيلين أو بولي بروبيلين بسمك 10-20 ميكرومتر) مغمور في محلول إلكتروليت (LiPF6 في مذيب عضوي). يجب أن يكون لكل من الفاصل والمحلول المنحل بالكهرباء موصلية أيونية أفضل. عادة ما يتم تصنيع الخلية في غلاف معدني على شكل هلام مع فاصل مغمور بالكهرباء بين القطبين. يظهر مخطط LIB في الأشكال ، حيث يتم عرض عمليات الشحن والتفريغ النموذجية.
تستخدم بطاريات ليثيوم أيون (Li-ion) القابلة لإعادة الشحن إدخال / استخراج عكسي لأيونات الليثيوم (Li + ) (أنواع الضيف) إلى أو من مصفوفة مضيفة (مواد نشطة للإلكترود الموجب والسالب) تسمى مركبات إدخال الليثيوم عند التفريغ والشحن تحدث العمليات. يشار إلى بطاريات أيون الليثيوم على أنها بطاريات كرسي هزاز لأن أيونات الليثيوم “صخرة” ذهابًا وإيابًا بين الأقطاب الموجبة والسالبة حيث يتم شحن الخلية وتفريغها.
عادة ما تكون المادة الفعالة الإيجابية عبارة عن أكسيد فلز بهيكل ذو طبقات ، مثل أكسيد الكوبالت الليثيوم (LiCoO 2 ) ، أو مادة لها بنية نفق ، مثل أكسيد منجنيز الليثيوم (LiMn 2 O 4 ) ، غالبًا على مجمّع تيار من الألومنيوم . عادةً ما تكون المادة الفعالة السلبية عبارة عن كربون جرافيتي ، وهو أيضًا مادة ذات طبقات ، وغالبًا ما توجد على مجمّع تيار نحاسي. في عملية تفريغ الشحنات ، يتم إدخال أيونات الليثيوم أو استخلاصها من الفراغ الخلالي بين الطبقات الذرية للمواد الفعالة.
تُستخدم الإلكتروليتات غير المائية أو الشوارد العضوية في خلايا الليثيوم.
الفواصل لبطاريات الليثيوم أيون هي أفلام البولي أوليفين الدقيقة التي يسهل اختراقها والبولي إيثيلين (PE) والبولي بروبيلين (PP).
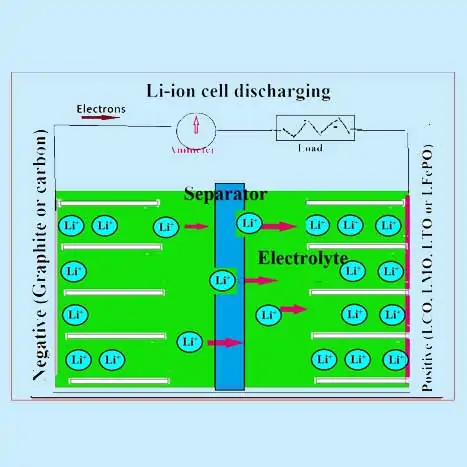

تفاعلات الخلايا الكهروكيميائية في بطارية ليثيوم أيون
في خلية أيون الليثيوم النموذجية ، تحدث التفاعلات العامة التالية.
تفاعل القطب الإيجابي:
LiMO 2 ، Li 1-x MO 2 + x Li + + xe –
تفاعل القطب السلبي:
C + y Li + + ye – ⇔ Li y C
تفاعل الخلية الكلي:
LiMO 2 + x / y C ⇔ x / y Li y C + Li 1-x MO 2
M = معادن مثل Co ، Mn ، Ni ، Ti ، إلخ.
عادةً ما تكون x حوالي 0.5 و y حوالي 0.16 ، وبالتالي فإن x / y حوالي 3. [جيف دان وغرانت إم إرليش. “بطاريات أيون الليثيوم” ، دليل البطاريات ليندن ، الطبعة الرابعة ، توماس بي ريدي (محرر) ، ماكجرو
الطور البيني المنحل بالكهرباء والصلب المنحل بالكهرباء (SEI)
كما ذكرنا سابقًا ، تُستخدم الإلكتروليتات غير المائية أو الشوارد العضوية في خلايا الليثيوم. تعمل خلايا Li بجهد أعلى نسبيًا ، حتى 4.2 فولت لكل خلية. على الرغم من أن أملاح الليثيوم الضخمة مثل سداسي فلورو الفوسفات الليثيوم (LiPF6) ، سداسي فلورو الليثيوم (LiAsF6) ، الليثيوم رباعي فلورو بورات (LiBF4) ، الليثيوم فوق كلورات (LiClO4) ، الليثيوم ثلاثي فلورو الميثان سولفونات (LiCF3) ، هي الإلكتروليتات الفعلية (التي تحافظ على أملاح الإلكتروليت) ، فهي تتطلب مذيبات مناسبة مستقرة عند مثل هذا الجهد العالي. تحتوي معظم هذه المذيبات على ثوابت عازلة عالية ، مما يسهل التفكك الأيوني ووجود أيونات الليثيوم عالية التركيز. تعمل هذه المذيبات أيضًا كأغلفة مذابة للوجود المستقر لأيونات Li ، مما يقلل من تأثير الأنيونات المضادة.
عيب وجود ثوابت عازلة عالية هو أنها تحتوي على قيم لزوجة أعلى مما يؤدي إلى ضعف حركة الأيونات. للتغلب على الموصلية الأيونية المنخفضة ، عادة ما يتم خلط المذيبات منخفضة اللزوجة بمذيبات عالية اللزوجة. ولكن ، نظرًا لأن المذيبات منخفضة اللزوجة لها تفكك أيوني أقل ، يصبح من الضروري تحقيق نسبة خلط مثالية بحيث يكون للخليط موصلية أيونية جيدة وحركة جيدة. كمذيبات غير مائية ، تُستخدم مخاليط كربونات الإيثيلين (EC) مع كربونات ألكيل خطية أقل لزوجة مثل كربونات ثنائي ميثيل (DMC) وكربونات ثنائي إيثيل (DEC) وكربونات إيثيل ميثيل (EMC) في LIBs المتاحة تجارياً.
المذيبات اللا بروتونية هي الإيثرات والإسترات وكربونات الألكيل: وهي ثنائي إيثيل الإيثر (DEE) ، رباعي الهيدروفوران (THF) ، ديوكسولين ، كربونات الإيثيلين (EC) ، كربونات البروبيلين (PC) ، كربونات ثنائي ميثيل (DMC) ، كربونات ثنائي إيثيل (DEC) ، إيثيل ميثيل كربونات (EMC) ، فورمات الميثيل ، بيتا-بيوتيرولاكتون (BL) ، أسيتات الميثيل ، أسيتونتريل (AN) ، ثنائي ميثيل سلفوكسيد (DMSO) ، ثنائي ميثيل فورماميد (DMF) ، كلوريد الميثيل ، نيترو ميثان إلخ.)
الإلكتروليتات السائلة عبارة عن محاليل ملح الليثيوم في واحد أو أكثر من المذيبات العضوية ، عادةً الكربونات
لا يمكن استخدام كربونات البروبيلين (PC) كإلكتروليت إذا كان الجرافيت سيستخدم كأنود ، حيث يتحلل السابق على سطح الجرافيت ؛ الكمبيوتر المستخدم بمفرده ، بدون EC أو إضافات صغيرة من LiBOB) Li bisoxalato borate) ، يمكن أن يتسبب في تدهور أقطاب الجرافيت لأنه يتداخل مع الليثيوم ، مما يؤدي إلى التقشير.
المنحل بالكهرباء ثابت (يدخل نفس عدد الأيونات عند ترك المنحل بالكهرباء أثناء الشحن و
إبراء الذمة). عادة ما يتم إذابة ملح الإلكتروليت في مذيبات كربونات عضوية. كل مصنع لديه مجموعة مختلفة من المذيبات مع كون كربونات الإيثيلين (EC) قاسم مشترك لمعظم
يعد تكوين طبقة الطور البيني الصلبة (SEI) وظيفة مهمة أخرى تؤديها الإلكتروليتات. عند غمر معدن قلوي في إلكتروليت للبطارية ، أو عند تطبيق جهد سلبي على كربون أو على قطب كهربي خامل مغمور في الإلكتروليت ، يبدأ SEI بالتشكل.
تتكون طبقة SEI على الفور عند ملامسة المعدن للمحلول ، وتتكون من منتجات اختزال غير قابلة للذوبان وقابلة للذوبان جزئيًا لمكونات الإلكتروليت. SEI هو العامل الرئيسي الذي يحدد السلامة ، وقدرة الطاقة ، ومورفولوجيا رواسب الليثيوم ، وعمر التخزين ، وعمر دورة البطارية. من المهم أيضًا الالتصاق الجيد بالقطب الموجب.
كما تم التأكيد أعلاه ، لا يمكن بناء بطاريات قلوية أو قلوية أرضية عملية أولية أو ثانوية إلا إذا كان من الممكن إيقاف انحلال القطب الموجب أو تآكله. لذلك ، يجب تصميم الإلكتروليت لاحتواء سلائف SEI واحدة على الأقل تتفاعل بسرعة مع الليثيوم (أو مع أنود فلز قلوي) لتكوين طور بيني صلب غير قابل للذوبان. عادةً ما تكون منتجات تقليل الأنيونات الملحية عبارة عن مركبات غير عضوية مثل LiF و LiCl و Li 2 O ، والتي تترسب على سطح القطب. يتبع اختزال المذيب تكوين مكونات SEI غير قابلة للذوبان مثل Li 2 CO 3 وكربونات شبه قابلة للذوبان جزئيًا وبوليمرات.
في حالة قطب الكربون ، يعتمد الجهد الذي يتكون عنده SEI على نوع الكربون ، والخصائص التحفيزية لسطحه (محتوى الرماد ، نوع المستوى البلوري ، نسبة المستوى القاعدية إلى الحافة) ، ودرجة الحرارة ، تركيز وأنواع المذيبات والأملاح والشوائب وعلى كثافة التيار. في الشحنة الأولى لبطارية ليثيوم أيون ، هناك خسارة في السعة تسمى “فقدان القدرة غير القابل للإصلاح” (Q IR ) اللازمة بشكل أساسي لتشكيل SEI.
بالإضافة إلى تكوين SEI ، قد يكون سبب Q IR هو فقدان السعة المرتبط بتكوين منتجات الاختزال القابلة للذوبان (Q SP ).
يعد SEI الخالي من التلوث ضروريًا لإطالة عمر البطارية. يصبح أكثر أهمية أثناء ركوب الدراجات بمعدلات عالية وعند عمق تفريغ أكبر.
يتميز SEI في محاليل سداسي فلورو فوسفات الليثيوم (LiPF6) و hexafluoroarsenate (LiAsF6) بمقاومة أعلى مقارنة بمحاليل الأملاح الأخرى. ويرجع ذلك إلى تغيرات المقاومة التي تساهم في المقاومة التي تتحكم فيها الأنواع والتي تؤدي إلى مقاومة عالية بينية لأنود الليثيوم في إلكتروليت LiPF6 و LiAsF6. بالإضافة إلى ذلك ، يُذكر أن Li2CO3 هو أحد أفضل عوامل التخميل لتعزيز كفاءة دورة الليثيوم [J Electrochem Soc.، 164 (7) A1703-A1719 (2017)].
فواصل لبطاريات الليثيوم أيون
الفواصل لبطاريات الليثيوم أيون عبارة عن أغشية دقيقة المسام من البولي أوليفين وعادة ما يتم سحبها بشكل أحادي من البولي إيثيلين (PE) والبولي بروبيلين (PP) أو PE المرسوم ثنائي المحور أو PP / PE / PP متعدد المحاور.
المواد الخام للمواد الفعالة في بطارية أيون الليثيوم
تستخدم بطاريات الليثيوم أيون مواد الكاثود المختلفة. الأنود هو دائمًا قائم على الكربون ، باستثناء عدد قليل مثل أنود أكسيد التيتانيوم والنيوبيوم ، وسبائك Li-Si ، إلخ. يعطي الجدول والشكل التاليان بعض الأفكار حول الكيميائيات المختلفة المستخدمة في هذه البطاريات.

الشكل 12. ملخص لبعض خيارات كيمياء القطب الحالية والمستقبلية لبطاريات ليثيوم أيون. السعة المقترحة لـ Li (Si) هي 50٪ من السعة النظرية للمادة ، على غرار الحالة الموجودة لبعض مواد القطب الموجب
[الائتمان: يو مياو ، باتريك هاينان ، أنيت فون جوان ، وألكسندر يوكوتشي ، إنرجيز 2019 ، 12 ، 1074 ؛ دوى: 10.3390 / en12061074]
الجدول 1.
خصائص خلايا أيونات الليثيوم بمواد الكاثود المختلفة
| مادة الكاثود | Li-Ni-Co-Al (NCA) | Li-Ni-Mn-Co (NMC) | Li-MnO2 (LMO) | فوسفات الحديد الليثيوم (LFP) | Li Titanate (LTO) | أكسيد الكوبالت Li (LCO) |
|---|---|---|---|---|---|---|
| الجهد الاسمي للخلية (V) | 3.6 | 3.65 (2.7-4.2) | 3.8 | 3.25 (2-3.6) | 3.2 | 3.6 |
| الطاقة النظرية المحددة (Wh / kg) | 279 | 256 | 148 | 128 (373) | 293 (175) | 274 (370) (س = 0.5) |
| القدرة النوعية للكاثودات (Ah / Kg) المحتملة مقابل Li / Li + (V) | 180-200 (3.8) | 200 | 148 (4.1) | 150-170 (3.45) | 175 | 274 (3.9) (س = 0.5) |
| طاقة محددة للكاثودات (Wh / Kg) | 680-760 | 610-680 | 410-492 548 | 518-587 544 | -- | 546 |
| أمان | آمنة | معتدل | آمن | عالي | حسن جدا | معتدل |
مواد الكاثود في بطارية ليثيوم أيون
يجب أن تفي مواد الكاثود بالعديد من المتطلبات التي يعتمد عليها اختيار مادة القطب الموجب.
- لتوفير سعة عالية ، يجب أن تشتمل هذه المواد على كمية كبيرة من الليثيوم كما هو مصنوع.
- علاوة على ذلك ، يجب أن يتم تقطيع المواد بشكل عكسي مع القليل من التغيير الهيكلي للسماح بدورة حياة طويلة وكفاءة عالية لساعة الأمبير وكفاءة عالية في استخدام الطاقة.
- لتحقيق جهد خلوي عالي وكثافة طاقة عالية ، يجب أن يحدث تفاعل تبادل الليثيوم عند إمكانات عالية بالنسبة لليثيوم.
- لتسهيل عمليات الشحن والتفريغ عالية السرعة ، يجب أن تكون الموصلية الإلكترونية وحركة أيون الليثيوم في المادة عالية.
- يجب ألا تذوب مادة القطب الموجب في المنحل بالكهرباء ويجب أن تكون متاحة بتكلفة معقولة. لتقليل التكلفة ، يفضل التحضير من مواد رخيصة في عملية منخفضة التكلفة
LiFePO 4 استثناء لهذه القاعدة. في LiFePO 4 ، يتم تحقيق نقل أيون الليثيوم الكافي عن طريق استخدام جزيئات قطب كهربائي لها حجم جسيم نانومتر. [جيف دان وغرانت إم إرليش. “بطاريات أيونات الليثيوم” ، دليل البطاريات ليندن ، الطبعة الرابعة ، توماس بي ريدي (محرر) ، ماكجرو هيل ، ص 26.6 ، 2011]
تختلف المواد الفعالة الإيجابية (PAM) في خلايا أيونات الليثيوم حسب الشركة المصنعة. يمكن تصنيف مواد الكاثود إلى ثلاث فئات عامة [ Arumugam Manthiram، Nature Communications (2020) 11: 1550]. هم انهم:
أكاسيد الطبقات - مواد الكاثود في بطارية ليثيوم أيون
تتبلور عدة أكاسيد من النوع العام LiMO 2 (حيث M = الفاناديوم والكروم والكوبالت والنيكل) في بنية ذات طبقات يشغل فيها أيون Li + و M 3+ [ممرات هيكل الملح الصخري لإعطاء تسلسل طبقة من O-Li-OMO.
في كاثود الأكسيد ذو الطبقات LiCoO 2 ، تؤدي الاختلافات الكبيرة في الشحنة والحجم بين أيونات Li + وأيونات Co 3+ ثلاثية التكافؤ إلى ترتيب الكاتيونات الجيد ، وهو أمر بالغ الأهمية لدعم الانتشار السريع لليثيوم أيون ثنائي الأبعاد والتوصيل في مستوى الليثيوم.
تتطلب مواد الكاثود مستويات نقاء عالية للغاية ويجب أن تكون خالية تمامًا تقريبًا من الشوائب المعدنية غير المرغوب فيها – لا سيما الحديد والفاناديوم والكبريت.

الشكل 13. تخطيطي مبسط لهيكل متعدد الطبقات يوجد فيه احتلال بديل لـ
طبقات الكاتيون بين طبقات أيون الأكسيد المتراصة.
[الائتمان: روبرت أ.هاغينز ، بطاريات متقدمة ، جوانب علوم المواد ، سبرينغر ، نيويورك ، 2009 ، ص 168]
يوفر الاستقرار الهيكلي الجيد جنبًا إلى جنب مع الموصلية الكهربائية العالية والليثيوم أيون خصائص تفريغ شحن سريع مع قابلية انعكاس جيدة. مع هذه الميزات ، يظل LiCoO2 كواحد من أفضل الكاثودات حتى الآن بجهد تشغيل عالٍ يبلغ حوالي 4 فولت. تم حل الكاثود LiCoO2
اثنين من التحديات الرئيسية المرتبطة كاثود كبريتيد متابعة في 1970s. لم يمكّن فقط من زيادة كبيرة في جهد التشغيل من< 2.5 فولت إلى ~ 4 فولت ولكن أيضًا تجميع الخلية دون الحاجة إلى استخدام أنود الليثيوم المعدني.
أكاسيد الإسبنيل - مواد الكاثود في بطارية الليثيوم أيون
الفئة الثانية من الكاثود هي الإسبنيل LiMn 2 O 4 . (الصيغة العامة هي AB 2 O 4 ). على الرغم من أن هذا الهيكل يتم تصويره بشكل عام في إحداثيات مكعبة ، إلا أنه يحتوي أيضًا على طبقات متوازية من أيونات الأكسيد على (111) طائرة ، وهناك مواقع منسقة ثماني السطوح ومواقع منسقة رباعي السطوح بين مستويات أيونات الأكسيد. عدد مواقع الاوكتاهدرا يساوي عدد أيونات الأكسيد ، ولكن هناك ضعف عدد مواقع التتراهدرا. يوفر الاستقرار الهيكلي ثلاثي الأبعاد والتوصيل الكهربائي العالي والليثيوم أيون خصائص تفريغ شحن أسرع لـ Li 1 – x Mn 2 O 4 مع قابلية انعكاس جيدة مقارنة بـ LiCoO 2 .
من المزايا المهمة عند الانتقال من LiCoO 2 إلى LiMn 2 O 4 التخفيض الكبير في التكلفة حيث أن تكلفة المنجنيز أقل بمقدار أمرين من حيث التكلفة من Co. ومع ذلك ، هناك مشكلة حرجة في LiMn 2 O 4 وهي انحلال المنجنيز من الشبكة في الإلكتروليت في وجود كميات ضئيلة (مستويات جزء في المليون) من أيونات H + (الحموضة) في المنحل بالكهرباء بسبب عدم تناسق Mn 3 المعروف. + إلى Mn 4+ و Mn 2+ في حامض.

الشكل 14. رسم تخطيطي لهيكل الإسبنيل الذي يتم فيه توزيع الكاتيونات بين (111) طائرة من أيونات الأكسيد بين مواقع التتراهدرا والأوكتاهدرا [ Credit: Robert A. Huggins، Advanced Binders، Materials Science Aspects، Springer، New York، 2009 ص 17].
تبدو مادة كاثود الليثيوم والنيكل وأكسيد المنغنيز (LNMO) ذات الجهد العالي واعدة في بطاريات الجيل التالي. لكن حجر العثرة هو عدم وجود إلكتروليت يمكنه التعامل مع ضغوط بطارية تعتمد على LNMO. تقدم خلايا البطارية القائمة على الكاثود LNMO نتائج مساوية للبطاريات الأخرى عالية الأداء القائمة على الليثيوم ، ولكن بتكلفة أقل بكثير.
ومع ذلك ، فإن مصنعي الإلكتروليت يحصلون على نتائج واعدة جدًا من البحث والتطوير المستمر الذي سينتج عنه ، في مرحلة ما ، إلكتروليتات تعمل بشكل جيد في خلية بطارية LNMO. https: //blog.topsoe.com/the-cathode-material-for-next-generation-lithium-ion-battery-is-ready
في الآونة الأخيرة ، أصبحت زيادة محتوى النيكل وخفض محتوى الكوبالت أو التخلص منه في كاثودات NMC أكثر بروزًا [ Li، W.، Erickson.، E. & Manthiram، A. كاثودات أكسيد طبقات النيكل العالية لبطاريات السيارات القائمة على الليثيوم نات. الطاقة 5 ، 26-24 ( 2020)].
أكاسيد بولي أنيون - مواد الكاثود في بطارية ليثيوم أيون
الفئة الثالثة من الأكاسيد هي أكاسيد بوليانيون. تم العثور على أكاسيد بوليانيون مثل Fe 2 (MoO 4 ) 3 و Fe 2 (WO 4 ) 3 لإدخال / استخراج عكسي لاثنين من أيونات الليثيوم لكل وحدة صيغة لإعطاء Li 2 Fe 2 (MoO 4 ) 3 أو Li 2 Fe 2 ( WO 4 ) 3 بالطرق الكيميائية والكهروكيميائية
[Manthiram ، A. ، Goodenough ، JB إدخال الليثيوم في إطارات Fe 2 (MO 4 ) 3 : مقارنة M = W مع M = Mo. J. علم الحالة الصلبة. 71, 349– 360 (1987)].
بناءً على أعمال مانثيرام وجوديناف ،
[Manthiram، A. & Goodenough، JB إدخال الليثيوم في إطارات Fe 2 (MO 4 ) 3 : مقارنة M = W مع M = Mo. J. علم الحالة الصلبة. 71 ، 349-360 (1987). Manthiram، A. & Goodenough، JB Lithium insertion in Fe 2 (SO 4 ) 3 framework. ياء مصادر الطاقة 26 ، 403-406 (1989).]
أدى استكشاف الفوسفات المحتوي على الليثيوم ككاثودات إلى تحديد أوليفين LiFePO 4 كاثود [Padhi، AK، Nanjundaswamy، KS & Goodenough، JB Phospho-Olivines كمواد إلكترود موجبة لبطاريات الليثيوم القابلة لإعادة الشحن. J. Electrochem. شركة 144 ، 1188-1194 (1997] في 1997.
لكن فئة أكسيد البوليانيون تعاني من الموصلية الإلكترونية السيئة. [ أروموجام مانثيرام ، نيتشر كوميونيكيشنز (2020) 11: 1550].
أدى استكشاف الفوسفات المحتوي على الليثيوم ككاثودات إلى تحديد أوليفين LiFePO 4 كاثود [Padhi، AK، Nanjundaswamy، KS & Goodenough، JB Phospho-Olivines كمواد إلكترود موجبة لبطاريات الليثيوم القابلة لإعادة الشحن. J. Electrochem. شركة 144 ، 1188-1194 (1997] في 1997.
لكن فئة أكسيد البوليانيون تعاني من الموصلية الإلكترونية السيئة. [ أروموجام مانثيرام ، نيتشر كوميونيكيشنز (2020) 11: 1550].
تصنيع مواد الكاثود - بطارية ليثيوم أيون
في وقت سابق ، تم تصنيع مركبات كاثود أكسيد معدن الليثيوم من كربونات الليثيوم وملح المعدن المختار عن طريق سلسلة من تفاعلات الاستبدال الكيميائي التي يتم إجراؤها في المحلول. يتم ترسيب المنتج المطلوب وتجفيفه بالرش.
تم تحضير LiCoO 2 لأول مرة بطريقة التوليف التقليدية الموضحة في الشكل . تم خلط Tricobalt tetraoxide (Co 3 0 4 ) وكربونات الليثيوم (Li 2 CO 3 ) جيدًا ، متبوعًا بالتكلس في تدفق الهواء عند درجة حرارة حوالي 950 درجة مئوية. ومع ذلك ، من خلال هذه الطريقة ، كان من الصعب جدًا تحضير الجسيمات الخشنة من LiCoO 2 ويمكن الحصول على الجسيمات الدقيقة التي يبلغ قطرها 1-3 مساءً فقط.
مواد القطب النشط الدقيقة غير مرغوب فيها من وجهة نظر السلامة. في حالة الانتهاكات مثل الدائرة القصيرة الخارجية أو التكسير ، تتفاعل الجسيمات الدقيقة ذات مساحة السطح المحددة الكبيرة بسهولة في وقت واحد ويتم إطلاق كل طاقة الخلية بشكل مفاجئ خلال فترة زمنية قصيرة جدًا مع ارتفاع درجة الحرارة المصاحب. في أسوأ الحالات ، يمكن أن تشتعل الخلية [Yoshio Nishi ، في بطاريات أيونات الليثيوم ، M. Wakihara و 0. Yamamoto (محرران). صفحة 192-193].
كيف يتم تصنيع بطارية ليثيوم أيون؟ مخطط
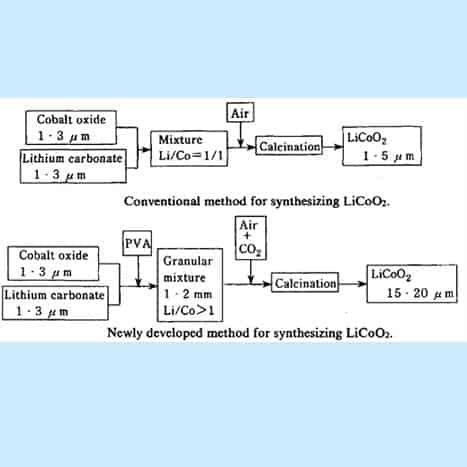
الشكل 15. مخطط انسيابي لصنع Li-CoO 2
[الائتمان: يوشيو نيشي ، في بطاريات أيونات الليثيوم ، M. Wakihara و 0. Yamamoto (محرران). صفحة 192-193].
عملية محسّنة لتصنيع كوبالت الليثيوم بحجم جسيم أكبر: النقطة الأولى هي إضافة كمية صغيرة من راتينج PVA في خلائط المواد الخام (Co 3 0 4 و Li 2 CO 3 )) لتشكيل كريات حبيبية باستخدام محبب . عن طريق تلبيد الحبيبات في تدفق هواء يحتوي على كمية مناسبة من غاز ثاني أكسيد الكربون ، يتم تصنيع جزيئات الليثيوم كوبالتايت بقطر متوسط 20 مساءً. النقطة الثانية هي أننا نستخدم كمية زائدة قليلاً من كربونات الليثيوم (Li 2 CO 3 ) في المواد الخام ، وبالتالي فإن النسبة الذرية Li / Co في المواد الخام أكبر من واحد. هذا الإجراء مناسب أيضًا للحصول على جسيمات خشنة ، بالإضافة إلى أن LiCoO 2 الناتج يحتوي على كمية صغيرة من Li 2 CO 3 المتبقي.
النقطة الأولى هي إضافة كمية صغيرة من راتينج PVA في مخاليط المواد الخام (Co304 و Li 2 CO 3 ) لتشكيل كريات حبيبية باستخدام محبب. عن طريق تلبيد أكسيد الكوبالت الليثيوم يمكن تحضيره بسهولة عن طريق الحرق بدرجة حرارة عالية لمزيج متكافئ من كربونات الليثيوم Li 2 CO 3 وأكسيد الكوبالت ، Co 3 O 4 أو الكوبالت المعدني عند 600-800 درجة مئوية ، ثم تلدين المنتج عند 900 درجة مئوية لعدة ساعات ، وكل ذلك تحت جو من الأكسجين.
يمكن الحصول عليها أيضًا عن طريق تكليس أكسيد الماء مع هيدروكسيد الليثيوم حتى 750-900 درجة مئوية.
تستخدم الطريقة الثالثة أسيتات الليثيوم وخلات الكوبالت وحمض الستريك بكميات مولارية متساوية في محلول مائي. التسخين عند 80 درجة مئوية يحول الخليط إلى هلام شفاف لزج. ثم يتم طحن الجل المجفف وتسخينه تدريجياً إلى 550 درجة مئوية. (https: //en.wikipedia.org/wiki/Lithium_cobalt_oxide).
بعض الأمثلة النموذجية هي: طريقة Sol-gel
في عملية سول-جل ، يتم خلط المحاليل المائية للمواد المتفاعلة ومحلول عامل مخلب. يؤدي التبخر البطيء للمذيب إلى توليد محلول مائي وتسخين معتدل من محلول مائي وبالتالي ينتج مادة هلامية. يتم تحميص الأخير عند درجة حرارة مناسبة للحصول على المنتج المطلوب.
مثال 1.
تخليق LiCoO 2 من عوامل معقدة مختلفة: الأملاح المستخدمة هي نترات الكوبالت هيكسا هيدرات (Co (NO 3 ) 2 6H 2 O ، ونترات الليثيوم ، LiNO 3 اللامائية. تم إنتاج الجل باستخدام أربعة عوامل معقدة مختلفة: حامض الستريك ، اللامائي ( C3H4 OH (COOH) 3 ، الجلايسين ، (H 2 NCH 2 COOH) ؛ النشا ( نشا الذرة التجاري والجيلاتين).
يتم تحضير خمسة محاليل تحتوي على LiNO 3 و Co (NO 3 ) 2 .6H 2 O في 20 مل من الماء ، مع نسبة Li: Co = 1.1: 1. يضاف عامل معقد محدد لكل محلول: ( 1 ) حمض الستريك (4.611 جم) مخفف في 5 مل من الماء ؛ ( 2 ) جلايسين (1.501 جم) ؛ ( 3 ) النشا (1.250 جم) ؛ ( 4 ) الجيلاتين (3.500 جم) و ( 5 ) اختبار فارغ.
تم تسخين المحاليل الأربعة الأولى عند درجة حرارة 70 إلى 80 درجة مئوية في حمام الجلسرين حتى تكوين الهلام. يختلف مقدار الوقت المستغرق في هذه العملية لكل عامل تبلور: ( 1 ) حامض الستريك (5 ساعات) ، ( 2 ) الجلايسين (3 ساعات) ، ( 3 ) النشا (ساعة واحدة) ، ( 4 ) الجيلاتين (3 ساعات) . تم إجراء إنتاج المساحيق البلورية لجميع العينات على مرحلتين في فرن دثر: أولاً بإطلاق المواد عند 300 درجة مئوية لمدة 20-30 دقيقة ثم تسخينها لاحقًا عند 700 درجة مئوية لمدة 24 ساعة. [برونو جي إيه فريتاس وآخرون ، ج. براز. علم. شركة 28 ، 11 نوفمبر 2017].
مثال 2.
محضرة بطريقة سول-جل
يذوب LiNO3 أولاً في محلول حامض الستريك. تم استخدام LiNO3 و Ni (NO3) 2.6H2O Co (Ac) 2.4H2O و Mg (NO) 2.6H2O كمواد أولية من الليثيوم والنيكل والكوبالت والمغنيسيوم في LiNi 0.7 – M 𝑥 Co 0.3 O2 (0 ⩽ 𝑥 ⩽ 0.1) ، على التوالي. كمية حامض الستريك تساوي إجمالي كمية المولي من Co و Ni و Mg. بعد ذلك ، تمت إضافة Co (Ac) 2 · 4H2O ، و Ni (NO3) 2 · 6H2O و Mg (NO) 2 · 6H2O إلى الخليط. يسخن الخليط كله بواسطة حمام مائي عند 80 درجة مئوية. أثناء عملية التسخين ، يتكون محلول وردي شفاف بدون أي ترسيب. أخيرًا ، تم تجفيف المحلول الصافي ببطء وتحويله إلى هلام. تم تجفيف xerogel ، وطحنه ، ثم معالجته حرارياً في فرن عند 120 درجة مئوية لمدة 12 ساعة.
تم تحميص المادة الهلامية عند 500 درجة مئوية في الهواء لمدة 6 ساعات ، وتم تبريدها إلى درجة حرارة الغرفة في فرن أنبوب. تم طحن المنتجات المعالجة حرارياً في ملاط من العقيق للحصول على مساحيق. ثم تم تحميص المسحوق عند 800 درجة مئوية لمدة 12 ساعة. لتصنيع الكاثودات ، تم أولاً خلط المنتجات المحضرة مع الأسيتيلين الأسود وفلوريد البولي فينيلدين (80: 8:12 بالوزن) في بيتا ميثيل بيروليدون (NMP). يتم بعد ذلك طلاء الملاط الناتج على رقائق Al وتجفيفه عند 80 درجة مئوية لمدة 18 ساعة لمزيد من ضغط اللفائف. . [ Hailang Zhang، Advances in Material Science and Engineering Vol 2014، Article ID 746341، ]

الشكل 16. مخطط انسيابي لعملية سول جل لتحضير منجنات الليثيوم
( Credit: YS Lee، YK Sun and KS، Nahm، Solid State Ionics 109 (1998) 285 كما قدمها ، M. Pasquali ، S. Passerini and G Pistoia، في بطاريات الليثيوم ، العلوم والتكنولوجيا ، أد. بقلم GA Nazri و G.Pistoia ، Springer ، New York ، (2009) ، p. 318)
تصنيع مواد الأنود في بطارية ليثيوم أيون
المسار المشجع الذي يؤدي إلى LIBs مع تحسين كثافة الطاقة والطاقة هو اختيار مواد الأنود المناسبة التي يمكن أن توفر سعة عالية وسهولة في انتشار أيونات Li-ion في الأنود ، جنبًا إلى جنب مع دورة حياة جيدة وخالية من مخاوف السلامة.
بناءً على المواد الأولية ، يمكن تصنيف أنودات الكربون إلى عدة أنواع على النحو المبين أدناه.
تحدد المادة الأولية ومعلمات المعالجة طبيعة الكربون المنتج. المواد التي يمكن رسمها عن طريق المعالجة عند درجة حرارة عالية (2000 إلى 3000 درجة مئوية) تسمى الكربون الناعم .
عند الرسم البياني ، تتم إزالة الاضطراب التوربيني بشكل تدريجي مع زيادة درجة الحرارة ، ويتم التخلص من الإجهاد في المادة [T. تشنغ وجين إن رايمرز وجيه آر دان ، فيز. القس ب 51 ، 734 (1995)] لا يمكن تحويل الكربونات الصلبة ، مثل تلك المحضرة من راتنج الفينول ، بسهولة إلى رسم بياني ، حتى عند معالجتها عند درجة حرارة 3000 درجة مئوية. يتم تحضير المواد من نوع فحم الكوك عند حوالي 1000 درجة مئوية ، عادةً من مادة نفطية عطرية [جيف دان وغرانت إم إرليش. “بطاريات أيون الليثيوم” ، دليل البطاريات ليندن ، الطبعة الرابعة ، توماس بي ريدي (محرر) ، ماكجرو هيل ، ص 26 ، 2011]

الشكل 17. تصنيف المواد الأولية لأنود الكربون
[ائتمان: جيف دان وغرانت إم إرليش. “بطاريات أيون الليثيوم” ، دليل البطاريات ليندن ، الطبعة الرابعة ، توماس بي ريدي (محرر) ، ماكجرو هيل ، ص 26 ، 2011]
يقسم Goriparti مواد الأنود من LIB إلى ثلاث فئات اعتمادًا على آلية تفاعلها مع الليثيوم [ Subrahmanyam Goriparti و Ermanno Miele و Francesco De Angelis و Enzo Di Fabrizio و Remo Proietti Zaccaria و Claudio Capiglia و J Power Sources 257 (2014) 421-443]
مجموعة الإقحام / إلغاء الإقحام
تشمل هذه الفئة من الأنود المواد الكربونية وأكاسيد التيتانيوم. ترتبط سعة التخزين التي تحدث من خلال مسار الإقحام ارتباطًا وثيقًا بمساحة السطح والتشكل والتبلور واتجاهه. يتم قبول الكربون الناعم بشكل عام واستخدامه في صناعة البطاريات. لقد لوحظ أن الكربون اللين هو تقنية ناضجة تمامًا ، في حين أن الكربون الصلب قد يقدم حلاً بديلاً مثيرًا للاهتمام خاصة للتطبيقات التي تتطلب سعة عالية مثل قطاع السيارات الكهربائية. تستخدم بعض صناعات البطاريات أنودات أكسيد التيتانيوم.


كما تم استعراض الجرافين على نطاق واسع. على وجه الخصوص ، لوحظ أن خواصها الكهربائية تجعل هذه المادة مناسبة بشكل خاص لأنودات الجرافين / المعدن الهجين (على سبيل المثال الجرافين مع SnO2 و Fe2O3). كانت أنابيب الكربون النانوية (CNTs) مهمة لنتائجها الأكاديمية الشيقة للغاية ، على الرغم من أن تكلفة الإنتاج قد تعيق تطبيقها كمواد نشطة للأنود في صناعة البطاريات في المستقبل.


ومع ذلك ، بالنسبة لبطاريات المركبات الكهربائية الكبيرة ، يُفضل عادةً استخدام الجرافيت منخفض التكلفة نظرًا لاعتبارات التكلفة.
في فئة ثانية ، تم وصف مواد صناعة السبائك مثل Si ، Ge ، SiO ، SnO2. يمكن أن توفر هذه المواد سعات أكبر وكثافة طاقة عالية مقارنة بالمجموعة السابقة ، من خلال التفاعل مع الليثيوم في سبيكة / آلية كهروكيميائية خالية من السبائك. ومع ذلك ، فإن هذه العملية تنطوي على توسيع حجم كبير مما يؤدي إلى خسارة كبيرة في السعة عند ركوب الدراجات. تم اقتراح التخفيض من الأبعاد السائبة إلى المقياس النانوي ، جنبًا إلى جنب مع تحقيق الهياكل المعقدة من خلال الدمج مع المصفوفات الموصلة ، للتغلب على المشكلات المحددة أعلاه ولتحسين أداء الأنود الكلي.
يعد السيليكون و SnO2 ومركبتهما مع الكربون أكثر المواد الواعدة للتطبيقات في بطاريات الليثيوم المستقبلية ، ومع ذلك ، لا تزال طريقة غير مكلفة لإنتاجها الضخم كمواد الأنود ضرورية. من ناحية أخرى ، فإن Ge ، على الرغم من كونها مثيرة للاهتمام لخصائصها الكهروكيميائية ونتائجها المعملية التجريبية الممتازة ، إلا أنها تعاني من عيب كونها العنصر الخمسين من حيث الوفرة في قشرة الأرض. لذلك ، يبدو أنه ليس خيارًا جيدًا للتطبيق الشامل لتكنولوجيا بطارية الليثيوم.
في المجموعة الثالثة ، تم وصف المواد التي تتفاعل مع الليثيوم بطريقة تفاعل التحويل. على وجه الخصوص ، تم النظر في أكاسيد الفلزات / الفوسفات / النتريدات / الكبريتيدات. ومع ذلك ، لا تزال هذه المواد بعيدة عن سوق بطاريات الليثيوم التجارية الكبيرة ، بسبب ضعف القدرة على الاحتفاظ بالسعة والتباطؤ المحتمل الكبير. لذلك ، تم أيضًا التحقيق في مجموعة متنوعة من الأشكال ذات البنية النانوية لهذه المواد لمعالجة المشكلات المحددة أعلاه.
إن تقنية النانو هي بالتأكيد نهج هائل لهندسة الجيل القادم من مواد الأنود لبطاريات الليثيوم. من أجل استخدام المواد الموصوفة كأنودات فعالة في LIBs التجارية ، خاصة لتطبيقات EV ، هناك حاجة إلى مزيد من العمل البحثي. في الواقع ، من الضروري تحقيق طاقة أعلى وكثافة طاقة أعلى جنبًا إلى جنب مع تطوير عمليات تصنيع غير مكلفة لتوليف المواد النانوية على نطاق واسع. علاوة على ذلك ، فإن التحقيق في الآليات التي تحكم التفاعل بين الليثيوم والأشكال النانوية للمواد الموصوفة جنبًا إلى جنب مع خصائص نقل الإلكترون في واجهة القطب / الإلكتروليت له أهمية حاسمة لتصميم الجيل التالي من المواد الفعالة للأنود المصممة بواسطة تقنية النانو .
تتضمن الأقطاب الكهربائية السالبة المستخدمة حاليًا في خلايا الليثيوم محلولًا صلبًا من الليثيوم في أحد أشكال الكربون. يجب بالضرورة أن تستخدم خلايا الليثيوم التي تعمل في درجات حرارة أعلى من نقطة انصهار الليثيوم السبائك بدلاً من عنصر الليثيوم. هذه بشكل عام أطوار معدنية ثنائية أو ثلاثية. هناك أيضًا اهتمام متزايد حاليًا بإمكانية استخدام السبائك المعدنية بدلاً من الكربون في درجات الحرارة المحيطة ، بهدف تقليل حجم القطب ، فضلاً عن تحقيق سعة أكبر بشكل ملحوظ. [روبرت أ.هاغينز ، بطاريات متقدمة ، جوانب علوم المواد ، سبرينغر ، نيويورك ، 2009 ، ص 123].
الجرافيت مذبذب ، ويمكن إدخال الكاتيونات أو الأنيونات فيه بين طبقات الجرافين. عندما يتم إدخال الكاتيونات ، تأخذ بنية الجرافيت المضيف شحنة سالبة. أمثلة الكاتيون هي Li + و K + و Rb + و Cs + . عندما يتم إدخال الأنيونات ، تأخذ بنية الجرافيت المضيف شحنة موجبة ، وأمثلة الأنيون هي Br – ، SO2 – ، SbF6 –
تم إثبات إدخال الفلزات القلوية في الكربون لأول مرة في عام 1926 [K. فريدنهاغن وج. كادنباخ ، ز. أنورغ. كلغ. علم. 158 ، 249 (1926)] وتم عرض التركيب الكيميائي للليثيوم-كربون في عام 1955 [ د. جيرارد ، إيه هيرولد ، كربون 13 ، 337 (1975 )]. الأشعة السينية أظهرت تجارب التحليل الطيفي للانبعاث الضوئي أن الليثيوم المُدرج يتخلى عن إلكترونته للكربون ، وبالتالي يمكن اعتبار الهيكل أيونات Li + الموجودة بين طبقات الكربون في بنية الجرافيت.
[GK Wertheim، PMTh.M. Van Attekum و S. Basu ، Solid State Commun. 33 ، 1127 (1980)]. يمكن الاطلاع على مراجعة عامة للعمل المبكر على إدخال الأنواع في الجرافيت في
[إل بي إيبرت ، مركبات الإقحام من الجرافيت ، في المراجعة السنوية لعلوم المواد ،
المجلد. 6 ، أد. بواسطة RA Huggins ، المراجعات السنوية ، Palo Alto ، CA (1976) ، p. 181].
العامل المهم في نقاء مادة الأنود هو الحاجة إلى التخلص من أي أنواع تحتوي على الأكسجين على السطح لأنها ستتفاعل مع الإلكتروليت. لمنع هذا التفاعل ، يقوم المصنعون بخبز الجرافيت عند 1100 درجة مئوية) في تقليل الغلاف الجوي أو خامله. هذا يزيد من تكلفة الاستخدامات الأخرى ، مقارنة بالجرافيت. يتم خلط الكربون (90٪) مع العديد من المكونات الأخرى لصنع عجينة الأنود أو الملاط. كما هو الحال مع الكاثود ، يتم استخدام فلوريد البوليفينيلدين (PVDF) كمادة رابطة (-5٪) ، وتضاف كمية صغيرة من أسود الكربون لضمان التوصيل. بالإضافة إلى ذلك ، يتم استخدام n-methyl pyrrolidone (NMP) لإذابة المواد لتشكيل خليط موحد. يضمن الضغط حجم حبيبات موحد (Sandi 1999).
يكتسب تيتانات الليثيوم (LTO) الكثير من الاهتمام. تعمل خلايا LTO عند درجة حرارة أقل من الكيماويات الأخرى وتوفر كثافة طاقة عالية. ومع ذلك ، فإن هذه الخلايا تعاني من انخفاض الجهد الاسمي ، في حدود حوالي 2.2-2.3 فولت لكل خلية. [نوريو تاكامي ، هيروكي إيناغاكي ، يوشيناو تاتباياشي ، هيديساتو سارواتاري ، كيزوه هوندا ، شون إيجوسا ، J Power Sources 244 (2013) 469-475]
تتمدد مادة القطب ، الجرافيت عادةً ، بنسبة 10٪ أثناء عملية الشحن. يستعيد الجرافيت حجمه الأصلي عندما تنفصل أيونات الليثيوم. لن يتم فقط إقحام أيونات الليثيوم في الجرافيت إذا تم استخدام الألومنيوم ولكن أيضًا يتم إدخالها في الموصل ، مما يؤدي إلى تكوين سبيكة من الألومنيوم والليثيوم. ستحدث العملية العكسية أثناء التفريغ. سوف يتحلل الألمنيوم بعد بضع دورات وسيكون عديم الفائدة كمجمع حالي.
ومع ذلك ، إذا كان القطب السالب مصنوعًا من تيتانات الليثيوم بدلاً من الجرافيت ، فإن الوضع يتغير بشكل كبير. إن جهد القطب الكهربائي لـ Li 4 Ti 5 O 12 أعلى بحوالي 1.4 فولت من الجرافيت (جهد الخلية أقل بحوالي 1.4 فولت ، 2.2 فولت مقابل 3.6 فولت). هذا من شأنه أن يمنع أيونات الليثيوم من أن يتم إقحامها في الألومنيوم. لذلك ، يُفضل الألومنيوم على النحاس لأسباب تتعلق بالتكلفة والوزن. يتم استخدام Li 4 Ti 5 O 12 بشكل أساسي في التطبيقات الثابتة بسبب جهد الخلية المنخفض. [ Călin Wurm et al.، in Lithium-Ion Bracelets، Reiner Korthauer (ed)، Translated by Michael Wuest et.al.، Springer، 2018. pp. 57 ].
عملية إنتاج تيتانات الليثيوم: خليط من ثاني أكسيد التيتانيوم ومركب الليثيوم (أي واحد من هذه: كربونات الليثيوم ، وهيدروكسيد الليثيوم ، ونترات الليثيوم ، وأكسيد الليثيوم) يتم تلبيده مسبقًا عند درجة حرارة تتراوح بين 670 درجة مئوية و 800 درجة مئوية . يتم الحصول على مركب يتكون من TiO2 و Li 2 TiO 3 أو مركب يتكون من TiO2 و Li 2 TiO 3 و Li 4 Ti 5 O 12 . ثم يتم تلبيد المركب عند درجة حرارة في حدود 800 إلى 950 درجة مئوية. [تيتسويا ياماواكي وآخرون ، براءة الاختراع الأمريكية رقم 6،645،673 B2 ، 2003 المخصصة لشركة Toho Titanium Co.، Ltd.، Chigasaki]
بطارية قابلة لإعادة الشحن SCiB ™ من Toshiba (https://www.scib.jp/en/)
يستخدم SCiB ™ أكسيد التيتانيوم والليثيوم (LTO) في الأنود لتحقيق الأمان والعمر الطويل وأداء درجات الحرارة المنخفضة والشحن السريع وقوة الإدخال / الإخراج العالية والقدرة الفعالة الكبيرة. وجدت SCiB ™ تطبيقات واسعة في تطبيقات المركبات والصناعية والبنية التحتية ، بما في ذلك السيارات والحافلات وعربات السكك الحديدية والمصاعد ومحطات الطاقة.
إنتاج فاصل بطارية ليثيوم أيون
يتوفر نوعان من العمليات: الرطب والجاف. يستخدم المصنعون اليابانيون عملية رطبة يتم فيها إذابة البوليمر في الزيت. ثم يتبخر الزيت ليترك طبقة مسامية. يستخدمون بوليمرات ذات وزن جزيئي مرتفع للغاية لإنتاج Celgard ، ويتم تصفيح ثلاث طبقات من فيلم البوليمر المنفوخ ، وسحبها لأسفل ، ولدين أسفل نقطة الانصهار للتحكم في بنية البوليمر. ثم يتم شد الصفيحة بسرعة للحصول على المسامية.
يتوفر نوعان من العمليات: الرطب والجاف. يستخدم المصنعون اليابانيون عملية رطبة يتم فيها إذابة البوليمر في الزيت. ثم يتبخر الزيت ليترك طبقة مسامية. يستخدمون بوليمرات ذات وزن جزيئي مرتفع جدًا لإنتاج Celgard ، ويتم تصفيح ثلاث طبقات من فيلم البوليمر المنفوخ ، وسحبها لأسفل ، وتصلبها أسفل نقطة الانصهار للتحكم في بنية البوليمر. ثم يتم شد الصفيحة بسرعة للحصول على المسامية.
[Pekala، RW، et al.، 2000، “الفواصل: فرصة مُغفلة لتحسين أداء البطارية؟” لودرديل ، فلوريدا ، 6-9 مارس]
هذه العملية حساسة للغاية لظروف التشغيل وحتى تختلف باختلاف دفعات المواد ، لذلك من الضروري التحكم الدقيق [Linda Gaines و Roy Cuenca ، تكلفة بطاريات ليثيوم أيون للمركبات ، ANL Report ANL / ESD-42 ، مايو 2000 ، ص 20] .
ومع ذلك ، فإن السماكة الإضافية المطلوبة في الفواصل لخلايا EV / HEV تعوض عن القوة المنخفضة. [Y. نيشي ، في: M. Wakihara ، O. Yamamoto (Eds.) ، بطاريات ليثيوم أيون ، Wiley / VCH / Kodansha ، Tokyo ، 1998 ، p. 195.
P. Arora، Z. Zhang، Chem. القس 104 (2004) 4419].
بالإضافة إلى الخصائص التقليدية مثل القوة الميكانيكية الجيدة ونفاذية الإلكتروليت ، تعرض هذه الفواصل المسامية الدقيقة خاصية الحماية أثناء إساءة استخدام الخلية. على سبيل المثال ، إذا ارتفعت درجة حرارة الخلية بشكل غير طبيعي بسبب الشحن الزائد المفرط ، على سبيل المثال ، فإن الحرارة المتولدة تخفف من البولي إيثيلين وتغلق المسام الدقيقة في الفيلم. وهذا ما يسمى الفاصل “إيقاف التشغيل”. بمجرد حدوث الإغلاق ، يتوقف النقل الأيوني بين الأقطاب بشكل فعال ويتوقف التيار عن التدفق. إذا كان بإمكان الفاصل الاحتفاظ بالسلامة الميكانيكية أعلى من درجة حرارة إيقاف التشغيل ، فيمكنه توفير هامش أمان للجهاز ؛ خلاف ذلك ، يمكن أن تتلامس الأقطاب الكهربائية بشكل مباشر ، وتتفاعل كيميائيًا ، مما يؤدي إلى هروب حراري.
ومع ذلك ، فمن الممكن أنه بسبب القصور الذاتي الحراري ، يمكن أن تستمر درجة الحرارة في الارتفاع حتى بعد الإغلاق. في ظل هذه الظروف ، يقوم الفاصل بإذابة الأقطاب الكهربائية وقصرها ، مما يؤدي إلى تفاعلات عنيفة وتوليد حرارة. هذه الظاهرة تسمى “الانهيار” أو “الانهيار” للفاصل. لذلك ، من أجل ضمان سلامة الخلية ، يجب أن يكون الفرق بين درجات حرارة “الإغلاق” و “الانهيار” كبيرًا قدر الإمكان.
الفواصل المصنوعة بالكامل من البولي إيثيلين عالي الكثافة تذوب عند 135 درجة مئوية وتفقد السلامة الميكانيكية فوق درجة الحرارة هذه. ومع ذلك ، فإن الفواصل المصنوعة من طبقات التصفيح من البولي بروبلين والبولي إيثيلين تحافظ على السلامة الميكانيكية على الأقل حتى 165 درجة مئوية ، وهي نقطة انصهار البولي بروبلين. من المثير للاهتمام ملاحظة أنه على الرغم من ذوبان البولي إيثيلين عالي الوزن الجزيئي عند 135 درجة مئوية ، فإن الفواصل المصنوعة من هذه المادة تحتفظ بسلامتها الميكانيكية حتى 180 درجة مئوية على الأقل لأن لزوجة المادة تحافظ على السلامة المادية.
تعتبر فواصل إيقاف التشغيل موثوقة ويختار مصنعو بطاريات الليثيوم أيون بشكل متزايد دمجها في منتجاتهم. تحتوي فواصل الإغلاق الأكثر شيوعًا على مادة البولي بروبيلين ذات الوزن الجزيئي المرتفع الممزوج بالبولي إيثيلين عالي الوزن الجزيئي. هنا ، يتم الجمع بين خاصية الإغلاق الفريدة للبولي إيثيلين بشكل إيجابي مع السلامة الميكانيكية العالية للبولي بروبلين في درجات الحرارة المرتفعة. نظرًا لأن الإغلاق لا رجوع فيه ، فبمجرد تشغيله ، تترك هذه الفواصل الخلايا تالفة بشكل دائم. [PG Balakrishnan، R. Ramesh، T. Prem Kumar ، J. Power Sources. 155 (2006) 401-414]
مواد أخرى في بطارية ليثيوم أيون
هناك مواد أخرى مثل المجمعات الحالية مثل رقائق الألمنيوم والنيكل والنحاس ، والمواد الرابطة مثل البوليمر المشترك تيرين بوتادين (SBR) ، وفلوريد فلوريد الأوليفينيليدين (PVDF) ، والإلكتروليتات والمذيبات ، والإضافات الموصلة للكاثود ، والفاصل.
مزايا وقيود بطارية ليثيوم أيون - تصنيع خلايا أيونات الليثيوم
نسبة وزن الأنود إلى الكاثود
من المهم جدًا عدم تكوين أي معدن من الليثيوم أثناء تشغيل الخلية. يشكل ترسب المعدن التشعبات التي تقصر الخلية داخليًا. يساعد التحكم في الجهد أثناء الشحن وتوازن الخلية على تقليل هذه المشكلة إلى حد كبير. الطريقة الرئيسية للتحكم في ترسب الليثيوم هي نسبة الأنود إلى قدرة الكاثود للألواح الفردية في الخلية. قطب الأنود لديه قدرة استخدام أعلى بحوالي 10٪ من الكاثود. هذا يمنع ترسب معدن الليثيوم على الأنود أثناء الشحن ، حيث يحدد الكاثود سعة الخلية. إذا ترسب معدن الليثيوم على سطح القطب ، فإنه يتفاعل مع المنحل بالكهرباء ويمكن أن يبدأ في الانفلات الحراري.

الشكل 21. نسبة سعة الأنود والكاثود في خلية أيون الليثيوم
( Credit: Ralph J. Brodd and Kazuo Tagawa، in Advances in Lithium-Ion Bugs، Walter A. van Schalkwijk and Bruno Scrosati (Eds)، Kluwer Academic Publishers، New York، pp. 272، 2002.)
عمليات تجميع خلايا أيون الليثيوم
تتطلب عمليات تجميع الخلايا لبطارية ليثيوم أيون الدقة والدقة عند طلاء مخزون القطب الموجب والسالب المطلي بالمادة الفعالة. تعتبر عملية الطلاء عنصرًا حاسمًا في ضمان منتج عالي السعة والموثوقية. إذا كانت الطلاءات ذات جودة رديئة ، فلن يتم إنتاج سوى بطاريات منخفضة الأداء. تحدد الخطوات الأولية في تحضير الكتلة النشطة النتيجة.
كوهين وجوتوف ، [إي. Cohen and E. Gutoff ، تكنولوجيا التجفيف والطلاء الحديثة ، Wiley-VCH ،
وصف نيويورك ، 1992] منهجية للوصول إلى أفضل تقنية طلاء لتطبيق معين ، بناءً على ريولوجيا ملاط الطلاء ، والدقة المطلوبة وسرعة الطلاء.

الشكل 22. عملية طلاء الأنود والكاثود
( Credit: Ralph J. Brodd and Kazuo Tagawain in Advances in Lithium-Ion Bugs، Walter A. van Schalkwijk and Bruno Scrosati (Eds)، Kluwer Academic Publishers، New York، pp. 273، 2002.)
مخطط انسيابي لتصنيع بطارية ليثيوم أيون

الشكل 23. مخطط تدفق لتصنيع خلايا أيونات الليثيوم
[رالف ج.برود وكازو تاغاوا في التقدم في بطاريات الليثيوم أيون ، والتر أ. فان شالكفيك وبرونو سكروساتي (محرران) ، كلوير للنشر الأكاديمي ، نيويورك ، ص 271 ، 2002.]

الائتمان: Electropaedia https: //www.mpoweruk.com/battery_manufacturing.htm
الشكل 24. مخطط تدفق لتصنيع الأقطاب الكهربائية من المواد الخام
تجميع خلية أيون الليثيوم




تهدف الشركات المصنعة لبطاريات ليثيوم أيون إلى النقاط التالية أثناء تجميع الخلايا:
- يجب أن ينتج عن تصميمات خلية أيونات الليثيوم كثافة تيار موحدة في جميع أنحاء منطقة القطب.
- لضمان اتصال جيد بين المواد النشطة (AM) والمجمع الحالي
- يتم استخدام أقطاب كهربائية ذات مساحة كبيرة لإعطاء الخلايا أداءً عالي السرعة. هذا يقلل من الاستقطاب ، أي فقدان الجهد بسبب حركية تفاعلات القطب ويقلل من انخفاض الجهد عبر الفاصل.
يعطي هيكل المسام ومزيج من الكربونات الموصلة اتصالًا جيدًا بين الجسيمات للمادة الفعالة.
يعد الاتصال الجيد أمرًا ضروريًا بين المواد الفعالة ، والكربون الموصل والمجمع الحالي ، من أجل الاستخدام الكامل للمواد الفعالة ولتحقيق الكفاءة الجيدة أثناء الأداء العالي المعدل.
يتم تحضير مزيج كاثود الكوبالت من LiCoO2 (مسحوق أسود) + مادة رابطة PVdF (لدن بالحرارة فلورو بوليمر أبيض شبه بلوري) + N-methyl pyrrolidone (NMP ، سائل عضوي عديم اللون) كمذيب. نظرًا لكون LICoO2 غير موصل ، يتم إضافة مادة مخففة موصلة ، دائمًا ما تكون أسود الكربون ، لتعزيز موصلية LiCoO2.
يتم تحديد نسبة وكميات المواد من خلال تصميم الخلية وحجم الخلاط. يتم استخدام إجراء خلط مكثف لتجفيف مزج المادة الفعالة غير الموصلة والكربون قبل إضافة مذيب الطلاء والموثق.
يُمزج الخليط جافًا لإعطاء طلاء موحد لجزيئات المادة الفعالة مع طبقة رقيقة من الكربون الموصل بحيث يتم تحسين التلامس الكهربائي بين AM وشبكة المجمع الحالية (رقائق الألومنيوم ، بسمك 20 مم) ، وبالتالي ضمان الاستخدام الكامل لجميع AM. يتم إذابة البوليمر NMP في مذيب الطلاء في وعاء منفصل. مزيج المزيج الجاف ثم يتم دمج محلول المذيب لتشكيل ملاط.
تُستخدم إضافات المذيبات لضبط لزوجة الملاط (أو الطلاء) لعملية الطلاء . Polyvinylenedifluoride (PVdF) هو الموثق المفضل و المذيب هو N- ميثيل بيروليدينون (NMP). يتم وضع الملاط الناتج عن عملية الخلط في حاويات محكمة الغلق ، والتي تعمل كخزان ووسيط نقل لعمليات الطلاء. يتم ضخ كميات دقيقة من ملاط الطلاء من حاوية التخزين باستخدام مضخة تروس ، أو مضخة دقيقة مماثلة ، لتجنب أي انحباس للهواء في السائل المتجه إلى رأس الطلاء.
يتم تحضير مزيج الأنود بطريقة مماثلة مع الكربون الصلب والموثق PVdF و NMP. هذا المزيج مغطى بورق نحاسي يستخدم كشبكة (بسمك 10 مم).
يتم الطلاء على كلا الجانبين بسماكة حوالي 100 مم لكل من الأنودات والكاثودات. من خلال تقليل سماكة الطلاء ، يتم تحقيق زيادة في إجمالي مساحة السطح لحجم محدد للخلية. تمتلك الإلكتروليتات العضوية المستخدمة موصلية أقل مقارنةً بالمواد المائية ، وبالتالي فإن مساحة السطح الأعلى هذه ستسهل إنشاء خلية تفريغ عالية الطاقة.
سمك القطب يعتمد على الطاقة القصوى المطلوبة. الميزة الفريدة لتقنية تصنيع بطاريات أيونات الليثيوم هي أنها تتيح مجموعة واسعة من تصاميم نسبة الطاقة / الطاقة بنفس تقنية تصنيع القطب الكهربائي [بروسلي ، نظري ص 651]. لكن المجموعة الحالية المناسبة والجدولة وشكل الخلية والتصميم مهمان.
تجميع الخلية: يمر الرقاقة المطلية عبر الفرن لتبخير المذيب وترك كمية محددة من الكتلة النشطة على الرقاقة. تصنف العديد من مذيبات الطلاء على أنها خطرة ولا يمكن إطلاقها في الغلاف الجوي. كإجراء لتوفير التكلفة ، يتم استرداد المذيب بشكل عام لإعادة استخدامه في العملية. لتجنب أي تلوث للبيئة ، يمكن حرق المذيب.
معظم خلايا أيون الليثيوم أسطوانية الشكل. يتم تسطيح لفة الهلام للحصول على عناصر للخلايا المنشورية .
الخلايا المنشورية مواتية لتعبئة حجم أفضل ، ولكنها مسؤولة عن الانتفاخ عند ركوب الدراجات أو الشيخوخة. توفر علب الخلايا الأسطوانية قوة ميكانيكية أفضل واستقرارًا جيدًا للأبعاد وضغطًا موحدًا في العناصر.
تنتج عملية الطلاء طلاءًا متقطعًا ليتناسب مع طول الملف. تم تصميم آلات اللف لتعمل تلقائيًا للاستخدام مع لفات جامبو مجففة من الكاثودات والأنودات والفاصل (بسمك 25 مم أو أقل ، إما PP أو PE أو مختلط).
تبدأ العمليات بلحام الألسنة على الجزء غير المطلي من الرقائق. تقوم آلة اللف بعد ذلك بقطع الشريط إلى الطول المناسب ولف كاثود فاصل الأنود المركب في ملف ضيق أو بكرة بطريقة جيلي رول. مع زيادة قطر قلب الجرح ، تعوض آلة اللف تلقائيًا للحفاظ على التوتر المستمر مع زيادة قطر الملف من أجل التسامح الوثيق مع القطر. تعتبر الرياح الإهليلجية للخلايا المنشورية عملية أكثر تعقيدًا وأبطأ.
بعد اللف ، يتم فحص الملف بحثًا عن شورتات داخلية قبل إدخاله في العلبة. يجب أن تكون العلب الفولاذية نظيفة ومطلية بالنيكل لتوفير سطح مستقر وتقليل تآكل العلب قبل تجميع الخلية. يتم لحام الرصاص الأنود في قاع العلبة ويتم لحام سلك الكاثود بفتحة الأمان. يضاف المنحل بالكهرباء إلى الخلية نصف المجمعة. تم الانتهاء من التجميع مع تجعيد الغطاء العلوي.
يعتبر الرفض المبكر لأخطاء الخلية المحتملة إجراءً اقتصاديًا ويمنع المزيد من العمل على الخلايا السيئة. يتم إدخال البكرة في العلبة بحيث توفر العلبة ضغطًا ثابتًا لإبقاء مكونات العنصر قريبة من بعضها ، وبالتالي القضاء على أي فرصة للفراغات بينها. قد تقوم بعض الشركات المصنعة بإدخال مغزل لتثبيت مركز الملف.
ما لم يتم تنفيذ جميع العمليات في غرفة جافة أو صندوق جاف ، يجب إزالة الماء الممتص في المواد الفعالة بالحرارة والفراغ قبل عملية ملء المنحل بالكهرباء.
يتم إجراء ملء الفراغ الدقيق للإلكتروليت للتأكد من أن المنحل بالكهرباء يتخلل ويملأ تمامًا المسامية المتاحة في هياكل الفاصل والإلكترود. تقيس المضخات الدقيقة الحجم المحسوب للإلكتروليت اللازم لتشغيل الخلية بشكل جيد. تستخدم جميع الشركات المصنعة دائمًا LiPF 6 (مركب بلوري أبيض غير عضوي) مثل المنحل بالكهرباء والحلق (EC ، كربونات الإيثيلين) أو الكربونات الخطية (DMC ، كربونات ثنائي ميثيل ، DEC ، كربونات ثنائي إيثيل ، أو EMC ، كربونات إيثيل ميثيل ، إلخ). المذيبات لهذا الملح المنحل بالكهرباء.
تُستخدم الإلكتروليتات القائمة على مخاليط المذيبات من كربونات الإيثيلين (EC) مع كربونات ثنائي ميثيل (DMC) و / أو كربونات ثنائي إيثيل (DEC) بشكل شائع في بطاريات الليثيوم أيون مع كاثودات “4 فولت” (الكوبالت والنيكل والمنغنات) بسبب إمكانية أكسدة عالية للمذيبات.
بعد ملء الخلية بالكهرباء ، يتم إغلاق الخلية عن طريق الضغط المحكوم بحشية البوليمر أو الحلقة الموضوعة بين علبة الخلية والصفيحة العلوية. يتم التحكم في الضغط على مانع تسرب البوليمر لإبقائه ضمن الحد المرن للبوليمر. إذا تم تجاوز الحدود المرنة ، يتدفق البوليمر البارد ويؤثر على الختم.
يستخدم كل مصنع بنية ميكانيكية مختلفة إلى حد ما لإغلاق الخلايا ولكن النتائج النهائية متطابقة بشكل أساسي. عادة ، يتم تشكيل كتف أو حافة بالقرب من الجزء العلوي من الخلية. يعمل هذا كقاعدة لمانع التسرب ولإبقاء أداة الهلام في مكانها ومنع تصغير أو تغيير موضع بكرة الجرح تحت تأثير الاهتزاز والصدمة.
يتسبب أي تغيير في الموضع في حدوث تغيير في التوزيع الحالي وينتج عنه ضعف دورة الحياة أو طلاء الليثيوم في الخلايا عالية الأداء. يحتوي ختم اللوحة العلوية للخلية على فتحة تهوية وعنصر معامل درجة حرارة موجب (PTC) وأجهزة أمان للمقاطعة الحالية (CID). يعتبر كل من CID و PTC من أجهزة السلامة المصممة لتنشيط ومنع درجات الحرارة والضغوط الخطرة من التطور الداخلي للخلية. يتم فحص كل مجموعة من الأجهزة للتأكد من أنها تعمل بشكل صحيح قبل دمجها في التجميع العلوي.
بعد تطبيق الختم ، يمكن غسل الخلايا وتغليفها ووضع العلامات عليها. يتم إعطاؤهم رقمًا تسلسليًا لتتبع يوم التصنيع وتحديد جميع مكونات الخلية (مواد الإلكترود ، والإلكتروليت ، والفاصل وما شابه ذلك). يتم تخزين المعلومات الخاصة بالسعة والجهد مع رقم الخلية واستخدامها لاحقًا لمطابقة الخلايا لتجميع العبوات.
يمكن لحام الخلايا بالليزر باستخدام أختام زجاجية إلى معدنية لتوفير أختام محكمة الغلق تدوم طويلاً. مع الخلايا الأكبر حجمًا ، يجب توخي مزيد من العناية لضمان التشغيل الآمن ، حتى في ظل ظروف سوء المعاملة.
بينما يتم وصف العمليات المذكورة أعلاه للخلايا الصغيرة المختومة المستخدمة في الإلكترونيات المحمولة ، تتبع عملية البطاريات الصناعية الأكبر لتخزين الطاقة وتطبيقات الفضاء والمركبات الكهربائية نفس المخطط العام.
بطارية ليثيوم أيون - التكوين والشيخوخة
عند تجميعها ، لا يتم تخدير أيونات Li في كربون الأنود وبالتالي لا تظهر الخلية أي جهد. أثناء الشحن الأولي ، يتم فك جزء من أيونات Li من PAM LiCoO 2 ليصبح Li 1-x CoO 2 ويتم تخدير أيونات الليثيوم هذه في أنود الكربون (C y ) لتصبح Li x C y . عندما يصل جهد الشحن إلى 4.1 إلى 4.2 فولت ، تكون قيمة x حوالي 0.5. (أي 50٪) تشير إلى أنه تم استخدام 50٪ من Li من LiCoO 2 .
جانب آخر يجب ملاحظته هو أن جزءًا من أيونات الليثيوم المخدرة لا يعود ويبقى في الأنود. حيث تبقى أيونات الليثيوم x-dx دون المساهمة في السعة. وهو عبارة عن حوالي 10 إلى 20٪ من الليثيوم غير القابل للعكس ، مما يعني أن كفاءة الشحن الأولي تتراوح من 80 إلى 90٪. من الدورة الثانية ، لا تزيد الكمية التي لا رجوع فيها وتظهر الخلية السعة 100٪ المصممة من قبل الشركة المصنعة.
بعد الغسيل والغطاء ، ولكن قبل بدء عملية التكوين ، يتم تسجيل الجهد والمقاومة لجميع الخلايا لفرز أي خلايا معيبة. ثم يتم شحن الخلايا لأول مرة
(الشحن الأولي أو شحن التكوين). تعتبر شروط الشحنة الأولى مهمة لسببين على الأقل:
1) تتكون طبقة الطور البيني للإلكتروليت الصلب (SEI) على الأنود لحمايته من التفاعل تلقائيًا مع المنحل بالكهرباء أثناء التشغيل الطبيعي للخلية ، و 2) تنشئ اتصالًا كهربائيًا جيدًا بين المواد الفعالة والإلكتروليت. تتبع الشحنة الأولى الإجراء الموصى به من الشركة المصنعة لشحن الخلايا ، ولكنها غالبًا ما تبدأ بتيار أقل ثم تزداد إلى تيار الشحن العادي عند حوالي ثلث الطريق في فترة الشحن. قد تستمر الخلايا في الدوران ضمن حدود الجهد للشحن والتفريغ لدورة أو دورتين إضافيتين بعد التكوين.
بعد التكوين أو التدوير ، يتم قياس جهد الخلية وسعتها وتخزينها لاستخدامها لاحقًا في عملية اختيار الخلية . تتراوح فترة التقادم بين أسبوعين وشهر واحد حسب الشركة المصنعة. يتم قياس جهد الخلايا مرة أخرى بعد التخزين. يتم استخدام الفروق في الجهد في بداية ونهاية فترة التخزين لفرز الخلايا ذات السراويل القصيرة “الناعمة” أو “الدقيقة”. الخلايا ذات القصور الداخلي سيكون لها جهد أقل بعد التخزين وستفصل نفسها عن التوزيع الطبيعي للجهد والسعة. قد يكون من الضروري إخلاء الخلايا الأكبر بعد التكوين لإزالة غازات التكوين.
للحصول على وصف مفصل لعملية التجميع ، يشار إلى القراء
- كاورو ناكاجيما ويوشيو نيشي الفصل الخامس في: أنظمة تخزين الطاقة للإلكترونيات ، Ed Tetsuya Osaka و Madhav Datta ، Gordon and Reach Science Publishers ، أمستردام ، 2000.
- عمليات إنتاج خلايا ليثيوم أيون ، رالف ج. .
- بطاريات الليثيوم ، العلوم والتكنولوجيا ، أد. بقلم جي إيه نازري وج.بيستويا ، سبرينغر ، نيويورك ، 2009.
- بطاريات الليثيوم أيون ، رينر كورثاور (محرر) (2018) ، ترجمه مايكل ويست وآخرون ، سبرينغر ، 2018.
- Kazuo Tagawa و Ralph J. Brodd ، عمليات الإنتاج لتصنيع بطاريات الليثيوم أيون في بطاريات الليثيوم أيون ، يوشيو إم ، برود آر جيه ، كوزاوا إيه (محرران) سبرينغر ، نيويورك ، نيويورك. https: //doi.org/10.1007/978-0-387-34445-4_8]
- Zhang Z.، Ramadass P. (2012) أنظمة وتقنيات بطاريات الليثيوم أيون. في: Meyers RA (محرر) موسوعة علوم وتكنولوجيا الاستدامة. سبرينغر ، نيويورك. https: //doi.org/10.1007/978-1-4419-0851-3_663
- كتيب كيمياء تصميم حزمة بطارية ليثيوم أيون ، المكونات والأنواع والمصطلحات ، جون وارنر ، إلسفير ، 2018