리튬 이온 배터리의 작동 원리
대중의 인식은 납축전지가 오래된 기술이라는 것입니다. 리튬 이온 배터리는 다른 인식을 가지고 있습니다. 현대적이고 깨끗하며 에너지 밀도가 3-4배이고 수명이 더 깁니다. 이 모든 것을 통해 150년 된 납산 기술이 테이블에 가져올 수 있는 가능한 이점은 무엇입니까? 사실, 모든 것이 보이는 것과 같지 않습니다. 마케팅 주장에 사용된 데이터의 헤드라인 뒤를 살펴본 다음 약간의 상식, 기본 연구 및 일부 기초 과학을 적용하십시오. 실제 이야기는 다소 다르다는 것을 알게 될 것입니다.
첫 번째 오해는 체적 및 비에너지 밀도에 관한 것입니다. 4~5배의 헤드라인 값은 특정 에너지 밀도와 제한된 수의 리튬 이온 배터리 화학 물질에만 관련되며 그 중 일부는 아직 상업적으로 사용되지 않습니다. 무화과. 2는 가장 안전한 Li-FePO4 화학의 경우 약 100Wh/kg에서 니켈-코발트-알루미늄 산화물 변형의 경우 200Wh/kg 이상인 리튬 이온 배터리 셀의 여러 음극을 비교합니다. 납산 배터리 다이어그램은 다음과 같습니다.


이러한 값은 포장 상태 또는 사용 중 상태가 아닌 단일 셀 수준에만 적용됩니다. 무화과. 3은 전지 및 시스템 수준에서 다양한 배터리 화학 물질의 에너지 밀도를 보여줍니다. 리튬 이온 배터리 셀의 에너지 밀도는 모든 연결, 냉각, 안전 및 배터리 관리 장비와 함께 완전히 설치될 때 거의 절반으로 줄어듭니다.
비에너지 밀도의 3~5배인 셀 레벨 이점이 2~3배로 감소합니다. 리튬 음극 화학에 따라 우리는 일부 응용 분야에서 완전히 설치된 배터리 시스템에 대한 리튬 이온 배터리와 납축 배터리 간의 에너지 밀도를 거의 동등하게 볼 수 있습니다.
다른 요인인 주기 수명도 혼란의 원인입니다. 용량이 명판 정격의 80% 아래로 떨어지기 전에 리튬 이온 배터리는 몇 번의 사이클을 수행할 수 있습니까? 2,300? 표 1은 성능 및 사이클 수명에 대한 다양한 리튬 이온 캐소드 재료에 대한 요약을 제공합니다.
납축전지 화학의 장점
배터리는 이상한 장치입니다. 아무도 원하지 않지만 모두가 필요합니다. 필요할 때만 구입합니다. 얼마나 많은 사람들이 배터리를 구입하기 위해 동네 쇼핑몰에 방문할 계획입니까? 원한 구매이며 절대적으로 필요할 때만 구매합니다. 좋은 세일즈맨은 돈만 있다면 신발 두 켤레, 자동차 두 켤레, 집 두 켤레를 팔 수 있지만 SLI 자동차 배터리 두 개는 팔 수 없습니다. 태양 전지판용 태양열 배터리 , 전기 자전거 또는 UPS 및 인버터 배터리 백업 시스템 또는 지게차용 트랙션 배터리를 구입할 때 이에 대해 더 알고 싶지 않으십니까?
납축전지는 어떻게 작동하고 유형과 모델의 차이점은 무엇이며 다른 화학 물질은 어떻습니까? 그들은 비쌀 수 있습니다. 상업용 또는 가정용 애플리케이션에서 납축전지의 수명과 교체 비용은 얼마입니까? 필요한 크기, 사용 가능한 공간, 납축전지의 에너지 효율 및 충전 시간은? 그리고 안전, 폐기 및 탄소 발자국에 대한 숨겨진 비용이 있습니다. 이 기사에서는 납축전지와 리튬 이온 배터리 를 비교하고 이 두 가지 화학 작용과 관련된 많은 오해를 다룹니다.
어떤 리튬 이온 배터리가 가장 좋습니까?
| 음극재 | 짧은 이름 | 공칭 전압 | 비에너지 Wh/kg(셀) | 주기 수명 | 코멘트 |
|---|---|---|---|---|---|
|
리튬 코발트 산화물 (LiCoO2) |
LCO | 3.6 | 150-200 | 500-1000 | 휴대용 장치 - 과충전 시 열폭주 |
| 리튬 망간 산화물(LiMn2O4) | LMO | 3.7 | 100-150 | 300-700 | 전동공구, 의료기기 - LCO보다 안전 |
| 리튬 니켈 망간 코발트 산화물(LiNiMnCO2) | NMC | 3.6/3.7 | 150-220 | 1000-2000 | 전기 자전거, EV, 산업용 - 긴 수명 |
| 인산철리튬(LiFePO4) | LFP | 3.2 | 90-120 | 1000-2000 | EV, SLI, 레저 - 모든 리튬 이온 배터리 화학 물질 중에서 가장 안전합니다. |
| 리튬 니켈 코발트 알루미늄 산화물(LiNiCoAlO2) | NCA | 3.6 | 200-260 | 500 | 산업용, EV 파워트레인(Tesla) TR at 150C, CL 500 |
| 티탄산리튬(Li4Ti5O12) | LTO | 2.4 | 50-80 | UPS, Solar, EV 파워트레인(Honda, Mitsubishi). CL 3000-7000 - 매우 안전함 |
보시다시피, 모두 800에서 2000 주기 범위에 속합니다. 이에 비해 잘 설계된 납축전지는 DOD 80%까지 1600회 이상 주기를 쉽게 달성할 수 있습니다. 소유 비용을 고려할 때 이 모든 것이 어떻게 합산됩니까? 이것은 우리를 납산 배터리 가격인 다음 요점으로 이끕니다. 납산 배터리와 비교하여 리튬 이온 배터리의 가격은 얼마입니까? 리튬 이온 배터리 제조 공장 비용은? 당연히 리튬 이온 배터리는 더 비싸지 만 얼마나 더 비쌉니다. 다시 말하지만, 이는 고려 중인 수준에 따라 다릅니다. 보도 자료에 따르면 리튬 이온 가격이 하락하고 있으며 현재 납산 가격의 2-3배 범위에 있습니다.
진짜? 리튬 이온 배터리와 납축전지 모두에 대해 상업적으로 이용 가능한 12V 및 100Ah의 레저 배터리 가격을 알아보기 위한 최근 영국 인터넷 검색의 평균 가격:
리튬 이온 배터리 $960 또는 $800/kwh
납축전지 $215 또는 $180/kwh
분명히 리튬 이온 배터리의 수명은 동일한 값을 얻으려면 납 축전지 등가의 4 배이어야합니다. 우리가 본 것처럼 이것은 사실이 아닙니다.


모든 경우에 납산 배터리 구조는 더 큰 납산 배터리가 장착되어 더 나은 충전 수용력과 더 긴 주기 수명을 제공하는 경우에도 가장 비용 효율적이었습니다. 이 예에서 애플리케이션은 인도의 통신 타워였습니다. 대부분의 응용 프로그램과 지역에서 동일한 원칙이 적용되며 추운 기후에서는 더욱 그렇습니다. 또 다른 오해는 리튬 이온이 납산보다 청정 기술이고 오염이 적다는 것입니다. 다양한 배터리 화학 물질에 대한 크래들 투 게이트 방출이 그림 1 및 2에 나와 있습니다. 5와 6.
이 그림은 배터리 제조 작업의 경계를 보여줍니다. 원자재 추출 및 운송에서 모든 공정 단계를 거쳐 배터리가 배송될 준비가 되는 시점까지.
표 2는 리튬이온 배터리와 납축전지를 서로 다른 수명 기간 동안 사용할 때의 경제성을 비교한 실제 상황입니다.
| 비용 항목 | 일일 운영 비용 USD | 일일 운영 비용 USD |
|---|---|---|
| 3 년 | 납축전지 | 리튬 이온 배터리 |
| 상각 | 8.30 | 16.90 |
| 디젤(납품) | 15.50 | 15.50 |
| 유지 | 2.46 | 2.46 |
| 전기 | 1.47 | 1.47 |
| 배터리 충전 | 0.65 | 0.50 |
| 총 일/월 | 28.38/851 | 36.83/1105 |
| 6년 | ||
| 상각 | 5.86 | 8.46 |
| 디젤 | 15.50 | 15.50 |
| 유지 | 2.46 | 2.46 |
| 전기 | 1.47 | 1.47 |
| 배터리 충전 | 0.54 | 0.50 |
| 총 일/월 | 25.83/775 | 28.39/852 |
Argonne National Laboratories의 이 데이터는 리튬 이온 배터리의 원료 추출 및 운송을 포함한 전체 제조 공정이 납산가의 4배 이상임을 보여줍니다. 재료 추출과 관련하여 코발트, 망간 및 리튬과 같은 기본 양극 재료의 공급이 완전히 확실하지 않습니다. 추출 및 회수 공정이 존재하지만 광산 및 제조 현장의 수로 인해 수요가 크게 증가할 경우 공급이 제한될 수 있습니다. 지정학적 지도는 또한 이러한 자료의 일부 출처에 대한 불확실성을 예측합니다.
리튬 이온 배터리는 재활용 가능한가요?
이러한 화학 물질의 재활용 가능성과 안전성은 중요한 요소입니다. 납축전지의 거의 모든 구성요소는 100% 재활용되는 것으로 알려져 있지만 리튬 이온 배터리를 재활용하는 상업적 공정은 없습니다. 이 상황은 Li, Co, Mn 등의 더 비싼 구성 요소가 전체 리튬 이온 배터리의 작은 부분에 불과하다는 것을 고려할 때 이해할 수 있습니다. 예를 들어, 리튬은 전체 셀 무게의 약 4%입니다. 여기에 리튬이 높은 반응성(높은 에너지 밀도의 기초)이라는 명백한 사실을 추가하여 폐기물에서 추출하는 데 비용이 많이 듭니다.
구조에 다양한 재료가 포함된 복잡성의 추가 요소는 기술적으로나 경제적으로 재활용을 어렵게 만듭니다. 결과? 이러한 배터리를 재활용할 상업적 인센티브는 없습니다. 이러한 이유로 재활용 시설은 아직 시범 단계에 있으며 대부분 정부 자금이 지원됩니다.
현재 폐기된 리튬 이온 배터리의 대다수는 기술 혁신이나 재활용을 강제하는 법안을 기다리며 비축되어 있습니다. 후자가 구현된다면 궁극적으로 소비에 비용이 발생합니다. 이것은 납 축전지 유형에 비해 리튬 이온 전지의 가격을 더욱 높일 것입니다.
리튬 이온 배터리가 폭발할 수 있습니까?
마지막으로 안전이 있습니다. 휴대용 전자 장치 및 심지어 전기 자동차의 리튬 이온 배터리의 경우와 같이 우리가 아는 한 납축 배터리 애플리케이션은 안전 리콜을 받은 적이 없습니다. 무화과. 7은 이 기사를 작성하는 시점에서 불과 몇 주 전 영국의 새로운 하이브리드 볼보에 무슨 일이 일어났는지 보여줍니다. 이 경우 리튬 이온 배터리가 충전 중일 때 불이 붙었습니다.
리튬 이온 배터리 화재
그림 7 볼보 하이브리드 전기 자동차의 리튬 이온 배터리로 인한 화재: 2018년 4월-영국 거주


이 비디오는 리튬 배터리로 인한 매우 최근의 화재를 보여줍니다. 세포의 불균형과 부적절한 BMS 때문일 수 있습니다.
리튬 이온 배터리를 보관하거나 운송하는 경우에도 심각한 화재의 원인이 되었습니다. 이러한 경우는 드물지만 이를 인지하고 적절한 안전 장비와 배터리 관리 소프트웨어를 설치해야 합니다. 예를 들어 뉴욕 소방서는 여전히 리튬 이온 배터리 화재를 처리하는 방법을 결정하는 과정에 있습니다. 이는 전 세계적으로 리튬 이온 배터리에 대한 기존 안전 조치를 검토해야 함을 강력하게 시사합니다.
다음은 뉴욕 소방서의 견해입니다.
뉴스 기사 인용문: AWS 유틸리티 드라이브 2016년 11월 15일 Rogers는 “화재는 가장 큰 문제가 아닙니다.”라고 말했습니다. 소방관은 화재를 처리하도록 훈련을 받았지만 화재에 대처하는 방법을 알아야 합니다. 리튬 이온 배터리는 독성 산과 가연성 증기를 방출할 수 있습니다. 이러한 증기 중 일부는 화재에 의해 소모되지만 그렇지 않은 경우 점화되거나 소방관에게 문제가 될 수 있습니다. 가장 큰 문제는 ‘수술 후’, 즉 화재가 진압된 후 발생하는 일입니다. 배터리가 꺼지더라도 최대 72시간 동안 다시 점화될 수 있다고 Rogers는 말했습니다. – 중위 뉴욕 위험 물질 운영 부서의 Paul Rogers 소방서”
리튬 이온 배터리 또는 납산 배터리?
리튬 이온 배터리는 납산보다 성능 특성이 가장 확실합니다. 그러나 이러한 이점은 안전 및 관리 요구 사항과 관련된 추가 하드웨어로 인해 심각하게 감소합니다. 최종 결과는 납축전지가 특히 무게나 충전 수용에 의해 제한되지 않는 애플리케이션을 고려할 때 뚜렷한 이점이 있다는 것입니다. 납축전지 제조 공장 비용의 낮은 초기 비용; 낮은 환경 영향 및 고유한 안전성과 결합된 납산의 낮은 구매 가격 및 낮은 상각 비용은 다음과 같은 이점을 제공합니다.
- 낮은 구매 가격. 가격은 리튬 이온에 해당하는 가격의 약 4분의 1입니다. 운영 비용이 낮아 대부분의 애플리케이션에서 총 소유 비용이 절감됩니다.
- 재활용성. 모든 납축전지 재료의 거의 100%가 재활용됩니다. 스크랩 가치는 배터리 재료 비용의 최대 20%까지 추가 수익을 제공할 수 있습니다. 리튬 배터리에는 재활용을 위한 인프라나 상업적 프로세스가 없습니다.
- 안전. 납산의 화학적 성질은 본질적으로 리튬 이온 배터리의 화학적 성질보다 더 안전합니다.
- 지속 가능성. 특히 재활용 시설에서 납산을 공급할 수 있는 잘 확립된 공급원이 많이 있습니다. 리튬 및 기타 양극 재료는 정치적으로 민감한 지역에서 공급될 수 있습니다. 현재의 글로벌 재료 추출 및 제조 능력은 리튬 이온 배터리 생산의 급격한 증가를 뒷받침하지 못합니다.
- 탄소 발자국. 납산 배터리 제조는 리튬 이온 배터리의 1/3에 해당하는 탄소 발자국을 게이트로 연결하는 요람을 가지고 있습니다.
리튬 이온 배터리 회사에서 그린 그림과 다른 그림. 납산이 에너지 밀도 면에서 단점이 있다고 주장할 수는 없지만 사실 납산 배터리는 여전히 매우 안전하고 경쟁력이 있으며 많은 응용 분야에서 배터리 기술의 최선의 선택입니다.
리튬 이온 배터리 란 무엇입니까?
음극 및 양극 재료: 1990년대 초반에 니켈-수소화물(Ni-MH) 전지가 선호되었지만, 세계 최초의 상용 리튬 이온 이차 전지 제품은 1991년 Sony Corporation에서 출시되었습니다. 이 배터리는 질량 및 부피 측면에서 높은 에너지 함량 외에도 우수한 저온 특성, 부하 특성 및 사이클 특성을 제공했습니다. 그 결과, 빠르게 시장을 장악하고 오디오 및 비디오 장비, 개인용 컴퓨터, 휴대용 전화기 및 기타 휴대용 장비에 없어서는 안될 동력원이 되었습니다.
오늘날의 고급 배터리 기술은 포드 자동차 연구소의 Kummer와 동료들이 나트륨 β-알루미나라고 하는 고체상 NaAl 11 O 17 의 높은 이온 전도도를 발견하면서 시작되었습니다. [1. 노벨 화학상을 수상한 올로프 람스톰스트롬(Olof Ramsrtomström)은 2019년 노벨 화학상의 과학적 배경; 2. YFY Yao 및 JT Kummer, J. Inorg. 핵 화학 29, 2453 (1967)].
이것은 고체의 이온 수송이 실제로 매우 빠르며 다양한 새로운 기술로 이어질 수 있다는 깨달음으로 이어졌습니다. 그 후 얼마 지나지 않아 Ford의 연구원들은 음극에서 용융 나트륨을 사용하고 양극으로 황에 용해된 나트륨 용액을 사용하여 완전히 새로운 유형의 배터리를 생산하기 위해 고 전도성 고체 전해질을 사용할 수 있음을 보여주었습니다. 사이의 고체 전해질 [N. Weber 및 JT Kummer, Proc. 연간 전원 Conf. 21, 37(1967)].
예상할 수 있듯이, 유사한 리튬 시스템의 가능성에 대한 고려가 곧 이루어졌는데, 이는 그렇지 않으면 동등한 리튬 전지가 나트륨 전지보다 더 높은 전압을 생성해야 한다는 것을 인식했기 때문입니다. 또한 리튬은 나트륨보다 무게가 가볍다는 또 다른 장점이 있습니다.
원소 리튬은 녹는점이 낮아 사용할 수 없었습니다. 대신에 주로 Li/Si 및 Li/Al 시스템인 고체 리튬 합금이 조사되었습니다 [ RA Huggins, J. Power Sources 81–82, 13(1999)].
그 당시 FeS 또는 FeS 2 의 사용에 가장 많은 관심을 두면서 많은 물질이 양극 반응물로 조사되었습니다. 리튬과 반응하면 이러한 물질은 재구성 반응 을 일으키며 초기 단계가 사라지고 새로운 단계가 형성됩니다 .DR Vissers, Z. Tomczuk 및 RK Steunenberg, J. Electrochem. 사회 121, 665 (1974)].
리튬 이온 배터리는 언제 발명되었습니까?
Whittingham 교수 는 이러한 물질의 전기화학적 층간삽입을 연구하여 1973년 배터리의 전극과 같은 물질을 제안했습니다. 이 작업으로 1976년 에 작동하는 충전식 배터리가 탄생했습니다. 성공적인 전지는 리튬 금속을 양극으로 , 황화티타늄(TiS 2 )을 음극으로 사용하고, 리튬 헥사플루오로포스페이트( LiPF 6 )를 용매로 프로필렌 카보네이트(PC)의 전해질로 사용했습니다. 이러한 유망한 연구는 Whittingham 이 배터리의 전극과 같은 재료에서 전기화학적 삽입을 탐구하도록 영감을 주었습니다. 작동하는 충전식 배터리는 1976년에 연속적으로 시연되었습니다.
[(a)Whittingham, 전이 금속 이황화물의 MS Electrointercalation. J. Chem. Soc., Chem. 통신. 1974, 328–329.] (Exxon Research and Engineering Company와 함께).
(b)Whittingham, MS Batterie à Base de Chalcogénures. 벨기에 특허 번호 819672, 1975.
(c)Whittingham, MS 전기 에너지 저장 및 삽입 화학. 과학 1976, 192(4244), 1126–1127.
그러나 성공도 잠시. 반복되는 사이클링에서 금속성 리튬은 사이클링 시 금속 표면에 덴드라이트를 형성하여 단락을 초래했습니다.
이 문제는 대체 솔루션에 대한 새로운 검색에 자극을 주었고 두 전극이 이온을 수용할 수 있는 “이온 전달 셀” 구성(“흔들 의자”라고도 함) 셀이 제안되었습니다.
양극 물질이 처음에 리튬을 포함하고 첫 번째 충전 중에 리튬의 일부 또는 전부가 제거되면 전지는 전위를 발생시킵니다. 따라서 이미 리튬이 함유되어 있으면 약 3V 이상의 전위에서 리튬과 반응하는 양극 물질을 가질 수 있으며 이 리튬을 전기 화학적으로 추출할 수 있습니다.
누가 리튬 이온 배터리를 발명했습니까?
리튬이 이미 존재하는 재료를 사용하는 이 접근 방식은 Goodenough 교수가 처음으로 시연했습니다. 처음에 리튬을 함유하고 그로부터 전기화학적으로 리튬을 제거하는 물질의 첫 번째 예는 1980년 Li1-xCoO2에 대한 작업이었습니다.
[케이. Mizushima, PC Jones, PJ Wiseman 및 JB Goodenough, Mater. 해상도 황소. 15, 783(1980)] 및 Li1-xNiO2
[JB Goodenough, K. Mizushima 및 T. Takada, Jpn. J. Appl. 물리. 19(부록 19-3), 305(1980)]
양극 개발과 병행하여 금속 리튬보다 더 높은 전위의 양극과 함께 더 높은 전지 기전력을 얻기 위해 더 나은 음극 재료도 모색되었습니다. 돌파구는 1979/1980년에 옥스포드에서 John B. Goodenough와 그의 동료들이
영국 대학은 MX2 유형의 또 다른 삽입 금속 칼코겐화물인 LixCoO2가 음극 물질로 작용할 수 있음을 발견했습니다.
[굿이너프, JB; Mizushima, K. 고속 이온 전도체. 미국 특허 번호 4,357,215, 1982].
[미즈시마, K.; 존스, PC; 와이즈먼, PJ; Goodenough, JB LixCoO2(0<x<-1): 새로운
고에너지 밀도 배터리용 음극재. 메이터. 해상도 황소. 1980, 15(6), 783–789].
재료의 구조는 Li와 유사합니다.x TiS2 이산화코발트(CoO2 ) 많은 격자 팽창 없이 리튬 이온이 결합될 수 있는 층. Goodenough 는 MX에서 X가2 는 작은 전기음성 요소이며, 결과적인 양이온 흡수 과정은 큰 음의 자유 에너지 변화 및 높은 셀 전압(ΔG = -nFE)과 연관됩니다. X 산소의 경우 리튬 이온이 밀집된 산소 어레이에서 충분히 이동할 수 있다고 제안되었다는 점을 감안할 때 상황이 특히 유망한 것으로 간주되었습니다.
추론이 정확하다는 것이 증명되었고 CoO2 물질은 Li+/Li에 비해 ~4~5V의 매우 높은 전위를 보였다. 이 경우 프로필렌 카보네이트에 리튬 테트라플루오로보레이트(LiBF4)로 구성된 전해질을 사용하여 전기화학적 연구를 수행했습니다.
이 발견으로 리튬 금속보다 전위가 높은 양극 재료를 사용할 수 있게 되어 적합한 탄소질 재료에 대한 연구가 더욱 활발해졌습니다. 흑연의 전기화학적 층간삽입 문제를 해결하는 어려움을 고려하여 대신 다른 옵션을 조사했습니다.
리튬 이온 배터리는 어디에서 발명되었습니까?
1985년 Akira Yoshino (Asahi Kasei Corporation의)가 이끄는 일본 그룹이 증기상 성장 탄소 섬유(VGCF)와 나중에 열처리된 석유 코크스 를 발견했을 때 돌파구가 생겼습니다. 후자의 물질은 결정질(흑연) 및 비결정질 도메인의 혼합물을 포함하는 것으로 알려져 있으며, 연구원들은 특정 정도의 결정화도를 갖는 특히 안정적이면서도 고성능의 품질을 식별할 수 있었습니다.
[아키라 요시노, 리튬 이온 배터리의 탄생, Angewandte Essays, Angew., Chem. 국제 Ed., 2012 , 51, 5798-5800]
이러한 효과적인 양극 재료를 사용하여 Yoshino는 이온 전달 셀 구성을 기반으로 하는 효율적이고 작동하는 리튬 이온 배터리를 개발했습니다. 따라서 확인된 탄소질 물질은 양극으로 사용되었으며 Goodenough의 LixCoO2 물질(일반적으로 소량의 주석을 함유함)이 음극으로 사용되었습니다. 폴리에틸렌 또는 폴리프로필렌으로 구성된 분리막 층을 사용하였고, 전해질은 프로필렌 카보네이트(PC)에 과염소산리튬(LiClO4)으로 구성하였다.
Yoshino는 또한 1986년 배터리에 무게를 실어 이 배터리의 안전성을 입증했습니다. 리튬 금속 음극을 사용하는 배터리는 격렬하게 반응하는 반면 화재나 폭발은 발생하지 않았습니다.

그림 8. 1986년 요시노가 리튬이온 배터리를 사용한 첫 번째 안전 테스트.
A) 철 덩어리가 배터리와 충돌하는 순간
B) 충돌 후 프로토타입 리튬 이온 배터리
C) 충돌 후 금속 리튬 양극 배터리
[제공: Akira Yoshino, 리튬 이온 배터리의 탄생, Angewandte Essays, Angew., Chem. 국제 Ed., 2012, 51, 5798-5800 ]
이러한 발견과 개발은 궁극적으로 상업용 리튬 배터리의 출시로 이어졌습니다.
1991년. 추가 개발로 리튬 이온 배터리는 1991년 Sony와 1992년 Asahi Kasei와 Toshiba의 합작 투자로 상용화되었습니다.
[Nishi, Y., 리튬 이온 이차 전지의 개발. 화학 기록 2001, 1, 406–413]
이 배터리는 석유 코크스 기반의 양극 물질인 LixCoO2를 음극으로 사용하고 리튬 헥사플루오로포스페이트(LiPF6)와 프로필렌 카보네이트(PC)로 구성된 무수 전해질을 기반으로 했습니다. 충전 전압은 ~80Wh/kg의 기록된 비에너지와 ~200Wh/리터의 에너지 밀도로 높았습니다(최대 4.1V).
당시 시장에 나와 있던 다른 배터리와 비교할 때 리튬 배터리는 빠르게 경쟁력을 갖추었고 본질적으로 다가오는 모바일 혁명의 기반을 마련했습니다.
거의 동시에 흑연이 실제로 적절한 전해질 조성과 함께 사용될 수 있다는 것이 발견되었습니다. [Fong R, Sacken U von, Dahn JR, 비수성 전기화학 전지를 사용한 탄소로의 리튬 삽입 연구. J. Electrochem. 사회 1990, 137(7), 2009–2013]
높은 융점으로 인해 지금까지 일반적으로 무시되었던 에틸렌 카보네이트를 포함하는 용매를 사용하여 충방전 사이클 동안 흑연 전극 표면에 고체 전해질 계면(SEI)이 형성되어 탄소 재료가 박리 및 추가 분해로부터 보호 . [Peled, E. 비수 배터리 시스템에서 알칼리 및 알칼리 토금속의 전기화학적 거동, 고체 전해질 간상 모델. J. Electrochem. 사회 1979, 126(12), 2047–2051.
이 발견은 배터리 커뮤니티에서 빠르게 채택되었으며 음극 재료로 흑연을 기반으로 하는 차세대 리튬 이온 배터리가 개발되었습니다. 이 양극 물질을 사용하여 충전 전압이 4.2V인 배터리가 곧 생산되어 에너지 밀도가 ~400Wh/리터가 되었습니다.
리튬 이온 배터리의 개발은 이러한 중요한 발견으로 그치지 않았지만 그 이후로 많은 개선과 대안이 보고되었습니다. 예를 들어, 특정 배터리 응용 분야에서 사용하기 위해 새로운 양극 재료가 지속적으로 확인되었으며, 이러한 두 가지 재료는 Goodenough 그룹에서 시작되었습니다. 스피넬 재료 Li1-xMn2O4와 감람석 재료 LixFePO4(LFP)입니다.
[파디, AK; 난준다스와미, 캔사스; Goodenough, 충전식 리튬 배터리용 양극 재료로서의 JB 인광 감람석. J. Electrochem. 사회 1997, 144, 1188-1194.
Thackeray, MM; 데이비드, WIF; 브루스, PG; Goodenough, 망간 스피넬에 JB 리튬 삽입. 메이터. 해상도 황소. 1983, 18, 461-472].
후자의 물질은 LixCoO2보다 Li+/Li에 비해 다소 낮은 전위에 의해 제한되지만 높은 안정성을 가지며 높은 충전율에서 사용할 수 있습니다. 여러 다른 전극 재료 및 전해질 시스템도 발견되어 사회의 이익을 위해 에너지 저장 재료를 계속 개선했습니다.
전기차에는 어떤 배터리가 사용되나요?
현재 대부분의 전기차는 리튬이온 배터리를 사용합니다. 이전에는 Ni-MH와 납산 배터리가 사용되었지만 비에너지와 에너지 밀도 값이 높은 리튬 이온 배터리의 등장으로 사용량이 점차 줄어들었습니다. 납축전지의 비에너지는 약 40-50Wh/kg인 반면 리튬이온 배터리는 약 150Wh/kg입니다. 납산 배터리의 에너지 밀도 값은 80-100Wh/리터인 반면 리튬 이온 배터리는 250Wh/리터 이상입니다.
최신 Tesla 배터리 팩(2019-2020)에 사용되는 것과 같이 니켈-코발트-알루미늄(NCA) 음극 및 실리콘/흑연 복합 양극이 있는 원통형 전지는 약 270Wh/kg 및 650Wh/리터에 도달했습니다. Sion Power의 Licerion이라는 새로운 기술은 500Wh/kg의 비에너지와 1000Wh/L의 에너지 밀도 및> 0.4 Ah 현상 셀에서 450 사이클.
소형 배터리의 경우 Wh로 말합니다. 고용량 시스템의 경우 kWh 단위가 사용됩니다. Wh 값을 103으로 나누면 kWh가 됩니다.
따라서 850Wh = 850/1000 = 0.850kWh입니다.
오늘날 EV 배터리 에 사용되는 셀은 140-170Wh/kg의 공칭 비에너지에 도달할 수 있습니다. 생성된 배터리 팩의 비에너지는 일반적으로 30~40% 더 낮거나 80 -120Wh/kg입니다. 감소는 여러 직렬 및 병렬 연결 리드, BMS 및 열 관리 시스템(냉각 또는 가열) 때문입니다. 2019년에는 비셀 구성 요소의 팩 비율이 약 28%로 떨어졌습니다.
지금까지는 세포를 먼저 모듈에 넣은 다음 팩에 넣었습니다. 둘 다 컨템포러리 Amperex Technology Co. 제한적, 중국 ( CATL) 과 Tesla는 모듈을 제거하고 셀을 팩에 직접 배치하기로 결정했습니다. CATL은 이미 그렇게 했으며 이를 cell-to-pack 기술 이라고 부릅니다. 이에 대한 정보는 부족하지만 회사는 이것이 비에너지를 10~15% 증가시키고 부피 활용도를 15~20% 향상시킬 수 있다고 주장합니다. 전체적으로 배터리 팩에 필요한 부품을 40% 줄일 수 있다고 합니다. [https://cleantechnica.com/2020/02/18/how-catl-lithium-iron-phosphate-batteries-could-be-leading-to-100-kwh-tesla-model-3/]
리튬 배터리 지정
IEC(International Electrotechnical Commission)와 인도 표준 기관(Indian Standards Institution)은 리튬 이온 전지의 화학적 성질과 크기를 설명하는 공통 명칭을 설정했습니다.
[ 휴대용 애플리케이션을 위한 이차 리튬 전지 및 배터리, 국제 전기 기술 위원회, IEC 61960-1 및 IEC 61960-2 및 IS 16047: 2012 ].
문자는 화학 및 폼 팩터를 지정하고 숫자는 셀의 물리적 치수를 지정합니다. 첫 번째 문자는 일반 화학을 설명하고 두 번째 문자는 특정 음극 화학을 지정하며 세 번째 문자는 모양을 지정합니다.
첫 글자: I – 리튬 이온 화학
두 번째 문자: C-코발트, F-철, Fp – 인산철, N-니켈, M-망간, Mp-인산망간, T-티타늄, V-바나듐 및 x-기타.
세 번째 문자: R-원통, P-기둥
뒤에 오는 처음 두 숫자는 mm 단위의 직경을 지정하고 마지막 세 숫자는 mm의 1/10 단위로 높이를 지정합니다. 따라서 ICR19/66으로 지정된 전지는 다음과 같은 직경을 갖는 코발트 음극이 있는 리튬 이온 전지입니다.> 18mm 및 ≤ 19mm 및 최대 전체 높이는> 65mm 및 ≤ 66mm.
각형 셀의 경우 첫 글자는 같은 의미를 갖지만 처음 두 숫자는 너비(mm)를 나타내고 다음 두 숫자는 높이(mm), 마지막 두 숫자는 길이(mm)를 나타냅니다. 따라서 셀 명칭 IMP9/35/150은 최대 두께가 > 8mm 및 ≤ 9mm 및 최대 너비 > 34mm 및 ≤ 35mm 및 최대 전체 높이는 > 149mm 및 ≤ 150mm.
리튬 이온 배터리는 어떻게 작동합니까?
리튬 이온 배터리는 어떻게 만들어지는가
원자 번호 3, 밀도 0.534g/cc, 표준 환원 전위(Li + /Li 커플 -3.05V vs. SHE)가 매우 낮고 이론 비용량이 3860Ah/kg(2061mAh/cc)인 리튬 금속은 다음과 같습니다. 모든 금속 중 가장 가벼운 무게, 가장 높은 전압, 가장 큰 에너지 밀도. (원자 번호 82의 납, 밀도 11.29g/cc, 이론 비용량 257.8Ah/kg, 표준 환원 전위 -0.35V vs. SHE와 비교).
리튬이온전지 - 활물질
양극의 활물질은 LiCoO2, LiMnO2, LiFePO4와 같은 혼합 산화물 중 어느 하나이다. 음극은 주로 흑연과 비정질 탄소 화합물입니다. 유기 전해질(LIPF6과 같은 해리된 리튬 전도성 염을 포함)이 사용됩니다. 폴리프로필렌(PP) 또는 폴리에틸렌(PE) 또는 혼합 분리막이 사용됩니다. 리튬 이온은 충전 및 방전 중에 리튬 이온 배터리의 전극 사이를 앞뒤로 이동하며 다음과 같이 활물질에 삽입됩니다.

그림 9. 리튬 이온 전지의 분해도
출처: Zhang Z., Ramadass P. (2012) 리튬 이온 배터리 시스템 및 기술. In: Meyers RA (eds) 지속 가능성 과학 및 기술 백과사전. Springer, New York, NY, pp 6124. http s://doi.org/10.1007/978-1-4419-0851-3_663
리튬 이온 배터리 충전 방법
리튬 이온 전지(LIB)의 방전 과정 에서 애노드의 리튬 이온은 전해질로 디인터칼레이션(또는 추출)되고 전해질 의 이러한 리튬 이온은 캐소드 재료로 인터칼레이션됩니다 . 양극에서 음극으로 이온의 이동은 외부 회로에서 흐르는 전자의 방출을 동반합니다. 역 과정은 리튬 이온이 음극에서 이동하고 전해질을 통해 양극에 삽입되는 충전 과정 에서 발생합니다. 상업용 LIB는 일반적으로 알루미늄 집전체 위에 코팅된 LiCoO 2 , LiMn 2 O 4 및 LiFePO 4 와 같은 전이 금속 산화물을 음극 물질로 사용합니다.
10~20%의 전도성 탄소와 5~ %–10% %의 폴리비닐리덴 디플루오라이드(PVDF) 및 폴리테트라플루오로에틸렌(PTFE)과 같은 고분자 바인더도 활물질과 함께 추가되어 각각 전자 전도성을 향상시키고 전극 재료의 더 나은 접착력을 달성합니다. 양극 물질은 필요한 경우 전도성 탄소와 PVDF가 있는 구리 집전체 위에 코팅됩니다.
두 전극은 전해질 용액(유기 용매에 용해된 LiPF6)에 적신 다공성 분리기(폴리에틸렌 또는 두께 10-20μm의 폴리프로필렌 필름)로 분리됩니다. 분리막과 전해액 모두 이온 전도성이 더 좋아야 합니다. 전지는 일반적으로 두 전극 사이에 전해질이 담긴 분리막이 있는 젤리롤 방식의 금속 케이스로 제작됩니다. LIB의 개략도가 그림에 나와 있으며 일반적인 충전 및 방전 프로세스가 표시됩니다.
리튬 이온(Li-ion) 이차 전지는 방전 및 충전 시 리튬 삽입 화합물이라고 하는 호스트 매트릭스(양극 및 음극 활물질)로 또는 그로부터 리튬 이온(Li + )(게스트 종)의 가역적 삽입/추출을 사용합니다. 프로세스가 발생합니다. 리튬 이온 배터리는 전지가 충전 및 방전될 때 양극과 음극 사이에서 리튬 이온이 앞뒤로 “흔들기” 때문에 흔들의자 배터리라고 불립니다.
양극 활물질 은 일반적으로 리튬 코발트 산화물 (LiCoO 2 )과 같은 층상 구조의 금속 산화물 또는 리튬 망간 산화물(LiMn 2 O 4 ) 과 같은 터널 구조를 갖는 물질이 대부분 알루미늄 집전체 상에 존재한다. . 음극 활물질 은 일반적으로 흑연 탄소 이며 대부분 구리 집전체에 적층된 물질입니다. 충방전 과정에서 활물질의 원자층 사이의 틈새 공간에서 리튬 이온이 삽입되거나 추출됩니다.
리튬 전지에는 비수전해질 또는 유기전해질이 사용된다.
리튬 이온 배터리의 분리막은 폴리올레핀 미세다공성 필름 폴리에틸렌(PE)과 폴리프로필렌(PP)입니다.
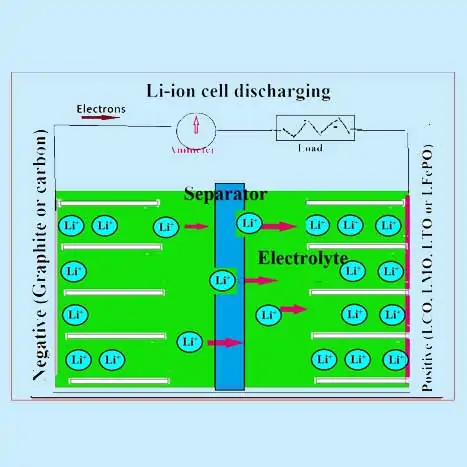

리튬 이온 배터리의 전기화학 전지 반응
일반적인 리튬 이온 전지에서는 다음과 같은 일반적인 반응이 발생합니다.
양극 반응:
LiMO 2 ⇔ Li 1-x MO 2 + x Li + + xe –
음극 반응:
C + y Li + + ye – ⇔ Li y C
총 세포 반응:
LiMO 2 + x/y C ⇔ x/y Li y C + Li 1-x MO 2
M = Co, Mn, Ni, Ti 등과 같은 금속
일반적으로 x는 약 0.5이고 y는 약 0.16이므로 x/y는 약 3입니다.. [Jeff Dahn 및 Grant M. Ehrlich. “리튬 이온 배터리”, Linden의 배터리 핸드북, 4판, Thomas B. Reddy (Ed.), McGraw
전해질 및 고체 전해질 계면(SEI)
앞서 언급한 바와 같이 리튬 전지에는 비수성 전해질이나 유기 전해질이 사용된다. 리튬 전지는 비교적 높은 전압(셀당 최대 4.2V)에서 작동합니다. 육불화인산리튬(LiPF6), 육불화비산리튬(LiAsF6), 사불화붕산리튬(LiBF4), 과염소산리튬(LiClO4), 삼불화메탄설포산리튬(LiCF3SO3), 이불화붕산리튬(LIODFB) 등과 같은 부피가 큰 리튬염 는 실제 전해질(유지 전해질 염)이므로 이러한 더 높은 전압에서 안정한 적절한 용매가 필요합니다. 이러한 용매의 대부분은 유전 상수가 높기 때문에 이온 해리가 용이하고 고농축 리튬 이온이 존재합니다. 이러한 용매는 또한 Li 이온의 안정적인 존재를 위한 용매화 피복의 역할을 하여 반대 음이온의 영향을 감소시킵니다.
높은 유전 상수를 갖는 단점은 점도 값이 높아 이온의 이동성이 손상 된다는 것입니다. 낮은 이온 전도도를 극복하기 위해 저점도 용매는 일반적으로 고점도 용매 와 혼합됩니다. 그러나, 저점도 용매는 이온 해리가 더 낮기 때문에 혼합물이 양호한 이온 전도도와 양호한 이동성을 모두 갖도록 최적의 혼합 비율을 맞추는 것이 필수적이 됩니다. 비수성 용매로서 에틸렌 카보네이트(EC)와 디메틸 카보네이트(DMC), 디에틸 카보네이트(DEC) 및 에틸 메틸 카보네이트(EMC)와 같은 덜 점성인 선형 알킬 카보네이트의 혼합물이 상업적으로 이용 가능한 LIB에 사용됩니다.
비양성자성 용매는 에테르, 에스테르 및 알킬 카보네이트입니다. 디에틸 에테르(DEE), 테트라히드로푸란(THF), 디옥솔란, 에틸렌 카보네이트(EC), 프로필렌 카보네이트(PC), 디메틸 카보네이트(DMC), 디에틸 카보네이트(DEC), 에틸 메틸 카보네이트(EMC), 메틸 포메이트, γ-부티로락톤(BL), 메틸 아세테이트, 아세토니트릴(AN), 디메틸 설폭사이드(DMSO), 디메틸포름아미드(DMF), 메틸 클로라이드, 니트로메탄 등)
액체 전해질은 하나 이상의 유기 용매, 일반적으로 탄산염에 리튬 염의 용액입니다.
프로필렌 카보네이트(PC)는 흑연을 양극으로 사용하는 경우 전해액으로 사용할 수 없습니다. 흑연 표면에서 분해되기 때문입니다. EC 또는 LiBOB) Li bisoxalato borate)의 소량 첨가 없이 단독으로 사용되는 PC는 리튬과 함께 삽입되어 박리를 초래하는 흑연 전극의 열화를 유발할 수 있습니다.
전해질은 불변(동일한 수의 이온이 충전 중에 전해질을 떠나고
해고하다). 전해질 염은 일반적으로 유기 탄산염 용매에 용해됩니다. 각 제조업체는 에틸렌 카보네이트(EC)가 대부분의 공통 분모인 용매의 다른 조합을 가지고 있습니다.
SEI(Solid-electrolyte interphase) 층 형성은 전해질이 수행하는 또 다른 중요한 기능입니다. 알칼리 금속을 전지 전해액에 담그거나 전해액에 담근 탄소나 불활성 전극에 음전위를 인가하면 SEI가 형성되기 시작한다.
금속과 용액이 접촉하는 순간 순간적으로 형성된 SEI 층은 전해질 성분의 불용성 및 부분 용해성 환원 생성물로 구성됩니다. SEI는 배터리의 안전성, 전력 용량, 리튬 침전물의 형태, 저장 수명 및 사이클 수명을 결정하는 핵심 요소입니다. 양극에 대한 우수한 접착력도 중요합니다.
위에서 강조한 바와 같이, 실제적인 1차 또는 2차 알칼리 또는 알칼리토류 전지는 음극의 용해 또는 부식을 멈출 수 있어야만 건설될 수 있습니다. 따라서 전해질은 리튬(또는 알칼리 금속 양극)과 빠르게 반응하여 불용성 고체-전해질 계면을 형성하는 하나 이상의 SEI 전구체를 포함하도록 설계되어야 합니다. 염 음이온의 환원 생성물은 일반적으로 전극 표면에 침전되는 LiF, LiCl 및 Li 2 O와 같은 무기 화합물입니다. 용매가 감소하면 Li 2 CO 3 와 같은 불용성 SEI 성분과 부분적으로 용해되는 반 탄산염 및 중합체가 형성됩니다.
탄소 전극의 경우 SEI가 형성되는 전압은 탄소의 종류, 표면의 촉매적 특성(회분 함량, 결정면의 종류, 기저면 대 모서리면 비율), 온도, 용매, 염 및 불순물의 농도 및 유형, 전류 밀도. 리튬 이온 배터리의 첫 번째 충전에는 SEI 형성에 주로 필요한 “가역적 용량 손실”(Q IR )이라는 용량 손실이 있습니다.
SEI의 형성에 더하여, Q IR 은 가용성 환원 생성물(Q SP )의 형성과 관련된 용량 손실에 의해 야기될 수 있다.
오염 없는 SEI는 배터리의 긴 수명을 위해 필수적입니다. 이는 높은 속도와 더 깊은 방전 깊이로 사이클링하는 동안 더욱 중요해집니다.
육불화인산리튬(LiPF6) 및 육불화비산리튬(LiAsF6) 용액의 SEI는 다른 염의 용액에 비해 저항이 더 높습니다. 이것은 LiPF6 및 LiAsF6 전해질에서 리튬 양극의 높은 계면 임피던스로 이어지는 종 제어 저항에 기여하는 저항 변화로 인한 것입니다. 또한 Li2CO3는 리튬 순환 효율 향상을 위한 최고의 부동태화제 중 하나로 알려져 있다[J Electrochem Soc., 164(7) A1703-A1719(2017)].
리튬 이온 배터리용 분리기
리튬 이온 배터리용 분리막은 폴리올레핀 미세다공성 필름이며 일반적으로 일축 연신 폴리에틸렌(PE) 및 폴리프로필렌(PP), 이축 연신 PE 또는 다축 연신 PP/PE/PP입니다.
리튬이온전지의 활물질 원료
리튬 이온 배터리는 다양한 양극 재료를 사용합니다. 양극은 티타늄-니오븀 산화물 양극, Li-Si 합금 등과 같은 몇 가지를 제외하고는 변함없이 탄소 기반입니다. 다음 표와 그림은 이러한 배터리에 사용되는 다양한 화학 물질에 대한 몇 가지 아이디어를 제공합니다.

그림 12. 리튬 이온 배터리의 현재 및 미래 전극 화학 옵션에 대한 요약입니다. Li(Si)의 제안된 용량은 일부 양극 재료에서 발견된 경우와 유사하게 재료의 이론 용량의 50%입니다.
[제공: Yu Miao, Patrick Hynan, Annette von Jouanne 및 Alexandre Yokochi, Energies 2019, 12, 1074; doi:10.3390/ko12061074]
1 번 테이블.
양극재가 다른 리튬 이온 전지의 특성
| 음극재 | Li-Ni-Co-Al(NCA) | Li-Ni-Mn-Co(NMC) | Li-MnO2(LMO) | 리튬-인산철(LFP) | 리튬 티타네이트(LTO) | 리튬 코발트 산화물(LCO) |
|---|---|---|---|---|---|---|
| 셀의 공칭 전압(V) | 3.6 | 3.65 (2.7-4.2) | 3.8 | 3.25 (2-3.6) | 3.2 | 3.6 |
| 이론 비에너지(Wh/kg) | 279 | 256 | 148 | 128 (373) | 293 (175) | 274 (370) (x=0.5) |
| 음극의 비용량(Ah/Kg) 전위 대 Li/Li+(V) | 180-200 (3.8) | 200 | 148 (4.1) | 150-170 (3.45) | 175 | 274 (3.9) (x=0.5) |
| 음극의 비에너지(Wh/Kg) | 680-760 | 610-680 | 410-492 548 | 518-587 544 | -- | 546 |
| 안전 | 안전한 | 보통의 | 안전한 | 높은 | 매우 좋은 | 보통의 |
리튬 이온 배터리의 음극 재료
양극 물질은 양극 물질의 선택에 따라 달라지는 몇 가지 요구 사항을 충족해야 합니다.
- 고용량을 제공하기 위해 이러한 재료는 제조된 대로 다량의 리튬을 포함해야 합니다.
- 또한, 재료는 긴 주기 수명, 높은 암페어 시간 효율 및 높은 에너지 효율을 허용하기 위해 구조적 변화가 거의 없이 가역적으로 삽입되어야 합니다.
- 높은 전지 전압과 높은 에너지 밀도를 달성하려면 리튬에 비해 높은 전위에서 리튬 교환 반응이 일어나야 합니다.
- 고속 충전 및 방전 프로세스를 용이하게 하려면 재료의 전자 전도도와 리튬 이온 이동도가 높아야 합니다.
- 양극 물질은 전해질에 용해되지 않아야 하고 저렴한 비용으로 사용할 수 있어야 합니다. 비용을 최소화하기 위해 저렴한 공정에서 저렴한 재료로 준비하는 것이 바람직합니다.
LiFePO 4 는 이 규칙의 예외입니다. LiFePO 4 에서, 나노미터 입자 크기를 갖는 전극 입자를 사용함으로써 적절한 리튬 이온 수송이 달성된다. [Jeff Dahn 및 Grant M. Ehrlich. “리튬 이온 배터리”, Linden의 배터리 핸드북, 4판, Thomas B. Reddy (Ed.), McGraw Hill, pp. 26.6, 2011]
리튬 이온 전지의 양극 활물질(PAM)은 제조사에 따라 다릅니다. 음극재는 크게 3가지로 분류할 수 있다[ Arumugam Manthiram, Nature Communications (2020) 11:1550]. 그들은:
층상 산화물 - 리튬 이온 배터리의 양극 재료
일반적인 유형의 LiMO 2 의 여러 산화물(M = 바나듐, 크롬, 코발트 및 니켈)은 Li + 및 M 3+ 이온이 교대로 점유하는 층 구조로 결정화됩니다. O-Li-OMO.
층상 산화물 캐소드 LiCoO 2 에서 Li + 와 3가 Co 3+ 이온 사이의 큰 전하 및 크기 차이는 우수한 양이온 정렬을 유도하며, 이는 리튬 평면에서 빠른 2차원 리튬 이온 확산 및 전도도를 지원하는 데 중요합니다.
음극 물질은 극도로 높은 순도를 요구하며 원치 않는 금속 불순물, 특히 철, 바나듐 및 황이 거의 완전히 없어야 합니다.

그림 13. 대체 작업이 있는 계층 구조의 단순화된 개략도
밀집된 산화물 이온층 사이의 양이온층.
[제공: Robert A. Huggins, Advanced Batteries, Materials Science Aspects, Springer, New York, 2009, p.168]
높은 전기 및 리튬 이온 전도성과 함께 우수한 구조적 안정성은 우수한 가역성과 함께 빠른 충방전 특성을 제공합니다. 이러한 기능을 통해 LiCoO2는 ~4V의 높은 작동 전압으로 현재까지 최고의 음극 중 하나로 남아 있습니다.
1970년대에 추구된 황화물 음극과 관련된 두 가지 주요 과제. 그것은 작동 전압의 상당한 증가를 가능하게 했을 뿐만 아니라< 2.5V ~ 4V이지만 금속 리튬 양극을 사용할 필요 없이 전지 조립도 가능합니다.
스피넬 산화물 - 리튬 이온 배터리의 양극 재료
음극의 두 번째 부류는 스피넬 LiMn 2 O 4 입니다. (일반식은 AB 2 O 4 ). 이 구조는 일반적으로 입방 좌표로 표시되지만 (111) 평면에 평행한 산화물 이온 층이 있으며 산화물 이온 평면 사이에 팔면체 배위 사이트와 사면체 배위 사이트가 모두 있습니다. 팔면체 자리의 수는 산화물 이온의 수와 같지만 사면체 자리의 두 배입니다. 3차원 구조적 안정성과 높은 전기 및 리튬 이온 전도성은 LiCoO 2 에 비해 우수한 가역성과 함께 Li 1 – x Mn 2 O 4 에 대해 훨씬 더 빠른 충방전 특성을 제공합니다.
LiCoO 2 에서 LiMn 2 O 4 로 전환할 때의 중요한 이점은 망간이 Co보다 비용이 100배 낮기 때문에 비용이 크게 절감된다는 것입니다. 그러나 LiMn 2 O 4 의 한 가지 중요한 문제는 잘 알려진 Mn 3 불균형으로 인해 전해질에 미량(ppm 수준)의 H + 이온(산도)이 존재할 때 격자에서 전해질로 망간이 용해된다는 것입니다. + 산에서 Mn 4+ 및 Mn 2+ 로.

그림 14. 양이온이 4면체와 8면체 사이트 사이의 산화물 이온의 밀집된 (111) 평면 사이에 분포되어 있는 스피넬 구조의 개략도 [ Credit: Robert A. Huggins, Advanced Batteries, Materials Science Aspects, Springer, New York, 2009, p.17].
고전압 LNMO(Lithium-Nickel-Manganese Oxide) 양극재는 차세대 배터리에서 유망한 것으로 보인다. 그러나 걸림돌은 LNMO 기반 배터리의 스트레스를 처리할 수 있는 전해질이 부족하다는 것입니다. LNMO 음극 기반 배터리 셀은 다른 고성능 리튬 기반 배터리와 동등한 결과를 제공하지만 상당히 저렴한 비용으로 제공됩니다.
그러나 전해질 제조업체는 지속적인 연구 개발을 통해 매우 유망한 결과를 얻고 있습니다. https://blog.topsoe.com/the-cathode-material-for-next-generation-lithium-ion-batteries-is-ready
보다 최근에는 NMC 캐소드에서 Ni 함량을 늘리고 코발트 함량을 낮추거나 제거하는 것이 훨씬 더 두드러지고 있습니다 [ Li, W., Erickson., E. & Manthiram, A. High-nickel layered oxide 캐소드 for 리튬 기반 자동차 배터리 , Nat. 에너지 5, 26 – 24(2020)].
폴리음이온 산화물 - 리튬 이온 배터리의 양극 재료
세 번째 종류의 산화물은 다중음이온 산화물입니다. Fe 2 (MoO 4 ) 3 및 Fe 2 (WO 4 ) 3 와 같은 다중음이온 산화물은 Li 2 Fe 2 (MoO 4 ) 3 또는 Li 2 Fe 2 ( WO 4 ) 3 화학적 및 전기화학적 방법 모두
[Manthiram, A., Goodenough, JB Fe 2 (MO 4 ) 3 프레임워크로의 리튬 삽입: M = W와 M = Mo의 비교. J. 고체 상태 화학. 71, 349– 360(1987)].
Manthiram과 Goodenough의 작품을 바탕으로,
[Manthiram, A. & Goodenough, Fe 2 (MO 4 ) 3 프레임워크에 JB 리튬 삽입: M = W와 M = Mo의 비교. J. 고체 상태 화학. 71, 349–360(1987). Manthiram, A. & Goodenough, JB Fe 2 (SO 4 ) 3 프레임워크로의 리튬 삽입. J. Power Sources 26, 403–406(1989).]
리튬 함유 인산염을 음극으로 사용하여 감람석 LiFePO 4 를 음극으로 식별했습니다[Padhi, AK, Nanjundaswamy, KS & Goodenough, JB Phospho-Olivines as positive electrode materials for 재충전 가능한 리튬 배터리. J. Electrochem. 사회 144, 1188–1194 (1997] 1997.
그러나 폴리음이온 산화물 계열은 전자 전도성이 좋지 않습니다. [ 아루무감만티람, 네이처커뮤니케이션즈(2020) 11:1550].
리튬 함유 인산염을 음극으로 사용하여 감람석 LiFePO 4 를 음극으로 식별했습니다[Padhi, AK, Nanjundaswamy, KS & Goodenough, JB Phospho-Olivines as positive electrode materials for 재충전 가능한 리튬 배터리. J. Electrochem. 사회 144, 1188–1194 (1997] 1997.
그러나 폴리음이온 산화물 계열은 전자 전도성이 좋지 않습니다. [ 아루무감만티람, 네이처커뮤니케이션즈(2020) 11:1550].
양극재 제조 - 리튬이온전지
이전에 리튬 금속 산화물 캐소드 화합물은 탄산리튬과 선택한 금속의 염으로 용액에서 수행되는 일련의 화학적 대체 반응을 통해 만들어졌습니다. 원하는 생성물을 침전시키고 분무 건조시킨다.
LiCoO 2 는 먼저 그림에 표시된 기존 합성 방법으로 제조되었습니다 . 사산화삼코발트(Co 3 0 4 )와 탄산리튬(Li 2 CO 3 )을 잘 혼합한 후, 약 950ºC의 온도에서 기류에서 소성하였다. 그러나 이 방법으로 LiCoO 2 의 조대 입자를 제조하는 것은 매우 어렵고 직경이 1-3㎛인 미세한 입자만을 얻을 수 있었다.
미세 활성 전극 재료는 안전 관점에서 바람직하지 않습니다. 외부 단락이나 파쇄 등의 남용의 경우 비표면적이 큰 미세입자가 한번에 반응하기 쉽고 온도 상승을 동반하여 매우 짧은 시간 내에 모든 세포 에너지가 갑자기 방출된다. 최악의 경우 셀에 불이 붙을 수 있습니다 [Yoshio Nishi, in Lithium ion Batteries, M. Wakihara and 0. Yamamoto (Eds.). 192-193페이지].
리튬 이온 배터리는 어떻게 제조됩니까? 순서도
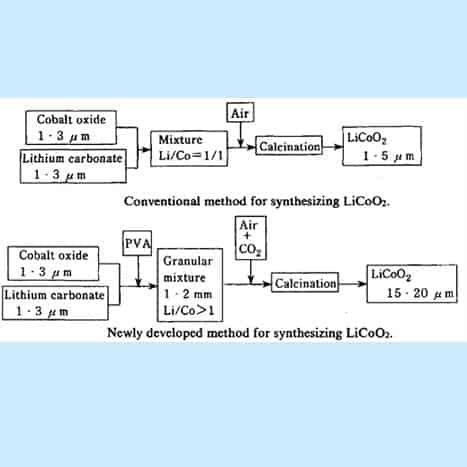
그림 15. Li-CoO 2 를 만들기 위한 순서도
[제공: Yoshio Nishi, 리튬 이온 배터리, M. Wakihara 및 0. Yamamoto(Eds.). 192-193페이지].
더 큰 입자 크기의 리튬 코발타이트 합성을 위한 개선된 공정: 첫 번째 요점은 소량의 PVA 수지를 원료(Co 3 0 4 및 Li 2 CO 3 )의 혼합물에 첨가하여 과립기를 사용하여 과립상 펠렛을 형성한다는 것입니다. . 적절한 양의 CO 2 가스를 포함하는 기류에서 펠릿을 소결함으로써 평균 직경이 20㎛인 리튬 코발타이트 입자가 합성된다. 두 번째 요점은 원료에 탄산리튬(Li 2 CO 3 )을 약간 과도하게 사용하기 때문에 원료의 Li/Co 원자비가 1보다 크다는 점이다. 이 절차는 조대 입자를 얻는 데에도 유리하며, 또한 생성된 LiCoO 2 에는 잔류 Li 2 CO 3 가 소량 포함됩니다.
첫 번째 요점은 ‘원료(Co304와 Li 2 CO 3 )’의 혼합물에 소량의 PVA 수지를 첨가하여 과립기로 과립형 펠렛을 형성한다는 점이다. 리튬 코발트 산화물을 소결함으로써 탄산리튬 Li 2 CO 3 와 코발트 산화물, Co 3 O 4 또는 금속 코발트의 화학량론적 혼합물을 600-800°C에서 고온 소성한 다음 제품을 어닐링하여 쉽게 제조할 수 있습니다. 900°C에서 여러 시간 동안 모두 산소 분위기에서.
또한 수산화 산화물을 수산화리튬으로 750-900°C까지 소성하여 얻을 수도 있습니다.
세 번째 방법은 수용액에서 리튬 아세테이트, 코발트 아세테이트 및 시트르산을 동일한 몰량으로 사용합니다. 80°C에서 가열하면 혼합물이 점성 투명 젤로 바뀝니다. 그런 다음 건조된 겔을 분쇄하고 550°C까지 서서히 가열합니다. (https: //en.wikipedia.org/wiki/Lithium_cobalt_oxide).
몇 가지 일반적인 예는 다음과 같습니다. 졸-겔 방법
졸-겔 공정에서는 반응물의 수용액과 킬레이트제 용액을 혼합한다. 용매를 천천히 증발시키면 졸이 생성되고 이렇게 얻은 졸을 적당히 가열하면 겔이 생성됩니다. 후자는 원하는 제품을 얻기 위해 적절한 온도에서 하소됩니다.
예 1.
다양한 착화제로부터 LiCoO2의 합성 : 사용된 염은 질산코발트 6 수화물(Co( NO3 ) 2 ·6H2O 및 질산리튬, 무수 LiNO3 ) 이었다. 젤은 4가지 다른 착화제를 사용하여 생성되었습니다: 시트르산, 무수(C 3 H 4 OH(COOH) 3 , 글리신, (H 2 NCH 2 COOH), 전분(상업용 옥수수 전분 및 젤라틴).
Li:Co = 1.1:1의 비율로 물 20ml에 LiNO 3 및 Co(NO 3 ) 2 ·6H 2 O를 포함하는 5개의 용액을 준비합니다. 특정 착화제가 각 용액에 첨가됩니다: ( i ) 5 ml의 물에 희석된 시트르산(4.611 g); ( ii ) 글리신(1.501g); ( iii ) 전분(1.250g); ( iv ) 젤라틴(3.500g) 및 ( v ) 공시험.
처음 4개의 용액은 겔이 형성될 때까지 글리세린 욕조에서 70~80°C의 온도로 가열되었습니다. ( i ) 구연산(5시간), ( ii ) 글리신(3시간), ( iii ) 전분(1시간), ( iv ) 젤라틴(3시간)과 같이 겔화제마다 이 과정의 시간이 다릅니다. . 모든 샘플에 대한 결정질 분말의 생산은 머플로에서 2단계로 수행되었습니다. 먼저 재료를 300°C에서 20-30분 동안 소성하고 나중에 700°C에서 24시간 가열합니다. [Bruno GA Freitas 외, J. Braz. 화학 사회 2017년 11월 28일, 11일].
예 2.
졸-겔법으로 제조
LiNO3는 먼저 구연산 용액에 용해됩니다. LiNi 0.7 – 𝑥 M 𝑥 Co 0.3 O2 (0 ⩽ 𝑥 ⩽ 0.1), 각각. 구연산의 양은 Co, Ni 및 Mg의 총 몰량과 같습니다. 이어서, Co(Ac)2·4H2O, Ni(NO3)2·6H2O 및 Mg(NO3)2·6H2O를 혼합물에 첨가하였다. 전체 혼합물을 80℃의 수욕으로 가열하였다. 가열 과정에서 침전물이 없는 투명한 분홍색 용액이 형성됩니다. 마침내 투명한 용액이 천천히 건조되어 겔이 되었습니다. xerogel을 건조, 분쇄한 다음 120°C의 오븐에서 12시간 동안 열처리하였다.
겔 전구체를 공기 중에서 500℃에서 6시간 동안 소성하고, 관로에서 실온으로 냉각시켰다. 열처리된 제품을 마노 절구에서 분쇄하여 분말을 얻었다. 그런 다음 분말을 800°C에서 12시간 동안 소성하였다. 음극 제조를 위해 제조된 제품을 먼저 아세틸렌 블랙 및 폴리비닐리덴 플루오라이드(중량 80:8:12)와 𝑁-methyl pyrrolidone(NMP)에 혼합하였다. 얻어진 슬러리를 Al 호일에 코팅하고 추가 롤 프레싱을 위해 80 ℃ 에서 18시간 동안 건조시켰다. . [ Hailang Zhang, Advances in Materials Science and Engineering Vol 2014, Article ID 746341, ]

그림 16. 망간산리튬을 제조하기 위한 졸-겔 공정의 흐름도
( 크레딧: YS Lee, YK Sun 및 KS, Nahm, Solid State Ionics 109(1998) 285, M. Pasquali, S. Passerini 및 G Pistoia 제공), 리튬 배터리, 과학 및 기술, ed. GA Nazri 및 G. Pistoia, Springer, New York, (2009), p. 318)
리튬이온전지 음극재 제조
에너지 및 전력 밀도가 개선된 LIB로 이어지는 고무적인 경로는 높은 용량과 양극으로의 리튬 이온 확산 용이성, 양호한 사이클 수명 및 안전 문제가 없는 적절한 양극 재료를 선택하는 것입니다.
전구체 물질을 기준으로 탄소 양극은 아래와 같이 여러 유형으로 분류할 수 있습니다.
전구체 재료와 공정 매개변수는 생성된 탄소의 특성을 결정합니다. 고온(2000~3000°C)에서 처리하여 흑연화할 수 있는 재료를 소프트 카본 이라고 합니다.
흑연화 시, 난층 장애는 온도가 증가함에 따라 점진적으로 제거되고 재료의 변형이 완화됩니다[T. Zheng, JN Reimers 및 JR Dahn, 물리. B 목사 51 , 734(1995)] 페놀 수지로 제조된 것과 같은 경질 탄소 는 3000°C에서 처리하더라도 쉽게 흑연화될 수 없습니다. 코크스 유형 물질은 일반적으로 방향족 석유 전구체로부터 약 1000°C에서 제조됩니다.Jeff Dahn 및 Grant M. Ehrlich. “리튬 이온 배터리”, Linden의 배터리 핸드북, 4판, Thomas B. Reddy (Ed.), McGraw Hill, pp. 26., 2011]

그림 17. 탄소 음극재 전구체 분류
[신용 거래: Jeff Dahn 및 Grant M. Ehrlich. “리튬 이온 배터리”, Linden의 배터리 핸드북, 4판, Thomas B. Reddy (Ed.), McGraw Hill, pp. 26., 2011]
고리파르티(Goriparti)는 리튬과의 반응 메커니즘에 따라 LIB의 양극재를 세 가지 로 분류한다 [ Subrahmanyam Goriparti, Ermanno Miele, Francesco De Angelis, Enzo Di Fabrizio, Remo Proietti Zaccaria, Claudio Capiglia, J Power Sources 257 (2014) 421-443]
인터칼레이션/디인터칼레이션 그룹
이 범주의 양극에는 탄소질 및 산화티타늄 재료가 포함됩니다. 삽입 경로를 통해 발생하는 저장 용량은 표면적, 형태, 결정도 및 방향과 밀접하게 관련되어 있습니다. 소프트 카본은 일반적으로 배터리 산업에서 잘 받아들여지고 사용됩니다. 소프트 카본은 상당히 성숙한 기술인 반면, 하드 카본은 특히 전기 자동차 부문과 같이 고용량을 요구하는 응용 분야에 흥미로운 대안 솔루션을 제시할 수 있습니다. 산화티타늄 양극은 이미 일부 배터리 산업에서 사용하고 있습니다.


그래핀도 광범위하게 검토되었습니다. 특히, 그들의 전기적 특성으로 인해 이 재료가 하이브리드 그래핀/금속 양극(예: SnO2 및 Fe2O3이 있는 그래핀)에 특히 적합하다는 것이 확인되었습니다. 탄소 나노 튜브(CNT)는 매우 흥미로운 학문적 결과로 인해 의미가 있었지만 생산 비용이 미래 배터리 산업에서 음극 활물질로의 응용을 방해할 수 있습니다.


그러나 대형 EV 배터리의 경우 일반적으로 비용을 고려하여 저가의 흑연이 선호됩니다.
두 번째 범주에서는 Si, Ge, SiO, SnO2와 같은 합금 재료가 설명되었습니다. 이러한 재료는 합금/탈합금 전기화학적 메커니즘에서 리튬과 반응하여 이전 그룹에 비해 더 큰 용량과 높은 에너지 밀도를 제공할 수 있습니다. 그러나 이 프로세스는 순환 시 상당한 용량 손실을 초래하는 큰 부피 팽창을 의미합니다. 위에서 언급한 문제를 극복하고 전반적인 양극 성능을 향상시키기 위해 전도성 매트릭스와의 조합에 의한 복잡한 구조의 실현과 함께 벌크 치수에서 나노 스케일로의 축소가 제안되었습니다.
규소와 SnO2, 그리고 탄소와의 복합물은 미래의 리튬 전지에 응용할 수 있는 가장 유망한 재료이지만, 음극 재료로 대량 생산하기 위해서는 저렴한 방법이 여전히 필요합니다. 반면 Ge는 전기화학적 특성과 우수한 실험 결과로 흥미롭지만 지각에 풍부하다는 면에서 50위라는 단점을 갖고 있다. 따라서 리튬 배터리 기술의 대량 적용에는 좋은 선택이 아닌 것으로 보입니다.
세 번째 그룹에서는 전환 반응 방식으로 리튬과 반응하는 물질을 설명했습니다. 특히, 금속 산화물/인화물/질화물/황화물이 고려되었습니다. 그러나 이러한 재료는 낮은 용량 유지 및 큰 잠재적 히스테리시스로 인해 대규모 상용 리튬 배터리 시장에서 아직 멀었습니다. 따라서, 이러한 물질의 다양한 나노구조 형태가 또한 위에서 확인된 문제를 해결하기 위해 조사되었다.
나노기술은 확실히 차세대 리튬 배터리용 양극 재료를 엔지니어링하기 위한 강력한 접근 방식입니다. 그러나 설명된 재료를 상업용 LIB, 특히 EV 애플리케이션의 효과적인 양극으로 활용하려면 더 많은 연구가 필요합니다. 사실, 나노크기 물질의 대규모 합성을 위한 저렴한 제조 공정의 개발과 함께 더 높은 에너지와 더 높은 전력 밀도를 모두 달성하는 것이 필요합니다. 또한, 전극/전해질 계면에서 전자 수송 특성과 함께 리튬과 기술된 물질의 나노 크기 형태 사이의 상호 작용을 지배하는 메커니즘에 대한 조사는 나노 기술로 설계된 차세대 음극 활물질 설계에 매우 중요합니다. .
현재 리튬 전지에 사용되는 음극은 탄소 형태 중 하나의 리튬 고용체를 포함합니다. 리튬의 융점 이상의 온도에서 작동하는 리튬 전지는 반드시 원소 리튬 대신 합금을 사용해야 합니다. 이들은 일반적으로 이원 또는 삼원 금속 상입니다. 또한 전극 부피를 줄이고 용량을 크게 증가시키는 것을 목표로 주변 온도에서 탄소 대신 금속 합금을 사용할 가능성에 대한 관심이 증가하고 있습니다. [Robert A. Huggins, Advanced Batteries, Materials Science Aspects, Springer, New York, 2009, p.123].
흑연은 양쪽성이고 양이온이나 음이온이 그래핀 층 사이에 삽입될 수 있습니다. 양이온이 삽입되면 호스트 흑연 구조가 음전하를 띠게 됩니다. 양이온의 예는 Li + , K + , Rb + 및 Cs + 입니다. 음이온이 삽입되면 호스트 흑연 구조는 양전하를 띠며 음이온의 예는 Br – ,SO2 – , SbF6 –
탄소에 알칼리 금속을 삽입하는 것은 1926년에 처음으로 입증되었습니다 [K. Fredenhagen 및 G. Cadenbach, Z. Anorg. Allg. 화학 158, 249 (1926)] 및 리튬-탄소의 화학적 합성은 1955년에 입증되었습니다. [ D. Guerard, A. Herold, Carbon 13, 337 (1975 )]. 엑스레이 광방출 분광기 실험은 삽입된 리튬이 탄소에 전자를 포기한다는 것을 보여주었고, 따라서 구조는 흑연 구조의 탄소 층 사이에 포함된 Li + 이온으로 볼 수 있습니다.
[GK Wertheim, PMTh.M. Van Attekum 및 S. Basu, 솔리드 스테이트 Commun. 33, 1127(1980)]. 흑연에 종을 삽입하는 초기 작업에 대한 일반적인 검토는 다음에서 찾을 수 있습니다.
[LB Ebert, 흑연의 층간삽입 화합물, 재료과학연보,
권. 6, 에드. by RA Huggins, Annual Reviews, Palo Alto, CA(1976), p. 181].
애노드 재료의 순도에서 중요한 요소는 전해질과 반응할 것이기 때문에 표면에 있는 모든 산소 함유 화학종을 제거할 필요가 있다는 것입니다. 이 반응을 방지하기 위해 제조업체는 환원성 또는 불활성 분위기에서 흑연을 1100ºC에서 굽습니다. 이것은 흑연에 비해 다른 용도의 비용을 증가시킵니다. 탄소(90%)는 양극 페이스트 또는 슬러리를 만들기 위해 여러 다른 성분과 혼합됩니다. 음극과 마찬가지로 폴리불화비닐리덴(PVDF)을 바인더(-5%)로 사용하고, 전도성을 확보하기 위해 소량의 카본블랙을 첨가했다. 또한, n-메틸 피롤리돈(NMP)은 재료를 용해시켜 균일한 혼합물을 형성하는 데 사용됩니다. 압력은 균일한 입자 크기를 보장합니다(Sandi 1999).
리튬 티타네이트(LTO)가 많은 관심을 받고 있습니다. LTO 셀은 다른 화학 물질보다 낮은 온도에서 작동하고 높은 전력 밀도를 제공합니다. 그러나 이러한 전지는 전지당 약 2.2~2.3V 범위의 더 낮은 공칭 전압을 갖는 문제가 있습니다. [타카미 노리오, 이나가키 히로키, 다테바야시 요시나오, 사루와타리 히데사토, 혼다 케이조, 에구사 슌, J Power Sources 244 (2013) 469-475]
전극 재료, 일반적으로 흑연은 충전 과정에서 10% 팽창합니다. 흑연은 리튬 이온이 디인터칼레이션될 때 원래의 부피를 회복합니다. 알루미늄을 사용하면 리튬 이온이 흑연에 삽입될 뿐만 아니라 도체에도 삽입되어 알루미늄-리튬 합금을 형성합니다. 방전 중에는 역 과정이 발생합니다. 알루미늄은 몇 번의 사이클 후에 열화되어 집전체로 쓸모가 없을 것입니다.
그러나 음극이 흑연 대신 티탄산리튬으로 만들어지면 상황은 극적으로 달라진다. Li 4 Ti 5 O 12 의 전극 전위는 흑연보다 약 1.4V 높습니다(셀 전압은 약 1.4V 낮고 3.6V에 비해 2.2V 낮음). 이것은 리튬 이온이 알루미늄에 삽입되는 것을 방지합니다. 따라서 알루미늄은 비용 및 무게 관련 이유로 구리보다 선호됩니다. Li 4 Ti 5 O 12 는 낮은 전지 전압 때문에 주로 고정식 응용 분야에 사용됩니다. [ Călin Wurm et al., in Lithium-Ion Batteries, Reiner Korthauer (ed), 번역: Michael Wuest et.al., Springer, 2018. pp. 57 ].
티탄산리튬의 제조방법: 이산화티타늄과 리튬화합물(탄산리튬, 수산화리튬, 질산리튬, 산화리튬 중 어느 하나)의 혼합물을 670~800℃의 온도에서 예비소결 . TiO 2 , 및 Li 2 TiO 3 로 이루어진 화합물 또는 TiO 2 , Li 2 TiO 3 , 및 Li 4 Ti 5 O 12 로 이루어진 화합물이 얻어진다. 그런 다음 화합물은 800~950°C 범위의 온도에서 소결됩니다. [Tetsuya Yamawaki et.al., 미국 특허 6,645,673 B2, 2003 Toho Titanium Co., Ltd.에 양도됨, Chigasaki]
Toshiba의 SCiB™ 충전식 배터리(https://www.scib.jp/en/)
SCiB™는 양극에 리튬 티타늄 산화물(LTO)을 사용하여 안전성, 긴 수명, 저온 성능, 급속 충전, 높은 입출력 전력 및 큰 유효 용량을 달성합니다. SCiB™는 자동차, 버스, 철도 차량, 엘리베이터 및 발전소를 포함한 차량, 산업 및 기반 시설 응용 분야에서 폭넓은 응용 분야를 찾아냈습니다.
리튬이온전지 분리막 생산
습식 및 건식의 두 가지 유형의 공정을 사용할 수 있습니다. 일본 제조업체는 폴리머가 오일에 용해되는 습식 공정을 사용합니다. 그런 다음 오일을 증발시켜 다공성 필름을 남깁니다. 그들은 Celgard를 생산하기 위해 초고분자량의 폴리머를 사용하고, 3층의 블로운 폴리머 필름을 적층하고, 끌어내리고, 융점 이하로 어닐링하여 폴리머 구조를 제어합니다. 그런 다음 시트를 빠르게 늘려 다공성을 얻습니다.
습식 및 건식의 두 가지 유형의 공정을 사용할 수 있습니다. 일본 제조업체는 폴리머가 오일에 용해되는 습식 공정을 사용합니다. 그런 다음 오일을 증발시켜 다공성 필름을 남깁니다. 그들은 Celgard를 생산하기 위해 초고분자량의 폴리머를 사용하고, 3층의 블로운 폴리머 필름을 적층하고, 끌어내리고, 융점 이하로 어닐링하여 폴리머 구조를 제어합니다. 그런 다음 시트를 빠르게 늘려 다공성을 얻습니다.
[Pekala, RW, et al., 2000, “Separators: An Overlooked Opportunity to Enhance Battery Performance?,” 17차 국제 세미나 및 1차 및 2차 배터리 전시회, Ft. 플로리다주 로더데일, 3월 6-9일]
이 프로세스는 작동 조건에 매우 민감하고 재료 배치에 따라 달라지므로 세심한 제어가 필요합니다 [Linda Gaines and Roy Cuenca, Cost of Lithium ion battery for Vehicles, ANL Report ANL/ESD-42, May 2000, pp. 20 ] .
그러나 EV/HEV 셀용 분리막에 필요한 추가 두께는 감소된 강도를 보상합니다. [와이. Nishi, in: M. Wakihara, O. Yamamoto (Eds.), Lithium Ion Batteries, Wiley/VCH/Kodansha, Tokyo, 1998, p. 195.
P. Arora, Z. Zhang, Chem. 104(2004) 4419].
우수한 기계적 강도, 전해질 투과성과 같은 기존의 특성 외에도 이러한 미세 다공성 분리막은 전지 남용 동안 보호 특성 을 나타냅니다. 예를 들어, 과도한 과충전으로 인해 셀 온도가 비정상적으로 상승하면 발생된 열에 의해 PE가 연화되고 필름의 미세 기공이 닫힙니다. 이를 분리기 “종료”라고 합니다. 셧다운이 발생하면 전극 사이의 이온 수송이 효과적으로 중단되고 전류가 흐르지 않습니다. 분리기가 차단 온도 이상에서 기계적 무결성을 유지할 수 있다면 장치에 안전 여유를 제공할 수 있습니다. 그렇지 않으면 전극이 직접 접촉하여 화학적으로 반응하여 열 폭주가 발생할 수 있습니다.
그러나 열 관성으로 인해 종료 후에도 온도가 계속 상승할 수 있습니다. 이러한 조건에서 분리막은 전극을 녹이고 단락하여 격렬한 반응과 발열을 일으킵니다. 이러한 현상을 분리막의 “멜트다운” 또는 “파괴”라고 합니다. 따라서 셀의 안전을 보장하려면 “셧다운” 온도와 “멜트다운” 온도의 차이가 최대한 커야 합니다.
고밀도 폴리에틸렌으로 완전히 만들어진 분리기는 135°C에서 녹고 이 온도 이상에서 기계적 무결성을 잃습니다. 그러나 폴리프로필렌과 폴리에틸렌을 적층하여 만든 분리막은 폴리프로필렌의 융점인 165°C까지 기계적 무결성을 유지합니다. 초고분자량 폴리에틸렌이 135°C에서 녹지만 이 재료로 만든 분리기는 재료의 점도가 물리적 무결성을 유지하는 것과 같기 때문에 최소 180°C까지 기계적 무결성을 유지한다는 점은 흥미롭습니다.
셧다운 분리기는 신뢰할 수 있으며 리튬 이온 배터리 제조업체는 점점 더 자사 제품에 통합을 선택하고 있습니다. 가장 일반적인 셧다운 분리기에는 고분자량 폴리프로필렌과 초고분자량 폴리에틸렌이 혼합되어 있습니다. 여기에서 폴리에틸렌의 독특한 셧다운 특성은 고온에서 폴리프로필렌의 높은 기계적 무결성과 유리하게 결합됩니다. 셧다운은 되돌릴 수 없기 때문에 일단 작동되면 이러한 분리기는 셀을 영구적으로 손상시킵니다. [PG Balakrishnan, R. Ramesh, T. Prem Kumar , J. Power Sources. 155 (2006) 401–414]
리튬 이온 배터리의 기타 재료
알루미늄, 니켈 및 구리 호일 과 같은 집전체, 타이 렌-부타디엔 공중합체(SBR) 및 폴리비닐리덴 플루오라이드(PVDF)와 같은 결합제, 전해질 및 용매, 음극 전도성 첨가제, 분리막과 같은 기타 재료가 있습니다.
리튬 이온 배터리의 장점과 한계 - 리튬이온셀 제조
양극 대 음극 중량비
전지 작동 중에 리튬 금속이 형성되지 않는 것이 매우 중요합니다. 금속의 증착은 세포를 내부적으로 단락시키는 수상돌기를 형성합니다. 충전 중 전압 제어 및 셀 균형은 이 문제를 매우 크게 줄이는 데 도움이 됩니다. 리튬 증착을 제어하는 주요 방법은 전지에 있는 개별 플레이트의 음극 용량에 대한 양극 용량의 비율입니다. 애노드 전극은 캐소드 보다 가용 용량이 약 10% 더 높습니다 . 이것은 음극이 전지의 용량을 결정하기 때문에 충전하는 동안 양극에 리튬 금속이 침착되는 것을 방지합니다. 리튬 금속이 전극 표면에 침전되면 전해질과 반응하여 열폭주가 발생할 수 있습니다.

그림 21. 리튬 이온 전지의 양극 및 음극 용량 비율
( 출처: Ralph J. Brodd 및 Kazuo Tagawa, in Advances in Lithium-Ion Batteries, Walter A. van Schalkwijk 및 Bruno Scrosati(Eds), Kluwer Academic Publishers, New York, pp. 272, 2002)
리튬 이온 전지 조립 공정
리튬 이온 배터리의 셀 조립 공정은 활성 물질로 코팅된 양극 및 음극 스톡을 코팅할 때 정밀도와 정확성이 필요합니다. 코팅 공정은 고용량, 고신뢰성 제품 확보에 있어 중요한 요소입니다. 코팅의 품질이 좋지 않으면 성능이 낮은 배터리만 생산됩니다. 활성 물질 준비의 초기 단계가 결과를 결정합니다.
코헨과 거토프 [E. Cohen 및 E. Gutoff, 현대 코팅 및 건조 기술, Wiley-VCH,
New York, 1992] 는 코팅 슬러리의 유동학, 필요한 정밀도 및 코팅 속도를 기반으로 특정 응용 분야에 대한 최상의 코팅 기술에 도달하는 방법론을 설명합니다.

그림 22. 양극 및 음극 코팅 공정
( 출처: Ralph J. Brodd 및 Kazuo Tagawain in Advances in Lithium-Ion Batteries, Walter A. van Schalkwijk 및 Bruno Scrosati(Eds), Kluwer Academic Publishers, New York, pp. 273, 2002.)
리튬이온전지 제조공정도

그림 23. 리튬 이온 전지 제조를 위한 흐름도
[Ralph J. Brodd 및 Kazuo Tagawa의 리튬 이온 배터리 발전, Walter A. van Schalkwijk 및 Bruno Scrosati(Eds.), Kluwer Academic Publishers, New York, pp. 271, 2002]

크레딧: Electropaedia https: //www.mpoweruk.com/battery_manufacturing.htm
그림 24. 원자재로 전극을 제조하기 위한 순서도
리튬 이온 전지 어셈블리




리튬 이온 배터리 제조업체는 셀을 조립할 때 다음 사항을 목표로 합니다.
- 리튬 이온 전지의 설계는 전극 영역 전체에 걸쳐 균일한 전류 밀도를 제공해야 합니다.
- 활성 물질(AM)과 집전체 사이의 양호한 접촉을 보장하기 위해
- 큰 표면적 전극은 세포에 높은 속도 성능을 제공하기 위해 사용됩니다. 이것은 극성화, 즉 전극 반응의 역학으로 인한 전압 손실을 감소시키고 분리기 양단의 전압 강하를 낮춥니다.
기공 구조와 전도성 탄소의 조합은 활성 물질의 우수한 입자 간 접촉을 제공합니다.
활물질, 전도성 탄소 및 집전체 사이의 양호한 접촉 은 활물질의 완전한 활용과 고속 성능 동안 우수한 효율을 위해 필수적입니다.
코발트 음극 혼합물 은 LiCoO2(검정색 분말) + PVdF 바인더(백색 반결정성 불소수지 열가소성 수지) + N-메틸 피롤리돈(NMP, 무색 유기 액체)을 용매로 사용하여 제조됩니다. 비전도성인 LICoO2는 전도성 희석제인 항상 카본 블랙을 첨가하여 LiCoO2의 전도성을 향상시킵니다.
재료의 비율과 양은 셀 디자인과 믹서의 크기에 따라 결정됩니다. 코팅 용매와 결합제를 첨가하기 전에 비전도성 활성 물질과 탄소를 건조 혼합하기 위해 집중 혼합 절차가 사용됩니다.
상기 혼합물을 건식 블렌딩하여 전도성 탄소의 박막으로 활물질 입자의 균일한 코팅을 제공하여 AM과 집전체 그리드(알루미늄 호일, 두께 20mm) 사이의 전기적 접촉을 개선하고, 따라서 모든 AM의 완전한 활용을 보장합니다. 폴리머 NMP는 별도의 용기에서 코팅 용매에 용해됩니다. 드라이 믹스 블렌드 그런 다음 용매 용액을 결합하여 슬러리를 형성합니다.
용제 첨가는 코팅 작업을 위한 슬러리(또는 페인트)의 점도를 조정하는 데 사용됩니다 . 폴리비닐렌디플루오라이드(PVdF)가 선택되는 바인더이며 용매는 N-메틸피롤리디논(NMP)입니다. 혼합 작업에서 나온 슬러리는 코팅 작업을 위한 저장소 및 전달 매체 역할을 하는 밀봉된 용기에 넣습니다. 코팅 헤드로 가는 유체에 공기가 혼입되는 것을 방지하기 위해 정확한 양의 코팅 슬러리가 기어 펌프 또는 이와 유사한 정밀 펌프를 사용하여 저장 용기에서 펌핑됩니다.
양극 혼합물 은 경질 탄소, PVdF 바인더 및 NMP와 유사한 방식으로 준비됩니다. 이 혼합물은 그리드로 사용되는 동박(두께 10mm)에 코팅됩니다.
코팅은 양극과 음극 모두 약 100mm 두께로 양면에 수행됩니다. 코팅 두께를 줄임으로써 전체 표면적의 증가는 전지의 특정 부피에 대해 달성됩니다. 사용된 유기 전해질은 수성 전해질에 비해 낮은 전도도를 가지므로 이러한 높은 표면적은 고전력 방전 전지를 용이하게 합니다.
전극 두께는 필요한 최대 전력에 따라 다릅니다. 리튬 이온 배터리 제조 기술의 독특한 특징은 동일한 전극 제조 기술로 다양한 전력/에너지 비율 설계가 가능하다는 것입니다. [Broussely, Nazri pp 651]. 그러나 적절한 전류 수집 및 탭, 셀 모양 및 디자인이 중요합니다.
셀 어셈블리: 코팅된 호일이 오븐을 통과하여 용매를 증발시키고 호일에 정확한 양의 활성 물질을 남깁니다. 많은 코팅 용제는 유해 물질로 분류되어 대기 중으로 방출될 수 없습니다. 비용 절감 조치로 용매는 일반적으로 공정에서 재사용하기 위해 회수됩니다. 환경 오염을 방지하기 위해 용매를 소각할 수 있습니다.
대부분의 리튬 이온 전지는 모양이 원통형입니다. 젤리 롤을 평평하게 하여 각형 셀의 요소를 얻 습니다.
각형 셀은 더 나은 부피 충전에 유리하지만 사이클링 또는 노화로 인해 부풀어 오르기 쉽습니다. 원통형 셀 캔은 더 나은 기계적 강도, 우수한 치수 안정성 및 요소의 균일한 압력을 제공합니다.
코팅 작업은 코일 길이에 맞게 단속 코팅을 생성합니다. 와인딩 머신은 건조된 캐소드 및 애노드 점보 롤 및 분리기(두께 25mm 이하, PP 또는 PE 또는 혼합)와 함께 사용하기 위해 자동으로 작동하도록 설계되었습니다.
작업은 호일의 코팅되지 않은 부분에 탭을 용접하는 것으로 시작됩니다. 그런 다음 감기 기계는 스트립을 적절한 길이로 자르고 양극-분리기-음극 조합을 젤리롤 방식으로 단단한 코일이나 보빈으로 감습니다. 권선 코어의 직경이 증가함에 따라 권선기는 코일의 직경이 증가함에 따라 일정한 장력을 유지하기 위해 자동으로 보정하여 직경에 대한 공차를 가깝게 합니다. 각형 셀에 대한 타원형 바람은 더 복잡하고 느린 과정입니다.
권선 후 코일을 캔에 삽입하기 전에 내부 단락 여부를 확인합니다. 강철 캔은 깨끗하고 니켈 도금되어 안정적인 표면을 제공하고 전지 조립 전에 캔 부식을 최소화해야 합니다. 양극 리드는 캔 바닥에 용접되고 음극 리드는 안전 통풍구에 용접됩니다. 전해질이 반조립된 전지에 추가됩니다. 상단 커버를 압착하면 조립이 완료됩니다.
잠재적인 셀 결함을 조기에 제거하는 것은 경제적인 조치이며 불량 셀에 대한 더 많은 작업을 방지합니다. 보빈은 캔에 삽입되어 캔이 일정한 압력을 제공하여 요소의 구성 요소를 서로 가깝게 유지하여 그들 사이에 빈 공간이 생길 가능성을 제거합니다. 일부 제조업체는 코일의 중심을 안정화하기 위해 맨드릴을 삽입할 수 있습니다.
모든 작업이 Dry Room 또는 Dry Box 에서 이루어지지 않는 한, 전해질 충전 공정 전에 열과 진공으로 활물질에 흡수된 수분을 제거해야 합니다.
전해질의 정밀한 진공 충전은 전해질이 침투하여 분리막 및 전극 구조에서 사용 가능한 다공성을 완전히 채우도록 하기 위해 수행됩니다. 정밀 펌프는 양호한 전지 작동에 필요한 전해질의 계산된 부피를 측정합니다. 항상 모든 제조업체는 LiPF 6 (무기 백색 결정성 화합물) 을 전해질로 사용하고 고리형(EC, 에틸렌 카보네이트) 또는 선형 카보네이트(DMC, 디메틸 카보네이트, DEC, 디에틸 카보네이트 또는 EMC, 에틸-메틸 카보네이트 등)를 사용합니다. 이 전해질 염의 용매.
에틸렌 카보네이트(EC)와 디메틸 카보네이트(DMC) 및/또는 디에틸 카보네이트(DEC)의 용매 혼합물 기반 전해질은 일반적으로 리튬 이온 배터리에 “4V” 음극(코발트산염, 니켈산염 및 망간산염)과 함께 사용됩니다. 용매의 높은 산화 가능성.
전지를 전해질로 채운 후 전지 캔과 상판 사이에 위치한 폴리머 가스켓 또는 그로밋의 제어된 압축에 의해 전지를 밀봉합니다. 폴리머 가스켓 씰의 압력은 폴리머의 탄성 한계 내에서 유지되도록 제어됩니다. 탄성 한계를 초과하면 폴리머가 차갑게 흐르고 밀봉이 손상됩니다.
각 제조업체는 셀을 밀봉하기 위해 약간 다른 기계적 구조를 사용하지만 최종 결과는 본질적으로 동일합니다. 일반적으로 숄더 또는 선반은 셀 상단 근처에 형성됩니다. 이것은 밀봉을 위한 베이스 역할을 하고 젤리롤을 제자리에 고정하고 진동 및 충격의 영향으로 감긴 보빈의 신축 또는 위치 변경을 방지합니다.
위치가 변경되면 전류 분포가 변경되어 사이클 수명이 저하되거나 고성능 셀에서 리튬 도금이 발생합니다. 셀 상단 플레이트 씰에는 통풍구, 양의 온도 계수 요소(PTC) 및 전류 차단(CID) 안전 장치가 포함되어 있습니다. CID와 PTC는 모두 위험한 온도와 압력이 셀 내부에서 발생하는 것을 활성화하고 방지하도록 설계된 안전 장치입니다. 각 로트의 장치는 상단 조립품에 통합되기 전에 적절한 작동 여부를 확인합니다.
봉인이 적용된 후 세포를 세척하고 재킷을 입히고 라벨을 붙일 수 있습니다. 제조일자를 추적하고 모든 전지 구성 요소(전극 재료, 전해질, 분리기 등)를 식별하기 위해 일련 번호가 부여됩니다. 용량 및 전압에 대한 정보는 셀 번호와 함께 저장되고 나중에 팩 조립을 위한 셀을 일치시키는 데 사용됩니다.
셀은 유리 대 금속 씰로 레이저 용접되어 오래 지속되는 밀폐 씰을 제공할 수 있습니다. 더 큰 셀을 사용하면 남용 조건에서도 안전한 작동을 보장하기 위해 더 많은 주의를 기울여야 합니다.
위의 프로세스는 휴대용 전자 제품에 사용되는 소형 밀봉 셀에 대해 설명되어 있지만 에너지 저장, 우주 및 EV 애플리케이션을 위한 더 큰 산업용 배터리의 프로세스는 동일한 일반 개요를 따릅니다.
리튬 이온 배터리 - 형성 및 노화
조립된 상태에서 Li 이온은 양극 탄소에 도핑되지 않으므로 셀에 전압이 표시되지 않습니다. 초기 충전 시 PAM LiCoO 2 에서 Li 이온의 일부가 undoping되어 Li 1-x CoO 2 가 되고 이 리튬 이온이 탄소 양극(C y )에 도핑되어 Li x C y 가 됩니다. 충전 전압이 4.1~4.2V에 도달하면 x 의 값은 약 0.5입니다. (즉, 50%) LiCoO 2 의 Li 50%가 사용되었음을 나타냅니다.
주목해야 할 또 다른 측면은 도핑된 리튬 이온의 일부가 반환되지 않고 양극에 남아 있다는 것입니다. 여기서 x-dx 리튬 이온은 용량에 기여하지 않고 유지됩니다. 이는 비가역 리튬이 약 10~20%로 초기 충전 효율이 80~90%임을 의미한다. 두 번째 사이클부터는 비가역량이 증가하지 않고 셀은 제조사에서 설계한 100% 용량을 나타냅니다.
세척 및 자켓팅 후, 그러나 형성 과정이 시작되기 전에 모든 셀의 전압 및 임피던스를 기록하여 결함 셀을 분류합니다. 그런 다음 셀이 처음으로 충전됩니다.
(초기 충전 또는 대형 충전). 첫 번째 충전 조건은 다음 두 가지 이유로 중요합니다.
1) SEI( Solid Electrolyte Interphase ) 층이 양극에 형성되어 정상적인 전지 작동 중에 전해질과 자발적으로 반응하지 않도록 보호하고 2) 활물질과 전해질 사이에 양호한 전기적 접촉을 설정합니다. 첫 번째 충전은 제조업체에서 권장하는 셀 충전 절차를 따르지만 종종 더 낮은 전류에서 시작하여 충전 기간의 약 1/3이 되면 정상 충전 전류로 증가합니다. 전지는 형성 후 1~2회 더 주기 동안 충전 및 방전을 위한 전압 한계 내에서 계속 순환할 수 있습니다.
형성 또는 순환 후, 전지 전압 및 용량이 측정되고 전지 선택 과정 에서 나중에 사용하기 위해 저장됩니다. 숙성 기간 은 제조사에 따라 2주에서 1개월 정도다. 셀의 전압은 보관 후 다시 측정됩니다. 저장 기간의 시작과 끝에서의 전압 차이는 “소프트” 또는 “마이크로” 단락이 있는 셀을 분류하는 데 사용됩니다. 내부 단락이 있는 셀은 보관 후 전압이 낮아지고 정상 전압 및 용량 분포에서 분리됩니다. 형성 가스를 제거하기 위해 형성 후 더 큰 셀을 비워야 할 수도 있습니다.
조립 과정에 대한 자세한 설명은 독자를 참조하십시오.
- Kaoru Nakajima 및 Yoshio Nishi 5장: 전자 제품을 위한 에너지 저장 시스템, Ed Tetsuya Osaka 및 Madhav Datta, Gordon 및 Reach Science Publishers, 암스테르담, 2000.
- 리튬 이온 전지 생산 공정, Ralph J. Brodd 및 Kazuo Tagawa, 9장: 리튬 이온 배터리의 발전, Walter A. van Schalkwijk 및 Bruno Scrosati(Eds), Kluwer Academic Publishers, New York, pp. 273, 2002 .
- 리튬 배터리, 과학 및 기술, ed. GA Nazri 및 G. Pistoia 작성, Springer, New York, 2009.
- 리튬 이온 배터리, Reiner Korthauer(ed)(2018), Michael Wuest 외 번역, Springer, 2018.
- Kazuo Tagawa 및 Ralph J. Brodd, 리튬 이온 배터리의 리튬 이온 배터리 제조를 위한 생산 공정, Yoshio M., Brodd RJ, Kozawa A. (eds) Springer, New York, NY. https: //doi.org/10.1007/978-0-387-34445-4_8]
- Zhang Z., Ramadass P. (2012) 리튬 이온 배터리 시스템 및 기술. In: Meyers RA (ed) 지속 가능성 과학 및 기술 백과사전. 스프링거, 뉴욕. https: //doi.org/10.1007/978-1-4419-0851-3_663
- 리튬 이온 배터리 팩 설계 화학, 구성 요소, 유형 및 용어 핸드북, John Warner, Elsevier, 2018




