Menyamakan muatan dalam baterai asam timbal
Maksud dari penyetaraan muatan adalah untuk membawa tegangan pengisian baterai timbal-asam ke tingkat gas sehingga semua timbal sulfat yang tidak terkonversi dibebankan ke timbal dan timbal dioksida, masing-masing, dalam NAM dan PAM.
Menyamakan biaya: Menyamakan Baterai
Perawatan baterai asam timbal yang tepat membantu meningkatkan masa pakai baterai. Equalizing charge adalah salah satu aspek terpenting dari prosedur perawatan ini.
Menyamakan definisi biaya
Untuk jenis baterai seperti itu, maksud penyetaraan muatan adalah untuk membawa tegangan pengisian baterai 12V ke tingkat gas sehingga semua timbal sulfat yang tidak dikonversi dibebankan masing-masing ke timbal dan timbal dioksida, dalam NAM dan PAM. Ketika ada gas bebas dan berlebihan, semua ion sulfat yang tidak bermuatan masuk ke elektrolit dan meningkatkan kerapatan asam.
Vinal dalam buku klasiknya memberikan hubungan tegangan sel dan tingkat gas.
Tingkat penyerangan dengan gas dan voltase sel pada pengisian sel yang tergenang
(Sumber: Vinal, GW, Baterai Penyimpanan, John Wiley & Sons, New York, 1954, halaman 262)
| Tegangan Sel (V) | Tingkat penyerangan dengan gas | Komposisi gas berevolusi H 2 Persen | Komposisi gas berevolusi O 2 Persen |
|---|---|---|---|
| 2.2 | Tidak ada gas | - | - |
| 2.3 | Sedikit | 52 | 47 |
| 2.4 | Normal | 60 | 38 |
| 2.5 | Banyak sekali | 67 | 33 |
Demikian pula, baterai yang tidak diisi daya awal dengan benar di pabrik memerlukan pengisian daya penyeimbang lebih lanjut . Hal ini dapat dibuktikan dengan peningkatan berat jenis elektrolit dalam beberapa bulan setelah pengoperasian baterai, misalnya baterai inverter. Biasanya, nilai berat jenis akan menjadi 1,240 sebelum pengiriman. Setelah nilai ini tercapai, beberapa produsen berhenti mengisi daya dan menganggap bahwa baterai telah terisi penuh.
Sebenarnya, jika mereka melanjutkan muatan awal lebih jauh, mereka bisa melihat peningkatan substansial dalam berat jenis. Aspek pengisian awal ini menunjukkan adanya timbal sulfat yang tidak bermuatan di pelat. Jumlah timbal sulfat ini membantu meningkatkan berat jenis elektrolit dalam proses pengisian lebih lanjut.
Bagaimana cara menyamakan muatan membantu?
Pengisian daya penyeimbang membantu mewujudkan masa pakai baterai yang dirancang, menghindari kegagalan prematur karena pengisian daya yang tidak mencukupi. Baterai yang menerima muatan penyeimbang reguler akan hidup lebih lama daripada baterai yang tidak. Hal ini terutama berlaku dalam kasus baterai forklift, baterai otomotif dan baterai inverter. Kita telah melihat bahwa memberikan baterai forklift dengan muatan yang sama memastikan kinerja baterai forklift yang lebih baik. Perpanjangan masa pakai baterai melalui kontrol pemerataan pengisian daya adalah cara yang sudah mapan untuk kinerja baterai yang lebih baik.
Di beberapa negara, UPS dan baterai catu daya stasioner tidak mengalami pemadaman listrik bahkan selama beberapa menit dalam setahun. Dalam situasi seperti itu, produsen baterai menyarankan konsumen untuk mematikan pasokan listrik selama beberapa menit. Ini akan menghindari “pasif mengambang”.
Apa yang dimaksud dengan muatan penyeimbang untuk baterai?
Semua aspek yang dibahas di atas juga berlaku untuk baterai VR. Satu-satunya perbedaan adalah bahwa tegangan pengisian untuk muatan penyeimbang lebih rendah. Baterai harus diisi tidak lebih dari 14,4 V (untuk baterai 12V) selama pengisian equalizer. Tarif gas adalah:
Tingkat penyerangan dengan gas dan voltase pelampung sel dengan mengisi sel yang Diatur Katup
Menyamakan tegangan muatan
| Tegangan sel (V) | Tingkat penyerangan dengan gas | Efisiensi rekombinasi (%) | Tingkat gas beracun * | Tingkat penyerangan dengan gas beracun relatif |
|---|---|---|---|---|
| 2,25 hingga 2,3 | Gas yang dapat diabaikan | ~ 99,87 | ~ 0,0185 | ~ 1 |
| 2.4 | Beberapa penyerangan dengan gas | ~ 99,74 | ~ 0,037 | ~ 2 |
| 2.5 | Penyerangan dgn gas beracun | ~ 97.4 | ~ 0.37 | ~ 20 |
*cc/h/Ah/sel dari: Kredit: Teknologi C&D : Buletin Teknis 41-6739, 2012.). 1 kaki kubik = 28317 cc (= (12*2,54) 3 = 28316,85
Menyamakan muatan - Bagaimana baterai VRLA berbeda dari baterai asam timbal yang tergenang?
Kimia dasar dari dua versi baterai asam timbal adalah sama. Reaksi pelepasan serupa, tetapi reaksi pengisian berbeda dalam langkah-langkah perantaranya.
Gas (hidrogen dan oksigen) berkembang di dekat akhir pengisian dalam baterai asam timbal yang dibanjiri dibuang. Gas oksigen yang berevolusi pada pelat positif sel VR dengan mudah berpindah ke pelat negatif dan mengoksidasi timbal, karena koefisien difusi yang lebih tinggi dalam media gas. Ini adalah reaksi cepat dalam sel VR. Pergerakan gas seperti itu tidak mungkin terjadi dalam sel yang tergenang karena koefisien difusi yang lebih rendah. Kondisi yang mirip dengan sel yang dibanjiri akan terjadi pada sel VR juga jika AGM sepenuhnya jenuh dan reaksi rekombinasi oksigen akan dimulai hanya ketika kondisi elektrolit yang kelaparan mulai berkembang karena elektrolisis air dan hilangnya sebagian air.
Dalam sel yang Diatur Katup, evolusi hidrogen dihambat oleh pembentukan timbal sulfat selama pengisian. Timbal sulfat ini membawa potensi pelat negatif ke nilai yang lebih positif sehingga evolusi hidrogen sangat berkurang. Paduan khusus juga digunakan dalam jaringan negatif yang akan memiliki tegangan lebih hidrogen yang lebih tinggi.
Menyamakan muatan: Baterai VRLA dari segi konstruksi memiliki perbedaan berikut:
- Volume elektrolit kurang dalam baterai VRLA. Hal ini sengaja disimpan demikian karena harus ada jalur untuk oksigen yang berevolusi dari PAM untuk menghubungi NAM melalui pori-pori tak jenuh di separator alas kaca serap (AGM). Untuk mengimbangi pengurangan volume elektrolit, asam densitas lebih tinggi digunakan dalam baterai VR. Ini juga akan mengkompensasi pengurangan kapasitas tingkat rendah.
Elemen-elemennya sangat terkompresi dalam baterai VRLA. Aspek ini memainkan peran paling penting dalam meningkatkan masa pakai baterai. Kompresi dinding pelat-separator-kontainer merupakan bagian integral dari desain. Ini memastikan difusi elektrolit yang baik antara pelat dan pemisah. Umur juga meningkat karena pengurangan ekspansi bahan aktif positif dan hilangnya kapasitas yang dihasilkan.
- Baterai VRLA memiliki katup penyegelan kembali satu arah di setiap sel atau mungkin ada katup umum untuk beberapa sel (terutama dalam sel berkapasitas kecil). Katup multifungsi ini bekerja dengan cara berikut:
Saya. Mencegah masuknya udara atmosfer (oksigen) secara tidak sengaja.
ii. Membantu transportasi oksigen dengan bantuan tekanan dari PAM ke NAM
aku aku aku. Mencegah ledakan jika terjadi pengembangan tekanan yang tidak semestinya di dalam baterai karena pengisian yang salah atau kegagalan fungsi pengisi daya.
- Berfungsinya baterai VRLA tergantung pada siklus oksigen internal, yang pada gilirannya tergantung pada konstruksi anti bocor: tutup untuk segel dan panci untuk menutup segel. Siklus oksigen internal membantu mengurangi evolusi hidrogen dan dengan demikian mengurangi kehilangan air.
Siklus oksigen internal
Selama pengisian baterai VRLA:
Pada pelat positif, gas O2 berevolusi dan proton dan elektron dihasilkan.
2H2O → 4H + + O2 + 4e- ……… Persamaan. 1
Gas oksigen, ion hidrogen, dan elektron berevolusi sebagai hasil elektrolisis air pada pelat positif melewati pori-pori kosong, pori-pori berisi gas dan saluran elektrolit di separator AGM (atau retakan halus pada matriks elektrolit gel dalam kasus baterai VR gel) dan mencapai pelat negatif. Gas ini bergabung dengan timbal dalam NAM menjadi PbO dan oksigen tereduksi bergabung dengan ion hidrogen untuk membentuk air. Oksida ini bergabung secara kimia dengan ion sulfat untuk membentuk timbal sulfat
2Pb + O2 → 2PbO
2PbO + 2H 2 SO 4 → 2PbSO 4 + 2H 2 O
——————————————————
2Pb + O2 + 2H 2 SO 4 → 2PbSO 4 + 2H 2 O + Panas ……… Persamaan. 2
—————————————————–
Tetapi, karena ini adalah proses pengisian, timbal sulfat yang dihasilkan lagi harus diubah menjadi timbal; asam sulfat dihasilkan melalui jalur elektrokimia dengan bereaksi dengan proton (ion hidrogen) dan elektron yang dihasilkan dari penguraian air pada pelat positif saat bermuatan.
2PbSO 4 + 4H + + 4e → 2Pb + 2H 2 SO 4 ……… Persamaan. 3
Ketika NAM diubah menjadi PbSO 4 selama pengisian, potensi pelat negatif menjadi lebih positif (seperti dalam kasus pelepasan). Ini membantu dalam menghambat reaksi evolusi hidrogen. Jumlah gas hidrogen yang dihasilkan sangat kecil, tetapi katup satu arah memastikan bahwa tekanan di dalam tabung tidak mencapai tingkat yang berbahaya dengan melepaskan hidrogen ke atmosfer, sehingga melindungi baterai dari penonjolan dan cacat lainnya.
Reaksi terakhir mengembalikan keseimbangan kimiawi sel. Jumlah bersih dari reaksi (Persamaan 1) hingga (Persamaan 3) menjadi nol, energi listrik yang dihabiskan selama pengisian diubah menjadi panas daripada menjadi energi kimia [Ref RF Nelson, Proc. Seminar Baterai Asam Timbal Int ke-4, 25-27 Apr 1990, San Francisco, AS, ILZRO, Inc., 1990, hlm.31-60].


Keuntungan terpenting dari sel VRLA adalah tidak diperlukan penambahan air sebagai prosedur perawatan. Keuntungan berikutnya adalah bahwa ia menghasilkan jumlah gas yang dapat diabaikan selama operasinya, karena rekombinasi hampir 100% pada voltase float yang direkomendasikan 2,25 hingga 2,3 V per sel. Selain itu, tidak ada batasan transportasi dalam memindahkan baterai ini dari satu tempat ke tempat lain.
Baterai utama dan isi ulang
Baterai didefinisikan sebagai perangkat elektrokimia yang dapat mengubah energi kimia menjadi energi listrik melalui reaksi redoks dan dengan demikian bertindak sebagai sumber daya elektrokimia. Tapi, itu bukan sumber kekuatan abadi. Baterai akan memasok daya hanya sampai ada bahan aktif yang cukup untuk mempertahankan reaksi penghasil energi. Setelah tingkat tegangan baterai mencapai tingkat tertentu yang lebih rendah yang ditentukan oleh kimia sistem, reaksi harus dibalik, yaitu baterai harus menerima arus searah. Tindakan memasok arus searah dalam arah kebalikan dari pelepasan ke baterai yang kosong untuk membalikkan reaksi pelepasan disebut “pengisian”.
Ini akan meregenerasi bahan aktif asli dari produk pelepasan dan juga akan meningkatkan tegangan baterai ke nilai yang lebih tinggi, sekali lagi ditentukan oleh sistem kimiawi. Pernyataan ini berlaku untuk baterai yang disebut baterai sekunder atau baterai penyimpanan. Ini tidak relevan dengan sel primer seperti yang digunakan dalam obor listrik dan jam tangan. Penurunan tegangan baterai selama pengosongan terjadi karena penipisan bahan aktif dan beberapa alasan lainnya.
Unit independen baterai disebut “sel”. Baterai adalah kombinasi dari dua atau lebih sel yang terhubung dalam beberapa cara yang berbeda untuk mencapai tegangan yang dirancang dan peringkat kapasitas atau peringkat kWh total. Paling umum, baterai monoblok digunakan di mobil dan baterai asam timbal yang diatur katup ( VRLA ) berkapasitas kecil dan baterai tabung (hingga 12V/200 Ah); di luar kapasitas ini sel tunggal digunakan untuk mendapatkan peringkat kWh yang diperlukan dengan menggabungkannya dalam susunan seri atau seri-paralel.
Baterai asam timbal dengan rating 48V/1500 Ah (atau 72 kWh) mungkin memiliki 24 nomor sel berkapasitas 2V/1500 Ah yang dihubungkan secara seri sederhana atau 48 sel dengan sel berkapasitas 2V/750 Ah yang dihubungkan secara seri-paralel. Yaitu 24 sel yang dihubungkan secara seri untuk menghasilkan baterai 48V/750Ah (atau 36 kWh). Baterai 48V/750 lainnya akan dihubungkan secara paralel dengan yang pertama untuk menjadikannya baterai 48V/1500 Ah (72 kWh).
Contoh lain dari baterai kendaraan listrik (EV) lithium-ion (Li-ion):
Bergantung pada ukuran paket baterai, pembuat EV Tesla menggunakan sekitar 6.000-8.000 sel per paket, masing-masing sel berkapasitas 3.6V/3.1 hingga 3.4 Ah untuk membangun paket baterai 70 atau 90 kWh.
Baterai Tesla EV 70 kWh menggunakan sekitar 6000 sel tipe 18650 sel NCA 3,7 V/3,4 Ah, dihubungkan dalam susunan seri-paralel yang rumit. Ini memiliki jangkauan 325 km per pengisian daya. (Di sini gambar 18650 mengacu pada jenis sel Li-ion tertentu yang memiliki perkiraan dimensi panjang (atau tinggi) 65 mm dan diameter 18 mm. Istilah “NCA” adalah singkatan dari bahan katoda yang digunakan dalam sel ini, misalnya N = Nikel, C = Cobalt dan A = aluminium, yaitu bahan katoda nikel-kobalt-aluminium oksida)
Paket 90kWh memiliki 7.616 sel dalam 16 modul. Beratnya 540kg. Ini memiliki jangkauan 426 km per pengisian daya.
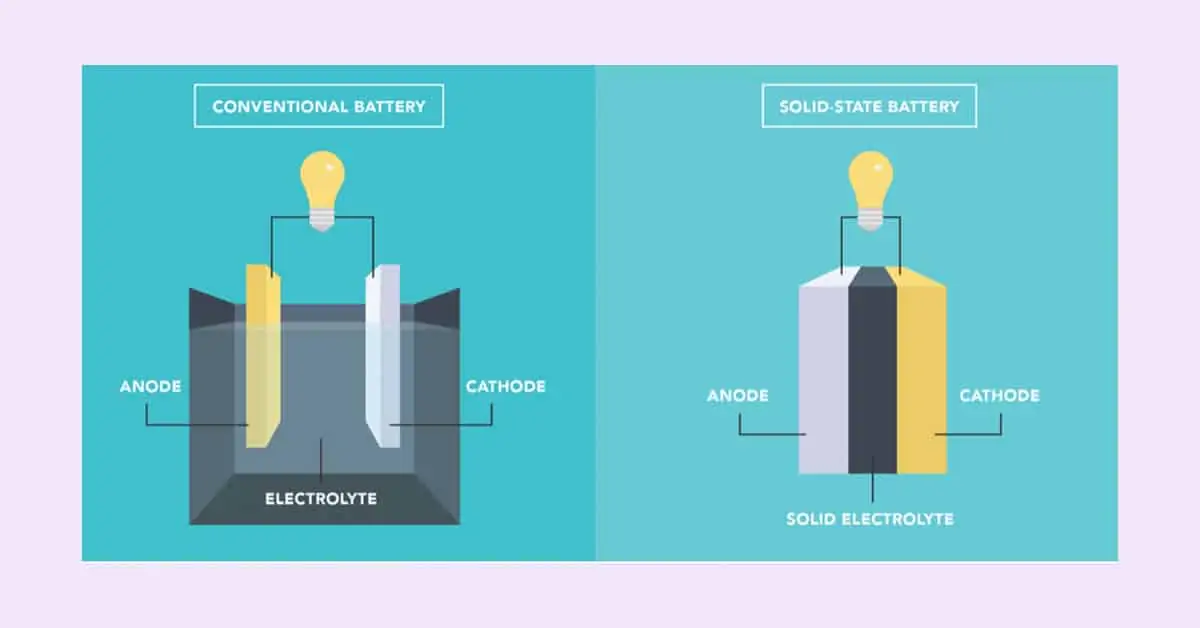
Komponen sel baterai:
Komponen yang paling penting dari baterai adalah:
sebuah. Anoda (pelat negatif)
B. Katoda (pelat positif)
C. Elektrolit (Dalam baterai asam timbal, elektrolit juga merupakan bahan aktif, tetapi tidak demikian di kebanyakan sistem lain)
Tiga di atas disebut komponen aktif
Tentu saja, ada komponen tidak aktif seperti
sebuah. Stoples
B. Grid pengumpul saat ini
C. Bilah bus atau tali konektor
D. pemisah
e. Konektor antar sel
F. Pos terminal, dll
Dalam baterai timbal-asam, elektrolit (asam sulfat encer) mengambil bagian dalam reaksi penghasil energi seperti yang dapat dilihat dari reaksi sel yang diberikan di bawah ini. Asam sulfat dikonsumsi untuk mengubah timbal dioksida dan timbal menjadi timbal sulfat sehingga densitas elektrolit menurun saat reaksi pelepasan berlangsung. Sebaliknya, ketika sel diisi, densitas elektrolit meningkat seiring dengan berlangsungnya reaksi pengisian. Alasannya adalah bahwa ion sulfat yang diserap oleh kedua bahan aktif selama pelepasan dilepaskan dalam elektrolit sehingga densitas elektrolit meningkat.
Reaksi pelepasan dan pengisian
Reaksi sel galvanik atau baterai khusus untuk sistem atau kimia:
Misalnya, sel asam timbal:
Pb + PbO 2 + 2H 2 SO 4 Debit Muatan 2PbSO 4 + 2H 2 O E° = 2,04 V
Dalam sel Ni-Cd
Debit Cd + 2NiOOH + 2H 2 O Muatan Cd(OH) 2 + 2Ni(OH) 2 E° = 1,32 V
Dalam sel Zn-Cl2 :
Debit Zn + Cl 2 Muatan ZnCl 2 E° = 2,12 V
Dalam sel Daniel (Ini adalah sel primer; di sini perhatikan tidak adanya panah reversibel)
Debit Zn + Cu 2+ Muatan Zn 2+ + Cu(s) E° = 1,1 V
Menyamakan tegangan pengisian: lebih banyak tentang pengisian baterai
Seperti dijelaskan di atas, baterai penyimpanan bukanlah sumber daya yang abadi. Setelah habis, itu harus diisi ulang untuk mendapatkan daya darinya lagi. Baterai diharapkan memberikan masa pakai tertentu, yang disebut harapan hidup. Untuk mendapatkan masa pakai dan keandalan yang dirancang, baterai penyimpanan harus diisi dan dirawat dengan benar sesuai instruksi yang diberikan oleh pabrikan. Metode pengisian daya yang tepat harus digunakan untuk mendapatkan masa pakai baterai semaksimal mungkin.
Reaksi dalam sel asam timbal:
Selama pelepasan : PbO 2 + Pb + 2H 2 SO 4 2PbSO 4 + 2H 2 O
Pelepasan akan berlangsung hanya sampai sejumlah bahan penghantar tertentu ada di dalam sel; setelah itu laju penurunan tegangan akan sangat cepat sehingga tegangan akhir akan segera tercapai. Jadi ada yang disebut cut-off voltage atau tegangan akhir, di luar itu pelepasan tidak boleh dilanjutkan. Pengosongan lebih lanjut akan membuat pengisian ulang menjadi sulit dan dapat menyebabkan hasil bencana yang tidak terduga.
Baterai harus diisi segera setelah dikosongkan dengan kecepatan yang direkomendasikan oleh pabrikan atau sesuai dengan instruksi yang diberikan oleh mereka.

Apa yang terjadi selama reaksi pelepasan dan pengisian di dalam sel?
Elektrolit: 2H 2 SO 4 = 2H + + 2HSO 4‾
Pelat negatif: Pb° = Pb 2+ HSO 4 + 2e
Pb 2+ + HSO 4‾ = PbSO4 + H +
⇑ ⇓
Pelat positif: PbO 2 = Pb 4+ + 2O 2-
Pb 4+ + 2e = Pb 2+
Pb 2+ + 3H + + HSO 4‾ +2O 2- =PbSO 4 + 2H 2 O
Asam sulfat menjadi elektrolit kuat, ia dipisahkan sebagai ion hidrogen dan ion bisulfat (juga disebut ion hidrogen sulfat).
Saat memulai pelepasan, timbal berpori di pelat negatif teroksidasi menjadi ion timbal (Pb2+) dan karena selalu kontak dengan elektrolit asam sulfat, ia diubah menjadi timbal sulfat (PbSO4); yang terakhir akan disimpan sebagai bahan putih pada pori-pori, permukaan dan retakan pelat negatif. Reaksi yang pertama (timbal menjadi ion timbal) bersifat elektrokimia sedangkan yang kedua (ion timbal menjadi timbal sulfat) adalah reaksi kimia.
Kami mengatakan bahwa timbal larut sebagai ion timbal di sekitar lokasi reaksi dan segera mengendap sebagai timbal sulfat setelah bergabung dengan ion bisulfat dari elektrolit pada bahan aktif negatif (NAM). Jenis reaksi seperti itu disebut mekanisme disolusi-deposisi atau disolusi-presipitasi dalam elektrokimia .
Demikian pula, bahan aktif positif (PAM) bergabung dengan elektron yang berasal dari NAM dan menjadi ion timbal, yang bergabung dengan ion bisulfat dari elektrolit dan mengendap sebagai timbal sulfat pada bahan aktif positif, mengikuti mekanisme disolusi-deposisi yang sama.
Selama pengisian ulang: 2PbSO4 + 2H2O Muatan→ PbO2 + Pb + 2H2SO4
Produk reaksi yang diperoleh selama pelepasan pada pelat positif dan negatif diubah kembali ke bahan aslinya selama pengisian. Di sini, reaksi memiliki sebutan kebalikan dari pelepasan. Pelat positif mengalami oksidasi, sedangkan pelat polaritas yang berlawanan mengalami reduksi.
Menyamakan biaya: Kapan pengisian penuh selesai?
Baterai dianggap telah menyelesaikan pengisian normal jika kondisi berikut terpenuhi:
| Parameter | Baterai Asam Timbal Terbanjiri | Baterai Asam Timbal yang Diatur Katup (VRLA) |
|---|---|---|
| Tegangan & arus pengisian | Muatan arus konstan diasumsikan di sini: tegangan baterai pada akhir pengisian harus konstan untuk arus tertentu. Nilainya mungkin 16,2 hingga 16,5v untuk baterai aa 12v | Untuk tegangan yang terkesan konstan (katakanlah 13.8v hingga 14.4v untuk baterai 12v), arus harus konstan setidaknya selama dua jam |
| Berat jenis elektrolit | Berat jenis elektrolit juga harus mencapai nilai konstan. Nilai ini akan tergantung pada baterai yang terisi penuh saat dipasok oleh pabrikan. | Berat jenis elektrolit tidak dapat diukur. |
| Sifat dari penyerangan dengan gas | Pelepasan gas yang seragam dan berlebihan di kedua pelat. Volume gas yang berkembang akan menjadi 1:2 seperti dalam air, yaitu, 2 volume hidrogen untuk 1 volume oksigen. | Pada tingkat tegangan pengisian yang direkomendasikan untuk VRLAB, gas yang dapat diabaikan diamati. Pada muatan mengambang 2,25 hingga 2,3 volt per sel (Vpc), tidak ada evolusi gas yang diamati. Pada 2,3 Vpc, VRLAB 12V 100Ah dapat memancarkan baterai 8 hingga 11 ml/jam/12V. Tetapi pada 2,4 Vpc hampir dua kali lipat, baterai 18 hingga 21 ml/jam/12V. (i. Baterai pbq VRLA, Januari 2010. ii. Teknologi C&D: Buletin Teknis 41-6739, 2012.) |
Equalizing Charge: apa yang dimaksud dengan equalizing charge untuk baterai
- Baterai asam timbal yang baru dirakit memerlukan pengisian awal dan pengisian awal.
- Baterai yang habis memerlukan pengisian ulang normal.
- Baterai yang terhubung ke peralatan dan perlengkapan biasanya tidak terisi penuh, dalam artian baterai tidak mencapai tegangan pengisian penuh sebesar> 16 V untuk baterai 12V. Sebagai contoh, pada aplikasi SLI (starting, lighting dan ignition) pada mobil, tegangan maksimum yang dapat dicapai baterai adalah sekitar 14,4 V untuk baterai 12V. Demikian pula, tegangan pengisian baterai inverter/UPS tidak melebihi 13,8 hingga 14,4 V. Dalam aplikasi seperti itu, proses akumulasi timbal sulfat yang tidak terkonversi di pelat positif dan negatif terus meningkat seiring dengan bertambahnya usia baterai.
Alasannya adalah bahwa nilai tegangan yang disebutkan di atas tidak cukup untuk mengembalikan semua produk yang dilepaskan ke bahan aktif aslinya. Baterai semacam itu memerlukan pengisian ulang secara berkala untuk membawa semua sel ke muatan penuh dan ke tingkat yang sama. Ini juga akan membantu menghilangkan efek stratifikasi elektrolit. Pengisian alat ekstra semacam itu disebut muatan bangku atau muatan penyeimbang.
Kesimpulan tentang Equalizing charge:
Biaya pemerataan adalah bagian dari prosedur pemeliharaan. Tegangan maksimum di mana muatan pemerataan dapat dilakukan tergantung pada jenis baterai asam timbal, apakah itu jenis banjir atau jenis VRLA. Jenis sel sebelumnya dapat diisi pada arus konstan hingga tegangan 16,5 V untuk baterai 12V untuk membawa semua sel dalam baterai ke tingkat yang sama.
Namun, sel VRLA harus diisi hanya dengan metode tegangan konstan dan tegangan ini tidak boleh melebihi tegangan maksimum yang disarankan yaitu 14,4 V untuk baterai 12V. Jika fasilitas pengisian tegangan konstan tidak tersedia, baterai VRLA dapat diisi pada arus konstan dengan pemantauan konstan tegangan terminal (TV) baterai. Setiap kali TV mendekati atau melebihi level 14,4 V, arus pengisian harus terus dikurangi sehingga TV tidak boleh melebihi 14,4 V