Carga de la batería, ¡de la forma correcta!
Una batería es un dispositivo electroquímico que almacena energía en una estructura de enlace químico y libera la energía en forma de electrones resultantes de las reacciones de descarga química de la batería. La carga de la batería proporciona los electrones para reformar los enlaces químicos que se almacenan en los materiales activos de la batería. Esto es válido para la carga de baterías de todas las químicas, incluidas las mencionadas en este blog: plomo-ácido, níquel-hidruro metálico, níquel-cadmio y variantes de iones de litio. En este blog, hablaremos de los procedimientos de carga óptimos para las baterías de 12 voltios.
Por regla general, hay tres tipos principales de cobro:
– Tensión constante (CV)
– Corriente constante (CC)
– Potencia constante (carga cónica)
Todos los perfiles de carga y todos los equipos de carga utilizan variantes, a menudo combinadas, de estos métodos básicos.
La velocidad de carga de la batería depende del número de electrones que fluyen por segundo (corriente) en la batería. La velocidad del flujo eléctrico, al igual que la de la luz, es fija, por lo que para aumentar la tasa de carga hay que aumentar la densidad de corriente o el número de amperios que fluyen por segundo. Si se aumenta la fuerza que empuja a los electrones hacia el AM, es decir, el voltaje, se incrementa el flujo de electrones. Mayores voltios = más amperios.
El voltaje y la resistencia interna de los diferentes tipos de baterías dependen de su química y los voltajes de carga variarán en consecuencia. En este blog, consideraremos las baterías de plomo-ácido, las de iones de litio, las de níquel-cadmio y las de níquel-hidruro metálico.
Empezando por el plomo-ácido, podemos describir las reacciones químicas que almacenan y descargan electrones, descritas como la «Teoría del doble sulfato»
- PbO2 + Pb + 2H2SO4 = 2PbSO4 + 2H2O……………………………………..eq. 1
En esta reacción el electrolito, ácido sulfúrico diluido, se convierte en agua al reaccionar con las placas positivas y negativas durante la descarga. La placa negativa se oxida al ceder electrones para formar sulfato de plomo y la positiva se reduce de óxido de plomo a sulfato de plomo al aceptar electrones para convertir el dióxido de plomo en sulfato de plomo. Durante este tiempo, la producción de agua provoca la dilución del electrolito ácido y la reducción de la diferencia de potencial entre las placas. Esto produce una menor SG del electrolito y un menor voltaje de la batería. En la carga de la batería, esto se invierte. Estos dos parámetros, la tensión de la batería y la SG del electrolito, son por tanto medidas del estado de carga de una batería de plomo.
La carga de una batería de plomo-ácido de 12 voltios requiere una tensión superior a la tensión de reposo de la batería cuando está completamente cargada, que normalmente se sitúa entre 12,60 y 12:84 para una batería nueva inundada y entre 12:84 y 13,08 para una batería nueva VRLA. Existen cuatro variantes básicas de baterías de plomo-ácido: inundadas de placa plana, inundadas tubulares y las versiones VRLA que son AGM (de placa plana) y GEL (principalmente tubulares). Los tipos de baterías, sus aplicaciones y los métodos de carga asociados se indican en la Tabla 1.
| Tipo de batería | Método de carga normal de la batería |
|---|---|
| Método de carga de la batería de plomo de placa plana inundada |
Carga cónica de corriente constante Carga cónica de corriente constante/tensión constante Carga cónica de tensión constante |
| Método de carga de la batería de plomo de placa tubular inundada |
Carga cónica de corriente constante Carga cónica de corriente constante/tensión constante Carga cónica de tensión constante |
| Método de carga de la batería VRLA de plomo (AGM SMF) |
Carga de corriente constante/tensión constante Carga a tensión constante Carga de corriente constante/tensión constante con impulso |
| Método de carga de baterías VRLA de gel tubular de plomo-ácido |
Carga de corriente constante/tensión constante Carga a tensión constante Carga de corriente constante/tensión constante con impulso |
| Método de carga de baterías de níquel-cadmio |
Corriente constante lenta con temporizador sin control Corriente constante con corte dT/dT Corriente constante con corte -dV/dT |
| Método de carga de la batería de iones de litio |
Corriente constante con corte de corriente final Corriente constante con corte de tensión Tensión constante con corte de corriente final |
Tabla 1 – Diferentes tipos de baterías y los métodos de carga pertinentes de los diferentes tipos de química de las baterías
- CC = corriente constante
- CV = tensión constante
- dT/dt = pendiente de la temperatura
- -dV/dt – pendiente de tensión negativa
Los métodos de cobro enumerados se describen a continuación:
- Carga de corriente constante
En este tipo de carga, la tensión aumenta a medida que la carga de la batería se completa. La corriente se limita a un valor que mantiene la tensión y la temperatura de la batería a niveles bajos. Por lo general, hay un temporizador para apagar el cargador para evitar una excesiva pérdida de gas y agua y reducir la corrosión de la red positiva Fig. 1a. Este método de carga no es adecuado para las baterías de plomo-ácido selladas o de bajo mantenimiento.
- Tensión constante, carga cónica limitada por la corriente
Con una carga de tensión limitada, el problema de la evolución del gas se minimiza o incluso se erradica. En la Fig.1b vemos que la tensión alcanza un pico, generalmente entre 13,38 y 14,70 voltios para una batería de 12 voltios. Es evidente que la corriente disminuye rápidamente una vez que se alcanza la tensión de carga máxima. Este tipo de carga suele durar mucho tiempo debido a los bajos niveles de corriente en la última etapa de carga. Por lo general, se utiliza para los SAI o la energía de reserva cuando hay largos períodos de carga.
- Carga de la cinta
Se trata de la forma más sencilla del cargador, normalmente basado en un transformador, que proporciona una potencia constante, es decir, vatios. La corriente disminuye a medida que aumenta la tensión, lo que mantiene una entrada de energía constante en la batería. La Fig.1c muestra una curva típica en la que la corriente se reduce a medida que aumenta la tensión de la batería. El EMF posterior también aumenta con el estado de carga SOC, lo que significa que la corriente caerá a niveles muy bajos ya que la batería no puede consumir más energía.
- Este tipo de cargador no es adecuado para las baterías de plomo-ácido selladas y sin mantenimiento, ya que la cantidad de gas generada depende de la tensión de la batería. En este caso, se podrían alcanzar tensiones de carga de hasta 16 ó 17 voltios, lo que provocaría una grave evolución de los gases y abriría la válvula de alivio de presión con la consiguiente pérdida de agua.
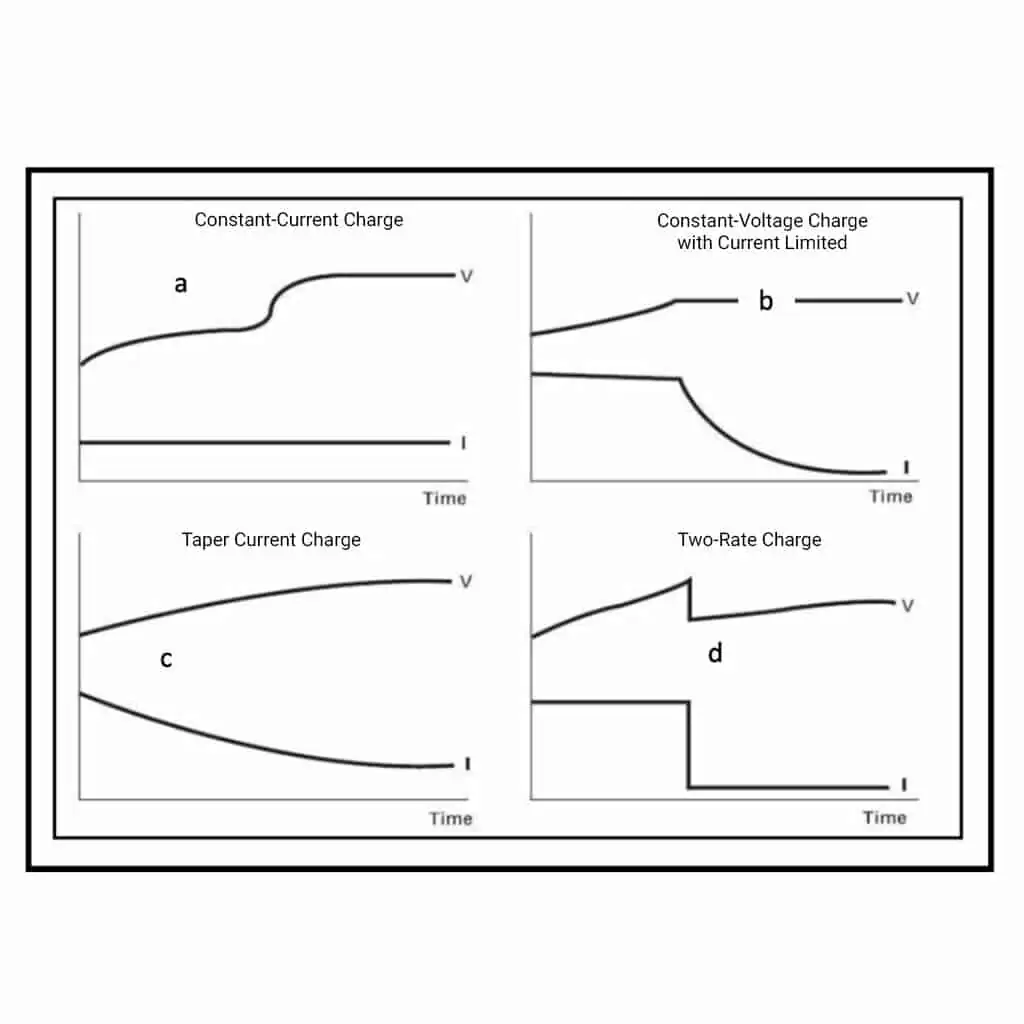
- Carga limitada en dos etapas de corriente y tensión
Otro perfil de carga popular se muestra en la Fig. 1d. De esta forma, se deja que la tensión aumente en la fase de masa hasta alcanzar la tensión de gaseado. A continuación, la corriente desciende a un nivel fijo bajo para reducir la tensión, que aumenta gradualmente hasta el nivel de gaseado. Por lo general, hay un tiempo de corte vinculado al tiempo de carga inicial de la fase masiva. Esto permite un periodo de gaseo fijo y una entrada de amperios-hora fija basada en el estado de carga de la batería
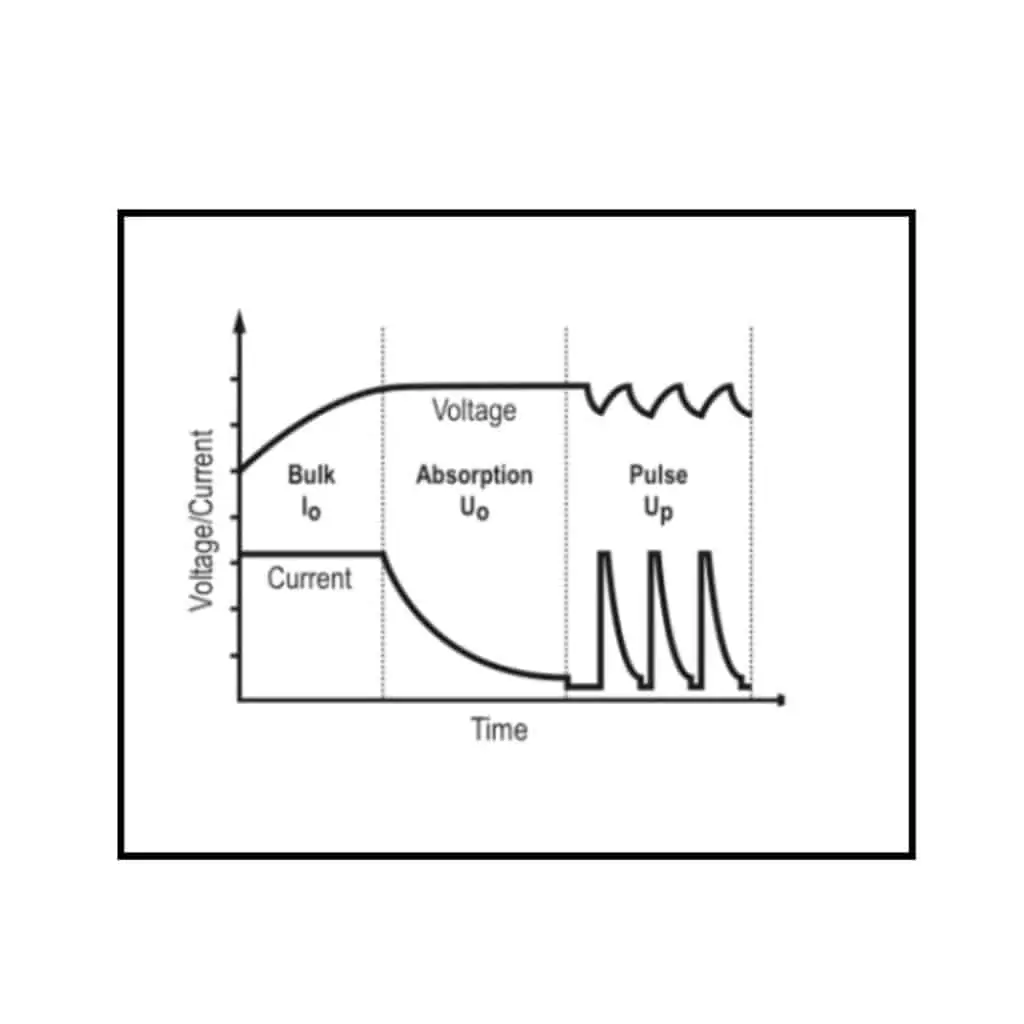
- Carga masiva de tensión limitada con impulso de corriente constante de ecualización.
Fig. 2 es una representación de un método común de carga por pulsos. Esto es generalmente beneficioso para los usuarios de baterías VRLA que tienen un tiempo limitado para recargar completamente sus baterías. En este método, hay una fase CC y CV donde se aplica la mayor parte de la carga.
- El pulso suele ser una ráfaga de corriente de 10 a 20 segundos con restricción de tensión, seguida de una pausa de hasta un par de minutos. Como la tensión va por detrás de la corriente, que tiene una duración limitada, no alcanza los niveles máximos antes de apagarse. De este modo, se restringe la evolución de los gases y el tiempo de pausa entre los pulsos de corriente permite que los gases se recombinen en agua, evitando la desecación.
Los comentarios hasta ahora se han dirigido a las baterías de plomo-ácido. La carga de las baterías de iones de litio, NiCd y NiMH requiere algoritmos de carga diferentes a los de las baterías de plomo. Empezando por la batería de iones de litio, lo primero que hay que tener en cuenta es que existen diferentes voltajes de carga para los distintos cátodos de iones de litio. Un ion de litio -FePO4 funciona a 3. 2V por celda mientras que un Li-Co es de 4,3v por celda. Esto significa que no puedes utilizar el mismo cargador para ambas baterías.
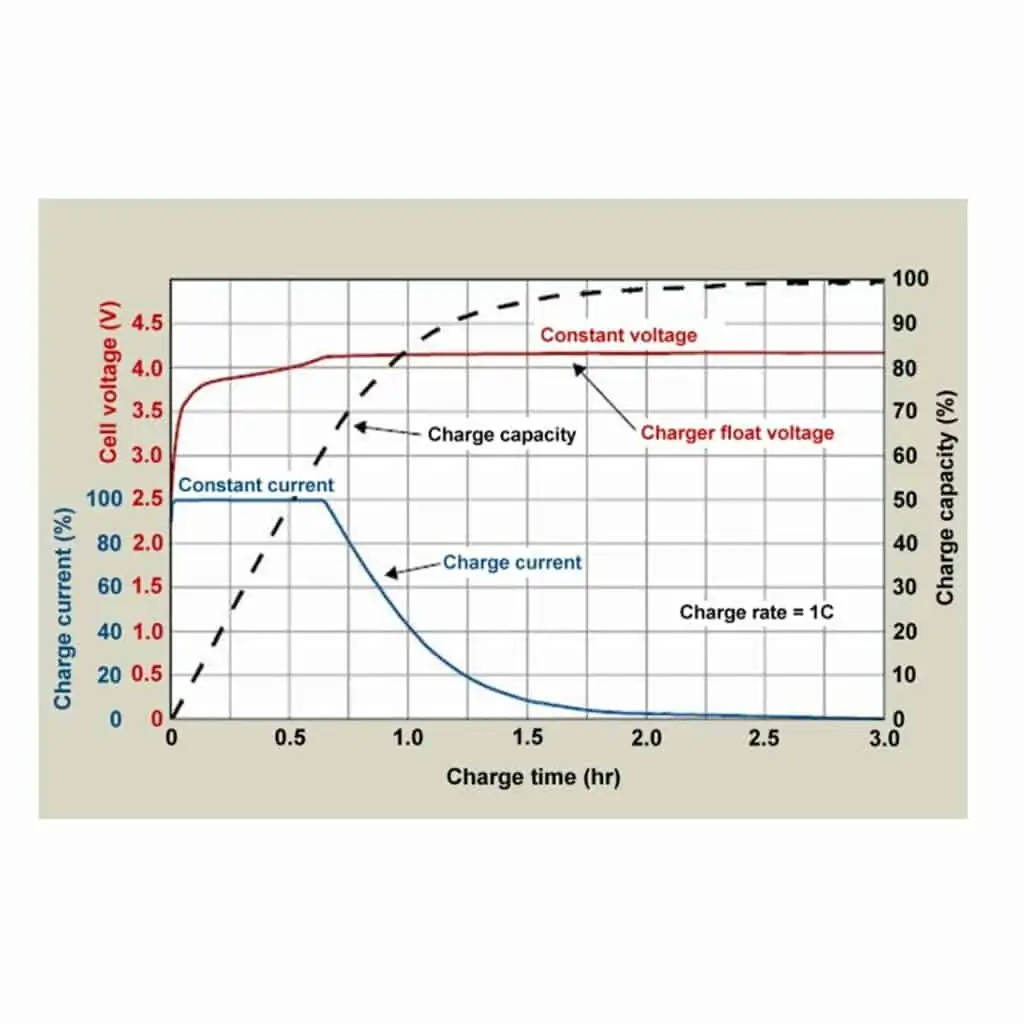
Sin embargo, el principio general es el mismo para todos los tipos de baterías de iones de litio y bastante diferente de una batería de plomo. Como no hay reacción química durante los procesos de carga y descarga, la transferencia es rápida a velocidades muy altas limitadas por la salida del cargador o el BMS (sistema de gestión de la batería). Normalmente, son habituales las tasas de entre 0,1C y 1C a corriente constante con corte de tensión. La figura 3 muestra un perfil de carga típico de una célula de iones de litio. El periodo de carga también puede finalizar cuando se alcanza una corriente mínima en torno al 2-3% del valor del amperaje de 1C.
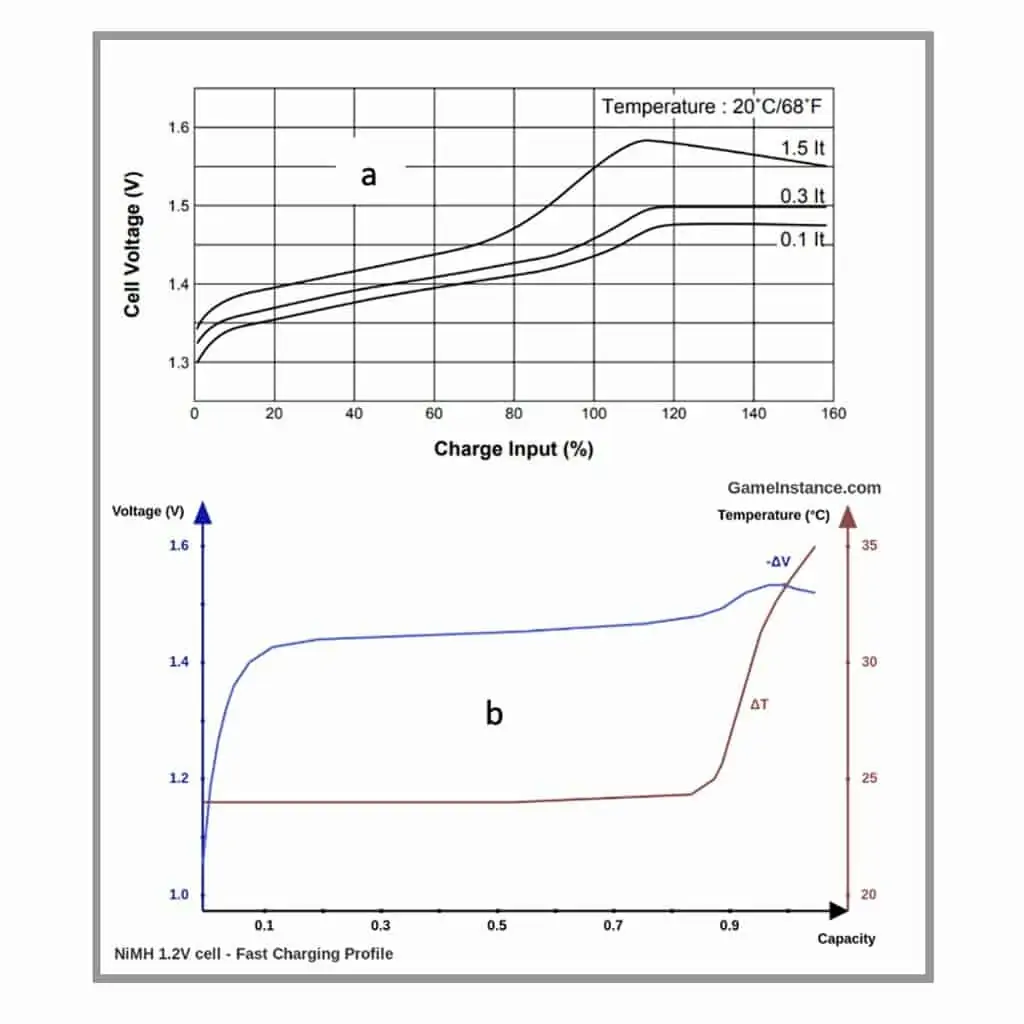
El NiMH y el NiCd también tienen diferentes patrones de carga y respuestas muy diferentes a la carga, tanto a otras químicas como entre sí. La Fig. 4 muestra un patrón de carga típico para ambos Ni-Cad (a) y NiMH (b). Aunque ambas variantes de níquel tienen la misma tensión de reposo y de funcionamiento, la tensión de carga puede variar considerablemente. Un cargador de ambos tipos no puede depender de la tensión como mecanismo de terminación de la carga. Por esta razón, los cargadores utilizan simplemente un cargador de corriente constante de una o dos etapas con una terminación basada en el tiempo, la pendiente de la tensión y el cambio de temperatura de la pendiente. El examen de las características de la carga muestra que hay tanto un aumento de la temperatura como una caída simultánea de la respuesta de la tensión cuando la carga alcanza el 100%.
Estas características se utilizan para determinar el final de la carga. Dado que la tensión absoluta varía con la temperatura y es diferente para ambos tipos de células. El inicio de la pendiente negativa de la tensión (-dV/dt) o el aumento rápido de la pendiente de la temperatura (dT/dt), son las características más utilizadas. Si se utiliza un método de temporización, la corriente debe ser muy baja para evitar la sobrecarga y la pérdida de oxígeno. En algunos casos, especialmente con celdas o baterías desequilibradas, es mejor descargar hasta 0,9-1,0 voltios por celda antes de cargar con el método del temporizador.
¿Cómo funciona un cargador de baterías?
Todos los cargadores toman la energía de la red de corriente alterna (CA) y la convierten en corriente continua. En el proceso, habrá algunas ondulaciones de CA que deben mantenerse por debajo del 3%. Algunos de los cargadores de baterías del mercado tienen funciones para filtrar las ondas, que de otro modo dañarían la batería durante la carga. En cualquier caso, es mejor utilizar una alimentación trifásica, ya que la corriente monofásica tiene una ondulación del 10%.
Todos los cargadores toman la energía de la red de corriente alterna (CA) y la convierten en corriente continua. En el proceso, habrá algunas ondulaciones de CA que deben mantenerse por debajo del 3%. Algunos de los cargadores de baterías del mercado tienen funciones para filtrar las ondas, que de otro modo dañarían la batería durante la carga. En cualquier caso, es mejor utilizar una alimentación trifásica, ya que la corriente monofásica tiene una ondulación del 10%.
Cargador de tensión constante
La tensión constante permite que toda la corriente del cargador de baterías fluya hacia la batería hasta que la fuente de alimentación alcance su tensión preestablecida. La corriente disminuirá hasta un valor mínimo cuando se alcance ese nivel de tensión. La batería puede dejarse conectada al cargador hasta que esté lista para su uso y permanecerá a esa «tensión de flotación», cargándose a cuentagotas para compensar la autodescarga normal de la batería.
Tensión constante Corriente constante
La tensión/corriente constante (CVCC) es una combinación de los dos métodos anteriores. El cargador limita la cantidad de corriente a un nivel preestablecido hasta que la batería alcanza un nivel de tensión preestablecido. A continuación, la corriente se reduce a medida que la batería se carga por completo. La batería de plomo utiliza el método de carga de corriente constante y tensión constante (CC/CV). Una corriente regulada eleva la tensión de los terminales hasta que se alcanza el límite superior de la tensión de carga, momento en el que la corriente cae por saturación.
Diferentes tipos de cargadores de baterías
La tecnología actual de carga de baterías se basa en microprocesadores (chips de ordenador) para recargar, utilizando 3 pasos de carga regulada. Estos son los «cargadores inteligentes». Son fáciles de conseguir. Los tres pasos de la carga de las baterías de plomo son las principales entradas de corriente para la conversión, y la carga de flotación en un período continuo. Es necesario realizar una carga de ecualización periódica para mantener la uniformidad. Utilice las recomendaciones del fabricante de la batería sobre los procedimientos de carga y los voltajes o un cargador de calidad controlado por microprocesador para mantener la capacidad y la vida útil de la batería.
Los «cargadores inteligentes» están perfilados teniendo en cuenta la tecnología de carga contemporánea, y también toman información de la batería para proporcionar el máximo beneficio de carga con la mínima observación.
VRLA – Las baterías de gel y AGM requieren diferentes ajustes de voltaje. Esto es para evitar el gaseado y la desecación. El proceso de recombinación de oxígeno en una batería de plomo-ácido regulada por válvula (VRLA) requiere un ajuste de tensión más bajo para evitar la evolución del hidrógeno y el secado de la celda.
La tensión máxima de carga de las baterías de gel es de 14,1 ó 14,4 voltios, que es inferior a la que necesita una batería de tipo húmedo o AGM VRLA para una carga completa. Superar esta tensión en una batería de gel puede provocar burbujas en el gel electrolítico y daños permanentes.
La clasificación de corriente de los cargadores de baterías recomienda dimensionar el cargador a una corriente máxima del 25% de la capacidad de la batería. Algunas baterías especifican el 10% de la capacidad Es más seguro utilizar una corriente menor, aunque se tarda más.
Un método de carga de corriente y tensión constantes (CCCV) es una buena opción. Una corriente constante aumenta la tensión en los terminales hasta que se alcanza el límite superior de la tensión de carga, momento en el que la corriente cae por saturación. El tiempo de carga es de 12 a 16 horas y mayor (36 horas) para las grandes baterías estacionarias. La batería de plomo es más lenta y no puede cargarse tan rápidamente como otros sistemas de baterías. Con el método CCCV, las baterías de plomo-ácido se cargan en tres pasos, [1] carga de corriente constante, [2] tensión constante y [3] carga de flotación al finalizar la carga.
La carga de corriente constante aplica la mayor parte de la carga y ocupa aproximadamente la mitad del tiempo de carga necesario; la carga de relleno continúa a una corriente de carga inferior y proporciona la saturación, y la carga de flotación continua compensa la pérdida causada por la autodescarga. Durante la carga de corriente constante, la batería se carga hasta un 70% en 5-8 horas; el 30% restante se llena con voltaje constante que dura otras 7-10 horas. La carga de flotación en el tercer paso mantiene la batería a plena carga.
Carga de la batería, ¿se puede sobrecargar la batería de 12V?
En todas estas químicas la sobrecarga puede crear daños o riesgos de seguridad. En el caso de las baterías de plomo-ácido, las tensiones de sobrecarga son limitadas y el exceso de corriente se disipa en la descomposición del agua, la liberación de hidrógeno y oxígeno y la creación de calor. El aumento de la corriente no aumentará la tensión, sino que aumentará la tasa de gaseo y de pérdida de agua y provocará un aumento de la temperatura. Se tolera un poco de sobrecarga, especialmente cuando se requiere la ecualización de la celda o de la batería.
En el caso de las baterías de iones de litio, la sobrecarga es difícil debido al BMS incorporado en la batería. Esto cortará el suministro de corriente una vez que se alcance la tensión de terminación, o la temperatura sea demasiado alta. Se trata de una precaución necesaria, ya que las células de iones de litio contienen un electrolito volátil que se desprende a altas temperaturas. Es el vapor del electrolito el que se incendia en las baterías de iones de litio, por lo que la sobrecarga es muy peligrosa. Las baterías de NiCad y NiMH no deben sobrecargarse, ya que perderán oxígeno y, por tanto, electrolito, incluso si son las versiones selladas.
Hay varios indicadores del SOC de una batería: la tensión en reposo medida en sus bornes, la gravedad específica del electrolito (baterías abiertas inundadas) o el valor de la impedancia. Son diferentes para cada química de la batería, y por esta razón, es mejor mirar cada tipo por separado:
1. Plomo-ácido.
Peso específico.
La reacción de las placas con el ácido sulfúrico en la carga y la descarga determina la proporción de ácido y agua en una célula.
Cuando se carga la concentración de ácido sulfúrico es alta, cuando se descarga es menor (ecuación 1). Debido a que la densidad del ácido es de 1,84 y la del agua es de 1 la gravedad específica, SG del electrolito aumenta en la carga y disminuye en la descarga.
La reacción tiene una relación de primer orden, lo que significa que el cambio en la concentración es lineal, por lo que la medición de la SG da una indicación directa del SOC de la batería, Fig. 5.

Una nota de precaución: esto no se aplica cuando la carga de la batería está en curso y en la fase de carga o pregasificación. Sin la agitación del electrolito, el ácido más denso producido en la carga se hundirá, dejando la mayor parte del electrolito más diluido hasta que se alcance una tensión de 2,4 voltios por célula. A partir de este punto, el gas desprendido en las placas creará una acción de agitación para mezclar el ácido.
Tensión de reposo: Puede ser una indicación del SOC y se relaciona con el peso específico de la célula en la siguiente relación:
- Voltios de reposo = SG + 0,84 …………………………………………………………..eq 2
Por ejemplo, una célula de 2V con un peso específico de 1,230 tendrá una tensión en reposo de 1,230 + 0,84 = 2,07 voltios
El uso de esta relación puede dar una indicación razonablemente precisa del SOC de la batería, sin embargo, diferentes baterías tienen diferentes rangos de funcionamiento para la SG y por lo tanto la condición de la parte superior de la carga de un VRLA SG podría ser 1,32 en comparación con un OPzS con una SG superior de 1,28. La temperatura también afecta a la SG y, por tanto, a la tensión de la célula. El efecto de la temperatura sobre la tensión en circuito abierto se indica en la tabla 2.
Otro factor es que las baterías recién cargadas tienen una alta concentración de ácido junto a las placas debido a la formación de ácido sulfúrico en una carga. Por ello, el voltaje después de la carga se mantiene alto durante algún tiempo, quizá hasta 48 horas, antes de estabilizarse en un valor constante. A menos que se haga una descarga corta a la batería, ésta tiene que descansar para permitir la igualación de la concentración de ácido antes de tomar una lectura de tensión.
Herramientas necesarias para la medición del SOC
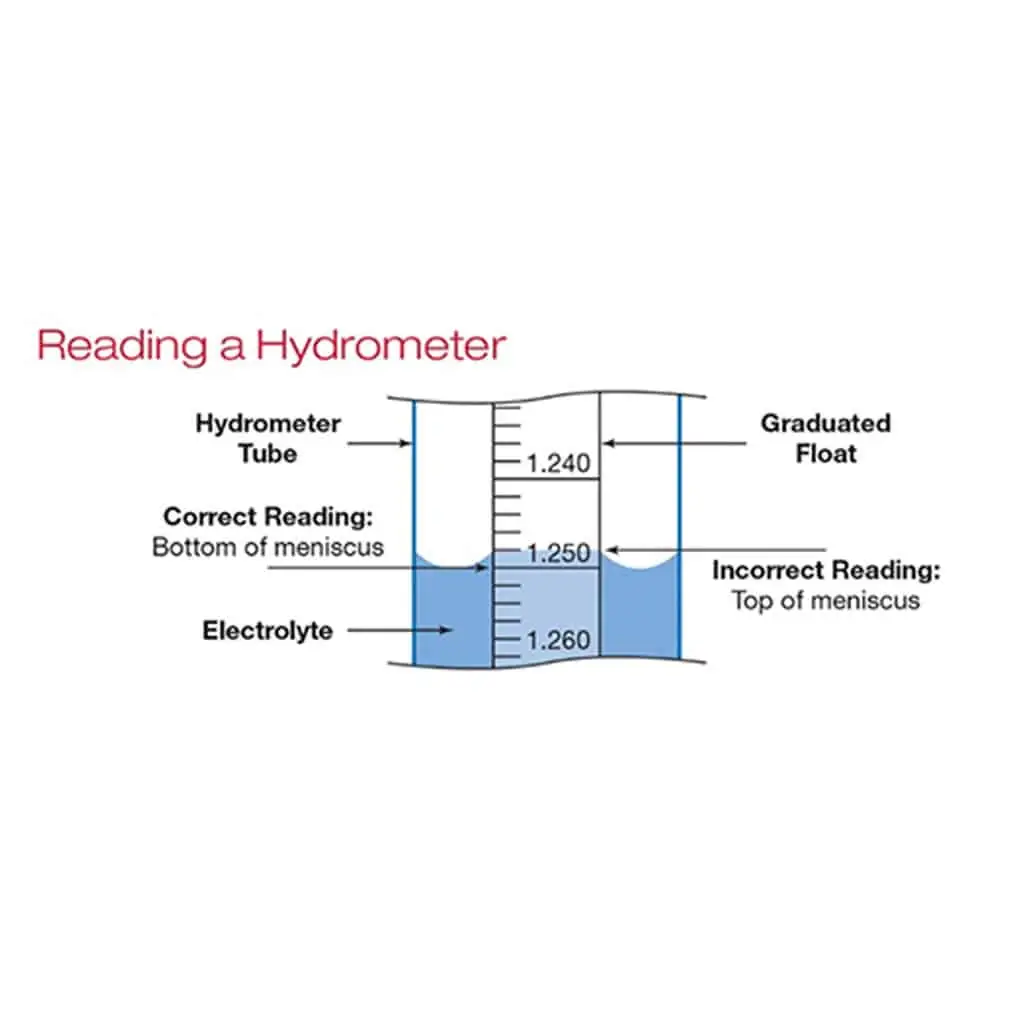
Consisten en un voltímetro de corriente continua o un multímetro para las mediciones de tensión y un hidrómetro para la lectura de la gravedad específica.
Para las celdas inundadas, aparte de la prueba de descarga, el hidrómetro es el mejor método para determinar el estado de carga. El uso del hidrómetro requiere cierta práctica y debe hacerse con mucho cuidado. El procedimiento consiste en colocar la pila en una posición adecuada para poder tomar la lectura del hidrómetro a la altura de los ojos (Fig. 6).
En el caso de las baterías selladas, no es posible utilizar un hidrómetro, por lo que la única opción es la medición de los voltios de reposo. Este método es aplicable tanto a las baterías de plomo-ácido selladas como a las inundadas.
Para ello, el multímetro debe ajustarse a un voltaje máximo adecuado para garantizar que pueda leer más de 12 voltios, pero también producir al menos 2 decimales de precisión. Utilizando la ec. 2, la tensión puede utilizarse, tras el ajuste de la temperatura, para estimar la SG y, por tanto, el SOC de la batería, siempre que se conozca el valor de SG del fabricante para la batería totalmente cargada.
En ambos casos de utilizar la tensión o un hidrómetro para medir el estado de carga, SOC, es necesario aplicar una compensación de temperatura. La tabla 2, suministrada por el ICB, indica los ajustes adecuados para las lecturas del hidrómetro y del medidor de tensión.
Tabla 2 Compensación de la gravedad específica del electrolito y de las lecturas de tensión con la temperatura
| Temperatura del electrolito Fahrenheit (°F) | Temperatura del electrolito Celsius (°C) | Suma o resta a la lectura de SG del hidrómetro | Suma o resta a la lectura del voltímetro digital |
|---|---|---|---|
| 160° | 71.1° | +.032 | +.192 V |
| 150° | 65.6° | +.028 | +.168 V |
| 140° | 60.0° | +.024 | +.144 V |
| 130° | 54.4° | +.020 | +.120 V |
| 120° | 48.9° | +.016 | +.096 V |
| 110° | 43.3° | +.012 | +.072 V |
| 100° | 37.8° | +.008 | +.048 V |
| 90° | 32.2° | +.004 | +.024 V |
| 80° | 26.7° | 0 | 0 V |
| 70° | 21.1° | -.004 | -.024 V |
| 60° | 15.6° | -.008 | -.048 V |
| 50° | 10° | -.012 | -.072 V |
| 40° | 4.4° | -.016 | -.096 V |
| 30° | -1.1° | -.020 | -.120 V |
| 20° | -6.7° | -.024 | -.144 V |
| 10° | -12.2° | -.028 | -.168 V |
| 0° | -17.6° | -.032 | -.192 V |
2. Li-ion, NiMH y NiCd.
Para todas estas químicas, la medición del SOC presenta serios desafíos. Todas tienen una curva de descarga muy plana con una diferencia de tensión muy pequeña entre el estado de carga completa y el de descarga. Las reacciones de carga-descarga dentro de las células de NiCd y NiMH no alteran de forma apreciable el SG del electrolito y todas las químicas de iones de litio funcionan con células completamente selladas. Esto hace que las comprobaciones estáticas o aleatorias de una batería en servicio sean casi imposibles, ciertamente para un usuario no profesional. El estado actual de las mediciones del estado de carga, SOC, para estas químicas se basa en lecturas dinámicas tomadas durante su funcionamiento.
Pueden basarse en el recuento de amperios-hora, en la respuesta de la tensión a las corrientes de descarga o incluso en pulsos de corriente constante. Los equipos de medición suelen estar integrados en dispositivos caros o sofisticados, como vehículos eléctricos o máquinas industriales, en los que es necesario conocer el tiempo de funcionamiento disponible. En equipos menos sofisticados, como las herramientas eléctricas manuales, la única indicación disponible es notar que la herramienta se detiene o funciona con menos rapidez.
Existen probadores comerciales de espectrómetros de impedancia que miden la impedancia interna de una batería para predecir su estado de carga. Estos dispositivos dependen de un algoritmo basado en la prueba de cientos de baterías en distintos estados de carga y de distintas edades para predecir el SOC. Los resultados son específicos para la química y la edad de una batería en particular. Cuantas más pruebas se hayan realizado para elaborar el algoritmo, más preciso será éste.
Mientras se carga la batería, ¿se puede sobrecargar una batería?
Independientemente de cómo se decida medir el estado de carga, hay reglas que se aplican a todos los tipos de baterías. Sirven para evitar la sobredescarga de una batería, que puede dañar las celdas individuales haciendo que entren en reversa, incluso que tengan tensiones negativas. La sobrecarga es menos clara, ya que en el caso del plomo-ácido a veces es necesario hacerlo para igualar las celdas o las baterías individuales de un banco. Sin embargo, una sobrecarga excesiva provoca la formación de gases con pérdida de agua y la corrosión de las placas positivas, lo que reduce la vida útil de la batería.
En el caso de las baterías con base de níquel, la pérdida de agua es el problema más común, lo que también conduce a la reducción de la vida útil. En el caso de las baterías de litio, normalmente es imposible sobrecargarlas debido al BMS incorporado que corta automáticamente la entrada de corriente a un voltaje preestablecido. En algunos diseños, hay un fusible incorporado que evita la sobrecarga. Sin embargo, esto suele inutilizar la batería de forma irreversible.
Carga de la batería, sobrecarga ¿cómo evitarla?
La decisión de recargar una batería depende de las circunstancias de uso y del grado de descarga. Como regla general para todas las químicas, la batería no debe bajar del 80% de DOD para maximizar su vida útil. Esto significa que el SOC final de la batería debe calcularse desde el punto de medición hasta el final de su funcionamiento diario. Si, por ejemplo, el SOC es del 40% al comienzo de la operación y va a utilizar el 70% de su capacidad al final de la misma, entonces la batería debe recargarse antes de permitir que continúe.
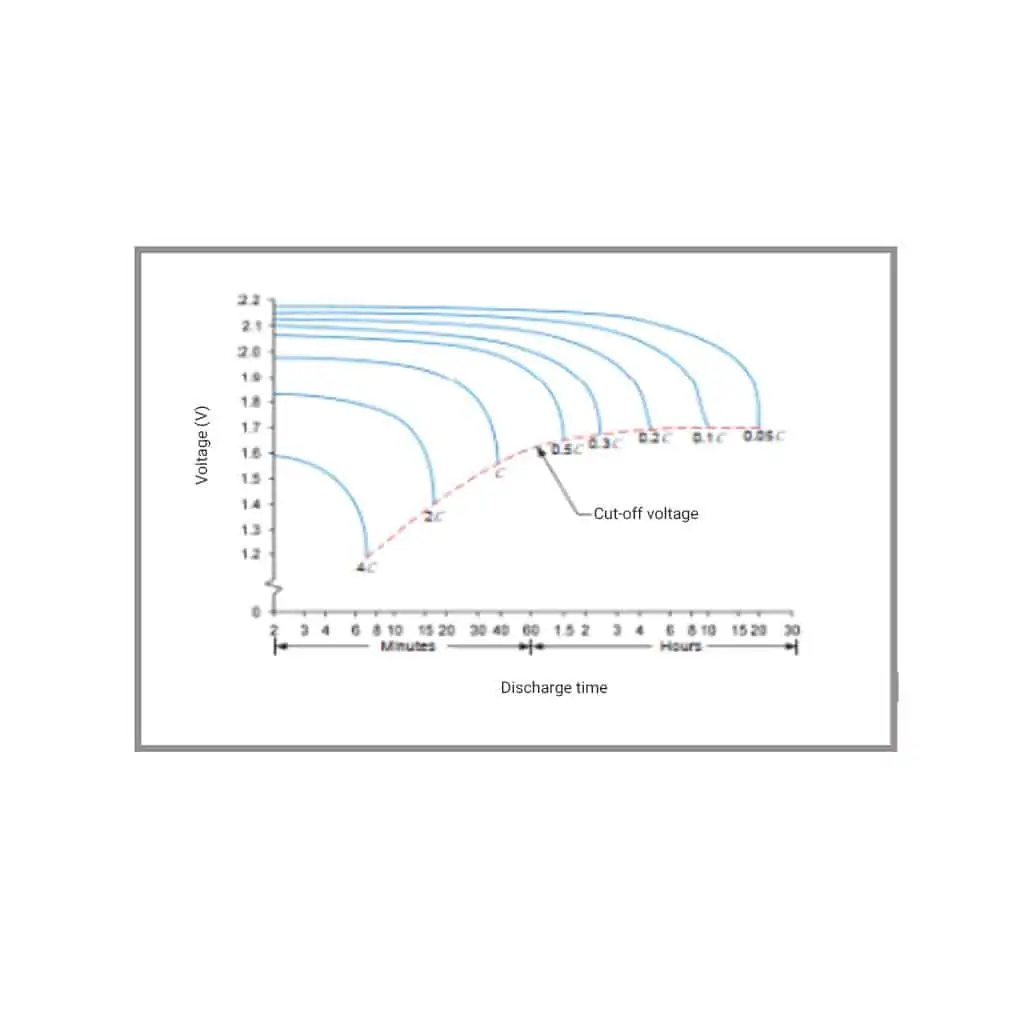
Para tomar esta decisión es necesario determinar la capacidad restante o el tiempo de funcionamiento que le queda a la batería. Esto no es sencillo, ya que la capacidad de la batería viene determinada por la velocidad de descarga. Cuanto mayor sea la tasa de descarga, menor será la capacidad disponible. Las baterías de plomo-ácido son muy susceptibles a esto, como se muestra en la Fig.8.
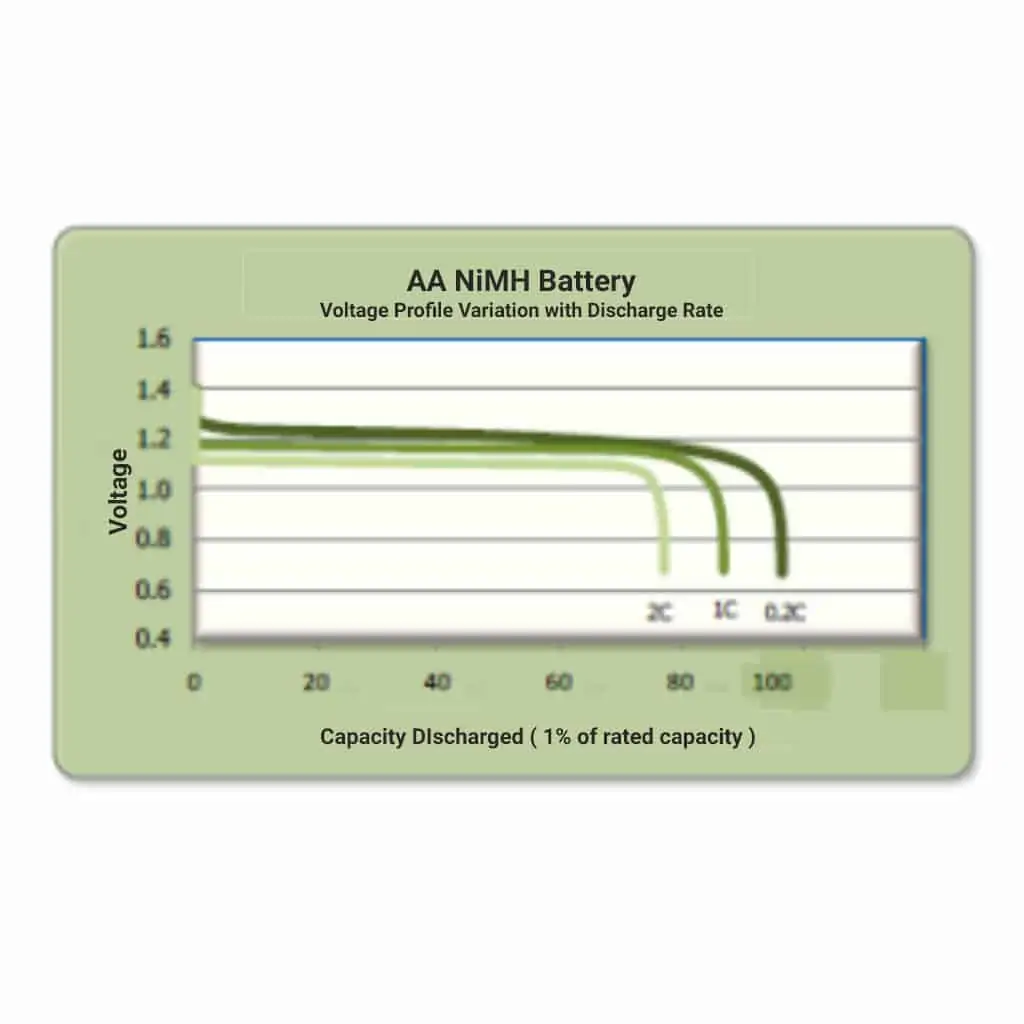
Las baterías de iones de litio y de NiCd tienen capacidades reducidas a tasas de descarga más altas, pero no son tan pronunciadas como las de plomo-ácido. Fig. 9 muestra el efecto de 3 tasas de descarga diferentes en la capacidad disponible de una batería de NiMH. En este caso, 0,2C (tasa de 5 horas), 1C (tasa de 1 hora) y 2C (tasa de 1/2 hora).
En todos los casos, el perfil de tensión se mantiene muy plano, pero a un nivel reducido, hasta el final del período de descarga, cuando la tensión se desploma repentinamente.
Carga de la batería: cálculo de los tiempos de carga y descarga de la batería
Cálculo de los tiempos de carga y descarga de la batería
Para establecer el tiempo de descarga de cualquier batería en un determinado estado de carga, hay que conocer la corriente consumida y la capacidad de la batería a una determinada velocidad de descarga. El tiempo de funcionamiento puede calcularse de forma aproximada utilizando una regla general para cada tipo de batería.
El conocimiento de la capacidad efectiva a una determinada tasa de descarga permitirá predecir el tiempo de funcionamiento de la siguiente manera:
Capacidad estándar de la batería (amperios hora) = C
Corriente de descarga (amperios) = D
Factor de descarga = D/C = N
Velocidad de descarga (amperios) = NC
Capacidad a la tasa de descarga D (amperios hora) = CN
Tiempo de descarga de una batería completamente cargada (horas) = CN /D
Utilizando la estimación del estado de carga como porcentaje, se puede calcular el tiempo de funcionamiento:
Tiempo de funcionamiento = % de estado de carga x CN /(100xD) = horas
El cálculo del tiempo de carga es complejo, ya que depende del estado de carga de la batería, del tipo de batería, de la potencia del cargador y del tipo de cargador. Es necesario conocer el estado de carga de la batería para determinar los amperios-hora que hay que introducir en la batería para recargarla. La velocidad a la que esto ocurre depende de la potencia del cargador y de cómo se cargue. Está claro que una batería de iones de litio puede recargarse en un par de horas desde que está completamente descargada si el cargador tiene suficiente potencia.
Una batería de plomo sellada con limitación en la salida del cargador tardará mucho más debido a la restricción de la tensión y a la reducción de la corriente en la fase de gasificación. Una vez que se determina el estado de carga, se puede calcular cuántos amperios-hora se necesitan para devolver a la batería. Conocer las características del cargador ayudará a realizar el cálculo del tiempo en función del ritmo de carga teniendo en cuenta el patrón de carga utilizado.
Otro factor es la temperatura ambiente (condiciones meteorológicas) que afecta a la tensión de carga y a la corriente que consume el cargador. Las temperaturas más elevadas reducirán la tensión de carga, pero también aumentarán la corriente consumida. Para las baterías en carga de flotación, es necesario aplicar una compensación de tensión con la temperatura. Microtex puede asesorar sobre el ajuste necesario cuando las temperaturas varían significativamente de los 25°C estándar.
Últimas palabras sobre la carga de la batería
Cargar correctamente la batería y conocer su estado de carga no es sencillo. A menudo, las baterías se compran sin ningún tipo de asesoramiento o servicio de apoyo por parte del vendedor. Por eso es importante comprar a un proveedor de confianza que dé prioridad a la satisfacción del cliente. Para asesorarse sobre cualquier mantenimiento o instalación de carga de baterías, lo mejor es ponerse en contacto con un proveedor profesional de confianza.
Como siempre, Microtex, un fabricante internacional de baterías con una trayectoria impecable de satisfacción del cliente, está siempre a mano para ayudar. Es una de las pocas empresas que tiene los conocimientos y los productos necesarios para suministrar y mantener baterías para prácticamente todas las aplicaciones industriales y de consumo. Si la carga de la batería te deja sin batería, ponte en contacto con la gente que no lo hace.
Para toda la carga de baterías, asuntos
póngase en contacto con Microtex.