Chargement de la batterie, la bonne méthode !
Une batterie est un dispositif électrochimique qui stocke l’énergie dans une structure chimiquement liée et libère l’énergie sous forme d’électrons résultant des réactions de décharge chimique de la batterie. La charge de la batterie fournit les électrons pour reformer les liaisons chimiques qui sont stockées dans les matériaux actifs de la batterie. C’est le cas pour toutes les batteries, y compris celles mentionnées dans ce blog : plomb-acide, nickel-métal-hydrure, nickel-cadmium et lithium-ion. Dans ce blog, nous allons aborder les procédures de charge optimales pour les batteries de 12 volts.
En règle générale, il existe trois grands types de facturation :
– Tension constante (CV)
– Courant constant (CC)
– Puissance constante (charge conique)
Tous les profils de charge et tous les équipements de charge utilisent des variantes, souvent en combinaison, de ces méthodes de base.
La vitesse de charge de la batterie dépend du nombre d’électrons qui circulent par seconde (courant) dans la batterie. La vitesse du flux électrique, comme celle de la lumière, est fixe. Pour augmenter le taux de charge, il faut donc augmenter la densité de courant ou le nombre d’ampères circulant par seconde. Si la force qui pousse les électrons dans l’AM est augmentée, c’est-à-dire la tension, alors le flux d’électrons est augmenté. Plus de volts = plus d’ampères.
La tension et la résistance interne des différents types de piles dépendent de leur composition chimique et les tensions de charge varient en conséquence. Dans ce blog, nous examinerons la chimie des batteries au plomb, des batteries au lithium-ion, des batteries au nickel-cadmium et des batteries à l’hydrure métallique de nickel.
En commençant par le plomb-acide, nous pouvons décrire les réactions chimiques qui stockent et déchargent les électrons, décrites comme la « théorie du double sulfate ».
- PbO2 + Pb + 2H2SO4 = 2PbSO4 + 2H2O……………………………………..eq. 1
Dans cette réaction, l’électrolyte, l’acide sulfurique dilué, est transformé en eau lorsqu’il réagit avec les plaques positives et négatives pendant la décharge. La plaque négative est oxydée car elle cède des électrons pour former du sulfate de plomb et la plaque positive est réduite de l’oxyde de plomb au sulfate de plomb car elle accepte des électrons pour convertir le dioxyde de plomb en sulfate de plomb. Pendant ce temps, la production d’eau entraîne une dilution de l’électrolyte acide et une réduction de la différence de potentiel entre les plaques. Cela produit un électrolyte plus faible SG et une tension de batterie plus faible. Lors de la charge de la batterie, c’est l’inverse. Ces deux paramètres, tension de la batterie et SG de l’électrolyte, sont donc des mesures de l’état de charge d’une batterie au plomb.
La charge d’une batterie plomb-acide de 12 volts nécessite une tension supérieure à la tension de repos de la batterie lorsqu’elle est complètement chargée, qui se situe normalement entre 12,60 et 12,84 pour une nouvelle batterie noyée et entre 12,84 et 13,08 pour une nouvelle batterie VRLA. Il existe quatre variantes de base d’accumulateurs au plomb : les accumulateurs à plaque plate, les accumulateurs tubulaires et les versions VRLA, qui sont des AGM (plaque plate) et des GEL (principalement tubulaires). Les types de batteries, leurs applications et les méthodes de charge associées sont indiqués dans le tableau 1.
| Type de batterie | Méthode de charge normale de la batterie |
|---|---|
| Méthode de charge d'une batterie plomb-acide de type plat et inondé |
Chargement conique à courant constant Charge conique à courant constant/tension constante Chargement conique à tension constante |
| Méthode de charge par inondation d'une batterie plomb-acide à plaques tubulaires |
Chargement conique à courant constant Charge conique à courant constant/tension constante Chargement conique à tension constante |
| Méthode de charge de la batterie plomb-acide VRLA (AGM SMF) |
Charge à courant constant / tension constante Charge à tension constante Charge à courant constant / tension constante avec impulsion |
| Méthode de charge d'une batterie plomb-acide tubulaire-gel VRLA |
Charge à courant constant / tension constante Charge à tension constante Charge à courant constant / tension constante avec impulsion |
| Méthode de charge d'une batterie nickel-cadmium |
Courant constant lent avec minuterie sans contrôle Courant constant avec coupure dT/dT Courant constant avec coupure -dV/dT |
| Méthode de charge d'une batterie au lithium-ion |
Courant constant avec coupure finale du courant Courant constant avec coupure de tension Tension constante avec coupure finale du courant |
Tableau 1 – Différents types de batteries et les méthodes de charge correspondantes pour différents types de batteries chimiques.
- CC = courant constant
- CV = tension constante
- dT/dt = pente de la température
- -dV/dt – pente de tension négative
Les méthodes de chargement énumérées sont décrites comme suit :
- Charge à courant constant
Dans ce type de charge, la tension augmente à mesure que la charge de la batterie s’achève. Le courant est limité à une valeur qui maintient la tension et la température de la batterie à des niveaux bas. En général, il y a une minuterie pour éteindre le chargeur afin d’éviter un gazage excessif et une perte d’eau et de réduire la corrosion du réseau positif Fig. 1a. Cette méthode de charge ne convient pas aux batteries plomb-acide scellées ou inondées à faible entretien.
- Tension constante, charge conique limitée en courant
Avec une charge à tension limitée, le problème du dégagement de gaz est minimisé, voire éliminé. Dans la figure 1b, nous voyons que la tension atteint un pic, généralement entre 13,38 et 14,70 volts pour une batterie de 12 volts. Il est clair que le courant diminue rapidement une fois que la tension de charge maximale est atteinte. Ce type de charge prend généralement beaucoup de temps en raison des faibles niveaux de courant dans la dernière phase de charge. Il est généralement utilisé pour les systèmes d’alimentation sans coupure (UPS) ou l’alimentation de secours lorsque les périodes de charge sont longues.
- Charge conique
Il s’agit de la forme la plus simple du chargeur, généralement basée sur un transformateur, qui donne une puissance de sortie constante, c’est-à-dire des watts. Le courant diminue à mesure que la tension augmente, ce qui maintient une alimentation constante de la batterie. La figure 1c montre une courbe typique où le courant diminue au fur et à mesure que la tension de la batterie augmente. La force contre-électromotrice augmente également avec l’état de charge SOC, ce qui signifie que le courant tombera à des niveaux très bas, la batterie étant incapable de tirer plus de puissance.
- Ce type de chargeur ne convient pas aux batteries plomb-acide scellées sans entretien car la quantité de gaz générée dépend de la tension de la batterie. Dans ce cas, des tensions de charge aussi élevées que 16 ou 17 volts pourraient être atteintes, ce qui provoquerait un grave dégagement de gaz et l’ouverture de la soupape de surpression avec une perte d’eau consécutive.
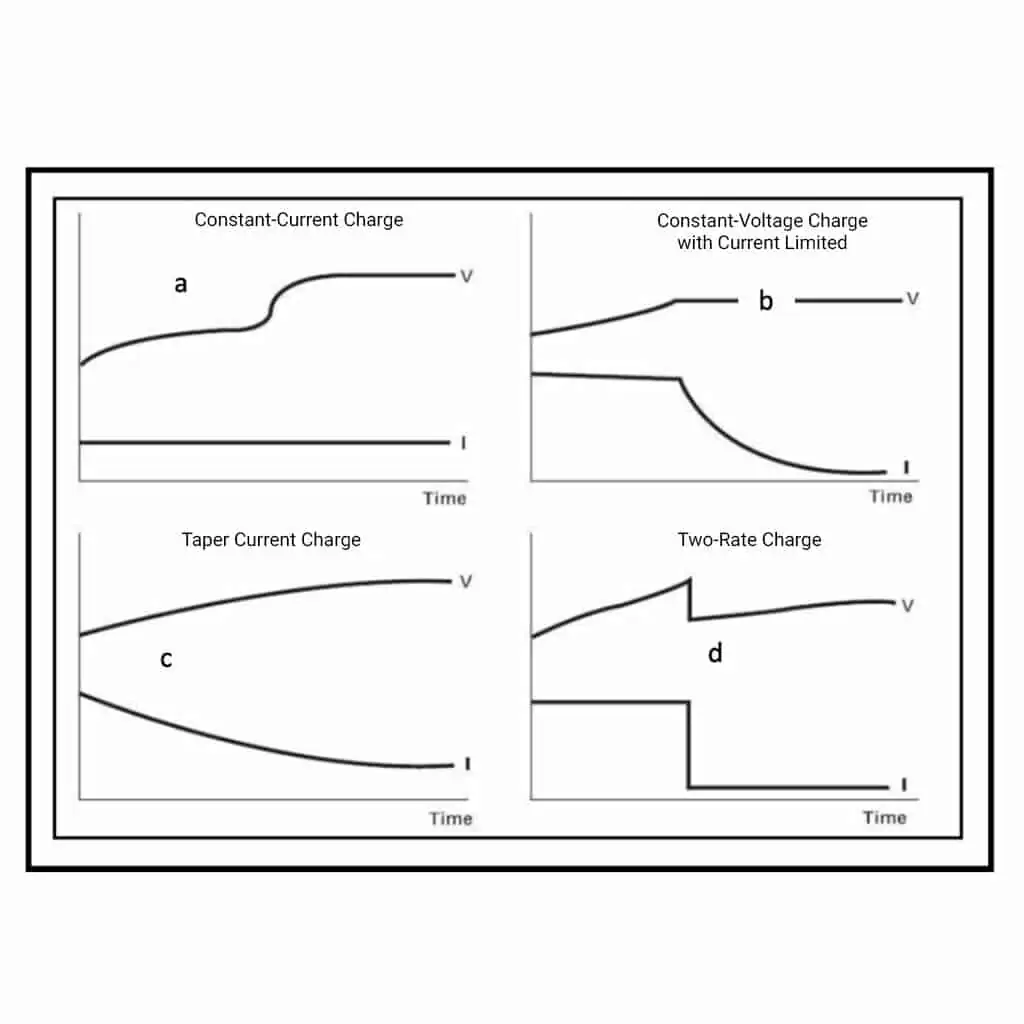
- Charge limitée à deux niveaux de courant et de tension
Un autre profil de charge populaire est illustré à la Fig. 1d. Ainsi, on laisse la tension augmenter dans la phase de masse jusqu’à ce qu’elle atteigne la tension de gazage. Le courant descend alors à un niveau faible et fixe pour réduire la tension qui augmente progressivement jusqu’au niveau de gazage. En général, il y a une limite de temps liée au temps de charge initial de la phase de masse. Cela permet une période de gazage fixe et une entrée d’ampères-heures fixe en fonction de l’état de charge de la batterie.
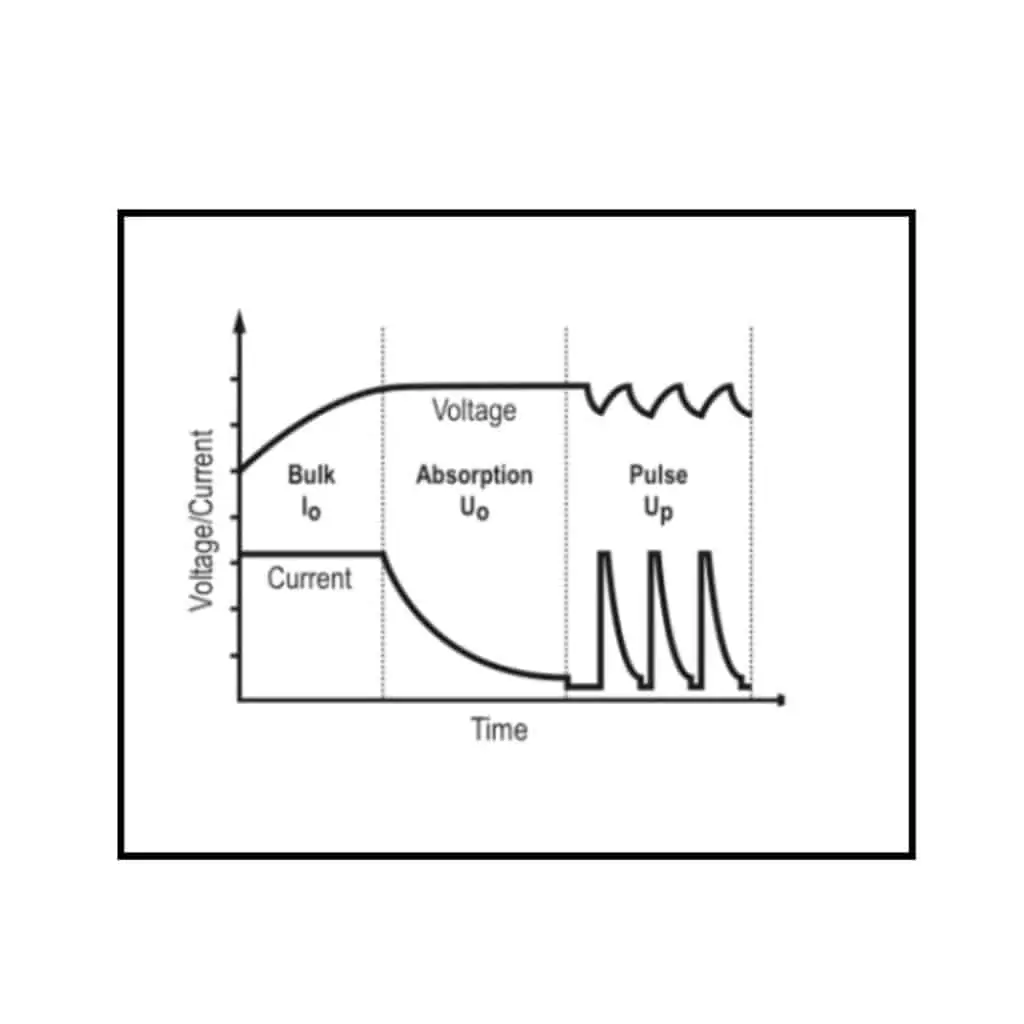
- Charge de masse limitée en tension avec impulsion de courant constant égalisateur.
Fig. 2 est une représentation d’une méthode courante de charge par impulsion. Ceci est généralement avantageux pour les utilisateurs de batteries VRLA qui disposent d’un temps limité pour recharger complètement leurs batteries. Dans cette méthode, il y a à la fois une phase CC et CV où la majeure partie de la charge est appliquée.
- L’impulsion est généralement une rafale de courant de 10 à 20 secondes avec restriction de tension, suivie d’une pause pouvant aller jusqu’à quelques minutes. Comme la tension est en retard sur le courant, qui a une durée limitée, elle n’atteint pas de pic avant de s’éteindre. De cette façon, l’évolution du gaz est limitée et le temps de pause entre les impulsions de courant permet aux gaz de se recombiner en eau, empêchant ainsi le dessèchement.
Jusqu’à présent, les commentaires ont porté sur les batteries au plomb. La charge des batteries Li-ion, NiCd et NiMH nécessite des algorithmes de charge différents de ceux d’une batterie plomb-acide. En commençant par les batteries au lithium-ion, le premier point à noter est qu’il existe des tensions de charge différentes pour les différentes cathodes Li-ion. Un Lithium-ion -FePO4 fonctionne à 3. 2V par cellule alors qu’un Li-Co est de 4.3v par cellule. Cela signifie que vous ne pouvez pas utiliser le même chargeur pour ces deux batteries.
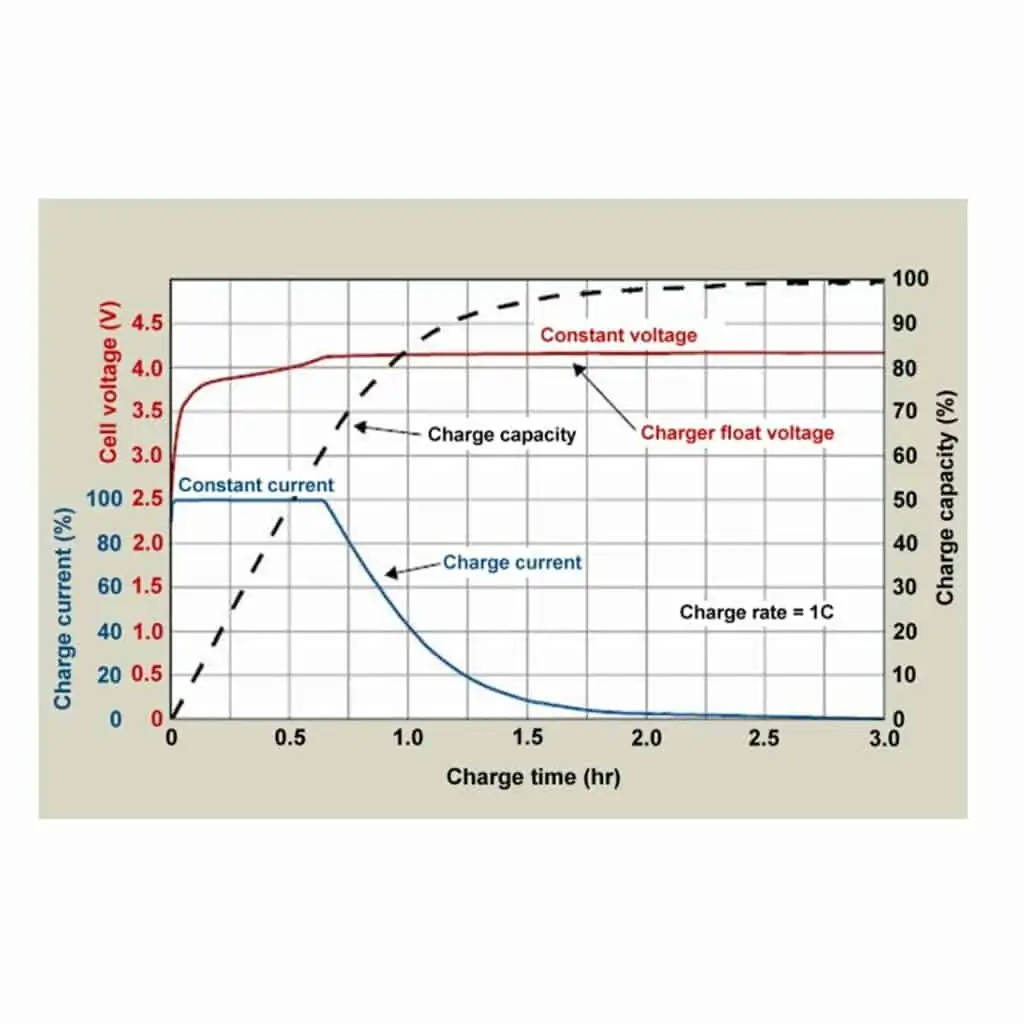
Cependant, le principe général est le même pour tous les types de batteries lithium-ion et est assez différent de celui d’une batterie plomb-acide. Comme il n’y a pas de réaction chimique pendant les processus de charge et de décharge, le transfert est rapide à des taux très élevés limités par la sortie du chargeur ou du BMS (Battery Management System). En général, les taux entre 0,1C et 1C à courant constant avec une coupure de tension sont courants. La figure 3 montre un profil de charge typique pour une cellule li-ion. La période de charge peut également être terminée lorsqu’un courant minimum est atteint, autour de 2-3% de la valeur de l’ampère 1C.
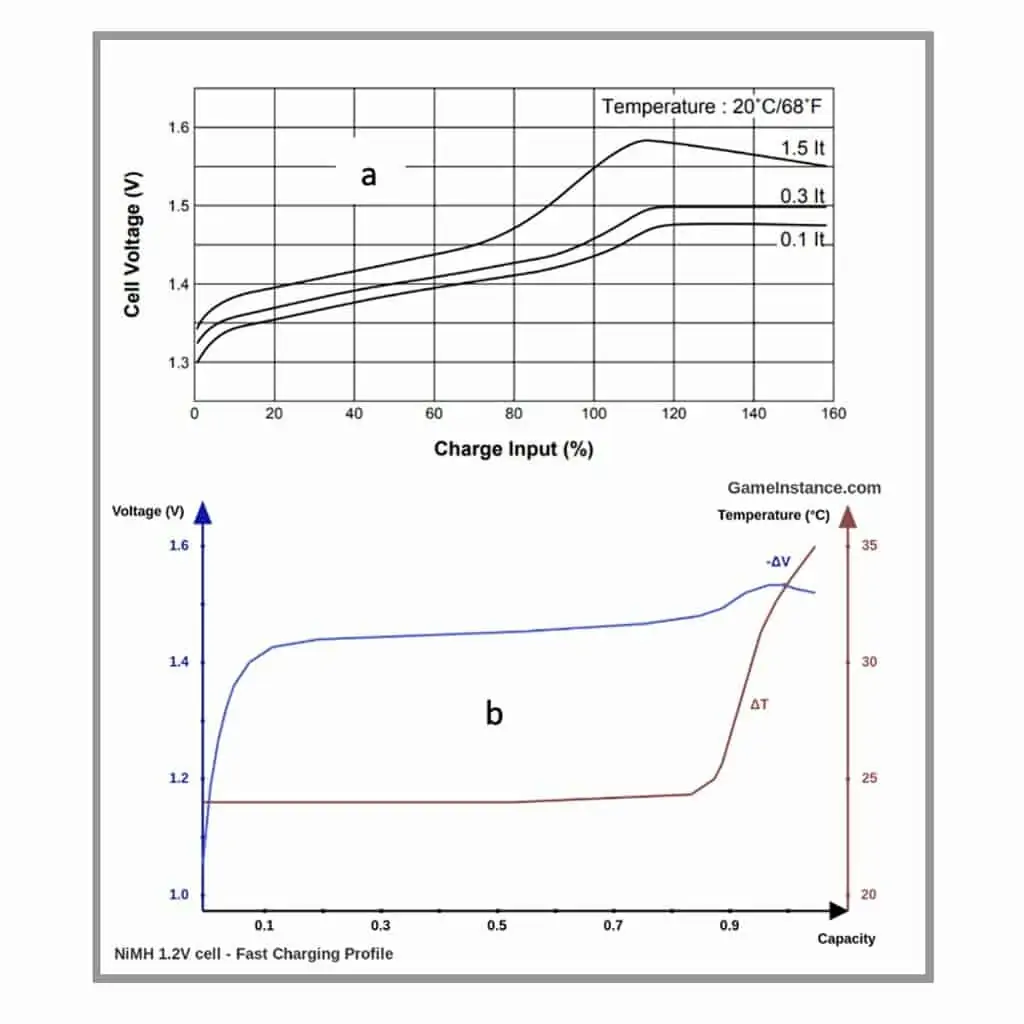
Les NiMH et les NiCd ont également des schémas de charge différents et des réactions très différentes à la charge, à la fois par rapport aux autres produits chimiques et entre eux. La figure 4 montre un schéma de charge typique pour les deux Ni-Cad (a) et NiMH (b). Bien que les deux variantes de nickel aient la même tension de repos et de fonctionnement, la tension de charge peut varier considérablement. Un chargeur pour les deux types ne peut pas compter sur la tension comme mécanisme de fin de charge. Pour cette raison, les chargeurs utilisent simplement un chargeur à courant constant à un ou deux étages avec une terminaison basée sur le temps, la pente de la tension et le changement de température de la pente. L’examen des caractéristiques de charge montre qu’il y a à la fois une augmentation de la température et une baisse simultanée de la réponse en tension lorsque la charge atteint 100%.
Ces caractéristiques sont utilisées pour déterminer la fin de la charge. Puisque la tension absolue varie avec la température et est différente pour les deux types de cellules. L’apparition de la pente de tension négative (-dV/dt) ou l’augmentation rapide de la pente de température (dT/dt), sont les caractéristiques les plus couramment utilisées. Si une méthode de chronométrage est utilisée, le courant doit être très faible pour éviter une surcharge et une perte d’oxygène. Dans certains cas, notamment avec des cellules ou des batteries déséquilibrées, il est préférable de décharger à 0,9-1,0 volt par cellule avant de charger en utilisant la méthode de la minuterie.
Comment fonctionne un chargeur de batterie ?
Tous les chargeurs tirent l’énergie du réseau en courant alternatif (CA) et la convertissent en courant continu. Au cours du processus, il y aura quelques ondulations du CA qui doivent être maintenues à moins de 3%. Certains des chargeurs de batterie disponibles sur le marché sont dotés de fonctions permettant de filtrer les ondulations qui, sinon, endommageraient la batterie pendant la charge. Dans tous les cas, il est préférable d’utiliser une alimentation triphasée car le courant monophasé a une ondulation de 10 %.
Tous les chargeurs tirent l’énergie du réseau en courant alternatif (CA) et la convertissent en courant continu. Au cours du processus, il y aura quelques ondulations du CA qui doivent être maintenues à moins de 3 %. Certains des chargeurs de batterie disponibles sur le marché sont dotés de fonctions permettant de filtrer les ondulations qui, sinon, endommageraient la batterie pendant la charge. Dans tous les cas, il est préférable d’utiliser une alimentation triphasée car le courant monophasé a une ondulation de 10 %.
Chargeur à tension constante
La tension constante permet au courant total du chargeur de batterie de circuler dans la batterie jusqu’à ce que l’alimentation atteigne sa tension préréglée. Le courant diminuera ensuite jusqu’à une valeur minimale une fois ce niveau de tension atteint. La batterie peut rester connectée au chargeur de batterie jusqu’à ce qu’elle soit prête à être utilisée et restera à cette « tension d’entretien », la charge de maintien compensant l’autodécharge normale de la batterie.
Tension constante, courant constant
La tension constante / courant constant (CVCC) est une combinaison des deux méthodes ci-dessus. Le chargeur limite la quantité de courant à un niveau prédéfini jusqu’à ce que la batterie atteigne un niveau de tension prédéfini. Le courant diminue ensuite lorsque la batterie est complètement chargée. La batterie au plomb utilise la méthode de charge à courant constant et tension constante (CC/CV). Un courant régulé augmente la tension de la borne jusqu’à ce que la limite supérieure de la tension de charge soit atteinte, auquel point le courant chute en raison de la saturation.
Différents types de chargeurs de batterie
La technologie actuelle de charge des batteries s’appuie sur des microprocesseurs (puces informatiques) pour recharger, en utilisant 3 étapes de charge régulée. Ce sont les « chargeurs intelligents ». Ils sont facilement disponibles. Les trois étapes de la charge d’une batterie plomb-acide sont les entrées de courant principales pour la conversion, et la charge flottante sur une période continue. Une charge d’égalisation périodique pour maintenir l’uniformité est nécessaire. Utilisez les recommandations du fabricant de la batterie concernant les procédures et les tensions de charge ou un chargeur de qualité contrôlé par microprocesseur pour maintenir la capacité et la durée de vie de la batterie.
Les « chargeurs intelligents » sont conçus en fonction de la technologie de charge actuelle et prennent également en compte les informations fournies par la batterie afin d’assurer une charge maximale avec un minimum d’observations.
Les batteries VRLA – Gel et AGM nécessitent des réglages de tension différents. Cela permet d’éviter le dégagement de gaz et le dessèchement. Le processus de recombinaison de l’oxygène dans une batterie plomb-acide à régulation par soupape (VRLA) nécessite un réglage de tension plus faible pour éviter le dégagement d’hydrogène et le dessèchement de la cellule.
La tension de charge maximale des batteries au gel est de 14,1 ou 14,4 volts, ce qui est inférieur à ce dont une batterie de type VRLA humide ou AGM a besoin pour une charge complète. Le dépassement de cette tension dans une batterie au gel peut provoquer des bulles dans le gel électrolyte et des dommages permanents.
Le courant nominal des chargeurs de batterie recommande de dimensionner le chargeur à un courant maximal de 25 % de la capacité de la batterie. Certaines batteries spécifient 10 % de leur capacité. Il est plus sûr d’utiliser un courant plus faible, même si cela prend plus de temps.
Une méthode de charge à courant constant – tension constante (CCCV) est une bonne option. Un courant constant augmente la tension aux bornes jusqu’à ce que la limite supérieure de la tension de charge soit atteinte, auquel cas le courant chute en raison de la saturation. Le temps de charge est de 12 à 16 heures et plus long (36 heures) pour les grandes batteries stationnaires. La batterie au plomb est plus lente et ne peut pas être chargée aussi rapidement que les autres systèmes de batterie. Avec la méthode CCCV, les batteries au plomb sont chargées en trois étapes : [1] charge à courant constant, [2] tension constante et [3] charge flottante à la fin de la charge.
La charge à courant constant applique la majeure partie de la charge et prend environ la moitié du temps de charge nécessaire ; la charge d’appoint continue à un courant de charge plus faible et assure la saturation, et la charge flottante continue compense la perte causée par l’autodécharge. Pendant la charge à courant constant, la batterie se charge à environ 70 % en 5 à 8 heures ; les 30 % restants sont remplis de tension constante qui dure encore 7 à 10 heures. La charge flottante de la troisième étape maintient la batterie à pleine charge.
Chargement de la batterie, peut-on surcharger une batterie 12V ?
Dans tous ces produits chimiques, une surcharge peut entraîner des dommages ou des risques pour la sécurité. Dans le cas des batteries au plomb, les tensions de surcharge sont limitées et le courant excédentaire est dissipé dans la décomposition de l’eau, le dégagement d’hydrogène et d’oxygène et la création de chaleur. L’augmentation du courant n’augmentera pas la tension, elle augmentera le taux de gazage et de perte d’eau et provoquera une augmentation de la température. Une certaine surcharge est tolérée, notamment lorsque l’égalisation de la cellule ou de la batterie est nécessaire.
Pour les batteries lithium-ion, la surcharge est difficile en raison du BMS intégré à la batterie. Cela coupera l’alimentation en courant une fois que la tension de terminaison est atteinte, ou que la température devient trop élevée. Il s’agit d’une précaution nécessaire car les cellules li-ion contiennent un électrolyte volatil qui se libère à des températures plus élevées. C’est la vapeur de l’électrolyte qui prend feu dans les batteries li-ion, ce qui rend la surcharge très dangereuse. Les batteries NiCad et NiMH ne doivent pas être surchargées car elles perdent de l’oxygène et donc de l’électrolyte, même s’il s’agit de versions scellées.
Il existe plusieurs indicateurs du SOC d’une batterie : la tension au repos mesurée à ses bornes, la gravité spécifique de l’électrolyte (batteries ouvertes inondées) ou la valeur de l’impédance. Ils sont différents pour chaque chimie de batterie, et pour cette raison, il est préférable d’examiner chaque type séparément :
1. Plomb-acide.
Gravité spécifique.
La réaction des plaques avec l’acide sulfurique lors de la charge et de la décharge détermine le rapport entre l’acide et l’eau dans une cellule.
Lorsqu’il est chargé, la concentration d’acide sulfurique est élevée, lorsqu’il est déchargé, elle est plus faible (éq. 1). Comme la densité de l’acide est de 1,84 et celle de l’eau de 1, la gravité spécifique, SG de l’électrolyte augmente à la charge et diminue à la décharge.
La réaction présente une relation de premier ordre, ce qui signifie que la variation de la concentration est linéaire. La mesure de la densité gazeuse donne donc une indication directe du SOC de la batterie, Fig. 5.

Une mise en garde : ceci ne s’applique pas lorsque la charge de la batterie est en cours et en phase d’accumulation ou de pré-gazage. Sans brassage de l’électrolyte, l’acide plus dense produit lors de la charge va couler, laissant le gros de l’électrolyte plus dilué jusqu’à ce qu’une tension de 2,4 volts par cellule soit atteinte. A partir de ce moment, le gaz dégagé au niveau des plaques va créer une action de brassage pour mélanger l’acide.
Tension de repos : Elle peut être une indication du SOC et est liée à la gravité spécifique de la cellule selon la relation suivante :
- Volts au repos = SG + 0,84 …………………………………………………………..eq 2
Par exemple, une cellule de 2V avec une gravité spécifique de 1,230 aura une tension au repos de 1,230 + 0,84 = 2,07 volts.
L’utilisation de cette relation peut donner une indication raisonnablement précise de l’état de charge de la batterie. Cependant, les différentes batteries ont des plages de fonctionnement différentes pour l’état de charge et ainsi, l’état de charge maximal d’une batterie VRLA peut être de 1,32 comparé à une batterie OPzS avec un état de charge maximal de 1,28. La température affecte également le SG et donc la tension de la cellule. L’effet de la température sur la tension en circuit ouvert est indiqué dans le tableau 2.
Un autre facteur est que les batteries fraîchement chargées ont une forte concentration d’acide à côté des plaques en raison de la formation d’acide sulfurique lors d’une charge. C’est pourquoi la tension après la charge reste élevée pendant un certain temps, peut-être jusqu’à 48 heures, avant de se stabiliser à une valeur constante. À moins qu’une courte décharge ne soit effectuée sur la batterie, celle-ci doit se reposer pour permettre l’égalisation de la concentration d’acide avant de prendre une mesure de tension.
Outils nécessaires à la mesure du SOC
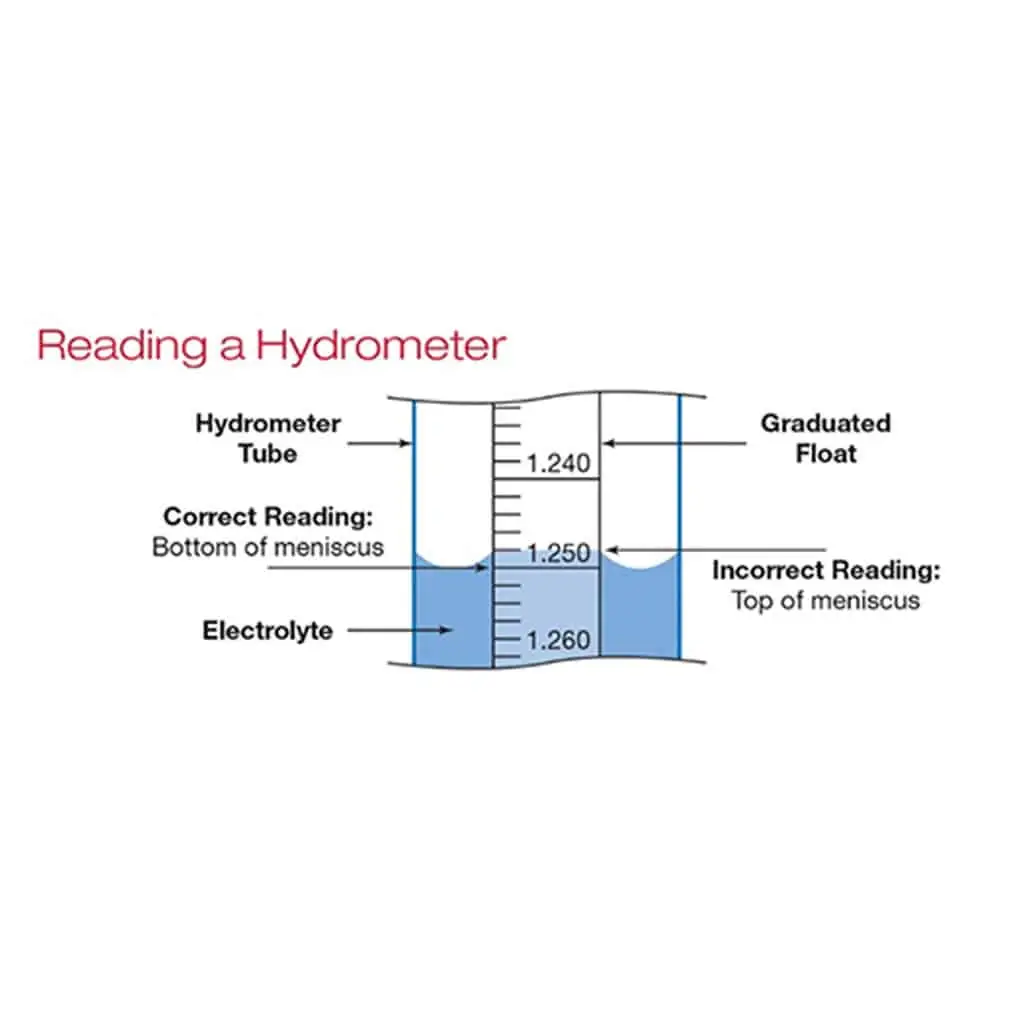
Il s’agit d’un voltmètre à courant continu ou d’un multimètre pour les mesures de tension et d’un hydromètre pour la lecture de la gravité spécifique.
Pour les cellules inondées, à part un test de décharge, l’hydromètre est la meilleure méthode pour déterminer l’état de charge. L’utilisation d’un hydromètre demande un peu de pratique et doit être effectuée très soigneusement. La procédure consiste à placer la batterie dans une position appropriée pour que la lecture de l’hydromètre puisse être effectuée à hauteur des yeux (Fig. 6 ci-dessus).
Pour les batteries scellées, il n’est pas possible d’utiliser un hydromètre, la mesure des volts au repos est donc la seule option. Cette méthode est applicable à la fois aux batteries au plomb scellées et inondées.
Pour cela, le multimètre doit être réglé sur une tension maximale appropriée afin de s’assurer qu’il peut lire plus de 12 volts, mais aussi produire au moins 2 décimales de précision. En utilisant l’eq. 2, la tension peut être utilisée après ajustement de la température, pour estimer la densité de charge et donc le SOC de la batterie, à condition de connaître la valeur de densité de charge du fabricant pour une batterie complètement chargée.
Dans les deux cas d’utilisation de la tension ou d’un hydromètre pour mesurer l’état de charge, SOC, il est nécessaire d’appliquer une compensation de température. Le tableau 2, fourni par la BCI, donne les ajustements appropriés pour les lectures de l’hydromètre et du voltmètre.
Tableau 2 Compensation de la gravité spécifique de l’électrolyte et des lectures de tension avec la température
| Température de l'électrolyte Fahrenheit (°F) | Température de l'électrolyte Celsius (°C) | Ajouter ou soustraire à la lecture du SG de l'hydromètre | Ajout ou soustraction à la lecture d'un voltmètre numérique |
|---|---|---|---|
| 160° | 71.1° | +.032 | +.192 V |
| 150° | 65.6° | +.028 | +.168 V |
| 140° | 60.0° | +.024 | +.144 V |
| 130° | 54.4° | +.020 | +.120 V |
| 120° | 48.9° | +.016 | +.096 V |
| 110° | 43.3° | +.012 | +.072 V |
| 100° | 37.8° | +.008 | +.048 V |
| 90° | 32.2° | +.004 | +.024 V |
| 80° | 26.7° | 0 | 0 V |
| 70° | 21.1° | -.004 | -.024 V |
| 60° | 15.6° | -.008 | -.048 V |
| 50° | 10° | -.012 | -.072 V |
| 40° | 4.4° | -.016 | -.096 V |
| 30° | -1.1° | -.020 | -.120 V |
| 20° | -6.7° | -.024 | -.144 V |
| 10° | -12.2° | -.028 | -.168 V |
| 0° | -17.6° | -.032 | -.192 V |
2. Li-ion, NiMH et NiCd.
Pour tous ces produits chimiques, la mesure du SOC présente de sérieux défis. Toutes ont une courbe de décharge très plate avec une très faible différence de tension entre l’état complètement chargé et l’état déchargé. Les réactions de charge-décharge dans les cellules NiCd et NiMH ne modifient pas sensiblement la densité de l’électrolyte et tous les produits chimiques Li-ion fonctionnent avec des cellules complètement scellées. Cela rend les contrôles statiques ou aléatoires d’une batterie en service presque impossibles, surtout pour un utilisateur non professionnel. L’état actuel de l’art des mesures de l’état de charge (SOC) pour ces produits chimiques est basé sur des relevés dynamiques effectués pendant leur fonctionnement.
Ils peuvent être basés sur le comptage des ampères-heures, la réponse en tension aux courants de décharge ou même des impulsions de courant constant. Les équipements de mesure sont généralement intégrés dans des dispositifs coûteux ou sophistiqués, tels que des véhicules électriques ou des machines industrielles, où il est nécessaire de connaître le temps de fonctionnement disponible. Pour les équipements moins sophistiqués tels que les outils électriques à main, le fait de remarquer que l’outil s’arrête ou fonctionne moins vite est la seule indication disponible.
Il existe dans le commerce des testeurs à spectromètre d’impédance qui mesurent l’impédance interne d’une batterie pour prédire son état de charge. Ces dispositifs dépendent d’un algorithme basé sur le test de centaines de batteries dans différents états de charge et de différents âges pour prédire le SOC. Les résultats sont spécifiques à la chimie et à l’âge d’une batterie particulière. Plus le nombre de tests effectués pour créer l’algorithme est élevé, plus l’algorithme est précis.
Pendant la charge de la batterie, peut-on surcharger une batterie ?
Quelle que soit la façon dont vous décidez de mesurer l’état de charge, il existe des règles qui s’appliquent à tous les types de batteries. Ils permettent d’éviter la décharge excessive d’une batterie, qui peut endommager les cellules individuelles en les faisant passer en sens inverse, voire en leur faisant subir des tensions négatives. La surcharge est moins évidente, car dans le cas de l’acide de plomb, il est parfois nécessaire de le faire pour égaliser les cellules ou les batteries individuelles dans une banque. Cependant, une surcharge excessive entraîne un dégagement gazeux avec perte d’eau et une corrosion des plaques positives, ce qui réduit la durée de vie de la batterie.
Pour les batteries à base de nickel, la perte d’eau est le problème le plus courant, ce qui entraîne une réduction de la durée de vie. Dans le cas des batteries au lithium, il est généralement impossible de les surcharger grâce au BMS intégré qui coupe automatiquement l’entrée de courant à une tension prédéfinie. Dans certains modèles, il existe un fusible intégré qui empêche la surcharge. Cependant, cela rend généralement la batterie irrémédiablement inopérante.
Charge de la batterie, surcharge : comment l'éviter ?
La décision de recharger une batterie dépend des circonstances d’utilisation et du degré de décharge. En règle générale, pour tous les produits chimiques, la batterie ne doit pas descendre en dessous de 80 % de DOD afin d’optimiser sa durée de vie. Cela signifie que le SOC final de la batterie doit être calculé à partir du point de mesure jusqu’à la fin de son fonctionnement quotidien. Si, par exemple, le SOC est de 40 % au début de l’opération et qu’il utilisera 70 % de sa capacité à la fin de l’opération, la batterie doit être rechargée avant d’être autorisée à continuer.
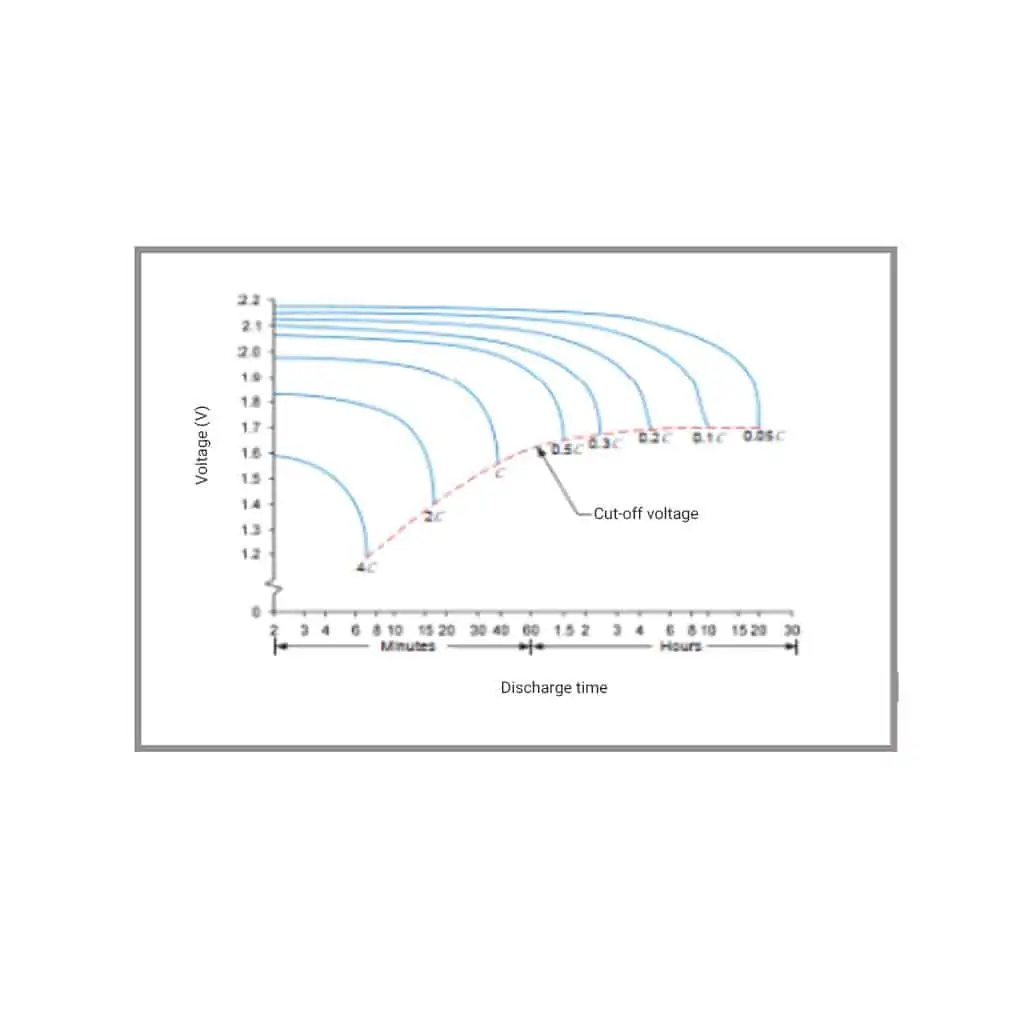
Pour prendre cette décision, il est nécessaire de déterminer la capacité restante ou l’autonomie d’une batterie. Ce n’est pas simple, car la capacité de la batterie est déterminée par le taux de décharge. Plus le taux de décharge est élevé, moins la capacité disponible est importante. Les batteries au plomb sont très sensibles à ce phénomène, comme le montre la figure 8.
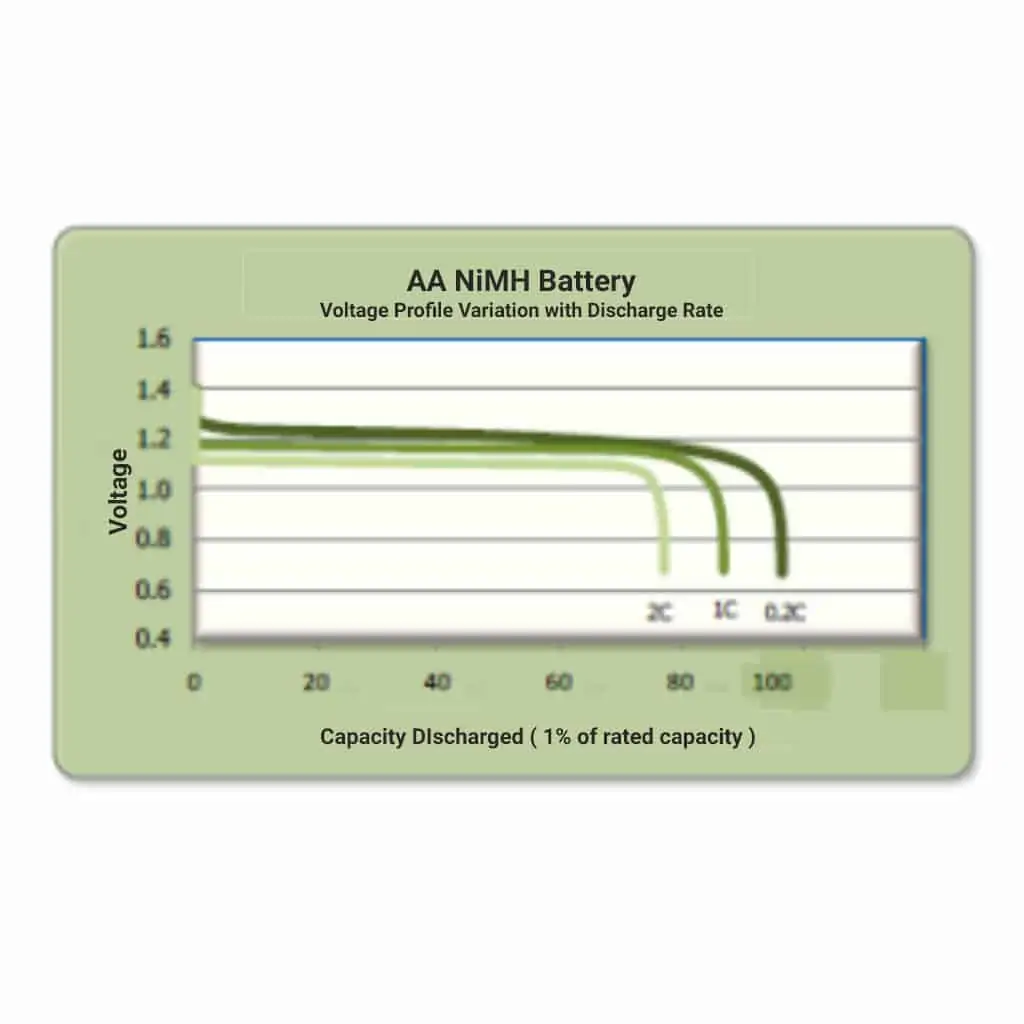
Les batteries Li-ion et NiCd ont des capacités réduites à des taux de décharge plus élevés, mais elles ne sont pas aussi prononcées que celles au plomb. Fig. 9 montre l’effet de 3 taux de décharge différents sur la capacité disponible d’une batterie NiMH. Dans ce cas, 0,2C (taux de 5 heures), 1C (taux de 1 heure) et 2C (taux de 1/2 heure).
Dans tous les cas, le profil de tension reste très plat mais à un niveau réduit jusqu’à la fin de la période de décharge où la tension s’effondre soudainement.
Charge de la batterie - calcul des temps de charge et de décharge de la batterie
Calcul des temps de charge et de décharge des batteries
Pour établir le temps de décharge d’une batterie dans un état de charge particulier, il faut connaître le courant consommé et la capacité de la batterie à un taux de décharge particulier. La durée de fonctionnement peut être calculée approximativement en utilisant une règle empirique pour chaque chimie de batterie.
La connaissance de la capacité effective à un taux de décharge particulier permet de prévoir la durée de fonctionnement comme suit :
Capacité standard de la batterie (ampères-heures) = C
Courant de décharge (ampères) = D
Facteur de décharge = D/C = N
Taux de décharge (ampères) = NC
Capacité au taux de décharge D (ampères-heures) = CN
Temps de décharge d’une batterie entièrement chargée (heures) = CN /D
En utilisant l’estimation de l’état de charge en pourcentage, le temps de fonctionnement peut être calculé :
Durée de fonctionnement = % d’état de charge x CN /(100xD) = heures
Le calcul du temps de charge est complexe car il dépend de l’état de charge de la batterie, du type de batterie, de la sortie du chargeur et du type de chargeur. Il est nécessaire de connaître l’état de charge de la batterie pour déterminer les ampères-heures qu’il faut mettre dans la batterie pour la recharger. La vitesse à laquelle cela se produit dépend de la puissance du chargeur et de la façon dont il se charge. Il est clair qu’une batterie li-ion peut se recharger en quelques heures à partir d’une batterie complètement vide si le chargeur a une puissance suffisante.
Une batterie plomb-acide scellée avec une limitation de la sortie du chargeur prendra beaucoup plus de temps en raison de la restriction de la tension et de la réduction du courant dans la phase de gazage. Une fois l’état de charge déterminé, vous pouvez calculer le nombre d’ampères-heures à réinjecter dans la batterie. En connaissant les caractéristiques du chargeur, il est plus facile de calculer le temps de charge en fonction de la vitesse à laquelle il se charge, compte tenu du schéma de charge utilisé.
Un autre facteur est la température ambiante (conditions météorologiques) qui influe sur la tension de charge et le courant consommé par le chargeur. Des températures plus élevées font baisser la tension de charge mais augmentent aussi le courant consommé. Pour les batteries en charge flottante, il est nécessaire d’appliquer une compensation de tension avec la température. Microtex peut vous conseiller sur l’ajustement nécessaire lorsque les températures varient considérablement par rapport à la norme de 25°C.
Un dernier mot sur la charge des batteries !
Il n’est pas simple de charger correctement une batterie et de connaître son état de charge. Souvent, les batteries sont achetées sans que le vendeur ne fournisse de conseils ou de services de soutien. C’est pourquoi il est important d’acheter auprès d’un fournisseur réputé qui accorde la priorité à la satisfaction du client. Pour obtenir des conseils sur l’entretien ou l’installation d’une charge de batterie, la meilleure solution consiste à contacter un fournisseur professionnel de confiance.
Comme toujours, Microtex, un fabricant international de batteries de longue date dont le taux de satisfaction de la clientèle est sans faille, est toujours prêt à vous aider. Elle est l’une des rares entreprises à posséder les connaissances et les produits nécessaires pour fournir et entretenir des batteries pour pratiquement toutes les applications industrielles et grand public. Si la charge de votre batterie vous laisse tomber, contactez les personnes qui ne le feront pas.
Pour tout ce qui concerne la charge des batteries, les questions
prenez contact avec Microtex.