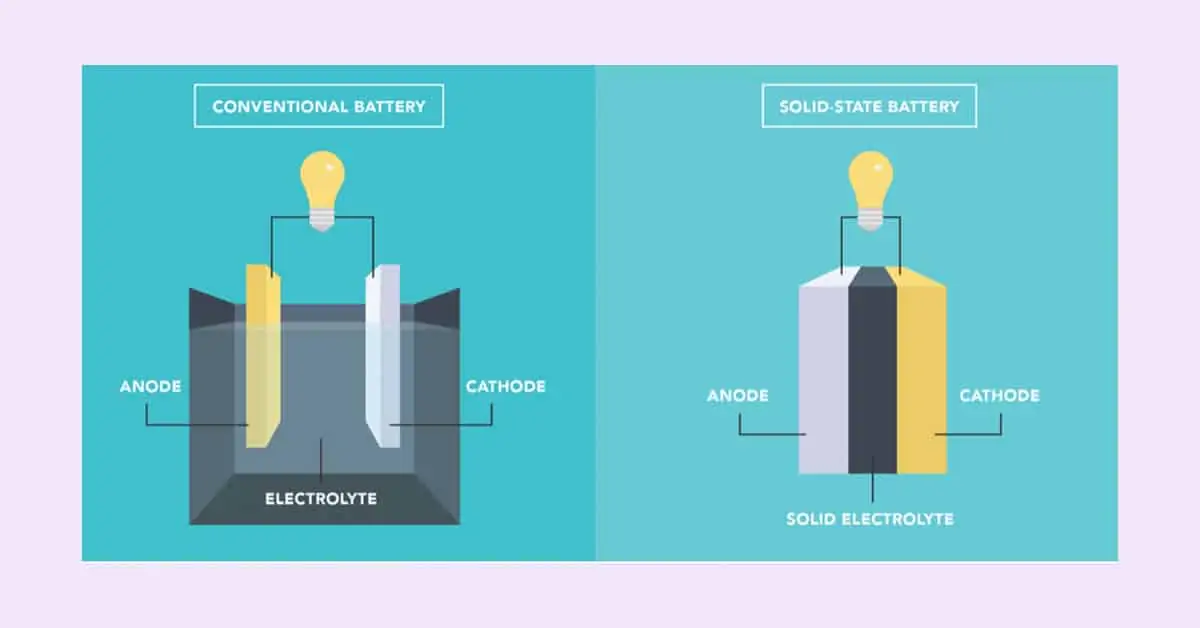
Einführung der Festkörperbatterie
In einer Batterie bewegen sich positive Ionen über einen Ionenleiter zwischen der negativen und der positiven Elektrode und geben Elektronen ab, um einen elektrischen Strom zu erzeugen. In herkömmlichen Batterien, z. B. Lithium-Ionen-Batterien, ist der Ionenleiter eine leicht brennbare flüssige organische Verbindung, was einen erheblichen Nachteil darstellt. In verschiedenen Forschungs- und Entwicklungsprozessen wurde eine Vielzahl von Verbindungen synthetisiert, um leistungsstarke feste Leiter zu finden, die flüssige Leiter ersetzen können. Forscher haben einen Festkörper-Ionenleiter entdeckt, der die Leistung eines herkömmlichen Lithium-Ionen-Leiters übertrifft. ex: LGPS-Sulfid-Feststoffelektrolyt (LGPS: Lithium, Germanium, Phosphor, Schwefel)
Was ist eine Festkörperbatterie? Es ist der Technologieansatz, der ein höheres Potenzial für mehr Sicherheit, höhere Energiedichte und Kosteneffizienz bietet. Festkörperbatterien sind die Zukunft der Batterietechnologie in der Unterhaltungselektronik und in Elektrofahrzeugen. Kathode, Anode, Separator und Elektrolyt bilden eine Lithium-Ionen-Batterie. Die flüssige Elektrolytlösung wird in Flüssigspeicherbatterien (Lithium-Ionen-Batterien) verwendet, die in Smartphones, Elektrowerkzeugen und Elektrofahrzeugen zum Einsatz kommen. Bei einer Festkörperbatterie hingegen wird ein fester Elektrolyt verwendet und nicht wie bei herkömmlichen Batterienein flüssiger Elektrolyt .
Der Elektrolyt in einer Batterie ist eine leitfähige chemische Mischung, die den Stromfluss zwischen Anode und Kathode ermöglicht. Trennvorrichtungen verhindern einen Kurzschluss. Festkörperbatterien sind elektrochemische Zellen mit einer Anode, einer Kathode und einem Elektrolyt, ähnlich wie jede andere Batterie. Die Elektroden und Elektrolyte sind im Gegensatz zu Blei-Säure-Batterien fest.
Die handelsübliche Li-Ionen-Batterie verfügt über einen Separator, in dem Kathode und Anode durch eine flüssige Elektrolytlösung getrennt sind. Festkörperbatterien hingegen verwenden feste Elektrolyte anstelle einer flüssigen Elektrolytlösung, und der feste Elektrolyt fungiert auch als Separator. Diese Batterien sind wichtig und werden dringend benötigt, um die Kapazität von Festkörper-EV-Batterien zu erhöhen. Sie sind entflammbar, und die Gefahr einer Explosion ist vernachlässigbar. Ein Beispiel für eine Festkörperbatterie ist Lithium-Phosphat-Glas. Die Energiedichte dieser Batterien ist hoch.
Die Energiekapazität einer Festkörperbatterie ist größer als die einer Lithium-Ionen-Batterie mit einer flüssigen Elektrolytlösung. Da es keine Explosions- oder Brandgefahr gibt, sind keine Sicherheitskomponenten erforderlich, was Platz spart. Die Batterien können im Vergleich zu Lithium-Ionen-Batterien doppelt so viel Energie aufnehmen, was ihre Leistung erhöht. Da nur wenige Batterien benötigt werden, kann eine Festkörperbatterie die Energiedichte pro Flächeneinheit erhöhen.
Festkörperbatterie-Technologie
SSB konzentriert sich hauptsächlich auf die folgenden Merkmale:
Höhere Energiedichte:
- Geringere Kosten: Verwendung billigerer Materialien und kostengünstigerer Verfahren und aufgrund der hohen Energiedichte.
- Höhere Sicherheit: Toleranz gegenüber Überladung, Toleranz gegenüber Tiefentladung
- Geringere Abhängigkeit von knappen Materialien: geringere geologische Abhängigkeit, Substitution von Materialien wie Lithium und Kobalt.
- Geringere Umweltbelastung: keine giftigen Materialien, keine Schwermetalle, keine gefährlichen Chemikalien, umweltfreundliche Produktion, leicht zu entsorgende oder zu recycelnde Materialien.
- Andere: Tiefentladefähigkeit, Schnellladefähigkeit oder Entladefähigkeit.
Der Festkörperelektrolyt ist die wichtigste Komponente in Festkörperbatterien. Es gibt drei Haupttypen von Festkörperelektrolytmaterialien.
Anorganische Materialien: anorganische kristalline Materialien, anorganische amorphe Materialien. Da anorganische Elektrolyte einen hohen Elastizitätsmodul, eine hohe thermische/chemische Stabilität, ein großes elektrochemisches Fenster, eine hohe Ionenleitfähigkeit und eine niedrige elektronische Leitfähigkeit aufweisen, eignen sich diese Elektrolyte besser für starre Batteriedesigns, die in rauen Umgebungen arbeiten können.
Feste Polymere: z. B. Polyethylenoxid. Polymerelektrolyte besitzen zwar eine geringere Ionenleitfähigkeit als anorganische Festelektrolyte, bieten aber eine Vielzahl von Geometrien, eine hohe Flexibilität und erfordern eine kostengünstige und vereinfachte Herstellung. Bei der Integration von Batteriezellen kann ein fester Polymerelektrolyt leicht eine wirksame Elektroden-Elektrolyt-Verbindung herstellen, was die elektrochemische Stabilität und die Zykluslebensdauer der Batterien erhöhen könnte. In herkömmlichen Lithium-Ionen-Batterien wird ein flüssiger Elektrolyt verwendet, der normalerweise einen guten Kontakt zu den Elektroden herstellt.
Die Elektroden saugen die Flüssigkeit dank ihrer strukturierten Oberfläche wie ein Schwamm auf, wodurch eine große Kontaktfläche entsteht. Theoretisch können zwei Festkörper nicht nahtlos miteinander verbunden werden. Daher ist der Widerstand zwischen den Elektroden und dem Elektrolyten hoch. Der Festelektrolyt dient als stabiles Trägermedium für die beidseitig bedruckten Phosphatelektroden. Die neue Festkörperbatterie ist im Gegensatz zu herkömmlichen Lithium-Ionen-Batterien völlig frei von giftigen oder gefährlichen Substanzen.
Anorganische und polymere Materialien werden kombiniert, um die Vorteile beider Materialarten zu nutzen. Diese Elektrolyte weisen eine hohe Ionenleitfähigkeit auf und sind relativ flexibel.
Die mechanischen, elektrischen und chemischen Eigenschaften des Festelektrolyten sowie die Grenzflächen/Interphasen mit den Anoden- und Kathodenelektroden haben einen erheblichen Einfluss auf die Effizienz der Festkörperbatterie.
Die grundlegenden Aspekte von Festkörperbatterien, mit Schwerpunkt auf drei wesentlichen Phänomenen:
(i) die Grundsätze der Herstellung fortgeschrittener Ionenleiter,
(ii) strukturelle Entwicklung an chemisch instabilen Elektrolyt-Elektroden-Grenzflächen, und
(iii) die Auswirkungen der Verarbeitung von Festkörperbatterien, einschließlich der Elektroden- und Elektrolytarchitektur. Festkörperelektrolyte (SSE) können nicht nur Sicherheitsprobleme lösen, sondern ermöglichen auch die Verwendung einer Metallanode und den Betrieb mit hohen Spannungen.
Die Festkörperbatterie (Solid-State-Battery, SSB) ist eine der besten Lösungen für die nächste Generation von Batterien, da feste Elektrolyte eine viel höhere thermische Stabilität aufweisen. Darüber hinaus können anorganische Festelektrolyte auch bei extremen Temperaturen funktionieren, z. B. bei Temperaturen von 50 bis 200 °C oder noch höher, wo organische Elektrolyte durch Gefrieren, Sieden oder Zersetzung versagen.
Um die erwartete elektrochemische Leistung bei der Verwendung von Festkörperelektrolyten zu erreichen, werden vier einzigartige Merkmale berücksichtigt. Zu diesen Merkmalen gehören:
( i )hohe Ionenleitfähigkeit (+Li > 104 S/cm);
(ii) ausreichende mechanische Festigkeit und wenige strukturelle Defekte, die das Eindringen von Lithiumdendriten verhindern;
(iii) kostengünstige Rohstoffe und einfache Zubereitungsverfahren; und
(iv) die niedrige Aktivierungsenergie für die Lithium-Ionen-Diffusion.
Vorteile der Festkörperbatterie
- Einfacher Aufbau: Festelektrolyte wirken als Separator und verhindern den Kontakt zwischen Anode und Kathode, was zu einer höheren Energiedichte führt und die Kosten für den Separator einspart.
- Hohe Spannung: Die Zersetzung von Festelektrolyten ist hoch, was wiederum zu einer hohen Energiedichte führt.
- Nicht brennbarer Festelektrolyt.
- Der Elektrolyt ist flammhemmend.
- Keine Gefahr des Auslaufens von flüssigem Elektrolyt.
- Kann bei höheren Betriebstemperaturen verwendet werden, was zu einem größeren Betriebstemperaturbereich führt.
- Möglichkeit der Zellenstapelung in einem Paket.
- Die einfache Zellstruktur und die geringen Herstellungskosten machen die Festkörperbatterie kostengünstig.
- Festkörperbatterien laden 6-mal schneller als Flüssigbatterien.
- Die Lebensdauer einer Festkörperbatterie kann bis zu 10 Jahre betragen.

Nachteile der Festkörperbatterie
- Dendriten sind das größte Problem bei Festkörperbatterien, abgesehen von den Kosten. Dendriten sind Lithium-Metall-Kristallisationen, die an der Anode beginnen und sich über die gesamte Batterie ausbreiten können. Dies geschieht, wenn sich die Ionen im Festelektrolyten mit den Elektronen verbinden und durch das Laden und Entladen mit hohen Strömen ein festes Lithiummetallblech entsteht.
- Diese Batterien werden in der Unterhaltungselektronik und in Elektrofahrzeugen nicht in großem Umfang eingesetzt, da sie sehr teuer sind. Festkörperbatterien zeigen eine langsamere Kinetik aufgrund von:
- Niedrige ionische Leitfähigkeit
- Hohe Grenzflächenbeständigkeit
- Schlechter Grenzflächenkontakt
Wie funktioniert eine Festkörperbatterie?
Wie bereits erwähnt, verwenden Festkörperbatterien eine Festelektrolytmembran mit festen positiven und negativen Elektrodenmaterialien. Beim Laden oder Entladen wandern die Ionen in eine ionenleitende Feststoffmatrix und nicht in ein in einer Lösung gelöstes ionisches Salz, wodurch die Lade- oder Entladereaktionen ausgelöst werden. Redoxreaktionen werden zur Speicherung und Verteilung von Energie in Festkörperbatterien verwendet. Die Anode wird oxidiert, während die Kathode reduziert wird, und die Batterie kann dieses Phänomen nutzen, um Energie nach Bedarf zu speichern (Laden) und abzugeben (Entladen).
Bei der Entladung von Energie verursachen die Ionen eine chemische Reaktion zwischen den Materialien der Batterie, die als „Redox“ bezeichnet wird. Dabei kommt es an der Anode zu einer Oxidation, bei der Verbindungen mit freien Elektronen entstehen, die elektrische Energie liefern, und an der Kathode zu einer Reduktion, bei der Verbindungen entstehen, die Elektronen aufnehmen und somit Energie erhalten. Der Mechanismus kehrt sich um, wenn eine Batterie geladen wird. Positiv geladene Ionen wandern beim Entladen von Festkörperbatterien (Kathode) durch den Elektrolyten von der negativen Elektrode (Anode) zur positiven Elektrode (Kathode). Dadurch entsteht eine positive Ladung in der Kathode, die Elektronen von der Anode aufnimmt.
Da die Elektronen jedoch nicht durch den Elektrolyten hindurchgehen können, müssen sie einen Stromkreislauf durchqueren, der die Energie an das Gerät weiterleitet, z. B. an einen Elektromotor. Bei der Aufladung wandern Ionen zur Anode und akkumulieren eine Ladung, die über einen Stromkreis Elektronen von der Kathode aufnimmt. Die Batterie gilt als vollständig geladen, wenn keine Ionen mehr zur negativen Elektrode fließen können. Festkörperbatterien benötigen verschiedene Additive und Bindemittel in ihren Schichten, um während des Zyklus eine hohe Leitfähigkeit zu behalten. Die Materialien müssen auch unter Druck gehalten werden, um den Kontakt während der Lade- und Entladezeiten aufrechtzuerhalten. Die normale Ausdehnung und Kontraktion von Materialien während der Lade- und Entladezyklen erschwert die Aufrechterhaltung eines festen Griffs zusätzlich.
Die Lebensdauer und Leistung der Zelle kann beeinträchtigt werden, wenn die Ausdehnung und Kontraktion die Verbindung im Laufe der Zeit schwächt. Solid-State-Batterien vereinfachen im Vergleich zu Li-Ionen-Batterien auch die Pack-Ebene, auf der die einzelnen Zellen befestigt werden. Festkörperbatterien benötigen keine große thermische Kontrolle, da sich ihr Wirkungsgrad mit steigender Temperatur verbessert.
Die Gesamtlade- und Entladeraten sowie die Ionenleitfähigkeit von Festelektrolyten nehmen mit steigender Temperatur zu. Folglich ist die ultimative Betriebstemperatur einer Festkörperzelle nur durch den Schmelzpunkt von Lithium begrenzt, der bei 180 °C liegt. Da außerdem kein entflammbarer flüssiger Li-Ionen-Elektrolyt verwendet wird, gibt es keine Bedenken hinsichtlich eines katastrophalen Ausfalls der Zelle oder des Akkus. Festkörperbatterien auf Lithium-Metall-Basis sollten als Alternative zu Lithium-Ionen-Batterien verwendet werden, da die in typischen Lithium-Ionen-Batterien verwendete Graphitanode im Vergleich zu Lithium ein niedriges Potenzial (0,20 V) aufweist und eine größere volumetrische Energiedichte bei gleicher Spannung und Leistung bietet.
Sind Festkörperbatterien verfügbar?
Herzschrittmacher, RFID und tragbare Geräte verwenden Festkörperbatterien. Einige dieser Batterien werden in der Raumfahrt eingesetzt. Kommerzialisierungsansätze für Festkörperbatterien im EV/HEV Automobilmarkt. Bei der Entwicklung von Festkörperbatterien geht es nicht nur um die Entwicklung eines geeigneten Festkörperelektrolyts, sondern auch um die Berücksichtigung von Merkmalen wie:
- Sicherstellung der Materialversorgung und des Verkaufs.
- Ausrüstung und Entwicklung für die Herstellung von Zellen und Verpackungen.
Trotz jahrelanger Entwicklung ist es vielen Akteuren nicht gelungen, Festkörperbatterien auf den Markt zu bringen. Bei Raumtemperatur sind die ionischen Elektrolyte in der Regel um mehrere Größenordnungen niedriger als die flüssigen Elektrolyte. Dies ist eines der Haupthindernisse für die Kommerzialisierung von Festkörperbatterien. Das Konzept der Festkörperbatterien gibt es zwar schon seit Jahrzehnten, aber erst jetzt werden dank der Investitionen von Elektronikfirmen, Automobilherstellern und allgemeinen Industrieanbietern Fortschritte erzielt.
Warum sind Solid-State-Batterien besser?
Festkörperbatterien bieten im Vergleich zu ihren flüssigkeitsgefüllten Pendants mehrere Vorteile, darunter eine längere Lebensdauer, kürzere Ladezeiten und ein angenehmeres Erlebnis. Anstatt die Elektroden in einem flüssigen Elektrolyten zu suspendieren, komprimieren Festkörperbatterien die Anode, die Kathode und den Elektrolyten in drei flache Schichten. Dadurch können sie kleiner gemacht werden – oder zumindest die gleiche Energiemenge wie eine größere Lösungsmittelbatterie liefern.
Wenn also ein Handy oder Laptop einen Lithium-Ionen- oder Lithium-Polymer-Akku mit einem Festkörperakku derselben Kapazität hat, hält es viel länger. Es wird ein System geschaffen, das die gleiche Ladungsmenge trägt, aber viel kleiner und dünner ist. Festkörperbatterien, die für die Stromversorgung von Stromgeräten oder sogar Elektrofahrzeugen eingesetzt werden, könnten sich viel schneller aufladen, da die Ionen viel schneller von der Kathode zur Anode gelangen könnten. Eine Festkörperbatterie könnte verschiedene wiederaufladbare Batterien in Bezug auf die Kapazität um 500 Prozent oder mehr übertreffen und sich in einem Zehntel der Zeit aufladen. Festkörperbatterien sind weniger schädlich für die Umwelt.
Festkörper-Dünnschichtbatterien sind weniger umweltschädlich als herkömmliche Batterien. Da Festkörperbatterien eine höhere Leistung und Energiedichte aufweisen, benötigen sie nicht die Kühl- und Steuerkomponenten wie Lithium-Ionen-Batterien, was zu einer geringeren Gesamtgröße, mehr Gerätefreiheit und einem geringeren Gewicht führt.
Da Festkörperbatterien resistent gegen Elektrodenkorrosion sind, die durch Chemikalien im flüssigen Elektrolyt oder durch den Aufbau fester Schichten im Elektrolyt verursacht wird, die die Lebensdauer der Batterie verkürzen, können Festkörperbatterien mehr Entlade- und Ladezyklen als Lithium-Ionen-Batterien überstehen. Festkörperbatterien können bis zu sieben Mal häufiger aufgeladen werden als Lithium-Ionen-Batterien, was ihnen eine Lebensdauer von zehn Jahren statt der wenigen Jahre ermöglicht, für die Lithium-Ionen-Batterien ausgelegt sind. Bildungseinrichtungen, Batteriehersteller und Materialexperten untersuchen, wie Festkörperbatterien zu Energiequellen der nächsten Generation für den breiten Einsatz umgewandelt werden können.
Werden Festkörperbatterien schneller aufgeladen?
Einige Festelektrolyte haben eine Ionenleitfähigkeit von mehr als 5 mS/cm und sind Ein-Ionen-Leiter. Dadurch wird bei hohen Strömen verhindert, dass sich im Festelektrolyten ein Polarisationswiderstand aufbaut. Folglich ist das Schnellladen potenziell machbar. Festkörperbatterien verwenden ein festes Material, in der Regel eine Polymer- oder Keramikverbindung, um den brennbaren flüssigen Elektrolyten in Lithium-Ionen-Batterien zu ersetzen. Lithium-Metall-Anoden wurden als Ersatz für traditionelle Graphit- oder Silizium-Anoden eingeführt. Diese Bemühungen zur Entwicklung von Lithium-Metall-Festkörperbatterien haben das Potenzial, die Energiedichte zu verdoppeln und gleichzeitig die Ladezeit erheblich zu verkürzen.
Wie wird eine Festkörperbatterie hergestellt?
In der Festkörperbatterie gibt es nur zwei Hauptschichten, die Kathode, eine positive Elektrode mit einem elektrischen Kontakt zu einem Festkörper-Keramikseparator, der den Polymerseparator ersetzt, der den porösen Polymerseparator ersetzt, der in herkömmlichen Lithium-Ionen-Batterien zu finden ist. All-Solid-State-Elektrolyte basieren auf superionischen Leitern und optimierten Grenzflächen.
Die Herausforderung bei der Entwicklung eines guten Festkörperelektrolyten besteht in der Überwindung der Dreiphasengrenze, an der positive Elektroden, Ionen und Elektronen gleichzeitig transportiert werden müssen, was eine sehr intermittierende Phase erfordert. Der gleichzeitige Transport von Elektronen und Ionen an der Grenzfläche und die Kontrolle der Grenzflächen sind eine Herausforderung.
Die Probleme der chemischen Stabilität mit positivem Elektrolyt und der oxidativen Stabilität des Elektrolyten in Gegenwart von Kohlenstoff sowie die Probleme der Metallionendendriten erfordern die Einbeziehung geschützter Grenzflächen. Feste Elektrolyte haben eine um Größenordnungen geringere Ionenleitfähigkeit als flüssige Elektrolyte. Auch der Widerstand an der Grenzfläche zwischen Elektrolyt und Elektrode muss optimiert werden.
Herausforderungen für einen festen Elektrolyten für Batterien:
Dicke positive Verbundelektroden mit hoher aktiver Masse: hohe Ionenleitfähigkeit von Festkörperelektrolyten. Stabile Schnittstelle mit Oxid und geringer Redoxaktivität mit elektronisch leitenden Zusätzen.
Dünne Festelektrolytmembranen mit geringer Masse sollten gute mechanische Eigenschaften, Duktilität und dynamische Druckkontrolle aufweisen.
Alle SSB-Elektrolyte bieten eine beispiellose Kombination aus hoher Ionenleitfähigkeit und ausgezeichneter Stabilität zwischen Anode und Kathode. Die Kompatibilität der Anode ist dabei der Schlüssel, denn sie bietet auf Zellebene einen Hauptvorteil gegenüber anderen herkömmlichen Lithium-Ionen-Batterien.
Es gibt drei wichtige feste Elektrolyte:
Polymerelektrolyt: Der Vorteil von Polymerelektrolyt ist die Verarbeitbarkeit der Zelle. Die Nachteile sind eine relativ schlechte Stabilität gegenüber dem Metall und eine relativ schlechte Leitfähigkeit, insbesondere bei niedrigen Temperaturen.
Geringere Ionenleitfähigkeit = geringerer Transport von Ionen = weniger Strom.
Oxid-Elektrolyt: Sie besitzen ideale mechanische Eigenschaften, sind sehr steif und chemisch stabil gegenüber Metallanoden. Zu den größten Nachteilen gehören die geringe Korrosionsbeständigkeit bei Verwendung eines Oxidelektrolyten und die schwierige Verarbeitung, da sie sehr hohe Temperaturen erfordern. Sie besitzen eine höhere thermische Stabilität, eine vernachlässigbare Zellverarbeitbarkeit, sind feuchtigkeitsempfindlich und weisen eine mäßige Leitfähigkeit auf. Elektrolyte auf Oxidbasis sind in der Regel chemisch stabil und können mit hochenergetischen Kathodenmaterialien verwendet werden.
Die Ionenleitfähigkeit ist jedoch geringer als die von Elektrolyten auf Sulfidbasis.
Materialien mit einem Perowskit (LLTO: Lithium-Lanthan-Titan-Oxid)
Die Granatstruktur (LLZO, Lithium-Lanthan-Zirkonium-Oxid) sowie NASICON (LAGP: Lithium-Aluminium-Germanium-Phosphat) sind beeindruckend unter den Elektrolyten auf Oxidbasis.
Sulfidelektrolyt: Sie besitzen mechanische Eigenschaften, die zwischen denen eines Polymers und eines Oxids liegen. Sie sind von allen Elektrolytklassen am leitfähigsten. Alle rekordverdächtigen Elektrolyte stammen aus Materialien der Sulfidklasse. Sie besitzen eine höhere Leitfähigkeit, eine bessere Verarbeitbarkeit der Zellen und eine höhere Wärmekapazität, sind aber feuchtigkeitsempfindlich. Die ionische Leitfähigkeit ist in der Regel bei Elektrolyten auf Sulfidbasis höher, aber sie sind chemisch instabiler.
Bei Raumtemperatur hat das amorphe Lithium-Zinn-Phosphor-Sulfid (LSPS) eine sehr hohe Ionenleitfähigkeit. Unverträglichkeiten mit Lithium-Metall sind dagegen ein Problem.
Ein Material, das die Elektrolyte bestimmt, wird als Additiv bezeichnet. Ein Additiv ist eine kleine Menge eines Materials, das eine Schutzschicht auf den Oberflächen von Kathode und Anode bildet. Es verhindert die Degradation der Batterie, indem es den reibungslosen Übergang von Lithiumionen zwischen Kathode und Anode erleichtert.
Kathoden- und Anodenadditive sind die beiden Arten von Additiven. Kathodenadditive verhindern die Alterung der Batterie, indem sie die Kathodenstruktur stabilisieren und die Oberfläche schützen, wodurch Überhitzung und Überladung verhindert werden. Anodenadditive lösen sich schneller auf als ein Lösungsmittel und bilden einen starken Film auf der Anode, der ihre Lebensdauer verlängert, Überhitzung verhindert und die Batterie geladen hält. Additive spielen eine wichtige Rolle im Gesamtsystem, indem sie die Lebensdauer verlängern, Probleme mit hohen Temperaturen verbessern und den Widerstand senken.
Ein Separator ist eine dünne isolierende Membran mit etwa vier Merkmalen, die Kathode und Anode voneinander trennen. Zweitens schützen Separatoren, wie der Name schon sagt, die Kathode und die Anode davor, sich in der Batterie zu berühren.
Zweitens haben die Separatoren Poren im Submikronbereich, die für das bloße Auge unsichtbar sind, und die Poren dienen als Kanäle für Lithiumionen, die zwischen der Kathode und der Anode passieren. Da die Abscheider über eine gute mechanische Stabilität verfügen, hält die Zugeigenschaft Nebenprodukte und Fremdstoffe fern und sorgt für Sicherheit. Als Separatoren können elektrochemisch stabile und hoch isolierende Materialien verwendet werden. Separatoren sollen die Wechselwirkung zwischen Kathode und Anode vermeiden, und es führt zu großen Problemen, wenn sie mit Lithiumionen oder anderen Ionen in einer Batterie interferieren. Die Separatoren sollten in der Lage sein, den Schutz zu gewährleisten, indem sie die Poren schließen und die Bewegung der Ionen verhindern, wenn die Temperatur in einer Batterie einen bestimmten Grenzwert überschreitet.
Schließlich sollten SSB-Separatoren so klein sein, dass mehr aktive Materialien in eine Batterie eingebaut werden können, was die Energiedichte erhöht. Um Schäden zu vermeiden und Schutz zu gewährleisten, sollten sie auch eine hohe mechanische Leistung aufweisen.
Anforderungen an Festelektrolyte
Für die Kommerzialisierung von Festkörperbatterien werden feste Elektrolyte mit einer spezifischen Kombination von Eigenschaften benötigt. Um als Ersatz für flüssige Elektrolyte geeignet zu sein, müssen feste Elektrolyte eine Lithium-Ionenleitfähigkeit von mehr als 0,1 mS/cm aufweisen. Entweder muss der Elektrolyt chemisch stabil gegenüber der Lithiumreduktion sein, oder es muss eine passivierende Reaktionsschicht gebildet werden. Um den Innenwiderstand der Zelle gering zu halten, muss der Elektrolyt niederohmige Grenzflächen bilden.
An der Alkalimetall-Grenzfläche, wo atmosphärisch umgesetzte Substratschichten, reduzierte Oxide und inhomogene Benetzung zu einem erheblichen Grenzflächenwiderstand führen können, wird die Schaffung von Grenzflächen mit geringem Widerstand noch komplexer. Der Elektrolyt muss eine ausreichende Festigkeit und Bruchzähigkeit aufweisen, um die Verbreitung von Lithiumfäden durch den Elektrolyten zu vermeiden. Der Elektrolyt muss sowohl auf dem Anoden- als auch auf dem Kathodenpotenzial stabil sein.
Feste Elektrolytformen
Da polymere Festelektrolyte eine geringe Ionenleitfähigkeit haben, werden sie in der Regel bei höheren Temperaturen (60°C-80°C) verwendet, um den Vorteil eines höheren Ionentransports zu nutzen. Obwohl Polymere einfach zu verarbeiten sind, reichen ihre mechanischen Eigenschaften nicht aus, um die Lithium-Metall-Anode stabil zu halten.
Infolgedessen haben anorganische Festelektrolyte die meiste Anerkennung erfahren. Die Leitfähigkeiten von festen Sulfidelektrolyten gehören zu den stärksten aller festen Elektrolyte.
Obwohl es viele verschiedene chemische Systeme gibt, wird das Li2 S-P2 S5-System am häufigsten verwendet. Im Li2 S-P2 S5-Gerüst können die Elektrolyte glasartig, kristallin oder teilkristallin sein. Nicht dotierte Li2 S-P2 S5-Elektrolyte weisen eine geringe elektrochemische Stabilität mit Lithium auf, während dotierte Versionen eine bessere Stabilität aufweisen. Bei Raumtemperatur oder unter 400 °C lassen sich Sulfidelektrolyte aufgrund ihrer Duktilität zu kompakten Gebilden mit guter elektrochemischer Überbrückung zwischen den Partikeln verdichten. Daher sind Sulfidelektrolyte die am einfachsten zu verarbeitenden anorganischen Festelektrolyte.
Die Reaktivität mit Wasserdampf in der Luft kann jedoch bei bestimmten Sulfid-Elektrolytzusammensetzungen ein Problem darstellen, da H2 S freigesetzt wird und der Elektrolyt sich zersetzt. Daher werden sie normalerweise in Argon oder in Trockenräumen mit niedriger Luftfeuchtigkeit verarbeitet.
Festelektrolyte auf Oxidbasis sind eine zweite Form eines anorganischen Festelektrolyten. Es gibt einige verschiedene Formen, wobei Granat Li7 La3 Zr2 O12 die häufigste ist. Feste Oxidelektrolyte haben bei Raumtemperatur eine hohe Ionenleitfähigkeit, den größten elektrochemischen Bereich und die höchste chemische Stabilität gegenüber Lithium. Darüber hinaus haben Oxidmaterialien die höchsten Elastizitätsmodule und Bruchzähigkeit aller Festelektrolyte, was sie ideal für die physikalische Stabilität der Lithium-Metall-Anode und die lange Lebensdauer der Zellen macht. Obwohl sie die beste Mischung elektrochemischer Eigenschaften aufweisen, benötigen dichte Elektrolyte mit hoher Ionenleitfähigkeit Sintertemperaturen von 1.000°C – 1.300°C.
Der Widerstand gegen die Entwicklung von Dendriten oder Lithiumfilamenten in Festelektrolyten hängt in der Regel mit der Stromdichte oder dem gesamten Zellstrom geteilt durch den Elektrolytquerschnitt zusammen. Infolgedessen kann die Zelle bei einer kritischen Stromdichte (CCD) versagen, wenn das Lithiummetall in die Zelle eindringt. Eine stabile Aufladung ist bei Stromdichten unterhalb dieses kritischen Wertes möglich. Die Konstantstromplattierung von Lithium in asymmetrischen Zellen mit Lithiumelektroden auf beiden Seiten eines festen Elektrolyten ist eine Standard-CCD-Untersuchung.
Bei der Herstellung des LGPS-Sulfid-Festelektrolyten wurde die Struktur des Materials mit Neutronenstrahlen analysiert. Die Forscher konnten die lineare Bewegung der Ionen in der Molekularstruktur des festen Leiters beobachten. Ein Tunnel wird in seiner 3D-Struktur beobachtet. In diesem Tunnel wurde die Bewegung von Lithium-Ionen beobachtet. Mit diesem Hinweis konnten die Forscher die Ionenleitfähigkeit und Stabilität des Materials verbessern und zwei neue Materialien entwickeln, indem sie LGPS eine geringe Menge Chlor hinzufügten. Diese Materialien wiesen die weltweit höchste Leistung als Ionenleiter auf.
Diese Materialien wurden mit einem Materialdesign-Diffraktometer analysiert. Die Ergebnisse zeigten eine innovative Struktur, die es den Ionen ermöglichte, sich in drei Dimensionen zu bewegen, anstatt nur in einer. Dies ermöglichte die höchste Leistung der Materialien. Unter einer Vielzahl von Zellen der neuen Generation, die entwickelt wurden, wurden diese Materialien zu starken Elektrolyten für den Einsatz in allen SSB.
Diese SSB haben im Vergleich zu Lithium-Ionen-Batterien eine etwas höhere Energiedichte und eine höhere Ausgangsleistung. Daher sind die Vorzüge aller SSB so konzipiert, dass sie über kompakte Batterien mit hoher Kapazität verfügen, die in kurzer Zeit wieder aufgeladen werden können. Als Produkt engagierter Forschung und atomarer Analyse von Elektrolytmaterialien könnten diese neuen SSB zu einer neuen Generation von Batterien führen.
In einer Lithium-Ionen-Festkörperbatterie verlässt das Lithium bei der Aufladung der Batterie durch das Atomgitter eines nicht porösen Festkörper-Keramikseparators den Speicher. Sobald das Lithium wirklich abgeschieden ist, lagert es sich zwischen dem Separator und dem elektrischen Kontakt ab und bildet eine Anode aus reinem metallischem Lithium. Mit einer Lithium-Metall-Anode kann die Energie einer Festkörperbatterie in einem kleineren Energievolumen gespeichert werden, was eine höhere Energiedichte im Vergleich zu herkömmlichen Lithium-Ionen-Batterien ermöglicht. Festkörper-Lithium-Metall-Batterien ermöglichen eine größere Reichweite durch die höhere Energiedichte einer fünfzehnminütigen Schnellladung und einen sichereren Betrieb durch den Wegfall des organischen Polymer-Separators.
Hochenergetischer Lithium-Ionen-Akku:
- Verwendung von hochenergetischen Materialien
- Nickelhaltige NMC- oder NCA-Kathoden bieten in Kombination mit einer Silizium-Verbundanode höhere gravimetrische und volumetrische Energiedichten.
- Für die Herstellung werden Kostensenkungen erwartet.
- Es sind nur geringfügige Änderungen im Produktionsprozess erforderlich.
Festkörper-Lithium-Batterie
Lithium-Schwefel-Batterie:
- Bei der Entladung reagiert Lithium mit Schwefel an der Kathode und bildet Lithiumsulfide.
- Schwefel ist ein weit verbreitetes und kostengünstiges Material, das preiswerte Batteriezellen ermöglicht.
- Die Ungewissheit hinsichtlich Zyklus und Lebensdauer sowie die Empfindlichkeit gegenüber hohen Temperaturen hemmen weiterhin das Wachstum des Marktsegments.
- Gegenwärtig ist die volumetrische Energiedichte für den Einsatz im Auto tendenziell zu gering.

Lithium-Luft-Batterie:
- Lithium wird bei der Entladung auf der Kathodenseite mit Sauerstoff oxidiert, wobei Lithiumperoxid und Lithiumoxid entstehen.
- Eine hohe Energiedichte und die Verwendung von Umgebungsluft sind technisch machbar.
- Riesige Hindernisse bei der Zyklenstabilität, die eine Anwendung im nächsten Jahrzehnt unwahrscheinlich erscheinen lassen.
Funktionsweise und Gestaltung aller SSB
- Ein ionenpermeabler Festelektrolyt wirkt als Separator und sorgt sowohl für eine räumliche als auch für eine elektrische Trennung zwischen der Kathode und der Anode einer All-SSB
- Es gibt eine Vielzahl von Zelldesigns, aus denen Sie wählen können. Eine Dünnschichtzelle ist in der obigen Abbildung dargestellt. Um dickere Schichten zu erzeugen, kann eine Verbundkathode verwendet werden.
- Bei der Entladung einer SSB gelangen Lithium-Ionen von der Anode über den Festelektrolyten zur Kathode. Gleichzeitig fließt eine Leistung an der externen Last.
- Der Widerstand an der Anoden-Elektrolyt-Grenzfläche ist ein entscheidender Faktor für den Wirkungsgrad der Batteriezelle. Eine äußere Folie, z. B. aus Gummi oder einer Aluminiumlegierung, kann dies abmildern.
- Die bipolare Stapelung ist aufgrund des starken Elektrolyten möglich. Folglich werden die Elementarzellen in Reihe geschaltet.
Woraus bestehen Festkörperbatterien?
Materialien für Festkörperbatterien:
Anode:
Aufgrund ihres theoretischen Potenzials, die höchste Energiedichte zu erreichen, gelten Lithiummetallanoden als ideal. Der starke Elektrolyt hingegen muss verhindern, dass das metallische Lithium Dendriten bildet. Da Lithium außerdem mit Luftsauerstoff eine Passivschicht bildet, ist eine Handhabung unter inerter Atmosphäre erforderlich.
Silizium als Anodenmaterial bietet eine sehr hohe Energiedichte, unterliegt aber einer starken Volumenveränderung, wenn es mit Lithium gemischt wird.
Kathode:
Das Metalloxid wird als Kathode verwendet. Da es viel weniger Materialien gibt, die speziell für den SSB-Bereich entwickelt wurden, werden in den meisten Fällen bestehende Kathodenmaterialien verwendet.
Grundsätzlich können je nach Elektrolyt eine Vielzahl von bewährten Kathodenmaterialien verwendet werden, die von preiswerten und sicheren Materialien wie Lithiumeisenphosphat (LFP) bis zu Lithium-Nickel-Mangan-Kobalt-Oxid (NMC) reichen. Nur Lithium-Kobalt-Oxid (LCO) als Kathodenmaterial und LLZO als Elektrolyt zeigen in der Praxis eine ausreichende Stabilität und Effizienz.
Verfahren zur Herstellung aller Festkörperbatterien
- Die Verarbeitung von Elektroden und Elektrolyten, die Montage der Zelle und die Endbearbeitung der Zelle sind die drei wichtigsten Schritte bei der Herstellung einer SSB.
- Es gibt keine allgemeingültige Prozesskette; alternativ kann eine Vielzahl von möglichen Prozessketten verwendet werden. Diese unterscheiden sich in mehrfacher Hinsicht vom Produktionsverfahren für Lithium-Ionen-Batterien.
- Bei dieser Methode werden zwei verschiedene Verfahren verglichen und gegenübergestellt, vor allem in Bezug auf die Elektroden- und Elektrolytleistung.
Elektrode und Elektrolyt
Produktion —- Zellenmontage——Zellenveredelung
Prozess A
Prozess B
Die Synthese von Grabenzellen mit anorganischen Festelektrolyten ist Gegenstand beider Verfahrensvarianten. Für reine Festkörperbatterien ist das Format der Pouch-Zelle am besten geeignet.
Eine prismatische oder runde Zelle:
Aufgrund der festen Komponenten einer Festkörperbatterie stehen die Wicklungen vor großen Herausforderungen. Keramische Schichten, die spröde sind, können Risse bekommen. Außerdem ist das Problem der richtigen Schichthaftung noch nicht gelöst.
Pouch-Zelle:
Festkörperbatterien profitieren vom Stapeln, da die flachen Schichten nicht verformt werden. Außerdem wird der Schichtverbund während der Elektroden- und Elektrolytverarbeitung hergestellt, so dass später nur noch die Grundzellen gestapelt werden müssen.
Für den Herstellungsprozess ist ein trockener Raum erforderlich, da die Materialien auf die Atmosphäre reagieren. Bei der Arbeit mit metallischem Lithium wird ein Inertgas wie Argon empfohlen.
Eine umfassende Bewertung der Anwendbarkeit der bei der Entwicklung von Lithium-Ionen-Batteriezellen erworbenen Kenntnisse wird für jede Prozessstufe durchgeführt.
Herstellung von Elektroden und Elektrolyten nach Verfahren A:
- Die Verbindung von Kathode, Elektrolyt und Anode wird bei der Elektroden- und Elektrolytverarbeitung gebildet.
- Nach der Entwicklung der Elektrode und des Elektrolyten liegt eine Elementarzelle vor.
- Das Hauptmerkmal der ersten Prozesskette, Prozesskette A, ist ein kontinuierlicher Extrusionsprozess, bei dem die Schichten geformt und anschließend laminiert werden.
- Diese Prozesskette eignet sich besonders gut für sulfidische Festkörpermaterialien.
Herstellung von Kathoden und Elektrolyten (Compoundierung):
- Das Produktionsverfahren
- Zwei verschiedene Compoundier-Industrien verwenden Kathoden- und Elektrolytschmelzen.
- Die Materialkomponenten werden dem beheizten Zylinder eines Doppelschneckenextruders zugeführt und können als Granulat oder Pulver bereitgestellt werden.
- Durch die Rotationsbewegungen des Extruders wird Energie in die Materialkomponenten übertragen. Infolgedessen ist die Schmelze homogen.
- Elektrolytpartikel, die den Widerstand zwischen Kathode und Elektrolyt verringern, sowie Bindemittel und Additive werden dem aktiven Kathodeninhalt beigemischt.
- Elektrolytmoleküle und polymere Bindemittel sind zwei wesentliche Bestandteile des Elektrolyts.
Parameter und Bedingungen für den Prozess:
- Menge der zu liefernden Einzelmaterialien
- Temperatur und Druck in der Flasche
- Die Geschwindigkeit und der Druck des Extruders
- Scherkraft
Qualitätsmerkmale:
- Die Homogenität der Schmelze
- Die Viskosität der Schmelze
- Maßstab und Menge verschmelzen
Technische Alternativen:
- Leistungsstarke Mischanlage
Herstellung von Kathoden und Elektrolyten (Co-Extrusion):
- Das Produktionsverfahren
- In einer geeigneten Düse werden die Kathoden- und die Elektrolytschmelze gemeinsam extrudiert. Dadurch entsteht eine Kombination aus Kathoden- und Elektrolytschicht.
- Die Kathode wird über getrennte Kanäle zugeführt, und der Elektrolyt schmilzt durch die Extrusionsdüse.
- Die Schmelze wandert durch die Kanäle zum Auslass des Strangpresswerkzeugs. Die Schmelzen werden mit Hilfe einer Breitschlitzdüse auf einen Stromleiter extrudiert.
Prozessparameter und Anforderungen:
- Einstellen der Schichtdicke
- Vorschubgeschwindigkeit der Schmelze
- Temperatur
- Druck
- Rollgeschwindigkeit
- Anpressdruck der Kalanderwalze
Qualitätsmerkmale:
- Dicke der Beschichtung
- Breite der Schicht
- Adhäsion zwischen den Schichten
Technische Alternativen:
- Siebdruck
Foliengießen
Anodenherstellung (Strangpressen und Kalandrieren):
- Eine reine SSB-Anode kann aus einer metallischen Lithiumfolie hergestellt werden. Diese Lithiumfolie kann durch Extrusion mit anschließender Kalandrierung hergestellt werden.
- Zu diesem Zweck wird flüssiges Lithium in den Zylinder eines Kolbenextruders gegossen. Das Lithium wird dann durch einen Kolben in eine Düse gepresst.
- Die Kalandrierung nach der Extrusion gewährleistet Homogenität und optische Schichtdicke. Die Folie wird von zwei Walzen unter Spannung aufgerollt, wobei zu diesem Zweck ein Schmiermittel aufgetragen wird.
- Die Walzen müssen in der Lage sein, mit der Klebrigkeit von Lithium zu arbeiten. Dies wird durch polymerbeschichtete Walzen, z. B. aus Polyacetal, erreicht.
Prozessparameter und Anforderungen:
- Extrusionsgeschwindigkeit
- Temperatur
- Geometrie der Düse
- Anpressdruck der Kalenderwalzen
- Fördergeschwindigkeit des Schmierstoffs
- Rollgeschwindigkeit
Qualitätsmerkmale:
- Dicke der Folie
- Breite der Folie
- Homogenität der Lithiumfolie
Technische Alternativen:
- Atomare Schichtabscheidung
PVD-Verfahren
Herstellung von Schichtverbunden (Laminieren):
- Die Lithiumfolie wird nach der Verarbeitung auf den Kathoden-Elektrolyt-Verbundstoff laminiert. Dazu werden die beiden Schichten mit Hilfe von Walzen zusammengefügt.
- Im nächsten Schritt werden die beiden Schichten durch zwei Walzen zusammengepresst. Um größere Haftkräfte zu erzielen, werden diese erhitzt. Die Polymere dringen beim Erhitzen und Pressen von einer Schicht in die nächste ein und stellen so die Verbindung zwischen Anode und Elektrolyt her.
- Die Begriffe „Trocken-“ und „Nasslaminierung“ können unterschieden werden. Bis zur Laminierung werden bei der Nasslaminierung die Kontaktflächen mit einem Lösungsmittel befeuchtet. Dies erleichtert die Laminierung bei niedrigen Temperaturen und niedrigem Druck.
Parameter und Anforderungen des Prozesses:
- Vorschubgeschwindigkeit der Schichten
- Rollgeschwindigkeit
- Druck
- Optionale Erwärmung der Schichten
Qualitätsmerkmale:
- Adhäsion zwischen den Schichten
- Gewünschte Verbundstoffdicke
- Die Geometrie des Verbundwerkstoffs
Technische Alternativen:
- Pressen und anschließendes Sintern
Verfahren zur Herstellung von Elektroden und Elektrolyten B
- Das Verfahren der physikalischen Gasphasenabscheidung (PVD), bei dem die einzelnen Schichten nacheinander aufgebracht werden, ist das Hauptmerkmal der unten dargestellten Verfahrenskette B.
- Dieses aktuelle Verfahren, das die Herstellungsschritte einer Dünnschichtbatterie zeigt, eignet sich besonders für oxidbasierte Festkörperbatterien.
Materialaufbereitung (Mahlen und Mischen):
- Methodik der Herstellung
- Eine Kugelmühle wird verwendet, um das Kathodenpulver vom Elektrolytpulver zu trennen.
- Das Rohmaterial wird dazu in eine zylindrische Mahltrommel gegeben. In dieser Mahltrommel werden Kugeln als Mahlkörper verwendet.
- Die Rotationsbewegungen des Zylinders verbinden die Ausgangsstoffe. Außerdem sorgt die Drehbewegung dafür, dass sich das Mahlgut und das Ausgangsmaterial beim Mahlen relativ zueinander verschieben.
- Anschließend wird das Pulver kalziniert, um die gewünschten Pulvereigenschaften zu erzielen.
Anforderungen und Parameter des Prozesses:
- Material der Kugel
- Geschwindigkeit
- Schleifzeit
- Material des Zylinders
- Menge des Ausgangsmaterials
Qualitätsmerkmale:
- Durchschnittliche Partikelgröße des Pulvers
- Homogenität des Pulvers (Grad der Durchmischung)
Technische Alternativen:
- Sol-Gel-Verfahren
Herstellung von Schichtverbindungen (Hochfrequenzsputtern):
Herstellungsverfahren:
- Die Kathoden- und Elektrolytschichten werden durch Hochfrequenzsputtern aus Kathoden- und Elektrolytpulvern erzeugt. Das Target für das Sputtering-Verfahren wird zunächst mit Hilfe einer Matrize oder eines Heißpresssystems aus Pulvern hergestellt.
- Der vorliegende Kollektor dient auch als Substrat für das Verfahren. In der ersten Phase wird die Kathodenschicht abgeschieden. Anschließend wird eine Elektrolytschicht auf die Kathodenschicht aufgebracht.
- Die Ionen werden auf das Ziel des Sputtervorgangs gerichtet. In diesem Schritt werden Atome aus dem Target herausgeschlagen, das dann in die Gasphase gelangt und sich zum Substrat bewegt. Die Schicht wird also Atom für Atom auf der Oberfläche des Substrats aufgebaut.
- Für das Hochfrequenzsputtern wird eine Vakuumkammer verwendet.
Anforderungen und Parameter des Prozesses:
- Temperatur
- Ablagerungszeit
- Prozessdruck
- Umgebungsatmosphäre
- Prozessleistung/Leistungsdichte
- Zieldurchmesser und Zieldistanz
Qualitätsmerkmale:
- Die Schichtdicke des Stromabnehmers
- Die Schichtdicke der Kathode und des Elektrolyten
Technische Alternativen:
- Chemische Gasphasenabscheidung
Abscheidung von Schichtverbindungen (Sintern)
Herstellungsverfahren:
- Die Kathoden- und Elektrolytschichten werden während des Sinterns komprimiert. Durch die Verbesserung der Verbindung zwischen den beiden Schichten kann der Widerstand an der Schnittstelle Elektrolyt-Elektrode verringert werden.
- Ein Sinterofen wird zum Sintern der Kathoden-Elektrolyt-Verbindung verwendet. Die Substanz wird bis knapp unter ihren Schmelzpunkt erhitzt.
- Die resultierende Porosität der Materialien kann je nach den gewählten Prozessparametern verändert werden.
- Um Reaktionen mit der Umwelt zu vermeiden, erfolgt der Sinterprozess in einer inerten Atmosphäre oder im Vakuum.
- Das Sintern ist vor allem bei Festelektrolyten auf Oxidbasis wichtig, um eine ausreichende Grenzflächentoleranz zu erreichen.
Herstellung von Schichtverbindungen (thermische Verdampfung):
Prozess der Herstellung:
- Die Anode kann durch thermisches Verdampfen auf die Kathoden-Elektrolyt-Verbindung aufgebracht werden. Der Anodeninhalt besteht aus metallischem Lithium.
- Bei der thermischen Verdampfung muss metallisches Lithium auf Temperaturen oberhalb des Siedepunkts erhitzt werden, z. B. mit einem Elektronenstrahlverdampfer, damit es in die Dampfphase übergehen kann. In der Vakuumkammer breitet sich der Dampf gleichmäßig aus.
- Die Kondensation bildet die Beschichtung auf der Niedrigtemperaturoberfläche des Elektrolyten.
- Die thermische Verdampfung erfolgt in einer Vakuumkammer, vergleichbar mit dem Sputtern.